ЭКСПРЕССИВНОСТЬ ГЕНА
Экспрессивность гена (латинский expressus явный, выразительный; ген; синоним выражение гена) — степень или мера фенотипического проявления гена, то есть степень и (или) характер выраженности наследственного признака среди особей определенного генотипа, у которых этот признак проявляется. Экспрессивность гена тесно связана с пенетрантностью (см. Пенетрантность гена), или проявлением, гена (см.), а также с его специфичностью. В совокупности пенетрантность и экспрессивность характеризуют изменчивость фенотипического проявления генов.
Понятие «экспрессивность гена» было введено в научную литературу Н. В. Тимофеевым-Ресовским и немецким неврологом О. Фогтом, которые впервые применили его в своей совместной работе, опубликованной в 1926 году. Необходимость введения этого понятия была обусловлена тем, что термин «генотип» однозначно и однообразно определял совокупность лишь тех генов, которые контролируют некоторые наследственные признаки, не изменяющиеся в течение всей индивидуальной жизни (см. Генотип). К таким признакам относятся, например, группа крови (см. Группы крови), антигены эритроцитов и лейкоцитов человека и животных (см. Антигены) и др. Однако чаще бывает так, что наличие в генотипе определенного гена является необходимым, но недостаточным условием для полного сходства носителей этого гена по соответствующему признаку. У части особей — носителей такого гена (в гомозиготном состоянии для рецессивных генов, а в гетерозиготном — для доминантных) он может вообще не проявиться (так наз. неполная пенетрантность), а у части особей, у которых этот ген проявился, его выраженность может быть различной, то есть экспрессивность этого гена может варьировать (так называемая варьирующая экспрессивность гена).
Варьирующая экспрессивность гена хорошо известна в медицинской генетике (см.). Так, полный синдром Марфана (см. Марфана синдром) характеризуется арахнодактилией (см.), разболтанностью суставов, формированием аневризм аорты и легочного ствола, подвывихом или вывихом хрусталика, кифозом (см.), сколиозом (см.) и др. Однако случаи проявления у одного больного всех клин, признаков, характерных для синдрома Марфана, редки. Чаще встречаются случаи «неполного» синдрома Марфана, причем даже в одной семье симптомокомплекс, как правило неодинаков у разных членов семьи.
От варьирующей экспрессивности одного гена следует отличать проявление полиморфных групп сходных признаков, которое обусловлено разными генетическими причинами (см. Генокопия). Например, в медицинской генетике известна полиморфная группа форм (не менее 7) синдрома Элерса — Данлоса, суммарно характеризующаяся разными сочетаниями, локализацией и выраженностью внутренних кровотечений, вызванных разрывами сосудов, повышенной растяжимости кожи, разболтанностью суставов. Общим патогенетическим фактором при всех этих состояниях является нарушение биосинтеза коллагена (см.). Однако при разных формах синдрома нарушения локализуются в различных местах биосинтетической цепи коллагенов. Различны и обусловливающие их генетические дефекты: четыре формы синдрома Элерса—Данлоса (см. Десмогенез несовершенный) наследуются по аутосомно-доминантному типу, две — по аутосомно-рецессивному, а одна — по рецессивному типу, сцепленному с X-хромосомой.
Причинами варьирующей экспрессивности гена могут быть межиндивидуальные генотипические различия (генотипическая среда), вариабельность проявления генов в индивидуальном развитии (см. Онтогенез) и влияние факторов окружающей среды. Для варьирующей экспрессивности гена имеют значение все три причины и взаимодействие между ними.
Влияние генотипической среды как на повышенную, так и на пониженную экспрессивность гена доказывается успешным искусственным отбором: подбор родительских пар с лучше выраженным наследственным признаком автоматически накапливает в соответствующей линии гены-модификаторы (см. Ген), благоприятствующие проявлению данного признака, и наоборот. В ряде случаев такие гены-модификаторы идентифицированы. О роли генотипической среды в варьирующей экспрессивности гена свидетельствует также меньший размах внутрисемейного изменения выраженности наследственных признаков по сравнению с их межсемейной изменчивостью. Влияние вариабельности проявления генов в индивидуальном развитии на их экспрессивность иллюстрирует неполная конкордантность (или дискордантность) генетически идентичных однояйцовых (монозиготных) близнецов (см. Близнецовый метод) по степени и характеру выраженности одних и тех же наследственных признаков.
Примером влияния факторов окружающей среды на экспрессивность гена служит различная пигментация шерсти у животных некоторых пород в зависимости от температуры воздуха или улучшение состояния больных наследственными болезнями (см.) при соответствующем патогенетическом лечении (например, диетотерапия и др.).
Каждая из трех названных причин варьирующей экспрессивности гена в любом конкретном случае может иметь больший или меньший удельный вес, общим же правилом является то, что экспрессивность гена определяется взаимодействием генов и онтогенетических факторов, а также влиянием окружающей среды на организм как целостную систему в процессе онтогенеза. Такое представление об экспрессивности гена имеет большое теоретическое значение для понимания механизмов онтогенеза живых организмов и патогенеза наследственных болезней человека. В медицинской генетике это создает основу для поисков патогенетических методов коррекции наследственных дефектов, а в селекции и выращивании сельскохозяйственных растений и животных помогает созданию новых сортов и пород и их разведению в условиях, оптимальных для лучшей выраженности хозяйственно-ценных признаков.
Что такое экспрессивность генов
Экспрессия генов
Эти продукты часто являются белками, но в генах, не кодирующих белки (интроны), таких как гены-переносчики РНК (тРНК) или малые ядерные РНК продукт представляет собой функциональную РНК.
Экспрессия гена управляет такими процессами, как транскрипция, сплайсинг РНК, трансляция и посттрансляционная модификация белка.
Регуляция генов дает клеткам контроль над структурой и функцией, и является основой для клеточной дифференцировки, морфогенеза и универсальности и адаптивности любого организма. Регуляция генов может также служить субстратом для эволюционных изменений, поскольку контроль времени, места и количества экспрессии генов может оказывают глубокое влияние на функции (действия) гена в клетке или в многоклеточном организме.
В генетике экспрессия генов является наиболее фундаментальным уровнем, на котором генотип порождает фенотип, то есть наблюдаемый признак. Генетический код, хранящийся в ДНК, «интерпретируется» экспрессией генов, а свойства экспрессии отображаются в виде признаков. Такие фенотипы часто выражаются синтезом белков, которые контролируют форму живой структуры, или которые действуют как ферменты, катализирующие специфические метаболические пути, характеризующие организм в целом.
Таким образом, регуляция экспрессии генов имеет решающее значение для развития живых существ.
Что такое экспрессивность генов
Многие генетические заболевания четко определяются в семье; т.е. аномальный фенотип легко отличить от нормального. Из клинического опыта, тем не менее, известно, что некоторые заболевания могут не проявляться, хотя человек имеет тот же генотип, который вызывает заболевание у других членов семьи. В других случаях одно и то же заболевание может иметь чрезвычайно вариабельное проявление с точки зрения клинической тяжести, диапазона симптомов или возраста начала.
Фенотипическая экспрессия аномального генотипа может модифицироваться эффектами старения, других генетических локусов или факторами окружающей среды. Различия в экспрессии могут часто приводить к трудностям в интерпретации диагноза и родословной. Есть два различных механизма, которые могут объяснить различия в экспрессии: пониженная пенетрантность и вариабельная экспрессивность.
Пенетрантность — вероятность того, что ген будет иметь любые фенотипические проявления. Если частота экспрессии фенотипа менее 100%, т.е. существуют лица, имеющие соответствующий генотип без каких-либо его проявлений, говорят, что ген имеет неполную пенетрантность. Пенетрантность — понятие типа «все или ничего». Это процент людей с патологическим генотипом и его проявлениями, хотя бы в некоторой степени.
Экспрессивность — тяжесть экспрессии фенотипа среди индивидуумов с одним патологическим генотипом. Когда тяжесть болезни различается у людей, имеющих тот же генотип, говорят, что фенотип имеет вариабельную экспрессивность. Даже в одной родословной два индивидуума, несущих те же мутантные гены, могут иметь некоторые одинаковые признаки и симптомы, а другие проявления болезни могут различаться в зависимости от пораженных тканей и органов.
Некоторые трудности в понимании наследования фенотипа болезни, возникающие вследствие возраст-зависимой пенетрантности и переменной экспрессивности, можно рассмотреть на примере аутосомно-доминантного нейрофиброматоза НФ1. Нейрофиброматоз 1-го типа — частое заболевание нервной системы, глаз и кожи, встречается приблизительно 1 на 3500 родов. Значимых различий в частоте болезни среди этнических групп нет.
Нейрофиброматоз 1-го типа (НФ1) характеризуется ростом в коже многочисленных доброкачественных объемных опухолей, нейрофибром; присутствием многочисленных плоских нерегулярных пигментированных участков кожи, известных как «кофейные» пятна или пятна цвета «кофе с молоком»; ростом небольших доброкачественных опухолей (гамартом) в радужке глаза (узелков Лиша); иногда умственной задержкой, опухолями ЦНС, рассеянными плексиформными нейрофибромами и развитием злокачественных опухолей нервной системы или мышц. Таким образом, заболевание имеет плейотропный фенотип.
Нейрофиброматоз 1-го типа (НФ1) впервые полностью описан врачом фон Реклингаузеном в 1882 г., но, вероятно, болезнь была известна с древних времен. Хотя взрослые гетерозиготы почти всегда имеют какие-нибудь признаки болезни (т.е. пенетрантность у взрослых 100%), некоторые могут иметь только «кофейные» пятна, веснушки в подмышечной области и узелки Лиша, тогда как другие могут иметь угрожающие жизни доброкачественные опухоли, затрагивающие спинной мозг или злокачественные саркомы конечностей.
Таким образом, существует вариабельная экспрессивность; даже в пределах одной родословной некоторые больные поражены сильно, а другие только слегка. Постановка диагноза усложняется у детей, поскольку симптоматика развивается постепенно с возрастом. Например, в периоде новорожденности менее чем половина всех пораженных имеет хотя бы наиболее легкий признак болезни, «кофейные» пятна. Пенетрантность, следовательно, зависит от возраста.
В гене NF1 обнаружено множество различных мутаций, вызывающих снижение функции продукта гена, нейрофибромина. Приблизительно в половине случаев НФ1 вызван новой, а не унаследованной мутацией.
Главная генетическая проблема при консультировании семей пациентов с НФ1 — необходимость выбора между двумя равновероятными возможностями: болезнь пробанда спорадическая, т.е. новая мутация, или пациент унаследовал клинически значимую форму заболевания от родителя, у которого ген представлен, но слабо проявляет себя. Если пробанд унаследовал дефект, риск, что любой из его или ее сибсов также унаследуют это заболевание — 50%; но если пробанд имеет новую мутацию, риск для сибсов очень небольшой.
Важно, что и в том, и в другом случае риск того, что пациент передаст ген потомству, составляет 50%. Учитывая эту неопределенность, семьям пациентов с НФ1 нужно знать, что заболевание сможет быть обнаружено пресимптоматически и даже пренатально с помощью молекулярного генетического анализа. К сожалению, молекулярная диагностика обычно может только ответить на вопрос, будет ли развиваться заболевание, но не может определить степень его тяжести. За исключением ассоциации полной делеции гена с дисморфиями, умственной задержкой и большим количеством нейрофибром в раннем возрасте, корреляции между тяжестью фенотипа и конкретными мутациями в гене NF1 не выявлено.
Другой пример аутосомно-доминантного порока развития с неполной пенетрантностью — нарушение разделения кисти типа эктродактилии. Порок развития возникает на шестой или седьмой неделе развития, когда формируются кисти и стопы. Заболевание демонстрирует локусную гетерогенность. Выявлено по крайней мере пять локусов, хотя фактически ответственный ген подтвержден только в нескольких из них. Неполная пенетрантность в родословных с пороками развития кисти может привести к пропуску поколений, и это усложняет генетическое консультирование, поскольку человек с нормальными руками может, тем не менее, передавать ген заболевания и таким образом иметь больных детей.
Хотя в целом правила наследования моногенных заболеваний могут быть легко классифицированы на аутосомные или Х-сцепленные и доминантные или рецессивные, наследование в индивидуальной родословной может затемняться множеством других факторов, которые делают трудной интерпретацию вида наследования.
Диагностические трудности могут быть следствием неполной пенетрантности или вариабельной экспрессивности болезни; на экспрессию гена могут влиять другие гены и факторы окружающей среды; некоторые генотипы не доживают до рождения; может отсутствовать точная информация о присутствии заболевания у родственников или о семейных отношениях; доминантные и Х-сцепленные болезни могут вызывать новые мутации; и наконец, при небольшом размере семьи, типичным сегодня для большинства развитых стран, пациент может случайно оказаться единственным больным в семье, когда очень трудно принять решение о типе наследования.
Генетическое заболевание может появляться в любое время в течение всей жизни человека, начиная с раннего внутриутробного развития до старости. Некоторые из них могут быть летальными внутриутробно, другие могут создавать помехи для нормального развития плода и выявляться пренатально (например, ультрасонографией), но совместимы с живорождением; третьи могут быть выявлены только после рождения. (Часто путают генетические и врожденные заболевания.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Факторы, влияющие на экспрессию гена
, MD, University of Pittsburgh
На экспрессию генов могут повлиять многие факторы. Некоторые из них заставляют экспрессию признаков отклоняться от моделей, предсказанных менделевским наследованием.
Пенетрантность и экспрессивность
Пенетрантность – это показатель того, как часто ген подвергается экспрессии. Она определяется как процент людей, которые имеют ген и которые развивают соответствующий фенотип ( Пенетрантность и экспрессивность Пенетрантность и экспрессивность На экспрессию генов могут повлиять многие факторы. Некоторые из них заставляют экспрессию признаков отклоняться от моделей, предсказанных менделевским наследованием. (См. также Обзор генетики. Прочитайте дополнительные сведения ). Ген с неполной (низкой) пенетрантностью не может быть выражен, даже когда признак является доминирующим или когда он является рецессивным, и ген, ответственный за эту черту, присутствует в обеих хромосомах. Пенетрантность того же гена может варьироваться от человека к человеку и может зависеть от возраста человека. Даже когда ненормальные аллели не экспрессируются (непенетрантность), здоровый носитель аномальной аллели может передать его детям, у которых могут наблюдаться клинические аномалии. В таких случаях, родословная пропускает поколение. Тем не менее, некоторые случаи очевидной непенетрантности обусловлены незнанием эксперта или неспособностью признать небольшие проявления заболевания. Иногда считается, что у пациентов с минимальной экспрессией наблюдается разновидность заболевания.
Экспрессивность является пределом, до которого ген экспрессируется в одного человека. Она может быть классифицирована как процент; например, когда ген имеет 50%-ную экспрессивность, присутствует только половина функции или тяжесть составляет только половину того, что может произойти при полной экспрессии. На экспрессивность могут оказывать влияние окружающая среда и другие гены, поэтому люди, обладающие одинаковым геном, могут изменяться в фенотипе. Экспрессивность может меняться даже среди членов одной семьи.
Что такое экспрессивность генов
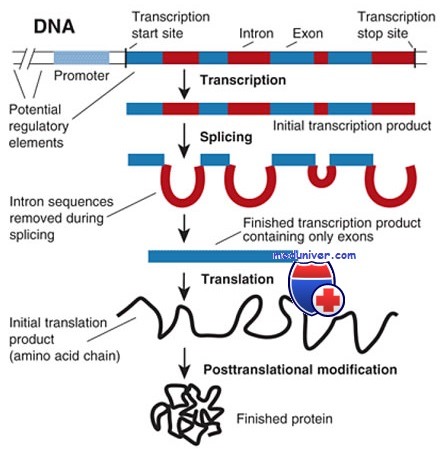
Для генов, кодирующих белки, движение информации от гена до полипептида включает несколько шагов. Инициация транскрипции гена происходит под влиянием промоторов и других управляющих элементов, а также специфических белков, известных как факторы транскрипции, взаимодействующих с определенными последовательностями в пределах управляющих областей гена и определяющих пространственную и временную схему экспрессии гена. Транскрипция гена начинается со «стартовой» точки в хромосомной ДНК в начале 5′-транскрибируемой, но не транслируемой области.
Процесс транскрипции идет непрерывно по ходу кодирующей последовательности вдоль хромосомы, проходя от нескольких сотен пар оснований до более миллиона пар, захватывая как интроны, так и экзоны, и завершаясь на конце кодирующей последовательности. После модификации обоих 5′ и З’-концов первичной копии РНК части, соответствующие нитронам, удаляются, а сегменты, соответствующие экзонам, сращиваются вместе.
После сплайсинга (сращивания) РНК результирующая мРНК (содержащая центральный сегмент, соответствующий кодирующей части гена), перемещается из ядра в цитоплазму клетки, где мРНК транслируется в аминокислотную последовательность закодированного полипептида. Каждая составляющая этого сложного пути подвержена ошибкам и мутациям, которые создают помехи и вызывают множество наследственных заболеваний.
Транскрипция
Транскрипция белок-кодирующего гена РНК-полимеразой-II (одна из нескольких классов РНК-полимераз) начинается в стартовом сайте транскрипции, в точке 5′-нетранслируемой области, соответствующей 5′-концу конечной РНК. Синтез первичной копии РНК идет по направлению от 5′ к З’-концу, поскольку нить считываемого гена, который служит шаблоном для синтеза РНК, действительно считывается в направлении от 3′ к 5′-концу в соответствии с направлением фосфатных связей дезоксирибозы.
Поскольку синтезированная РНК соответствует расположению и последовательности нуклеотидов (с заменой урацила на тимин) 5′-3′-нити ДНК, такую нить ДНК часто называют кодирующей или комплементарной ДНК (кДНК). 3′-5′-нить ДНК носит название некодирующей или антисмысловой. Транскрипция осуществляется как для интронных, так и для экзонных частей гена, до позиции в хромосоме, которая записывается на 3′-конец зрелой мРНК. Неизвестно, заканчивается ли транскрипция в определенной точке терминации на 3′-конце.
Затем в области 5′-конца первичной копии РНК происходит кэпирование, а в специфической точке 3′-конца — расщепление. Расщепление заканчивается присоединением к 3′-концевым звеньям множества остатков аденозина — поли-(А), что увеличивает стабильность полученной РНК. Позиция точки полиаденилирования частично определяется последовательностью AAUAAA (или вариантами этой последовательности), обычно обнаруживаемой в 3′-нетранслируемой части копии РНК. Описанные посттрансляционные модификации, как и процесс сплайсинга РНК, происходят в ядре.
Полностью обработанная РНК, теперь называющаяся мРНК, перемещается в цитоплазму, где происходит трансляция.
Трансляция и генетический код
В цитоплазме мРНК транслируется в белок под действием молекул тРНК, специфичной для каждой конкретной аминокислоты. Эти замечательные молекулы, каждая всего от 70 до 100 нуклеотидов длиной, добавляют к растущей полипептидной цепи определенную аминокислоту в соответствии с шаблоном мРНК. Белковый синтез происходит в рибосомах, макромолекулярных комплексах, состоящих из рРНК (кодируемой генами 18S и 28S) и нескольких десятков рибосомальных белков.
Ключ трансляции — код, который связывает специфическую аминокислоту с комбинацией из трех смежных оснований на мРНК. Каждое сочетание трех оснований составляет кодон, специфичный для конкретной аминокислоты. В теории существует почти бесконечное множество вариантов размещения оснований вдоль полинуклеотидной цепи. В каждом положении может быть один из четырех нуклеотидов (А, Т, С или G); таким образом, для трех оснований есть 43 или 64 возможные комбинации триплетов. Эти 64 кодона и составляют генетический код.
Поскольку на 20 аминокислот приходится 64 возможных кодона, некоторые аминокислоты определяются более чем одним кодоном; поэтому генетический код называют вырожденным. Например, основание в третьей позиции триплета часто может быть или пуриновым (А или G), или пиримидиновым (Т или С), а в некоторых случаях любое из четырех оснований не изменяет смысл сообщения. Лейцин и аргинин определяются сразу шестью кодонами. Только метионин и триптофан кодируются единственным, уникальным триплетом. Три кодона называются стоп-кодонами (или нонсенс-кодонами), поскольку они определяют завершение трансляции мРНК.
Трансляция зрелой мРНК всегда начинается с кодона, определяющего метионин. Следовательно, метионин — всегда первая аминокислота каждой полипептидной цепи, хотя обычно он удаляется до завершения синтеза белка. Кодон метионина (или кодон-инициатор, AUG) устанавливает рамку считывания мРНК; каждый последующий кодон считывается поочередно, указывая аминокислотную последовательность белка.
Молекулярные связи между кодонами и аминокислотами обеспечивают специфические молекулы тРНК. Конкретный участок (сайт) на каждой тРНК формирует антикодон из трех оснований, комплементарный (дополнительный) к специфическому кодону на мРНК. Соединение между кодоном и антикодоном приводит соответствующую аминокислоту на следующую позицию в рибосоме для присоединения с образованием пептидной связи к карбоксильному концу растущей полипептидной цепи. Рибосома затем скользит вдоль мРНК точно на три основания, захватывая следующий кодон для опознавания другой тРНК со следующей аминокислотой.
Таким образом, белки синтезируются, начиная от аминогруппы к карбоксильной группе, что соответствует трансляции мРНК в направлении от 5′-конца к 3′-концу.
Как упоминалось ранее, трансляция заканчивается, когда в той же рамке считывания, что и кодон-инициатор, встречается стоп-кодон (UGA, UAA или UAG). Стоп-кодоны в любой из других неиспользованных рамок считывания не читаются и, следовательно, не оказывают эффекта на трансляцию. Завершенный полипептид отделяется от рибосомы, и она становится доступной для начала синтеза другого белка.
Множество белков проходят существенную посттрансляционную модификацию. Полипептидная цепь, первичный продукт трансляции, скручивается и складывается в специфическую трехмерную структуру, определяемую аминокислотной последовательностью цепи.
Две и более полипептидные цепи, продукты одного или различных генов, могут объединяться, формируя один готовый белковый комплекс. Например, две цепи b-глобина и две цепи а-глобина нековалентно объединяются, формируя тетрамер молекулы гемоглобина. Белковые продукты также могут быть модифицированы химически, например добавлением в специфических местах метильных или фосфатных групп или углеводов.
Такие модификации могут иметь значимое влияние на функцию или количество модифицированного белка. Другие модификации могут включать расщепление белка с потерей специфических аминокислотных последовательностей после того, как они выполнили свою функцию, направив белок в правильную позицию в пределах клетки (например, белки, которые функционируют в пределах ядра или митохондрий) или разделение белковых молекул на меньшие полипептидные цепи.
Например, две цепи, формирующие готовый инсулин, содержащие одна 21, а вторая 30 аминокислот, первоначально представляют собой части проинсулина — первичного продукта трансляции из 82 аминокислот.
Транскрипция митохондриального генома
В предшествующих разделах описаны основы экспрессии генов, содержащихся в ядерном геноме. Митохондриальный геном имеет отличающуюся систему транскрипции и белкового синтеза. Для транскрипции митохондриального генома используется специализированная РНК-полимераза, закодированная в ядерном геноме, содержащая две взаимосвязанные последовательности промотора, для каждой нити кольцевой митохондриальной хромосомы. Каждая нить транскрибируется полностью, а полученные копии затем обрабатываются, порождая различные митохондриальные мРНК, тРНК и рРНК.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021