Питание и диета при раке
Диета при раке — правильная перемена рациона питания, благодаря чему возможно замедление развития онкологического процесса и укрепления организма в целом.
Главными задачами изменения питания больных раком считаются:
В заграничных клиниках пациенту уделяется особое внимание, которое включает среди прочего выбор правильной диеты, которая бы способствовала хорошему самочувствию и повышению сопротивляемости организма. При этом врачи внимательно следят за переменами в здоровье, и, если появляется необходимость, корректируют приемы пищи.
В Турции для лечения онкологических больных используется комплексный подход, поэтому специалисты составляют сбалансированную программу питания при раке. Это помогает поддерживать силы пациента, а также минимизировать побочные проявления радикальной терапии.
Диета для больных раком
Диета и питание при лечение рака невероятно важны. Сбалансированный и рациональный режим питания необходим независимо от того, какая стадия развития болезни у пациента.
Диета при раке способствует улучшению общего самочувствия, сохранению нормального веса тела, регенерации здоровых клеточных структур после применения химиотерапии и лучевого облучения, поддержанию баланса питательных веществ и их правильному обмену, а также препятствует появлению очагов инфекции и воспаления, истощению.
Питание при раке составляется с применением таких полезных продуктов:
Ученые выяснили, что диета и питание при лечении рака, которая содержит коричневые морские (также известна как японская ламинария) и сине-зеленые водоросли, способствует уменьшению размера опухоли.
Хорошее действие оказывают различные свежевыжатые соки и морсы.
Питание больных раком обязательно должно включать еду, в составе которой есть омега-3-жирные кислоты. Лучшим примером служат рыбий жир и морская рыба жирного типа. Также важные кислоты содержатся в льняном масле и семени.
Обязательно нужно поддерживать в кишечном тракте благоприятную микрофлору. Чтобы ее обеспечить, врачи рекомендуют включить в повседневный рацион оптимальное количество спаржи, чеснока, помидоров, лука, проросшей пшеницы. Если нужно вызвать слабительный эффект, то можно использовать чернослив. Черника способствует уменьшению гнилостных процессов и брожению, а также скоплению газов.
При раке врачи также рекомендуют включить в рацион такие продукты:
Материал подготовлен по согласованию с врачами клиники «Анадолу».
Что тормозит рост раковых клеток
После сердечно-сосудистых заболеваний рак является второй по значимости причиной смерти в большинстве стран. По прогнозам, новые случаи рака в 2030 году обойдутся мировому здравоохранению в 458 миллиардов долларов США (Всемирный экономический форум 2011 года).
Более половины всех случаев рака и смерти от онкологических заболеваний во всем мире считаются предотвратимыми. С самого начала приоритетным направлением по борьбе с заболеваниями являлась их профилактика, то есть проведение эффективных медицинских мероприятий, которые могут привести к резкому снижению смертности и инвалидности при относительно скромных затратах. Это междисциплинарный подход, соответствующие рекомендации были основаны на фактических данных, масштабируемыми и адаптируемыми в различных условиях. Мы знаем, что питание является одним из важнейших составляющих здоровья.
Продукты питания и пищевые компоненты, помимо базового питания, обеспечения нашего организма необходимыми пищевыми веществами, могут приносить пользу нашему здоровью, поддерживая его и, тем самым, снижая риск заболеваний.
Есть несколько исследований, показывающих связь между питанием и раком. Например, цистеин из чеснока или ликопин из томатов, при комбинированном употреблении, подавляют развитие химически индуцированного рака желудка. Аналогичным образом, витамин D 3 с генистеином при одновременном употреблении ускоряют ингибирование роста клеток рака предстательной железы. При этом концентрация в комбинации этих веществ более низкая, чем когда они давались парой.
В мире проводится не так много исследований о влиянии пищевых продуктов на здоровье, различные заболевания или связанных с ними состояний.
Мы знаем, что в процессе нормального функционирования организма образуются активные формы кислорода, в том числе супероксид, перекись водорода и гидроксильный радикал. Кроме того, синглетный кислород может образовываться в результате фотохимических реакций (например, в коже и глазах), а перекисное окисление липидов может вызывать образование пероксильных радикалов. Эти окислители приводят к старению нашего организма, а также к развитию дегенеративных заболеваний, таких как
рак и атеросклероз. Не только окисление является причиной рака; скорее всего не менее, а, возможно, и более важным фактором для канцерогенеза является воспаление. Воспаление вызывает рак по нескольким механизмам, включая выработку свободных радикалов воспалительными клетками.
Онкологические заболевания являются одной из основных проблем со здоровьем и причиной 1/8 смертей во всем мире.
Лечение онкологических заболеваний обычно включает в себя дорогостоящее и, нередко, травмирующее использование лекарств, хирургических вмешательств и радиационной терапии.
Питание и пищевые продукты связывают примерно с 30% всех случаев рака. Существуют многочисленные исследования, показывающие связь между питанием и снижением риска развития онкологических заболеваний.
Во всем мире люди используют питание, лекарственные травы и их экстракты или компоненты для предотвращения или лечения рака. Известно, что ряд пищевых продуктов имеют дополнительную пользу для нашего здоровья. Пища снабжает организм необходимым количеством витаминов, жиров, белков, углеводов и других питательных веществ, нужных нам для нормальной жизнедеятельности. Ряд соединений, естественным образом встречающихся в пищевых продуктах, в частности, антиоксиданты, показали себя как потенциальные профилактические вещества. Вероятно, антиоксиданты способны уменьшить повреждение свободными радикалами ДНК, что считается основной причиной большинства раковых заболеваний. Предполагается, что антиоксиданты могут снижать мутагенез и, следовательно, канцерогенез, как за счет уменьшения окислительного повреждения ДНК, так и за счет уменьшения клеточно-стимулированного деления клеток.
Фитохимические вещества делятся на различные группы, такие как каротиноиды, каротиноидные пигменты, ксантин, ликопин, астаксантин и другие фитохимические вещества.
Астаксантин является альфа-гидроксил-кетокаротиноидом. Он принадлежит к группе насыщенных кислородом каротиноидов или ксантофиллов, таких как лютеин и зеаксантин. Астаксантин уникален в том смысле, что он не только удаляет свободные радикалы, но и защищает от окисления и ограничивает выработку свободных радикалов. Астаксантин также повышает функцию других антиоксидантов, таких как витамины Е и С.
Астаксантин защищает наш организм от воздействия ультрафиолетового излучения. Также астаксантин может преодолевать гематоэнцефалический барьер и, таким образом, защищать ЦНС от свободных радикалов. Существуют исследования, подтверждающие противовоспалительную активность астаксантина и противораковую эффективность астаксантина, хотя механизм такого действия пока неизвестен. Астаксантин ингибируют развитие раковых клеток в печени, молочной железе, желудке.
Известно, что УФ-излучение является основным возбудителем в патогенезе опухолей кожи. Астаксантин и экстракты водорослей, обогащенные астаксантином, обеспечивают значительную защиту от УФ- излучения.
Лютеин и зеаксантин относятся к семейству ксантофиллов. Особенно высокая концентрация лютеина в зеленых листовых овощах, многих фруктах и цветных растениях, таких как сладкий перец, сладкая кукуруза, горох и яичный желток, киви, виноград, шпинат, апельсиновый сок, кабачки и различные виды тыквы. Кукуруза содержит наиболее количество лютеина (60%). Лютеин особенно активно проявляет свои антиоксидантные свойства в хрусталике глаза. Существуют исследования, подтверждающие, что лютеин более эффективен в подавлении перекисного окисления липидов, и сам лучше защищен от вторичного окислительного распада в присутствии мелатонина, глутатиона, альфа-токоферола и аскорбата.
Лютеин значительно уменьшает риск ишемической болезни сердца (ИБС) и риск инсульта. Потребление лютеина и зеаксантина обеспечивает защиту от отеков и гиперплазии кожи, вызванной воздействием УФ-излучения. Лютеин и зеаксантин снижают риск рака молочной железы, особенно в период пременопаузы. Есть исследования, указывающие на защитное воздействие лютеина от рака толстой кишки и от рака легких (но не у пожилых людей).
β-криптоксантин является углеводородным каротиноидом. β-криптоксантин
Кантаксантин является углеводородным каротиноидом. Кантаксантин впервые был выделен из съедобного гриба Cantharellus cinnabarinus. Кроме того, он обнаружен в нескольких зеленых и сине-зеленых водорослях. Он в ракообразных и различных видах рыб, включая карпа, кефаль. Кантаксантин обычно не считается диетическим каротиноидом, но он может быть включен в рацион человека благодаря его широкому применению в качестве красителя в пищевом производстве. Кантаксантин может предотвращать неконтролируемую пролиферацию клеток толстой кишки, молочной железы и кожи. Кантаксантин также доказал свою эффективность в предотвращении канцерогенеза в полости рта.
Противоопухолевые препараты ингибиторов роста рака

Достать лекарства от рака с гарантией оригинального происхождения препарата просто, если вы обратились в компанию Tlv.Hospital.
Мы предлагаем сертифицированные фармацевтические группы для традиционных методов коррекции онкологии и реализации авторских программ.
Факторы роста опухоли
Факторы роста – это химические вещества, производимые организмом для контроля роста клеток. Существует много различных типов факторов роста, и все они работают по-разному. Некоторые из них передают информацию, каким видом клетки должна стать данная, конкретная клетка. Другие побуждают клетки расти и делиться; есть те, которые передают информацию, когда клетка должна перестать расти или умереть.
Факторы роста работают, подключаясь к рецепторам на поверхности клеток. Они посылают сигнал внутрь клетки, запуская целую сеть сложных химических реакций.
Существует целый ряд различных факторов роста:
Каждый фактор роста присоединяется к соответствующим рецепторам на поверхности клетки, чтобы оказывать воздействие на нее.
Ингибиторы факторов роста блокируют факторы, которые дают сигнал раковым клеткам делиться и расти. Ученые разрабатывают различные способы, чтобы осуществить это:
Большинство этих методов работают, блокируя процессы передачи сигнала, которые используют злокачественные клетки, чтобы начать деление.
Раковые клетки обладают повышенной чувствительностью к факторам роста опухоли. Поэтому если есть возможность заблокировать их, можно остановить рост некоторых видов онкологии. Ученые разрабатывают различные ингибиторы для разных типов факторов роста.
Есть сложности с классификацией различных типов биологической терапии, поскольку они часто пересекаются. Некоторые ингибиторы факторов роста блокируют рост кровеносных сосудов в растущей опухоли. Такое же действие оказывают моноклональные антитела.
Существуют различные типы ингибиторов, их можно сгруппировать в соответствии с химическими веществами, которые они блокируют.
Виды ингибиторов роста рака
Ингибиторы тирозинкиназы также называют ИТК. Они блокируют ферменты под названием тирозинкиназы. Эти ферменты помогают передавать сигналы роста к клеткам. Таким образом, предотвращают рост и деление клетки. Может быть блокирован один тип тирозинкиназы или несколько. ИТК, оказывающие воздействие на несколько видов ферментов, называют мультиингибиторами.
ИТК, которые применяют в лечебной практике, а также в рамках клинических испытаний:
Данные препараты принимают в таблетках или в капсулах, обычно один или два раза в день.
Протеасомы – крошечные структуры всех клеток, по форме напоминающие бочку. Они помогают расщеплять белки, которые не нужны клетке, на более мелкие части. Эти белки потом используются для создания новых, необходимых белков. Работу протеасом блокируют ингибиторы протеасом. Это вызывает накопление нежелательных белков в клетке, приводя к ее смерти.
Бортезомиб (Velcade) – ингибитор протеасом, который применяют в лечении меланомы. В организм его вводят внутривенно.
MTOR – тип белка под названием протеинкиназа. Он воздействует на клетки, чтобы они синтезировали химические вещества под названием циклины, которые способствуют развитию клеток. Кроме того, они содействуют синтезу белков клетками, провоцирующих развитие новых кровеносных сосудов, которые необходимы опухолям.
Некоторые типы белка mTOR одновременно способствуют росту злокачественных клеток и созданию новых сосудов. Ингибиторы таких белков являются инновационными препаратами, блокирующими рост опухолевого процесса. К ингибиторам данного белка относят:
PI3K (фосфатидилинозитол-3-киназы) – группа близкородственных белков киназ. Они выполняют несколько действий в клетках. Например, активируют другие белки – к примеру, mTOR. Активация PI3K приводит к росту и делению клеток, развитию кровеносных сосудов, помогает клеткам передвигаться.
При некоторых видах рака PI3K постоянно активированы, что означает бесконтрольный рост раковых клеток. Исследователи разрабатывают новые методы лечения, которые блокируют PI3K, что останавливает рост злокачественных клеток и приводит к их гибели. Этот тип ингибитора пока доступен только в рамках клинических испытаний. Необходимо некоторое время, прежде чем убедиться, что препарат эффективен в лечении рака.
Ингибиторы гистондеацетилазы также называют ингибиторами HDAC или HDIS, ингибиторами селективного действия. Они блокируют действие группы ферментов, которые удаляют вещества из ацетильной группы конкретных белков. Это останавливает рост и деление злокачественных клеток, а иногда и полностью их уничтожает.
Ингибиторы гистондеацетилазы – новый тип ингибиторов факторов роста. Препараты, которые используются в лечении рака и в рамках клинических испытаний:
Данные блокаторы нацелены на группу белков под названием Hedgehog pathway. У развивающегося эмбриона эти белки посылают сигналы, которые помогают клеткам расти в правильном направлении и в правильном месте. Данный белок также контролирует рост кровеносных сосудов и нервов. У взрослых Hedgehog pathway обычно не активен. Но у некоторых людей изменения в генах включают его. В настоящее время разработаны блокаторы Hedgehog pathway, которые выключают белок и останавливают рост рака.
Этот вид биологической терапии достаточно новый. Vismodegib (Erivedge) – пример такого ингибитора, участвующего в клинических испытаниях.
Ингибиторы ангиогенеза
Опухоль нуждается в хорошем кровоснабжении, чтобы поступали питательные вещества, кислород и удалялись отходы. Когда она достигает в ширину 1-2 мм, ей необходимо вырастить новые кровеносные сосуды, чтобы увеличить объем необходимых поступающих веществ. Некоторые раковые клетки создают белок под названием фактор роста эндотелия сосудов (VEGF). Этот белок прикрепляется к рецепторам на клетках, выстилающих стенки кровеносных сосудов внутри опухоли. Эти клетки называются эндотелиальными. Они дают импульс к росту кровеносных сосудов, чтобы опухоль могла расти.
Ангиогенез означает рост новых кровеносных сосудов. Если удается остановить создание новых сосудов, снижается рост опухолевого процесса, а иногда и уменьшается. Ингибиторы ангиогенеза как раз направлены на остановку создания новых кровеносных сосудов у опухоли.
Существуют разные препараты, блокирующие рост кровеносных сосудов:
Возможные побочные эффекты ингибиторов факторов роста
Все препараты способны вызывать побочные эффекты, у всех – разные. Но есть несколько общих потенциальных нежелательных последствий:
Убийцы рака. Часть 2
Убийцы рака – продукты, систематическое употребление которых снижает риск возникновения раковых опухолей, что доказано современными исследованиями. Продолжим серию статей рассказом о зеленом чае, малине и немного поговорим о ликопине.
Зеленый чай
L-теанин— это водорастворимая аминокислота, содержащаяся в зеленом чае и в грибах. Очищенная аминокислота используется как пищевая биодобавка. Она употребляется для оказания антиоксидантного и релаксирующего (успокаивающего) действия. Несколько исследований на животных и в лабораторных условиях показали, что L-теанин обладает противоопухолевыми свойствами. В одном исследовании обнаружено, что L-теанин блокирует рост опухоли легочной ткани. Также эта аминокислота отчетливо снижает токсичность воздействия препаратов химиотерапии. За это по праву, подтвержденному научными исследованиями, зеленый чай попадает в наш список «Убийцы рака».
Малина
Исследования на животных моделях показали его способность потенцировать противоопухолевый эффект химиопрепаратов в раковых клетках печени, защищая нормальные клетки печени.
Результаты систематического обзора свидетельствуют о том, что кверцетин, полученный при обычном питании не может снизить риск рака яичников. Также не достаточно данных для определения противоопухолевой активности кверцетина у женщин с раком молочной железы.
Ликопин
Натуральный пигмент, синтезируемый растениями и микроорганизмами, ликопин применяют в первую очередь как антиоксидант, а также для профилактики и лечения рака, болезней сердца и дегенерации желтого пятна (макулы). Находится в помидорах, всех томатных продуктах, арбузе, гуаве, плодах шиповника и розового грейпфрута.
Небольшие клинические исследования показывают возможную пользу при астме, доброкачественной гиперплазии предстательной железы (ДГПЖ) и рака, но оптимальная дозировка не была установлена.
Эпидемиологические исследования показывают обратную зависимость между потреблением ликопина и риском развития рака легких, желудка, предстательной железы, рака молочной железы. А вот связь между потреблением ликопина и риском рака эндометрия не выявлена.
Недавние исследования не нашли никакой связи между уровнем сывороточного ликопина и риском развития рака предстательной железы.
Соревнуясь с раком
Соревнуясь с раком
Победить не берусь, перехитрить попробую (М.И. Кутузов).
Авторы
Редактор
Статья на конкурс «био/мол/текст»: На поиски новых способов борьбы с раком и усовершенствование существующих человечество уже потратило миллиарды долларов, а проблема всё так и остается нерешенной. Бесконечные войны с раком зачастую оканчиваются нашим поражением. Можно ли придумать волшебную пилюлю от рака и с гордостью заявить: «Всё, теперь-то мы победили»? К сожалению, ответ на этот вопрос для нас весьма неутешительный. Несмотря на то, что ученые по всему миру придумывают всё новые способы борьбы с онкологическими заболеваниями, рак тоже способен учиться: онкологическая терапия постоянно сталкивается с возникновением мультилекарственной резистентности.
Конкурс «био/мол/текст»-2018
Эта работа опубликована в номинации «Биофармацевтика» конкурса «био/мол/текст»-2018.
Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Спонсором приза зрительских симпатий выступил медико-генетический центр Genotek.
Раковое ралли
Рак — это собирательное название группы смертельных и крайне разнородных заболеваний [1]. Однако все раковые клетки обладают набором характерных биологических признаков [2], позволяющих нам применять общие стратегии противораковой терапии.
Одним из таких признаков является хроническая пролиферация (бесконтрольное деление) клеток. Нормальные клетки нуждаются в ростовых факторах, продуцируемых товарищами [3], в то время как раковые могут обеспечивать себя сигналом «роста» самостоятельно. Представим, что опухоль в организме — это автомобиль, несущийся по трассе. В таком случае у автомобиля постоянно работает педаль газа (рис. 1).
Рисунок 1. Ракомобиль. В сравнении со здоровыми клетками организма, раковые — гоночный автомобиль: мощный, скоростной и небезопасный.
С другой стороны, в регуляцию клеточного роста включаются ингибиторные сигналы. Раковые клетки научились такие сигналы игнорировать. То есть наш «ракомобиль» оказывается еще и со сломанными тормозами.
Согласитесь, такое авто на дороге просто опасно для окружающих. Обычно водитель может понять, что скорость превышена, взглянув на спидометр. У клетки роль спидометра выполняет белок р53 — ключевой сенсор повреждения ДНК, запускающий гибель раковой клетки апоптозом (одним из видов программируемой клеточной смерти). Однако многие виды рака сопряжены с потерей функции р53, в результате чего механизмы самоликвидации не запускаются.
Пробег «раковой машины» определяют теломеры (концевые участки хромосом), сокращающиеся с каждым клеточным делением. Около 90% раковых опухолей обладают белком, способным увеличивать длину теломер [4], [5]. Таким образом, «ракомобиль» всегда кажется новенькой моделью, хотя на самом деле этой старой кляче просто скрутили показания одометра.
Несущийся по шоссе автомобиль поглощает литры горючего. Так и раковым клеткам необходимы питательные вещества и кислород, поэтому опухоли стимулируют прорастание кровеносных сосудов вокруг себя — ангиогенез, что облегчает доставку «топлива» к опухолям [6].
Многие опухоли обладают инвазивностью и способностью метастазировать [7–9]. И хотя первый процесс происходит в тканях, где опухоль появилась, а второй заключается в построении колоний в других тканях, генетически и биохимически оба процесса очень похожи. Скажем, что наша машина вдруг превращается в летающую.
Клетки иммунной системы, как инспекторы на дороге, сражаются со свихнувшимися раковыми клетками — нарушителями ПДД — и восстанавливают нормальные функции организма. Однако с иммунной системой не всё так просто. Как коррумпированные полицейские, входящие в состав преступного синдиката, иммунная система иногда способствует росту опухоли [10].
Терапия и резистентность. Кто кого?
Очевидно, что физиологически здоровая клетка должна претерпеть множество изменений, прежде чем превратиться в раковую. С одной стороны, все эти характерные изменения делают нормальную клетку очень опасной раковой, а с другой — служат основными мишенями лекарственной терапии. Противоопухолевая терапия сродни стрельбе из лука: чем выше дальность (селективность и биодоступность) и точность (наименьшее количество побочных эффектов), тем больше очков мы выигрываем в борьбе с опухолью. Не зря одним из самых популярных терминов в области является «таргетная терапия» (от англ. target — «цель», «мишень»). Именно отсюда возникает такое разнообразие групп препаратов [11]. Основные мишени противоопухолевой терапии — ДНК (как основной регулятор всех внутриклеточных процессов) и белки, выполняющие специфические функции.
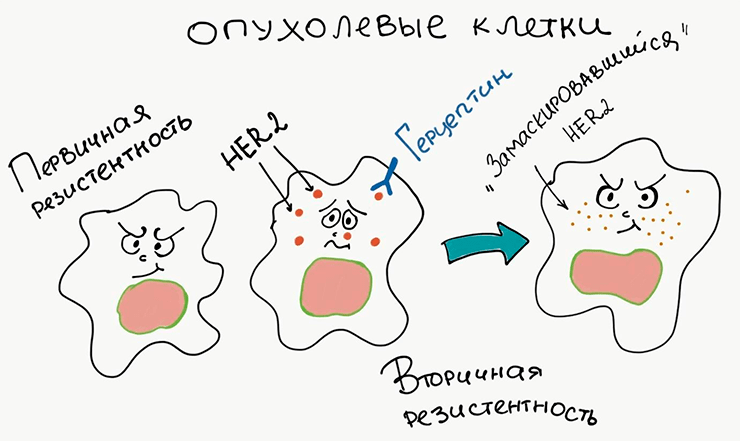
Многие из противоопухолевых препаратов весьма эффективны, однако к ним возникает устойчивость, в результате чего лечение ставится под угрозу. Резистентность может быть первичной (особенность конкретной опухоли) или вторичной (приобретенной, возникающей в ответ на прием препаратов). Попробуем разобраться на примере препарата «Герцептин».
«Герцептин» — высокоэффективный препарат, применяемый при раке груди [12], и механизм его действия связан с блокировкой рецептора HER2, помогающего опухолевым клеткам активно пролиферировать (выжимать педаль газа). Однако в случае, если у опухолевых клеток нет рецептора HER2, его блокировка «Герцептином», очевидно, совершенно бесполезна. Это значит, что опухоль обладает первичной резистентностью к этому препарату. Другое дело, когда в опухолевых клетках мутируют внутриклеточные каскады, связанные с рецептором HER2, и мишень теряется [13]. Так развивается вторичная резистентность (рис. 2).
Рисунок 2. Возникновение резистентности. Первичная резистентность к лекарству характерна для клеток, у которых изначально нет его мишени. Вторичная резистентность возникает в результате изменения мишени, при котором препарат теряет способность с ней связываться.
Самый очевидный способ обмануть опухоль и побороть резистентность — использовать как можно больше лекарственных препаратов, отличающихся по структуре и механизму действия. Однако, как ни парадоксально, опухоли способны спонтанно развивать резистентность к различным противоопухолевым агентам одновременно. Это и называется мультилекарственной резистентностью.
Интересно, что из всей пестрой популяции раковых клеток, совсем как в эволюционной теории Дарвина, выживают наиболее приспособленные. Часть клеток, вероятно, гибнет под действием лекарства, тогда как другая часть выживает и оказывается еще более неуловимой для терапии. Поэтому у онкологов есть препараты I, II и прочих линий. Как только одно лекарство перестает работать, нужно быстро назначить пациенту другое, а когда опухоль приспособится и к нему, дать третье, и так далее. К сожалению, список лекарств не бесконечен, именно поэтому вопрос изучения механизмов мультилекарственной резистентности очень важен.
Механизмы развития резистентности
Каким образом раковые клетки способны приобретать устойчивость? Как ученые могут эту устойчивость обойти? Борьбу с резистентностью можно сравнить с партией в шахматы. На каждый наш ход — новое противораковое лекарство — клетки опухоли придумывают маневр для ухода. Рассмотрим несколько таких ответных ходов: поговорим о мембранных переносчиках, особенностях метаболизма, мутации терапевтической мишени, клеточной гибели и о том, как раковые клетки придумали скрываться от «иммунных полицейских».
Ход 1. Шах от мембранных переносчиков
Как проникнуть внутрь клетки?
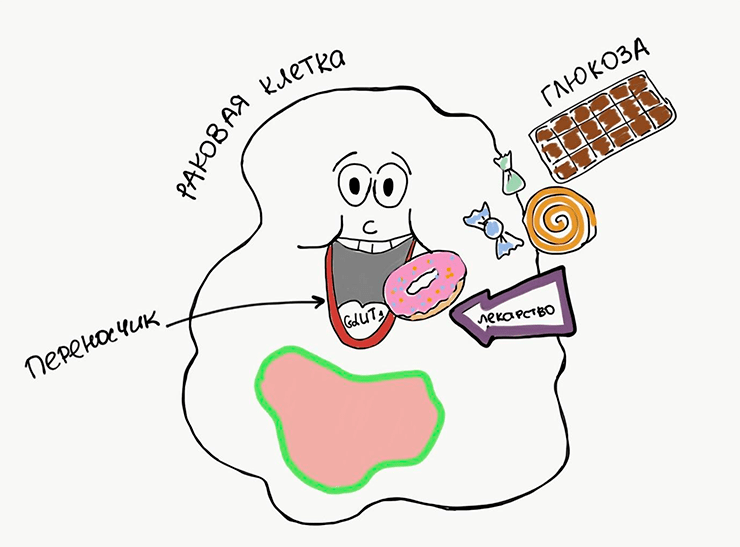
Все клетки нашего организма окружены мембраной — двойным слоем липидов, основная задача которого — поддерживать целостность и постоянство внутриклеточного содержимого [14]. Большинство молекул, необходимых для жизнедеятельности клетки, водорастворимы, а значит, через липидную мембрану они не проходят. Именно поэтому клеточная мембрана содержит сотни различных белков-переносчиков [15]. Вернемся к нашему примеру с «раковым автомобилем», нуждающимся в топливе: для закачки бензина необходим бензобак, им-то как раз и служат мембранные переносчики. Увеличение количества мембранных переносчиков, таких как селективный переносчик глюкозы GLUT1, отмечают в различных типах опухолей (рис. 3).
Глюкоза — лучшее «топливо» для клеток, а ее переносчик довольно хорошо изучен. Казалось бы, почему нельзя просто взять и заблокировать этот переносчик, ведь ни одна машина без бензина не поедет? Дело в том, что абсолютно идентичные переносчики работают и на мембранах здоровых клеток, которые нам еще пригодятся. Поэтому в терапии преобладает другой подход — ученые постоянно ищут способы, как можно использовать некоторые переносчики в своих целях. Например, доставить лекарство в клетку вместе с естественными для организма молекулами. Почему так сложно? Дело в том, что не всякое лекарство сможет проникнуть через липидную мембрану. Если это заряженная или водорастворимая молекула, то попасть в клетку она сможет только с помощью переносчика. К примеру, белок OCT1, находящийся в клеточной мембране лейкоцитов, переносит через нее противоопухолевый препарат иматиниб [16]. Этот переносчик не только повышает эффективность терапии хронического миелоидного лейкоза, но и позволяет врачам подбирать оптимальную эффективную дозу для пациентов [17].
Рисунок 3. Мембранные переносчики нужны для транспорта питательных веществ в клетку. Например, глюкоза поступает через переносчик GLUT1. Вместе с питательными веществами переносчики иногда могут транспортировать и молекулы лекарств.
Краеугольный камень мультилекарственной резистентности — это совсем другая группа мембранных транспортеров. В отличие от предыдущих переносчиков, они, наоборот, выкачивают из клетки всё ей ненужное. В первую очередь, конечно же, противоопухолевые препараты, которые мы с таким трудом в клетку доставили. Это семейство переносчиков со скромным названием «ABC» [18] в разы усложняет работу ученых и несет ответственность за возникновение резистентности к большей части лекарственных препаратов [19]. Главой семейства ABC-переносчиков можно назвать белок P-gp (P—гликопротеин, он же — MDR1, белок множественной лекарственной устойчивости 1) [20]. Каждый день он буквально спасает нас от смерти, выкачивая из клеток организма попавшие туда чужеродные и токсичные вещества.
Однако P-гликопротеин — двуликий Янус! Противоопухолевые препараты, которые назначают пациенту, он принимает за вражеских агентов и спешит поскорее избавить от них раковую клетку (рис. 4). Важно отметить, что все представители семейства ABC-транспортеров — переносчики неспецифические, которые переносят многие (главным образом, гидрофобные) молекулы, не различая их. Поэтому, увеличивая количество хотя бы одного белка-переносчика в мембране, раковая клетка автоматически приобретает навык выкачивать разные лекарства. Таким образом, рак сразу вычеркивает из нашего списка лекарств значительную их часть.
Рисунок 4. ABC-переносчики удаляют продукты жизнедеятельности и токсины из клетки. Такие переносчики (например, P-gp) неселективны, то есть удаляют из клетки всё подряд, в том числе лекарства.
Ход 2. Метаболический
Основная сложность противоопухолевой терапии состоит в том, что раковые клетки, пусть и немного свихнувшиеся, но всё же родственники здоровых клеток организма. А те в процессе эволюции разработали десятки защитных механизмов, спасающих их от чужеродных токсинов. Что в общем-то хорошо, ведь мы не хотим, чтобы лекарство блуждало по нашему организму целую вечность. Некоторые препараты обладают довольно высокой токсичностью, и их необходимо удалить как можно быстрее — ну, только после достижения эффекта. Однако раковые клетки научились менять метаболизм лекарства, что тоже приводит к резистентности.
Вместе с P-гликопротеином в команду резистентности попадает еще один белок — цитохром P450 (сокращенно его называют ЦИП. Не путать с цыплятами!). Этот белок — будем называть его для простоты P450 — является основным ферментом метаболизма лекарств. Если задуматься, это удивительно: как один белок может влиять на эффективность практически всех лекарств?
Попадая в организм, противоопухолевые препараты претерпевают изменения. Как мы помним, организм стремится поскорее избавиться от всего чужеродного, поэтому он меняет структуру противоопухолевого препарата так, чтобы тот не мог задерживаться в тканях и скорее выводился. Этой нелегкой работой как раз и занимается P450 (рис. 5a). И опять: как и все белки-защитники, P450 работает со всеми веществами подряд. Интересно, что цитохромы могут реагировать на сигнал от некоторых лекарств, активирующих или угнетающих их работу.
Рисунок 5а. Цитохром Р450 участвует в метаболизме лекарств: модифицирует их так, чтобы они легко выводились из организма.
Рисунок 5б. Р450 превращает пролекарства в активные лекарства.
Пытаясь использовать деятельность P450 на благо человечества, ученые разработали пролекарства — молекулы, которые P450 не лишает, а наделяет лекарственной активностью (рис. 5б). То есть в таблетке находится «спящая» молекула, а после «обработки» цитохромом она начинает работать: становится токсичной для опухоли. Однако в случае потери или снижения активности P450 такие противоопухолевые препараты остаются неактивными. Поэтому принимающим их пациентам советуют не пить грейпфрутовый сок — известный ингибитор P450 [21].
Казалось бы, вот они — пути борьбы с мультилекарственной резистентностью. Но стόит признаться, что тут рак поставил человечеству шах, от которого оно не может ускользнуть. Мы уже упоминали, что такие белки-защитники, как Р450 или P-gp, работают неселективно: помимо выкачивания противоопухолевых препаратов, Р-gp защищает наш мозг от попадания токсичных веществ, а цитохром Р450 окисляет эндогенные гормоны и метаболиты. Вмешиваясь в деятельность Р450 или P-gp, мы рискуем лишить организм естественной защиты и регуляции, что приводит к появлению токсинов.
Ход 3. Рокировка мишени
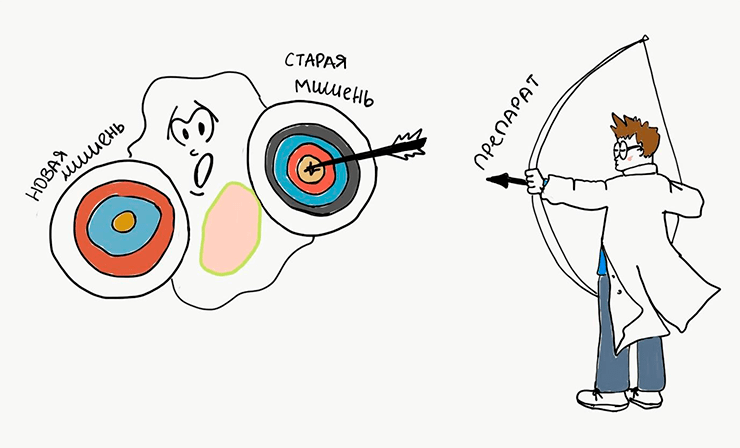
Помимо того, что наш организм и так усиленно пытается всеми возможными путями избавиться от противоопухолевых препаратов (ход 2), опухолевые клетки всегда начеку и в случае эффективности препарата стараются избавиться от его мишени (рис. 6). Как такое возможно? В условиях бесконтрольности раковые клетки накапливают мутации (изменения в ДНК), служащие резервным механизмом выживания клеток. Хитрость хода раковых клеток впечатляет: вместо того, чтобы пытаться всеми правдами и неправдами избавиться от лекарства, они в одну секунду делают препарат неактивным, избавляясь от его мишени. В случае с тем же «Герцептином», например, клетки просто теряют рецептор HER2, на который направлено действие препарата.
Рисунок 6. Как только опухолевая клетка изменит мишень лекарства, препарат сразу перестанет действовать. Тогда ученым нужно будет придумывать лекарство, бьющее по новой мишени.
Ход 4. Клеточный гамбит
Апоптоз (вид программируемой клеточной гибели) — это не только естественный механизм устранения опухолевых клеток, но и желаемый результат использования противоопухолевых препаратов. Апоптоз постоянно запускается в клетках, в которых что-то пошло не так — например, повреждена ДНК или не работают необходимые белки (рис. 7). Он проходит тихо, и клетка, умирая, оставляет после себя только безвредные ошмётки, легко удаляемые соседями. Должно быть, читателю уже стало понятно, что апоптоз — один из ключевых пунктов, против которого будет бороться раковая клетка. Здоровые физиологически клетки имеют много механизмов, запускающих апоптоз, и белков — регуляторов апоптоза, что позволяет клетке-герою надежно отличить опасную для всего организма ситуацию и пожертвовать собой, тихонечко скончавшись. Это умение, конечно, достается по наследству и раковым клеткам, однако они быстро учатся справляться с апоптозом.
Рисунок 7. Один из механизмов программируемой клеточной гибели — апоптоз — работает в многоклеточном организме постоянно. Отслужившие клетки тихонечко самоликвидируются, оставляя после себя лишь безвредные крохотные тельца.
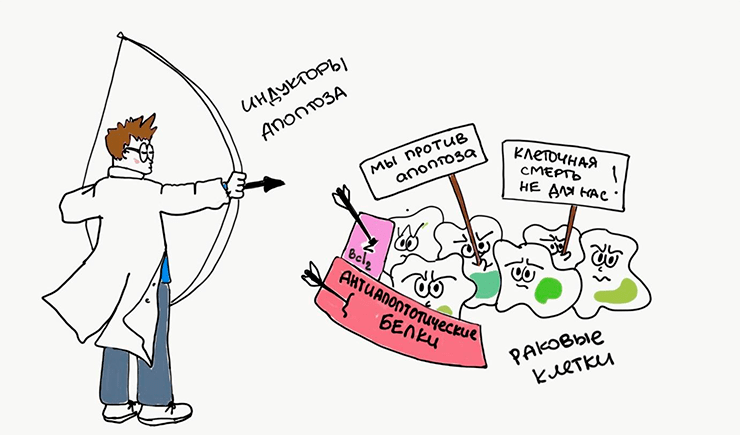
Апоптоз может инициироваться целым рядом противоопухолевых препаратов, повреждающих ДНК. Однако опухолевые клетки научились противостоять нашим атакам. Дефекты апоптотических каскадов дают им преимущество выживать даже тогда, когда в нормальных условиях клетки бы уже давно почили (рис. 8). Несмотря на то, что в этом противостоянии опухолевые клетки пока что одерживают победу, ученые не опускают руки. Разветвленность апоптотических путей позволяет нам разрабатывать всё новые препараты, облегчающие ход уже запущенного апоптоза [22]. Так действует, например, новая группа лекарственных средств — миметики проапототических белков [23].
Рисунок 8. Раковые клетки стремятся избежать апоптоза. Они усиливают работу антиапоптотических белков, а ученые, наоборот, пытаются апоптоз индуцировать.
Ход 5. Микропешки
Клетки никогда не находятся в одиночестве, они образуют «коммуну» — объединяются в ткани и активно взаимодействуют с клетками других тканей. Кроме того, клетки должны прочно закрепиться на одном месте, а не болтаться по организму. А вот раковые клетки иногда, как мы уже упоминали, игнорируют это правило и образуют метастазы, когда «теряют сцепление» с окружающей их средой. Также для опухоли очень важно иметь вокруг себя кровеносные сосуды, через которые она получает питательные вещества. Если опухоль большого размера, она может сдавливать кровеносные сосуды. Но не нужно радоваться слишком рано: такое сдавление усложняет доставку и противоопухолевых препаратов к центру опухоли. Ее периферические клетки лекарство победит, а вот находящиеся в самом сердце опухоли выживут, мутируют, и всё начнется сначала.
Помимо того, что одна популяция раковых клеток может стать резистентной к лекарству, она может обучить другую популяцию, спасая таким образом чувствительные к лекарству опухолевые клетки от смерти и сводя на нет все усилия врача. Информация о том, как сопротивляться лекарству, зашифрована в виде микро-нуклеиновых кислот. Обычно это регуляторные микроРНК, упакованные в очень маленькие пузырьки — микровезикулы (рис. 9). Всё это «мимимикро» — очень коварный ход со стороны рака. МикроРНК регулируют экспрессию генов устойчивости. А микровезикулы защищают «ценную» информацию от разрушителей РНК (РНКаз) [24]. Микровезикулы могут передаваться от одних клеток к другим, высвобождать микроРНК. Бороться с таким транспортом ученые пока не научились.
Рисунок 9. Микровезикулы переносят от одной раковой клетки к другой микроРНК, регулирующие экспрессию генов устойчивости. Таким образом гетерогенная группа клеток становится устойчивой к терапии.
Ход 6. Иммунный ферзь
Иммунная система — хранитель благополучия организма. И раковые клетки, разумеется, всеми возможными путями пытаются скрыться от грозных стражей, снующих по организму. «Раковая машина» скрывает свои настоящие водительские права — антигены (молекулы, способные вызвать иммунный ответ), которые позволяют «инспекторам» различать свои и чужеродные клетки.
Иммунная система в научной среде сейчас по-настоящему в тренде. И конечно, фармацевтические компании не могут обойти эту тему стороной. В онкотерапии истинный бум вызвали две новые группы препаратов — моноклональные антитела и перепрограммированные модифицированные Т-клетки (CAR T-клетки) [25]. Про модифицированные Т-клетки «Биомолекула» уже не раз писала [26], [27], как и про идею моноклональных антител [28], [29]. Мы же в очередной раз хотим обратить внимание на конкретную группу лекарств — чек-поинт ингибиторы [30], [31], за которые Джеймс Эллисон (James Allison) и Тасуку Хоньо (Tasuku Honjo) получили Нобелевскую премию по физиологии или медицине 1 октября этого года. [32] Подробнее об этом событии читайте в нашем специальном выпуске! [33]
Началось всё с открытия белка PD-L1 на поверхности раковой клетки, что, на самом деле, никого не впечатлило. Открыли какой-то там белок — молодцы! Ну и что? А вот когда обнаружили его рецептор PD-1 на поверхности Т-клеток, началось самое интересное. Расшифровываются эти аббревиатуры как programmed death ligand 1 и programmed cell death protein 1. То есть удалось обнаружить настоящих вестников смерти раковых клеток! PD-L1 есть и у здоровых клеток иммунной системы. В норме при взаимодействии этих молекул — рецептора и лиганда — посылается ингибиторный сигнал Т-клеткам, которые должны распознавать чужеродные фрагменты и уничтожать их. Получая ингибиторный сигнал, Т-клетки понимают, что эту конкретную клетку убивать не нужно. Эта проверка (чек-поинт) позволяет сохранять нормальные, здоровые клетки. Как уже, вероятно, догадался читатель, хитрые раковые клетки научились экспрессировать на своей поверхности PD-L1, вводя в заблуждение иммунных полицейских. Ингибиторы такого взаимодействия — новое слово в борьбе против рака (рис. 10).
Рисунок 10. Раковые клетки научились обманывать иммунный надзор: они показывают PD-L1, который обычно есть у нормальных иммунных клеток. PD-L1 (мячик) связывается с рецептором PD-1 на Т-клетках (щенок на страже), в этом случае иммунные клетки принимают раковые «за своих» и не атакуют. Препараты — ингибиторы PD1-PDL1-взаимодействия (косточка) позволяют иммунным клеткам обойти обманный маневр врагов.
Шах и мат?
Борьба с возникновением мультилекарственной резистентности сродни игре в шахматы. Каждый раз ученые придумывают новые способы терапии, к которым рано или поздно раковые клетки вырабатывают резистентность. Возможно, эта партия будет длиться до бесконечности, пока мы не узнаем чего-то принципиально нового о механизмах развития онкологических заболеваний [34]. Современная онкотерапия постоянно дополняется рекомендациями, часто авторитет и интуиция врача играют большую роль. К сожалению, у онкологов не всегда есть время для раздумий над следующим ходом. Но не унывай, читатель! Каждый раз, когда ученые открывают очередную маленькую молекулу на поверхности раковой клетки или придумывают, как обойти тот или иной механизм возникновения лекарственной резистентности, человечество делает еще один шаг к победе над раком.