Медвежья желчь: лечебные свойства и противопоказания, отзывы
Медвежья желчь – это секрет, вырабатываемый печенью медведя и скапливающийся в желчном пузыре. Сотни лет целебная жидкость используется в народной и китайской медицине для избавления от заболеваний печени, ЖКТ, желчевыводящих путей. Анализируя лечебные свойства и противопоказания медвежьей желчи, отмечают своеобразие этого вещества, выливающееся в необходимость при использовании соблюдать точно врачебные рекомендации.
Химический состав
Целебный препарат получают для промышленных целей из желчного пузыря специально выращиваемых медведей — бурых или гималайских. Разводят животных в Корее (Южной и Северной), Китае, а также во Вьетнаме, Лаосе, Бирме.
Преимущественно состав медвежьей желчи представлен урсодезоксихолевой кислотой, известной как УДХК. Присутствуют в небольших количествах:
Чем полезна медвежья желчь
Присутствие в химической формуле базового действующего вещества (УДХК) определяет лечебные свойства медвежьей желчи:
Полезные свойства медвежьей желчи проявляются в выведении токсичных соединений, снижении уровня холестерина, укреплении иммунитета, предупреждении развития атеросклероза и злокачественных новообразований.
Известна польза медвежьей желчи в защите клеток и тканей печени от негативного воздействия лекарственных средств и алкоголя.
Анализируя, от чего помогает медвежья желчь, отмечают несколько направлений:
От каких болезней помогает
Применение медвежьей желчи в лечебных целях обусловлено многообразие известных полезных качеств этого препарата.
От каких болезней медвежья желчь сможет помочь:
Лечебное средство используют только после получения рекомендаций врача, учитывая основные показания медвежьей желчи.
Издавна используется медвежья желчь при онкологии, так как считается, что это средство способствует замедлению развития опухолей, снижает степень побочных проявлений химиотерапии. Если врач разрешает, то принимают препарат до химиотерапии, чтобы легче переносить процедуру.
Считается полезной медвежья желчь для печени, поскольку нейтрализует негативное воздействие токсинов, снимает воспалительные проявления. Применяют средство при не осложненной печеночной недостаточности, гепатитах, холангите, циррозе, алкогольном стеатозе. Помогает лекарство при травматических повреждениях печени.
Полезна медвежья желчь при диабете, так как при правильном приеме удается стабилизировать уровень сахара.
Приносит пользу медвежья желчь для суставов. Позволяет ускорить лечение гематом, различных травматических поражений, способствует сращиванию переломов, снимает боль. Помогает устранить отложение солей, подагру, облегчает состояние при радикулите, ревматизме, артрите.
Лечебное средство находит применение для мужчин, предупреждая развитие эректильной дисфункции, аденомы предстательной железы, нарушения кровообращения, простатита.
Противопоказания и вред
Обязательно учитывают при выполнении любых целебных мероприятий противопоказания медвежьей желчи:
Аллергическая реакция на качественный препарат проявляется редко. Но при негативных побочных эффектах в виде диареи, тошноты, кожной сыпи нужно прекратить прием.
Как принимать медвежью желчь
Практикуют по показаниям лечение медвежьей желчью после получения детальных рекомендаций врача.
Можно приобрести в аптеках готовые препараты на основе продукта, включающие в состав синтезированное вещество — УДХК. Например, «Урсосан», выпускаемый в капсулах.
Рекомендуется средство для лечения билиарного цирроза печени. Дозировка медвежьей желчи рассчитывается в соответствии с весом больного человека. В среднем за сутки принимают 2-3 капсулы.
Инструкция по применению медвежьей желчи включает использование готовой спиртовой настойки. При назначении врач учитывает тип и тяжесть заболевания.
Внутренний прием обязательно базируется на показателях веса тела пациента. Для лечения:
В профилактических целях препарат употребляют вдвое меньшей дозировке. Начинают лечебные процедуры с небольшой дозы, контролируя реакцию организма.
Для получения нужного результата требуется ежедневный прием средства, в определенное время. Запивать не следует. Иногда разрешается выпить после препарата только остывшую до комнатной температуры кипяченую воду. Нельзя в период лечения употреблять алкоголь.
Стандартный курс лечения медвежьей желчью составляет один месяц. Для профилактики употребляют неделю, а потом устраивают семидневный интервал. Если необходимо, повторяют прием.
При наружном использовании на больные суставы рекомендуется на ночь делать компресс с медвежьей желчью. При гематомах используют примочки или аккуратно втирают в пораженный участок кожи.
Настойка оказывает благотворное воздействие при разнообразных кожных болезнях. Средство рекомендуют применять наружно при псориазе, язвенных проявлениях, дерматите, экземе.
Благодаря бактерицидным характеристикам, препарат активизирует заживление ссадин, ожогов, ран. В этом случае настойку рекомендуется в равных долях разводить отфильтрованной водой. Делают примочки, которые способствуют устранению воспаления, интенсификации процесса регенерации, обеззараживанию поврежденных участков кожных покровов.
Применение в народной медицине
Лечебные свойства вещества издавна используется в народной медицине. Средства на его основе изготавливают самостоятельно, но при приеме важно не превышать рекомендуемых дозировок.
Практикуют приготовление медвежьей желчи на водной или спиртовой основе, ориентируясь на тип и степень выраженности диагностируемого заболевания.
Водная настойка
Менее концентрированная настойка на воде используется при первых симптомах болезни печени. Помогает снимать усталость, повышает иммунитет. Рекомендуют применять рецепт водной настойки, если больному запрещается спиртное в любом виде.
Для приготовления: 1/2 ч. л. порошка просушенного желчного пузыря тщательно растворить в половине стакана теплой воды. Принимают после процеживания по 2 ч. л. до еды дважды за сутки.
Порошок
Может для внутреннего приема использоваться сухая медвежья желчь, растертая до состояния мелкодисперсного порошка. Используют перед едой, запивая отфильтрованной водой.
Для наружного применения пригодится мазь, для которой берут порошкообразное или свежее вещество. Объединяют с любым животным жиром и вымешивают до однородности. Используют при лечении ожогов, ссадин, ран.
Другой вариант приготовления мази:
Охладившуюся пасту держат при комнатных условиях в стеклянном сосуде под крышкой. Эта мазь результативно лечит гноящиеся раны.
Настойка на водке
Для приготовления потребуется высушенный продукт. Перед тем как настаивать медвежью желчь, ее нужно растолочь:
Готовая настойка медвежьей желчи на водке должна храниться в стеклянном флаконе. Препарат принимают, ориентируясь на вес тела.
Спиртовая настойка
Хорошим целебным эффектом при наружном использовании обладает медвежья желчь на спирту. Лекарство чаще готовят из свежего сырья:
Где купить, срок годности, отзывы
Приобрести качественный препарат можно в форме настойки. Часто реализуется медвежья желчь в капсулах или в виде просушенного желчного пузыря, который при необходимости служит сырьем для самостоятельного приготовления целебных средств.
Решая, где купить медвежью желчь, целесообразно обращаться в специализированные магазины. Требуется осторожность во время приобретения продукта у охотников, на рынке или через интернет.
Цена вяленой (сушеной) медвежьей желчи: 230-400 рублей за грамм, настойку продают по 5000 р. – 250 мл.
В среднем срок годности медвежьей желчи в засушенном виде составляет 3 года. Держат продукт в прохладном сухом месте без освещения.
Если удалось купить свежий качественный пузырь, его следует завялить. Перевязывают прочным шнуром по верхним протокам, а затем тщательно удаляют сгустки крови и жир. Сушат в сухом теплом помещении 25-40 дней. Готовый пузырь при ощупывании напоминает пластилин.
Анализируя отзывы о медвежьей желчи, отмечают, что при грамотном выполнении врачебных рекомендаций, наблюдаются значительные улучшения от использования продукта.
Уникальные лечебные свойства медвежьей желчи не служат оправданием для бесконтрольного применения средства. Дозировку утверждает врач только индивидуально, что позволит исключить негативные последствия.
О полезных свойствах и противопоказаниях медвежьего жира, читайте тут.
Восстановление легких после коронавируса
Восстанавливаются ли легкие после COVID-19? Да. Но нужно не пропустить сроки реабилитации и серьёзно отнестись к рекомендациям врача.
Новая коронавирусная инфекция, вызванная SARS-CoV-2, недостаточно изучена, однако ясно, что она наносит вред всем органам и тканям человека. Вирус проникает в организм через слизистые оболочки носа, глаз, глотки. Первые симптомы появляются на 2-14 день. Обычно это повышение температуры выше 37.5 градусов Цельсия, насморк, потеря обоняния, сухой кашель, послабление стула, слабость и головная боль. На 6–10 сутки от момента появления первых симптомов могут начать беспокоить одышка, боль в груди, усиление кашля. Это тревожные симптомы, говорящие о поражении легких и требующие проведения дополнительного обследования: компьютерной томографии легких, измерения насыщения крови кислородом (сатурации).
Легкие после COVID-19
Попадая в организм человека через слизистые оболочки дыхательных путей SARS-CoV-2 вызывает мощнейшую воспалительную реакцию. Активируются иммунные клетки, вырабатывается колоссальное количество воспалительных веществ (воспалительных цитокинов). Интенсивность этой реакции скорее всего обусловлена генетически. Именно интенсивностью воспалительной реакции и определяется тяжесть поражения легочной ткани по данным исследований. В легочной ткани поражение при COVID-19 обусловлено как поражением самих альвеол (в которых происходит газообмен и кровь насыщается кислородом из воздуха) нашими собственными иммунными клетками так и поражением легочных сосудов, оплетающих альвеолы. Степень поражения легких можно определить при помощи КТ (компьютерной томографии).
Таблица 1. Поражение лёгких при COVID-19
Процент поражения легочной ткани
Поражена часть лёгкого. Небольшое затруднение дыхания.
Лечение пяточной шпоры
Что же такое пяточные шпоры и откуда они берутся?
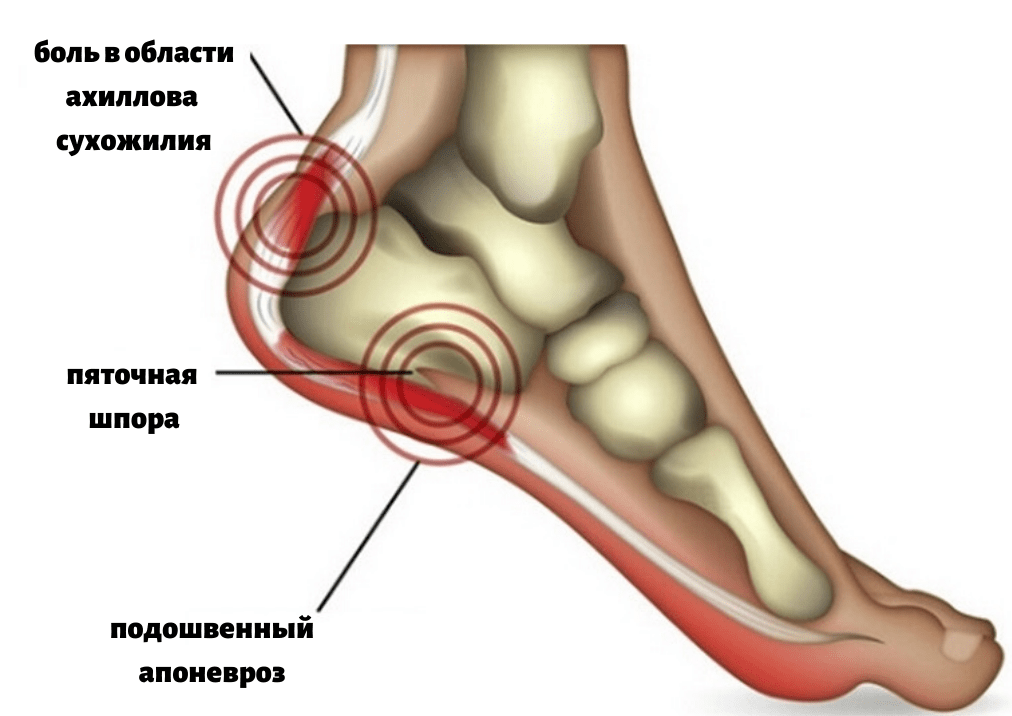
В результате различных процессов (избыточный вес, травма и др.) в данной области возникает хроническая травматизация сухожилия с образованием микронадрывов и постепенное развитие воспалительного процесса. Как компенсаторная реакция на травму и воспалительный процесс начинает образовываться костный вырост, он принимает форму шипа и, передавливая мягкие ткани подошвы стопы, вызывает характерные сильные боли в пяточной области. Самым значимым симптомом пяточной шпоры является сильная боль при ходьбе, особенно в самом начале ходьбы (так называемая, стартовая боль), при вставании со стула, с постели.
Основные причины образования пяточных шпор:
Проявления заболевания
Боли, возникающие при опоре на больную пятку, развиваются постепенно с ростом самой шпоры, характеризуются как жгучие или острые, с ощущением «гвоздя в пятке». Они могут локализоваться на внутренней поверхности больной пятки и переходить на всю стопу. При осмотре пяточной области нет никаких видимых изменений, редко отмечается отечность, болезненность определяется при надавливании на пятку. Интересно, что интенсивность боли не зависит от размера шпоры, что обусловлено, прежде всего, не наличием самой шпоры, а воспалительными изменениями в мягких тканях пятки. Диагноз пяточной шпоры подтверждается рентгенографией.
Основные принципы лечения пяточных шпор
1. Вначале необходимо выяснить причину развития воспалительного процесса в области подошвы и постараться максимально устранить ее. Т.е. выяснить, какой патологический процесс мог привести к избыточной травматизации фасции и возникновению воспаления. С этой же целью следует нормализовать вес, если он избыточный, дозировать физические нагрузки и ношение тяжестей, подобрать удобную, правильную обувь для занятий спортом и для повседневной носки. Снять и отложить в сторону неудобную обувь. На время экспресс-лечения следует ограничить нагрузку на ноги — сократить ходьбу и тем более бег или переноску тяжести насколько это возможно. Лучше носить удобные легкие кроссовки с хорошим супинатором.
2. Необходимо максимально возможное обеспечение физической разгрузки болезненной области, для чего рекомендуется подбор индивидуальных ортопедических стелек с выкладкой внутреннего и наружного продольного сводов, углублением и мягкой прокладкой под пяткой, а также временное ношение подпяточника с углублением или отверстием в центре. Как временную меру при лечении пяточной шпоры можно рекомендовать ношение обуви без задника;
3. Консервативное лечение направленно на ликвидацию воспалительного процесса и включает местное применение нестероидных противовоспалительных препаратов (гели и мази), обладающих противовоспалительным и рассасывающим эффектом. Но эти методы, как правило, приносят лишь только временный эффект, их обязательно нужно сочетать в комплексе с другими методами.
4. Наружное применение мазей при пяточной шпоре лучше сочетать с массажем стоп. Массаж при пяточной шпоре удобно делать самостоятельно.
5. В комплекс лечения пяточной шпоры включают теплые ванны с морской солью, содой. Ванночки необходимо делать перед применением мазей и массажа.
6. Определенные упражнения лечебной гимнастики с проведением массажа мышц стопы и голени — рекомендуются для улучшения кровоснабжения тканей стопы, с этой же целью можно проводить тепловые процедуры парафино- или озокеритотерапии.
7. В некоторых случаях (если развитие пяточной шпоры происходит на фоне артроза) в комплексной терапии рекомендуют прием хондропротекторов с анальгетическим и противовоспалительным эффектом, что останавливает прогрессивный воспалительный процесс, но эффект от внутреннего применения препаратов развивается только через 6 недель от начала лечения и сохраняется в течение 2–3 мес. после его отмены.
8. Методы медикаментозного лечения пяточной шпоры.
Официальная медицина на сегодняшний день разработала большое количество схем фармакологической терапии данного заболевания. Среди препаратов, применяемых для лечения пяточной шпоры: нестероидные противовоспалительные средства, гели, мази, кремы и пластыри для лечения пяточной шпоры местного применения, обладающие рассасывающим и противовоспалительным эффектом.
При малой эффективности консервативного лечения выполняются лекарственная блокада пяточной шпоры — обкалывание болезненного места шприцом с лекарственным веществом. Например, стойким эффектом обладает однократное местное введение дипроспана.
Препараты, применяемые с этой целью, оказывают выраженный местный противовоспалительный эффект, что быстро подавляет воспалительный процесс и снижает болевой синдром.
Данная процедура требует знаний и большого опыта, поэтому проводить ее может только квалифицированный специалист. Однако при частом использовании метода возможно разрушение связки или фасции.
9. К хирургическому лечению прибегают крайне редко, так как встречается много недостатков при данной методике. При проведении операции удаляют пяточную шпору. После чего конечность фиксируют гипсовой повязкой примерно на один месяц.
После снятия гипса назначают ортопедические стельки и проводят курсы восстановительного лечения. Помните, что в большинстве случаев пяточные шпоры вполне поддаются терапии и без операций.
10. Любой метод лечения необходимо сочетать с физиотерапевтическими воздействиями.
Ударно-волновая терапия пяточной шпоры
Является наиболее эффективным методом: терапия воздействует непосредственно на костные разрастания и способствует их уменьшению или даже рассасыванию. Ударно-волновая терапия — относительно новый метод лечения.
В нашей стране данная процедура начала практиковаться не очень давно, но первые результаты уже обнадеживают.
Имеющийся опыт позволяет утверждать, что при использовании данного метода лечения эффективность лечения пяточной шпоры очень высока. Метод основан на воздействии импульсов ударных волн определенной частоты. Эффект ударной волны разрыхляет отложения кальция в пяточной шпоре.
Это позволяет в дальнейшем вымывать разрыхленные отложения из организма с кровотоком. Пораженная связка избавляется таким образом от накопленных солей кальция.
Кроме того, при этом активизируются процессы регенерации тканей, уменьшаются отечность и воспалительные явления. С каждой проведенной процедурой болевой синдром становится все меньше и, как правило, значительно уменьшается или исчезает к концу лечения.
Пораженный участок во многом восстанавливает свою естественную структуру и возвращает себе способность переносить каждодневные нагрузки, не вызывая болезненных ощущений.
На начальных стадиях заболевания лечение требует небольшого количества процедур от 3 до 5 на курс, а при большой длительности процесса длительность лечения до 5-10 процедур на курс. Между сеансами обязателен перерыв 5-7 дней.
Продолжительность одного сеанса составляет 15-20 минут на одно поле. На кожу пятки наносят специальный гель, воздействие осуществляется с помощью излучателя.
Существуют противопоказаниями к лечению пяточной шпоры: нарушения свертываемости крови и тромбофлебит, злокачественные новообразования, беременность.
Нежелательно проведение процедур ударно-волновой терапии в течение месяца после введения в область пятки гормональных противовоспалительных препаратов.
Лучевая терапия (рентгенотерапия) пяточной шпоры
Использование рентгеновского излучения в лечении пяточной шпоры показывает весьма эффективные результаты. Метод заключается в том, что на область пятки направляются четко сфокусированные рентгеновские лучи, несущие пониженную дозу радиации.
Они вызывают блокирование нервных окончаний, и пациент перестает испытывать болевые ощущения.
Курс лечения чаще всего состоит из десяти сеансов, каждый из которых имеет продолжительность в 10 минут.
Рентгенотерапия в лечении пяточной шпоры обладает следующими преимуществами: полная безболезненность процедуры, высокая эффективность, минимум противопоказаний, воздействие излучения только на пяточную шпору, противоаллергическое и противовоспалительное действие, возможность амбулаторного лечения.
Противопоказанием к использованию данного метода является только беременность.
При применении рентгенотерапии сама шпора не исчезает, блокируются только болевые ощущения, исходящие от нее. Поэтому после проведения курса рентгенотерапии необходимо обязательной позаботиться о разгрузке стопы.
Лазерное лечение пяточной шпоры
В настоящее время низкоинтенсивная лазерная терапия — популярный и достаточно широко используемый метод лечения данного заболевания. Лазерная терапия воздействует на мягкие ткани, находящиеся вокруг шпоры.
Сфокусированное излучение вызывает увеличение кровообращения в области воспаления, что способствует уменьшению болей.
Среди пациентов бытует мнение о том, что лазерная терапия способна устранять саму пяточную шпору. Однако это является заблуждением. Проникая в ткани стопы, низкоинтенсивный лазерный луч на сам костный нарост не оказывает практически никакого действия.
Его эффект проявляется только на мягких тканях. А значит, после проведения курсов лазерной терапии также необходимо применять все методы, направленные на профилактику данного заболевания.
УВЧ-СВЧ-терапия
Этот метод заключается в применении переменного электромагнитного поля ультравысокой и сверхвысокой частоты. Влияние этих токов приводит к расширению капилляров в мягких тканях и к значительному усилению кровообращения. При этом уменьшается болевой синдром и воспаление.
Длительность одного сеанса составляет 10-15 минут. Для лечения пяточной шпоры требуется около 10-12 сеансов терапии.
Чаще врачи назначают пациентам переменное магнитное поле. Образуются слабые токи в крови и лимфе, которые влияют на метаболизм, а также на структуру воды и белков. Повышается сосудистая и кожная проницаемость, рассасываются отеки, уменьшается воспаление.
Данная методика позволяет достичь те же результаты, что и УВЧ-терапия.
Лечить шпоры на пятке можно и с помощью электрофореза или СМТ-ДДТ-фореза
Электрический ток повышает ионную активность в проводящих тканях, при этом увеличивается синтез многих биологически активных веществ. Лечебное действие обусловлено поступлением ионов лекарственных веществ (именно в ионной форме вещества наиболее активны), а также формированием кожного депо, из которого ионы постепенно поступают в ткани в последующие дни.
При электрофорезе используют специальные прокладки, пропитанные лекарством. Прокладки располагают между кожей пятки и пластинами электродов. Для лечения пяточной шпоры используют йодистый калий, гидрокортизон, новокаин и прочие препараты.
Эффективность таких методов физиолечения, как ультразвука и фонофореза (сочетанное применение ультразвука и лекарственного препарата) при пяточных шпорах составляет более 30%.
Основной эффект физиотерапии ультразвуком при лечении пяточной шпоры заключается в устранении воспалительного процесса, учитывая, что лучше всего ультразвук поглощается костной тканью.
При этом не следует бояться, что ультразвуковое лечение будет влиять на здоровую костную ткань пятки. Проведенные исследования низкочастотным ультразвуком показали, что разрушений костных тканей не вызывалось, но локальное применение ультразвуковых волн на область шпоры способствовало снижению содержания в ней кальция с замещением волокнистой соединительной тканью.
Также ультразвук оказывает рассасывающее и спазмолитическое действие, улучшая процессы локальной микроциркуляции.
Эффект от ультразвукового лечения усиливается сочетанным применением противовоспалительных мазевых препаратов. Озвучивание низкочастотным ультразвуком повышает проницаемость клеточных мембран, улучшает проницаемость и введение лекарственных веществ.
Наиболее часто применяют гидрокортизоновую мазь. Фонофорез способствует более глубокому проникновению лекарственного вещества в пораженную область, нежели применять мазь как самостоятельное средство лечения.
Метод фонофореза основан на свойстве ультразвука изменять проницаемость кожных покровов, в связи с чем лекарства, нанесенные на кожу, всасываются более активно.
Продолжительность самой процедуры — до 10 минут. На курс лечения может понадобится 5-10 процедур, с возможными повторными курсами.
Профилактика пяточной шпоры
Профилактические меры должны быть направлены, в первую очередь, на предупреждение преждевременного износа, старения и травм костно-суставного аппарата:
Медвежья желчь для чего используется
НАЖБП — неалкогольная жировая болезнь печени
ПБЦ — первичный билиарный цирроз
ПСХ — первичный склерозирующий холангит
РКИ — рандомизированное контролируемое исследование
ССЗ — сердечно-сосудистые заболевания
УДХК — урсодезоксихолевая кислота
ФНО — фактор некроза опухоли
Препараты урсодезоксихолевой кислоты (УДХК) на протяжении многих лет привлекают к себе внимание клиницистов. Это обусловлено многими причинами, основные среди них, на наш взгляд, заключаются в том, что, во-первых, УДХК является одним из звеньев энтерогепатической циркуляции желчных кислот (ЖК) в организме, во-вторых, палитра эффектов УДХК красочна и многообразна и, наконец, в-третьих, ее препараты окружены «интригами» — непрекращающимися спорами об их положительных и отрицательных эффектах.
Последние пять—семь лет ознаменовались неким бумом на так называемые гепатопротекторы, к которым многие причисляют и УДХК. Сам термин не сходит с уст выступающих на различных конференциях, множество публикаций об этом заполонило медицинские (и не только) интернет-сайты. Только ленивый участковый терапевт не назначает эти препараты практически всем пациентам «для защиты печени». Сами пациенты готовы платить деньги за «протектор», не вполне понимая, зачем он им нужен и нужен ли вообще. Возможно, именно поэтому врачебное сообщество усилило внимание к этим препаратам, стали весьма критично относиться к показаниям, вопросам эффективности и безопасности данной терапии.
УДХК (3α, 7β-дигидрокси-5β-холан-24-оевая кислота) — это гидрофильная третичная ЖК, которая, как и другие ЖК, относится к стероидам и способна эмульгировать жиры кишечного содержимого (рис. 1). В организме человека она синтезируется в весьма незначительных количествах (менее 3—5% пула ЖК, по данным разных авторов). Считается, что основное место ее синтеза в организме тонкая кишка, в которой УДХК образуется из 7-кето-литохолевой кислоты путем 7b-эпимеризации при участии нормальной кишечной микрофлоры [2, 3].

Интересна история открытия УДХК. Изначальное ее добывали из медвежьей желчи, что закреплено в латинском названии кислоты — Ursodeoxycholic acid (ursus переводится как «медведь»). Известно, что еще врачи Древнего Китая использовали сухую медвежью желчь для лечения не только заболеваний печени и желчного пузыря, но и расстройств зрения. Основным компонентом этой желчи была, конечно, УДХК, концентрация которой особенно высока в период зимней спячки медведей [4]. Терапевтический эффект медвежьей желчи оставался загадкой до начала XX века.
Годом открытия УДХК можно считать 1902, когда шведский биохимик Олаф Хаммарстен (О. Hammarsten) выделил это вещество из желчи медведя и дал его молекуле название «урсохолеиновая кислота». Однако имеются данные [5], что в своих трудах О. Хаммарстен на самом деле описал не урсодезоксихолевую, а хенодезоксихолевую кислоту (3α, 7α-диокси-5β-холановая кислота). Современное название молекуле УДХК подарил японский исследователь Shoda. Он получил кислоту в кристаллическом виде, а ее точная химическая структура была определена другим японским химиком — Т. Iwasaki в 1936 г. (цит. по [6]). В 1954 г. японский ученый T. Kanazawa и соавт. впервые синтезировали УДХК и описали метод ее синтеза [7]. Официальное применение этой кислоты в медицине началось во второй половине XX века, когда в 1957 г. компания Tokyo Tanabe (Япония) впервые синтезировала УДХК высокой очистки и зарегистрировала ее под торговым названием «Urso» [6].
1972 г. ознаменовался внедрением УДХК в практику: Hofmann с коллегами доказал эффективность применения УДХК при калькулезном холецистите для растворения рентгенонегативных камней небольшого диаметра в случаях, когда проведение холецистэктомии было невозможно [8]. Опубликованные в 1985 г. результаты пилотного исследования Leuschner и соавт. впервые показали позитивное воздействие УДХК на биохимические показатели при хроническом гепатите [9], именно оно способствовало старту большого числа клинических испытаний УДХК, проведение которых продолжается и в наши дни [3].
Об эффективности применения УДХК при холестатических заболеваниях печени, таких как первичный билиарный цирроз (ПБЦ) — основное показание для назначения УДХК, впервые заявили M. Fisher и M. Paradine [10] в 1986 г. Эффективность и безопасность длительного курса терапии УДХК у пациентов с ПБЦ была продемонстрирована в работе Poupon и соавт. [11], опубликованной в 1987 г. И на этом история УДХК не заканчивается. В 2002 г. появляется публикация K. Tsubakio и соавт. о положительном влиянии УДХК при лечении аутоиммунного панкреатита, а в 2005 г. — статья K. Tarao и соавт. о возможности применения УДХК для профилактики гепатоцеллюлярной карциномы (ГЦК) при циррозе печени вирусной (HCV) этиологии [12, 13].
Говоря о фармакокинетических особенностях УДХК, нужно отметить, что как соединение она более гидрофильна в сравнении с основными Ж.К. Единственным возможным путем введения УДХК в организм человека является пероральный. Растворимость УДХК напрямую зависит от pH среды: оптимальное ее значение равно 8. При pH менее 7,8 растворимость УДХК резко снижается, угнетается образование метаболитов с таурином и глицином, замедляется всасывание препарата [14]. Абсорбция УДХК происходит путем пассивной диффузии в проксимальной части тонкой кишки и активной в дистальной части подвздошной кишки. Интересно, что у пациентов с резекцией подвздошной кишки обнаруживали в отделяемом илеостом более 50% введенной дозы этой ЖК [15].
Переносчиком УДХК в кровотоке человека служит альбумин. В исследовании S. Ceryak и соавт. показано, что кроме альбумина УДХК может связываться с липопротеидами высокой, низкой и очень низкой плотности (около 28, 16 и 11% соответственно) [16]. Метаболизм УДХК, наблюдаемый при первом прохождении через печень, достигает 50%. ЖК захватывается гепатоцитами и конъюгируется с таурином или глицином (соотношение между этими конъюгатами составляет 1 к 3). Эти соединения с помощью специфических переносчиков BSEP (Bile Salt Export Pump) активно экспортируются в желчные протоки, накапливаются в желчном пузыре, выделяются в кишечник и снова реабсорбируются в систему воротной вены посредством специфических для ЖК натрийзависимых транспортных белков [17].
Основным органом экскреции препарата УДХК из организма человека служит кишка. Как уже отмечалось выше, в просвете кишечника УДХК может окисляться или восстанавливаться до 7-кетолитохолевой или литохолевой кислоты. Продолжительный период полувыведения УДХК из организма (который, по данным разных авторов, варьирует от 3 до 5 сут и более) объясняют наличием энтерогепатической циркуляции [18, 19]. Выделение УДХК почками с мочой весьма незначительно, но оно приобретает большее значение у пациентов с холестазом, когда концентрация УДХК в плазме увеличивается [20, 21].
Механизмы действия УДХК многообразны. Наблюдаемые у пациентов в процессе лечения эффекты этого препарата также различны. Накопленные данные позволяют выделить из них следующие:
2) антиапоптотический: обеспечивается снижением концентрации ионизированного кальция в клетках, что предотвращает выход цитохрома С из митохондрий и блокирует активацию каспаз;
3) цитопротективный: встраивает УДХК в фосфолипидный слой клеточной мембраны и приводит к стабилизации последней и повышению устойчивости к повреждающим факторам;
4) иммуномодулирующий: проявляется в снижении экспрессии молекул HLA I класса на гепатоцитах и HLA II класса на холангиоцитах, а также в подавлении продукции Тh1- и Th2-цитокинов (фактор некроза опухоли,γ-интерферон, интерлейкины 1, 2, 4 и 6) и синтеза иммуноглобулинов;
5) гипохолестеринемический: заключается в уменьшении всасывания холестерина (ХС) в кишечнике, снижении его синтеза в печени и экскреции в желчь;
6) литолитический: выражается в понижении литогенности желчи вследствие формирования жидких кристаллов с молекулами ХС, предупреждении образования и растворении холестериновых камней [22—25].
В настоящее время активно изучаются и обсуждаются выявленные антиоксидативный, противоопухолевый и другие механизмы действия УДХК, установлено также еe взаимодействие с глюкокортикоидным рецептором. Такое количество эффектов определяет разнообразие нозологических форм, при которых данное вещество может успешно использоваться.
В настоящее время применение УДХК при желчнокаменной болезни вследствие низкой эффективности и высокой частоты рецидивов (30—50% в течение 5 лет) имеет ограниченное значение. Пероральная литолитическая терапия возможна при следующих условиях: невыраженной клинической симптоматике, сохраненной двигательной функции пузыря, небольшом размере конкрементов, которые должны быть рентгенонегативными (плотностью менее 100 HU) и насыщенными ХС [26]. Работы по изучению эффективности УДХК при холелитиазе продолжаются и в настоящее время. Однако их результаты не опровергают данные метаанализа, опубликованные в 1993 г., согласно которым эффективность УДХК при калькулезном холецистите составила 38% [27].
Влияние УДХК на течение ПБЦ оценивалось во многих рандомизированных контролируемых исследованиях (РКИ), в большинстве из которых доза препарата составляла 13—15 мг/кг/сут. Результаты этих исследований выявили не только положительное влияние УДХК на биохимические показатели (билирубин, трансаминазы, щелочную фосфатазу), но и замедление прогрессирования болезни и улучшение качества жизни больных (связанное прежде всего с уменьшением выраженности основной жалобы — кожный зуд). Терапия в большинстве случаев начиналась непосредственно после установления диагноза. В более ранних исследованиях выявлено, что длительная терапия УДХК может замедлять прогрессирование цирроза ранних стадий, улучшает выживаемость и снижает потребность в трансплантации печени [28, 29]. Авторы систематического Кокрейновского обзора, включавшего анализ 16 рандомизированных клинических испытаний УДХК в сравнении с плацебо или отсутствием вмешательства у пациентов с ПБЦ, пришли к выводам, можно сказать, противоположным тем, что были сделаны по результатам предыдущих метаанализов. Никакого статистически значимого влияния УДХК на смертность и потребность в трансплантации, а также на морфологическое строение печени и выраженность кожного зуда обнаружено не было, а действие УДХК было сведено только к улучшению показателей некоторых неспецифических биохимических маркеров — билирубина, щелочной фосфатазы, трансаминаз [30]. В настоящее время установлено, что эффективность терапии УДХК зависит от клинического фенотипа ПБЦ [31, 32]:
I. Женщины среднего возраста: клиническая симптоматика скудная или отсутствует; хороший ответ на УДХК; благоприятный прогноз.
II. Пациенты любого возраста: слабый ответ на УДХК; медленное, но неуклонное прогрессирование до цирроза.
III. Дебют в среднем возрасте: неяркая клинико-биохимическая симптоматика; декомпенсация на 7—8-м десятилетии жизни.
IV. Пациентки старческого возраста: прогрессирование до цирроза, который остается компенсированным.
V. Молодые женщины: быстропрогрессирующая дуктопения; абсолютная резистентность к УДХК.
Еще одно холестатическое заболевание, при котором предполагается эффективность УДХК терапии, — первичный склерозирующий холангит (ПСХ). Прием УДХК в средних (13—15 мг/кг) и высоких (25—30 мг/кг) дневных дозах приводил к улучшению биохимических и гистологических параметров в пилотных исследованиях [33—35]. В настоящее время отношение к этому препарату при лечении ПСХ неоднозначно. В исследовании K. Lindor и соавт. терапия УДХК в стандартной дозе (13—15 мг/кг) оказалась неэффективной. Увеличение дозы в 2 раза (до 30 мг/кг в день) не повлияло на течение заболевания, а лишь привело к росту числа осложнений, и это повлекло за собой досрочное прекращение клинического испытания по причинам, основными из которых стали: увеличение смертности и потребности в трансплантации печени, варикозное изменение вен пищевода, что увеличивало риск кровотечений (p=0,01 в сравнении с плацебо). У всех пациентов с ПСХ был достигнут контроль над уровнем печеночных трансаминаз, но стало очевидно, что нормализация аланин- и аспартатаминотрансферазы (АЛТ и АСТ) в процессе терапии УДХК совсем не означает клинического улучшения или благоприятного изменения прогноза [36].
Схожие результаты получены и во многих других исследованиях влияния УДХК на течение и прогноз при ПСХ, но были и те, где выводы авторов в отношении эффективности этого препарата разнились. В метаанализе 8 РКИ (n=465), проведенном J. Shi и соавт., они приходят к заключению, что УДХК нормализует уровень биохимических маркеров, статистически значимо улучшает гистологическую картину печени, но не оказывает при этом серьезного влияния на выраженность кожного зуда и общей слабости и, что более важно, на показатели смертности и потребности в трансплантации печени [37].
В систематическом обзоре с метаанализом, проведенном Кокрейновским сообществом, изучены 8 РКИ эффективности УДХК (n=592) средней продолжительностью около 3 лет (от 3 мес до 6 лет). Результатом этой работы явились констатация убедительных доказательств отсутствия пользы или вреда назначения УДХК пациентам с ПСХ и необходимость в проведении высококачественных мультицентровых плацебо-контролируемых исследований высоких (более 20 мг/кг) доз УДХК [38].
Количество исследований, посвященных вопросам эффективности и безопасности УДХК у пациентов с алкогольной болезнью печени, невелико в сравнении с испытаниями по указанным вопросам у пациентов с желчнокаменной болезнью, ПБЦ и ПСХ.
Положительное влияние УДХК на биохимические показатели отмечено у пациентов с циррозом алкогольного генеза, причем такая активность была зафиксирована как для монотерапии препаратом, так и для его комбинации с силимарином [39, 40]. Недостатком многих работ по этой проблеме является отсутствие морфологического исследования печени. В публикациях последних лет было показано, что у пациентов с алкогольным циррозом на фоне полного отказа от употребления алкоголя и приема УДХК выявлено достоверно более выраженное снижение показателей холестаза и цитолиза, а также значимое уменьшение плотности печени по данным ультразвуковой эластографии [41].
Имеются также публикации о положительном влиянии УДХК при лечении пациентов с хроническим вирусным гепатитом С, которые получали препарат ЖК в дополнение к интерферонотерапии. Результаты тех биохимических печеночных проб могли бы увеличить приверженность к этой терапии как врачей, так и пациентов [42]. Однако данные достаточно большого количества исследований по этой нозологии в целом не свидетельствуют в пользу замедления прогрессирования заболевания [43, 44]. В работе K. Tarao и соавт. показано, что среди наблюдавшихся в течение 5 лет независимо от уровня АЛТ 102 пациентов с циррозом печени вирусной (HCV) этиологии класса, А по шкале Чайлд—Пью ГЦК развилась в 17,9% случаев (56 пациентов, которые получали УДХК) и 39,1% случаев (46 пациентов, которых не лечили препаратами ЖК), p=0,025 [13]. Безусловно, одного этого исследования слишком мало, чтобы говорить о профилактической роли УДХК в отношении ГЦК.
Известна также негативная роль первичных и вторичных ЖК в составе дуоденогастроэзофагеального рефлюкса. ЖК повреждают клетки эпителия, способствуют снижению количества фосфолипидов желудочной слизи и потере ее гидрофобности. Морфологически доказано, что желчный рефлюкс ассоциирован с формированием пищевода Баррета и очагов кишечной метаплазии в желудке, что свидетельствует о связи ЖК с канцерогенезом. Применение УДХК приводит к снижению отрицательного влияния эндогенных ЖК при рефлюкс-гастрите и повреждении пищевода в результате желчного рефлюкса. Цитопротективные свойства УДХК объясняются образованием смешанных мицелл УДХК с токсичными ЖК, ее антиоксидантным эффектом, а также влиянием на клеточное деление и апоптоз [45].
Актуальным представляется рассмотрение возможности применения УДХК в лечении внутрипечeночного холестаза беременных, который ассоциируется с повышенной частотой преждевременных родов, гипотрофией плода и перинатальной смертностью. Во многих обзорах, включая Кокрейновский, усомнились в эффективности УДХК в отношении данной патологии беременных. В 2014 г. был опубликован метаанализ 11 РКИ (n=625) и 6 нерандомизированных исследований (n=211), в которых беременным по показанию назначалась УДХК в дозе 750—1000 мг/сут. Результаты оказались обнадеживающими: уменьшение кожного зуда (основного симптома), а также улучшение биохимических показателей отмечено у 73—100% беременных, что, несомненно, благоприятствует прогнозу для плода [46].
Кроме указанных состояний, описано применение УДХК в схеме иммуносупрессивной терапии после трансплантации печени [47], в 2014 г. в печати появились данные об эффективности УДХК при остром панкреатите билиарной этиологии [48]. Есть публикации о противоопухолевой активности этой ЖК [49]. Но все эти и многие другие сведения не имеют в настоящее время убедительной доказательной клинической базы.
Пристальное внимание врачей-интернистов привлекает неалкогольная жировая болезнь печени (НАЖБП). С одной стороны, эта патология печени рассматривается как потенциальное фоновое заболевание для развития ГЦК [50], с другой стороны, как плацдарм для прогрессирования всех проявлений метаболического синдрома (МС). В долговременном исследовании, проведенном в Швеции, показано, что из 129 пациентов с морфологически доказанной НАЖБП, сопровождавшейся «хронической гипертрансаминаземией», за 15 лет наблюдения умерли 12,7% от сердечно-сосудистых заболеваний (ССЗ) и только 1,6% — от печеночной патологии [51]. Сегодня многими исследователями признается, что НАЖБП выступает не только фактором риска прогрессирования атеросклероза и развития заболеваний сердечно-сосудистой системы, но, как утверждается в последних исследованиях, определяет их исход в большей степени, чем исход заболеваний печени [52]. Значит, основная цель, которую прежде всего должен стремиться достичь интернист, — снижение кардиоваскулярного риска, обусловленного высоким атерогенным потенциалом.
Во всем мире золотым стандартом в профилактике и лечении ССЗ, а значит и атерогенной дислипидемии, выступают статины. Наличие НАЖБП при этом служит камнем преткновения для большинства врачей. Поэтому если больному показан прием статинов, а уровень печеночных трансаминаз превышает норму в 2—3 раза, то на помощь клиницисту может прийти УДХК, так как ее назначение патогенетически обосновано при НАЖБП [19, 53]. В этом случае применение УДХК в дозе 10—15 мг/кг в сутки, длительностью 6 мес и более оказывает положительное влияние на биохимические показатели, ведет к снижению активности АЛТ, АСТ, щелочной фосфатазы, γ-глутамилтранспептидазы и уменьшению выраженности стеатоза и воспаления, согласно гистологическому исследованию печени [54]. После нормализации уровня АСТ, АЛТ на фоне приема УДХК больному можно назначать статины.
При неалкогольном стеатогепатите V. Ratziu и S. Zelber-Sagi представили первые обнадеживающие результаты применения УДХК в высоких дозах [55]. Но они были подвергнуты сомнению U.F. Leuschner и соавт., представившими данные РКИ с парными биопсиями печени [56]. Между тем в 2013 г. Z. Xiang и соавт., проанализировав 12 РКИ, суммарно включавших 1160 пациентов, установили, что монотерапия УДХК вела к улучшению функции печени в пяти исследованиях и уменьшала выраженность стеатоза и фиброза в двух. Во всех пяти исследованиях, в которых оценивалась эффективность комбинации УДХК с другими препаратами, было продемонстрировано существенное улучшение функциональных печеночных показателей, при этом в двух из них констатировано уменьшение стеатоза и воспаления [57].
В литературе также имеются данные о том, что эффективность комбинации УДХК и малых доз статинов выше, чем использование удвоенной дозы последних. В испанском исследовании при комбинированной терапии симвастатином (20 мг/сут) и УДХК (300 мг/сут) в течение 4 мес по сравнению с монотерапией симвастатином (40 мг/сут) было достигнуто более выраженное снижение уровня липопротеидов низкой плотности (р=0,0034). Аналогичный результат был получен в этом же исследовании в группе больных, принимавших аторвастатин (20 мг/сут) и УДХК (300 мг/сут) 4 мес, по сравнению с монотерапией аторвастатином в дозе 40 мг/сут (р=0,0037) [58].
Нужно отметить, что исследования, в которых изучалась комбинированная терапия статинами и УДХК, немногочисленны, но вместе с тем добавление УДХК в схему гиполипидемической терапии статинами у больных с НАЖБП оправдано. На кафедре пропедевтики внутренних болезней лечебного факультета ПМГМУ под руководством д.м.н. проф. О.М. Драпкиной была выполнена диссертационная работа, посвященная изучению особенностей липидного обмена у больных с МС, оценке эффективности схем гиполипидемической терапии в зависимости от генотипа N291S липопротеидлипазы. Результаты этой работы продемонстрировали статистически достоверную эффективность комбинации симвастатина и УДХК (Урсосан) у пациентов с прогностически благоприятным AA- и AG-генотипом полиморфизма данного фермента. Был разработан алгоритм диагностики и лечения нарушений липидного обмена у больных с диагностическими критериями определения МС (рис. 2), согласно рекомендациям Международной диабетической федерации (International Diabetes Federation — IDF) 2005 г. (цит. по [59]).

Исследования проф. О.М. Драпкиной и соавт., посвященные изучению эффективности и безопасности комбинированной терапии статинами и УДХК, продолжаются и по настоящее время. Так, представляется интересным и необходимым обращать внимание на вопросы межлекарственного взаимодействия при лечении пациентов с ожирением и сопутствующей патологией печени: например, комбинация УДХК и аторвастатина является перспективной схемой терапии таких пациентов [60]. Во всех работах важен вывод о том, что УДХК в содружестве со статинами не только проявляет свои плейотропные эффекты, но и несколько усиливает ожидаемые эффекты статинов. Такая схема лечения представляется весьма перспективной, особенно в отношении пациентов, имеющих НАЖБП в рамках МС [61, 62].
На вопрос, влияет ли УДХК самостоятельно на дислипидемию, однозначного ответа нет. Воздействие на липидный обмен связывается с ее способностью влиять на экспрессию фарнезоидного Х-рецептора α (FXRα), который, кроме регуляции активности ферментахолестерин-7-α-гидроксилазы (CYP7A1), увеличивает количество ядерных пероксисомных пролифератор-активируемых рецепторов альфа (PPARα), рецепторов липопротеидов очень низкой плотности и усиливает активность липопротеидлипазы сыворотки крови (рис. 3) [63, 64]. Следует отметить, что УДХК является гораздо более слабым стимулятором экспрессии FXRα, чем первичные Ж.К. Также можно предположить, что УДХК, увеличивая концентрацию первичных и вторичных ЖК в кишечнике, стимулирует их воздействие на FXRα, поэтому влияние УДХК на уровни липопротеидов может иметь значение только при использовании ее в комбинации с другими липидоснижающими препаратами.
Опыт применения УДХК в качестве лекарственного препарата насчитывает более 40 лет, а в традиционной китайской медицине — многие столетия. За это время данный лекарственный препарат смог заявить о себе с положительной стороны, показав клиническую эффективность и относительную безопасность. По сути УДХК является лекарственным препаратом плейотропного действия, что выражается в наличии у него холеретического, цитопротективного, иммуномодулирующего, антиапоптотического, гипохолестеринемического и литолитического механизмов действия. Для того чтобы расширить представление о механизмах действия УДХК, еe эффективности и безопасности, возможности увеличивать или уменьшать диапазон терапевтического воздействия, необходимо и в дальнейшем проводить крупные многоцентровые контролируемые исследования.