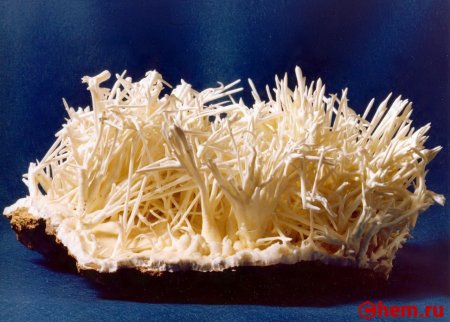
Мел, состав, происхождение, виды и применение
Мел, состав, происхождение, виды и применение.
Мел – это разновидность известняка, осадочная горная порода органического (зоогенного) происхождения, состоящая из скрытокристаллического кальцита.
Мел, свойства, состав и происхождение:
Мел – это разновидность известняка, осадочная горная порода органического (зоогенного) происхождения, состоящая из скрытокристаллического кальцита.
Мел представляет собой разновидность слабоцементированной мажущейся тонкозернистой карбонатной породы, состоящей в основном из карбоната кальция природного происхождения или полученного искусственным путем.
Мел – это горная порода, в основном, белого цвета. Иногда встречается мел желтоватого белого или кремового цвета, что обусловлено наличием в его составе различных примесей (глины и пр.).
Мел – очень мягкий и рассыпчатый материал. Твердость мела по шкале Мооса составляет 1. Его твердость аналогична с твердостью другой горной породой – тальком. Мел и тальк легко чертятся ногтём.
Мел состоит из скелетов крохотных живых существ, которые десятки миллионов лет назад при жизни поглощали из воды древних морей соли кальция и углекислый газ как сырьё для строительства маленьких оболочек вокруг своих тел. По мере того как они умирали, в меловом периоде мезозойской эры происходило накопление меловых отложений, которые в конечном итоге образовали горную породу. Меловой период – это последний период мезозойской эры и самый продолжительный из периодов мезозойской эры: начался 145,0 миллионов лет назад, закончился 66,0 миллионов лет назад, таким образом, продолжался около 79 миллионов лет. Название мелового периода произошло от мела.
Наиболее значительная полоса отложений мела залегает в Европе – от реки Эмба в Западном Казахстане до Великобритании (включительно), и частично в Азии – в Сирии и Ливийской пустыне. Мощность пластов мела достигает нескольких сотен метров.
Мел добывают из меловых месторождений как надземных, так и подземных.
Виды, марки и сорта мела:
В зависимости от способа производства и области преимущественного применения мел подразделяют на виды, марки и сорта (согласно ГОСТ 17498-72 Мел. Виды, марки и основные технические требования).
| Вид | Марка | Способ производства | Сорт | Область преимущественного применения |
| Природный | МК1 | Комовый | 1 | В строительстве и для ремонта зданий и сооружений, для производства извести, в стекольной, керамической и других отраслях промышленности |
| То же | МК2 | То же | 2 | “ |
| “ | МК3 | “ | 3 | “ |
| “ | ММ1 | Молотый | 1 | То же, кроме производства извести |
| “ | ММ2 | То же | 2 | “ |
| “ | ММ3 | “ | 3 | “ |
| “ | ММИП1 | “ | 1 | В сельском хозяйстве для известкования кислых почв |
| “ | ММИП2 | “ | 2 | “ |
| “ | ММЖП | “ | – | В сельском хозяйстве для подкормки животных и птиц |
| “ | ММПК | “ | – | В сельском хозяйстве и для производства комбикормов |
| “ | ММС1 | Молотый сепарированный | 1 | В кабельной, лакокрасочной и других отраслях промышленности |
| “ | ММС2 | То же | 2 | В полимерной и других отраслях промышленности |
| “ | ММСГ1 | Молотый сепарированный гидрофобизированный | 1 | В кабельной, резиновой, лакокрасочной и полимерной промышленности |
| “ | ММСГ2 | То же | 2 | То же, кроме кабельной |
| “ | ММО | Молотый обогащенный | – | В кабельной, резиновой, лакокрасочной и других отраслях промышленности |
| Химически осажденный | МХО1 | Химически осажденный | 1 | В парфюмерной, косметической, резиновой, медицинской, пищевой и других отраслях промышленности |
| То же | МХО2 | То же | 2 | “ |
| “ | МХО3 | “ | 3 | “ |
Примечание. В обозначениях марок мела буквы означают: МК – мел комовый, ММ – мел молотый, ИП – известкование почв, ЖП – животные и птицы, ПК – производство комбикормов, С – сепарированный, СГ – сепарированный гидрофобизированный, О – обогащенный, ХО – химически осажденный.
Применение и использование мела:
Мел используется в быту и различных отраслях народного хозяйства:
– в строительстве и для ремонта зданий и сооружений – для побелки, окраски заборов, стен, бордюров и пр.,
– для защиты стволов деревьев,
– как необходимый компонент мелованной бумаги, используемой в полиграфии для печати качественных иллюстрированных изданий,
– для письма на больших (школьных и пр.) досках для общего обозрения,
– в фармацевтике в лекарственных препаратах как вспомогательное вещество (наполнитель),
– в животноводстве как кормовая добавка, обеспечивающая необходимое количество кальция в рационе птиц и скота,
– в качестве дисперсного наполнителя для полимерных композиций (полипропилена, полиэтилена и пр.), резины, керамики и пр.,
– при производстве строительных материалов – извести, портландцемента, стекла и пр.,
– в пищевой промышленности – для очистки свекловичного сока,
– в парфюмерии и косметике – в качестве наполнителя,
Из чего делают мел: меловые отложения, добыча, состав и применение
Из чего делают мел? Что это за соединение такое? Ответы на эти и другие вопросы вы найдете в статье. Его можно именовать «свидетелем эпох», которые исчезли десятки миллионов лет тому назад. Это соединение имеет биологический источник, поэтому обладает физическими и химическими качествами. Из чего делают мел, выясним ниже.
Особенности возникновения
Немногие знают, из чего делают мел. Уделим внимание его возникновению в природе. Когда на Земле жили динозавры (а это было примерно 80 млн лет назад), был Меловой период. В крохотных морях того времени обитали миллионы маленьких моллюсков, которые свои скелеты и раковины строили из кальция, находящегося в воде. В донных отложениях скапливались останки существ многометровыми слоями и трансформировались в белый мел.
Структура минерала
Многие люди спрашивают: «Из чего делают мел?» В процентном соотношении выделяют такие составные части этого минерала:
Химический состав
Итак, вы уже знаете, из какого камня делают мел. Теперь рассмотрим его состав. Известно, что белый минерал содержит до 50 % оксида кальция, и примерно 2 % оксида магния. Какие субстанции придают окраску этому минералу?
Мел иногда может содержать даже 3-4 % оксида алюминия, а также немного оксидов железа. В этом случае он будет иметь розовый или красный оттенок.
В его состав входят:
Кстати, высокое содержание кремния увеличивает плотность мела.
Интересные факты
Вы знаете, из чего делают школьный мел? Можно ли его есть? Если у человека в организме недостаточно кальция, у него возникает тяга к поеданию мела. Доктора к данному вопросу относятся неоднозначно. Когда он оказывается под влиянием желудочного сока (соляной кислоты концентрированной), он значительно меняет свои качества.
Мел проходит через большое число окислительных процессов. В итоге он лишается первичной нейтральности, превращается в химическое агрессивное соединение, похожее по свойствам на гашеную известь (гидроксид кальция).
Именно поэтому слизистая оболочка ЖКТ при контакте с окисленным минералом серьезно страдает.
Если мел употреблять в пищу в больших количествах, это спровоцирует известкование сосудов. При недостатке кальция намного безопаснее принимать особые медпрепараты, к примеру, глюконат кальция.
Доктора предупреждают пациентов о недопустимости применения в пищу аграрного кормового, канцелярского, строительного мела.
Применение и добыча
Как делают мел? В основном его получают путем карьерных открытых разработок. Добытые глыбы крошат, затем погружают в воду. При беспрестанном размешивании частички кальция всплывают на поверхность. Их высушивают и используют для разнообразных целей. Кстати, в виде кладочного сырья мел применять неразумно, так как у него малая твердость.
Камни, которые не прошли подобную переработку, отправляют на обжиг. В результате образуется известь, которую долгое время использовали для побелки потолков внутри строений. Сегодня такая сфера применения почти отсутствует, так как были созданы иные отделочные материалы.
Нынче мел добавляют в разные цементные смеси для того, чтобы придать им дополнительную мягкость. Также минерал востребован при создании стекла, пластмасс, резины, каучука, смесей композитных и лакокрасочных материалов.
В огромных количествах породу применяют в ковровой и линолеумной промышленности. С его помощью регулируют вязкие качества латексного клея, улучшают теплосберегающие свойства изделий, придают им прочность.
Кальций необходим для изготовления удобрений почвенных и комбикормов. Порошок меловой – это база для создания многих косметических средств: помады губной, пудры, кремов. Сложно представить функционирование бумажной и картонной промышленности без этого материала.
Физико-химические характеристики
В зависимости от своеобразия месторождений, в природных свойствах мела могут быть значительные отличия. Существенно влияет на минерал влажность воздуха. Он в воде не растворяется, а формует суспензию. Карбонат кальция при впитывании влаги свою прочность теряет. Пластичность материала при этом значительно увеличивается.
Это вносит серьезные проблемы в переработку и добычу мела, он прилипает к ковшу экскаватора. Имеет незначительную морозостойкость. После размораживания он распадается на большое число мелких отдельных частиц. Данное свойство применяют в сельском хозяйстве для снижения кислотности почвы.
Чем мел отличается от извести?
Несмотря на общие корни, эти материалы отличаются по составу, свойствам. Оба считаются экологически безопасными, но известь получают путем обжига природного известняка, а в составе мела имеется углекислый газ.
Желаете собственными силами отличить известь от мела? Возьмите маленькую горсть каждого сырья, разотрите в пыль, а затем смойте тонкой струей воды. Мел тот час же исчезнет вместе с водой, а вот для того чтобы удалить известь, придется порядочно потрудиться.
От известковой побелки следов не остается. Мел же будет долгое время напоминать о себе даже после окончания ремонта. У извести обнаружены великолепные антисептические свойства, поэтому ее применяют для защиты кустарников и деревьев от поражения насекомыми.
Применение в школе
Каждый должен знать, из какого камня делают школьный мел. На первый взгляд, этот продукт имеет невзрачный вид. Он весьма актуален для учеников и учителей в учебных заведениях, его расходуют малыши, рисуя на городских тротуарах. Потребитель требует качества от любой продукции, и мел исключением не является.
Многие учителя жалуются, что он кожу разъедает, сыпется с доски, сильно руки пачкает, раздражает голосовые связки. В чем причина?
Известно, что школьный мел на 40 % состоит из карбоната кальция и на 60 % из гипса или иной любой связующей субстанции (крахмала, клея ПВА). Также в нем есть немного оксидов металлов, карбоната магния, примесей кварца, морских ископаемых организмов (фораминиферов, радиолярий).
Когда с морского дна слои породы были подняты на поверхность, они образовали меловые скалы, самые известные из которых расположены в Англии и Франции. В РФ самые большие месторождения размещены в Белгородской и Воронежской областях, а также в Ульяновской, Саратовской и Брянской.
Самый древний в России завод по изготовлению мела находится в Белгороде. В районе этого города минерал, как горную породу, добывают и сегодня. Именно из белгородских карьеров его развозят по всем предприятиям, производящим материал поштучно.
Производство
Как делают мелки? В Белгороде мел изготавливали и раньше и создают теперь экструзионным методом. При этом мокрый минерал в виде тоненьких колбасок поступает из устройства, похожего на мясорубку. Колбаску укладывают на противень, режут и в печах сушат. В итоге получаются круглые мелки. Технологическое своеобразие этой продукции – ее «связывание» осуществляется за счет клея (чаще всего ПВА), что для здоровья малышей не совсем безопасно (известно, что белый мел едят ребятишки, впрочем, как и взрослые). Зато она почти не пачкает руки, мягкая, приятная на ощупь.
Мел для рисования применялся издавна. Археологи и ныне обнаруживают пещерные рисунки, сделанные этой породой. Некоторые художники рисовали эскизы своих картин. Именно тогда мел для удобства приобрел свою общепринятую форму в виде палочки.
Так как мел – это рассыпчатая и мягкая горная порода (порошок), его часто смешивают со связующими субстанциями – водой и глиной. После полученную массу помещают в формочки и сушат. Если необходим цветной материал, в смесь добавляют разнообразные примеси. Для получения черных мелков, к примеру, добавляют углерод, а для ярко-красных – оксид железа.
Некоторые производители в виде связующего вещества добавляют декстрин или гипс. И уже из этой смеси далее делают школьный мел. Для получения цветных мелков на последнем этапе иногда добавляют красители.
Базовые требования
Мы уже ответили на вопрос, из чего делают школьный мел. Состав его довольно-таки разнообразен. Базовые требования, предъявляемые к писчему материалу, такие:
Почти не крошится мел от ООО «Пегас» (г. Клин), так как он достаточно плотный. А вот продукция производства ООО «Центрум инт» и ООО «Алгем» сильно пачкает руки. В качестве загустителя в этих образцах используют гипс, а не крахмал.
Кстати, мел кожу рук разъедать не может, так как реакция его среды нейтральна. Беспрестанная работа с этим минералом может вызывать сухость кожи рук. Поэтому чаще мойте их, смазывайте защитным кремом.
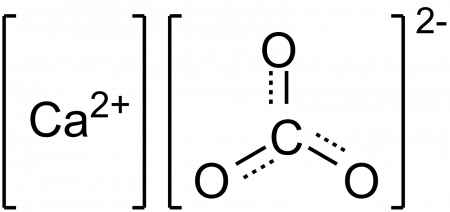
Карбонат кальция
| Карбонат кальция | |||
|---|---|---|---|
| |||
 | |||
| Систематическое наименование | карбонат кальция | ||
| Традиционные названия | углекислый кальций | ||
| Хим. формула | CaCO3 | ||
| Состояние | твёрдые белые кристаллы | ||
| Молярная масса | 100.0869 г/моль | ||
| Плотность | (кальцит) 2.74 г/см³ (арагонит) 2.83 г/см³ | ||
| Температура | |||
| • плавления | (кальцит) 825 °C, (арагонит) 1339 °C | ||
| • разложения | 900−1000 °C | ||
| Давление пара | 0 ± 1 мм рт.ст. | ||
| Константа диссоциации кислоты pKa | 9.0 | ||
| Растворимость | |||
| • в воде | (25 °C) 0,0014 г | ||
| Показатель преломления | 1,60 | ||
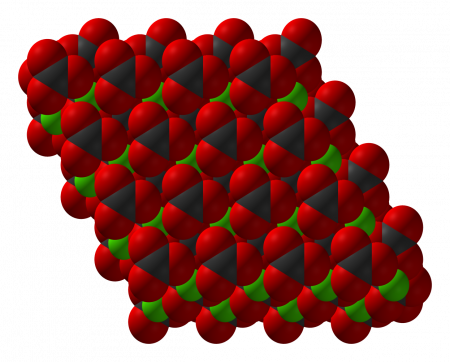
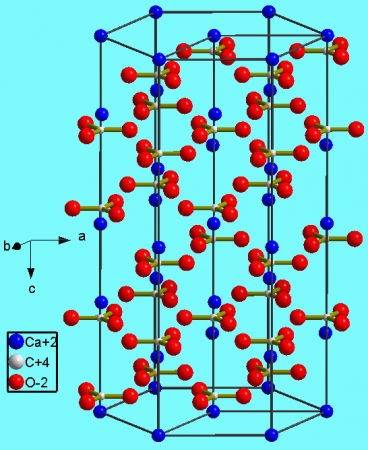
| Кристаллическая структура | тригональная, пространств. гр. 2/m | ||
| ГОСТ | ГОСТ 4530-76 | ||
| Рег. номер CAS | 471-34-1 | ||
| PubChem | 10112 | ||
| Рег. номер EINECS | 207-439-9 | ||
| SMILES | |||
| Кодекс Алиментариус | E170 | ||
| RTECS | FF9335000 | ||
| ChEBI | 3311 | ||
| ChemSpider | 9708 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
В природе встречается в виде многочисленных минералов, например, кальцита, арагонита и ватерита, является главной составной частью известняка, мрамора, мела, входит в состав скорлупы яиц птиц.
Нерастворим в воде и этаноле.
Зарегистрирован как белый пищевой краситель (E170).
Содержание
Применение
Используется как белый пищевой краситель E170. Являясь основой мела, используется для письма на досках. Используется в быту для побелки потолков, покраски стволов деревьев, для подщелачивания почвы в садоводстве.
Массовое производство/использование
Очищенный от примесей, карбонат кальция широко используется в бумажной и пищевой промышленности, в качестве наполнителя при производстве пластмасс, красок, резины, продукции бытовой химии, в строительстве.
При производстве бумаги карбонат кальция применяют одновременно в качестве отбеливателя, наполнителя, а также раскислителя.
Используется при производстве силикатного стекла, — материала для производства оконного стекла, стеклянных бутылок, стекловолокна.
Применяется при производстве предметов гигиены (например, зубной пасты), в медицине.
В пищевой промышленности часто используется в качестве препарата препятствующего слеживанию и для препятствования слипания в комки сухих молочных продуктах.
При употреблении сверх рекомендованной дозы (1,5 г в день) может вызывать молочно-щелочной синдром (синдром Бернетта). Рекомендован при болезнях костных тканей.
Производители пластмассы — одни из основных потребителей чистого карбоната кальция (более 50% всего потребления). Используемый в качестве наполнителя и красителя, карбонат кальция необходим при производстве поливинилхлорида (PVC), полиэфирных волокон (кримплен, лавсан, и т. п.), полиолефинов. Изделия из данных видов пластмасс распространены повсеместно — это трубы, сантехника, кафельная плитка, черепица, линолеум, ковровые покрытия, и т.п. Карбонат кальция составляет порядка 20% красящего пигмента, используемого при производстве красок.
В строительстве
Строительство — ещё один из основных потребителей карбоната кальция. Например, в качестве наполнителя шпаклёвок и герметиков.
Также карбонат кальция является важным составным элементом при производстве продукции бытовой химии — средств для чистки сантехники, кремов для обуви.
Карбонат кальция широко применяется для раскисления кислых почв.
Нахождение в природе
Карбонат кальция находится в минералах в виде полиморфов:
Тригональная кристаллическая структура кальцита является наиболее распространенной.
Минералы карбоната кальция находятся в следующих горных породах:
Геология
Залежи карбоната кальция в виде меловых пластов — отложений известковых раковин моллюсков, в основном, мелового периода является распространенным минералом на всех континентах.
В природе встречаются три кристаллические модификации (минералы с одинаковым химическим составом, но с различной кристаллической структурой): кальцит, арагонит и фатерит (ватерит).
Некоторые горные породы (известняк, мел, мрамор, травертин и другие известковые туфы) практически полностью состоят из карбоната кальция с различными примесями.
Кальцит является устойчивой кристаллической модификацией карбоната кальция и встречается в самых разнообразных геологических условиях: в осадочных, метаморфических и магматических горных породах.
Около 10 % всех осадочных пород составляют известняки, сложенные преимущественно кальцитовыми остатками раковин морских организмов. Арагонит является второй по распространённости кристаллической модификацией CaCO3 и в основном формируется в раковинах моллюсков и скелетах некоторых других организмов.
Также арагонит может образовываться и в неорганических процессах, например в карстовых пещерах или гидротермальных источниках.
Фатерит является наименее стабильной разновидностью этого карбоната, и очень быстро превращается в воде либо в кальцит, либо в арагонит. В природе встречается относительно редко, когда его кристаллическая структура стабилизирована теми или иными примесями.
Получение
Подавляющее количество карбоната кальция, добывающееся из полезных ископаемых, используется в промышленности. Чистый карбонат кальция (например, для производства продуктов питания или использования в фармацевтических целях), может быть изготовлен из природного минерала с малым количеством вредных примесей, например, из мрамора.
В лаборатории карбонат кальция может быть приготовлен предварительным гашением оксида кальция — негашеной извести. При этом образуется гидроксид кальция, и затем в суспензию продувается углекислый газ для получения карбоната кальция:
Химические свойства
При нагревании до 900—1000 °C разлагается на кислотный оксид — углекислый газ CO2 и основный оксид — негашёную известь CaO:
Растворяется в воде при избытке углекислого газа образуя кислую соль — гидрокарбонат кальция Ca(HCO3)2:
Из-за этой реакции образуются сталактиты, сталагмиты. Природные подземные воды, обильные углекислом газом, растворяют плохо растворимый карбонат кальция с образованием много лучше растворимого в воде гидрокарбоната кальция, при выделении подземной воды в виде капель с потолков пещер при попадании в воздух с низкой концентрацией углекислого газа происходит обратная реакция превращения гидрокарбоната кальция в плохо растворимый осадок карбоната кальция, образующего красивые природные формы в пещерах, и из-за этого же механизма образуются карстовые пещеры.
При обжиге с температурой свыше 1500 °C с углеродом, например, в форме кокса, образует карбид кальция и угарный газ: