Онкологические аспекты гиперпластических процессов эндометрия
Гиперплазия — это увеличение количества клеток без увеличения их размеров. Гиперпластические процессы могут предшествовать развитию онкологического заболевания. Гиперплазия эндометрия — одна из форм патологических пролиферативных изменений эндометрия, с преимущественной пролиферацией железистого компонента по сравнению со стромальным компонентом [1].
Существует гистологическая классификация гиперпластических процессов эндометрия, предложенная ВОЗ (2014) [2]:
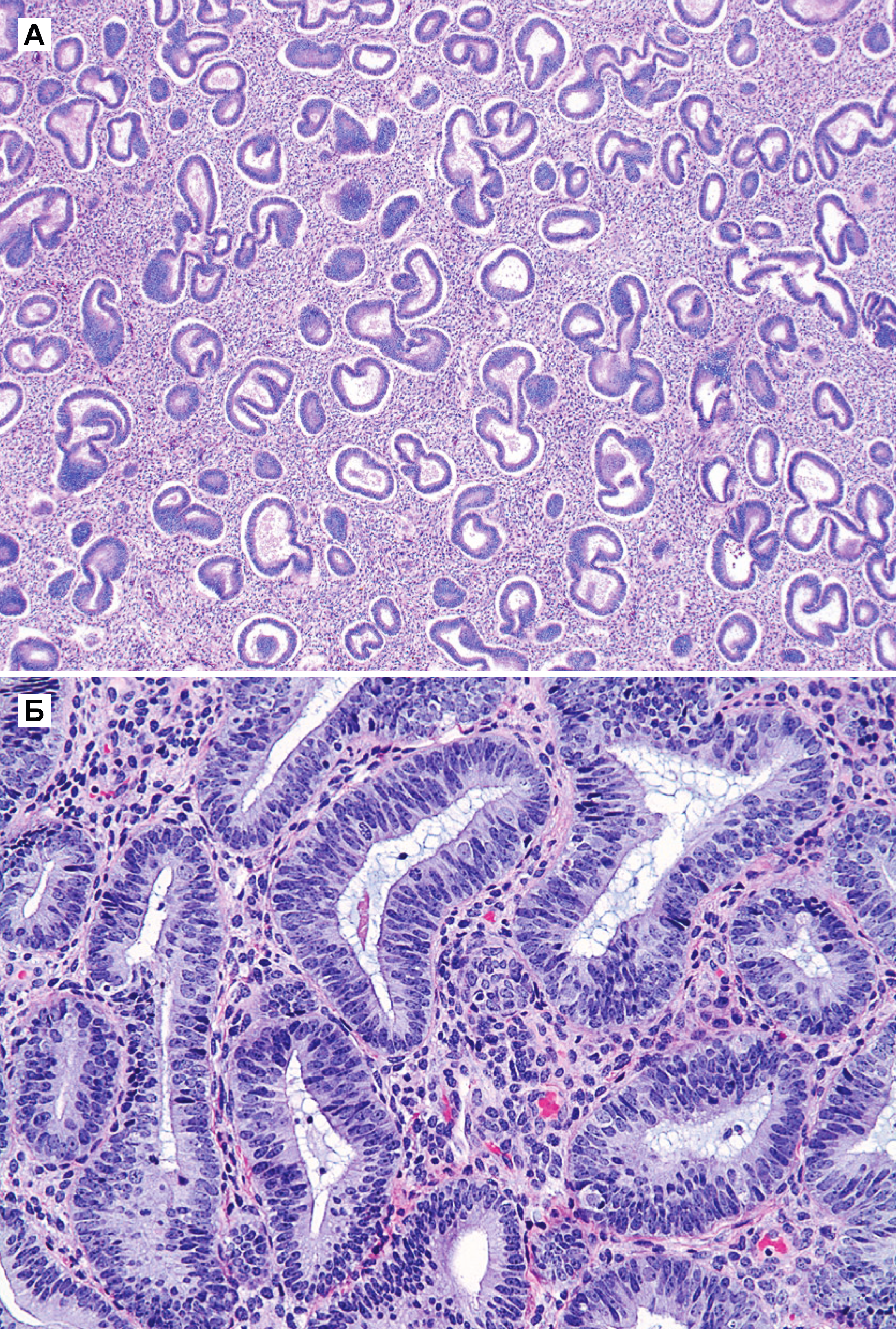
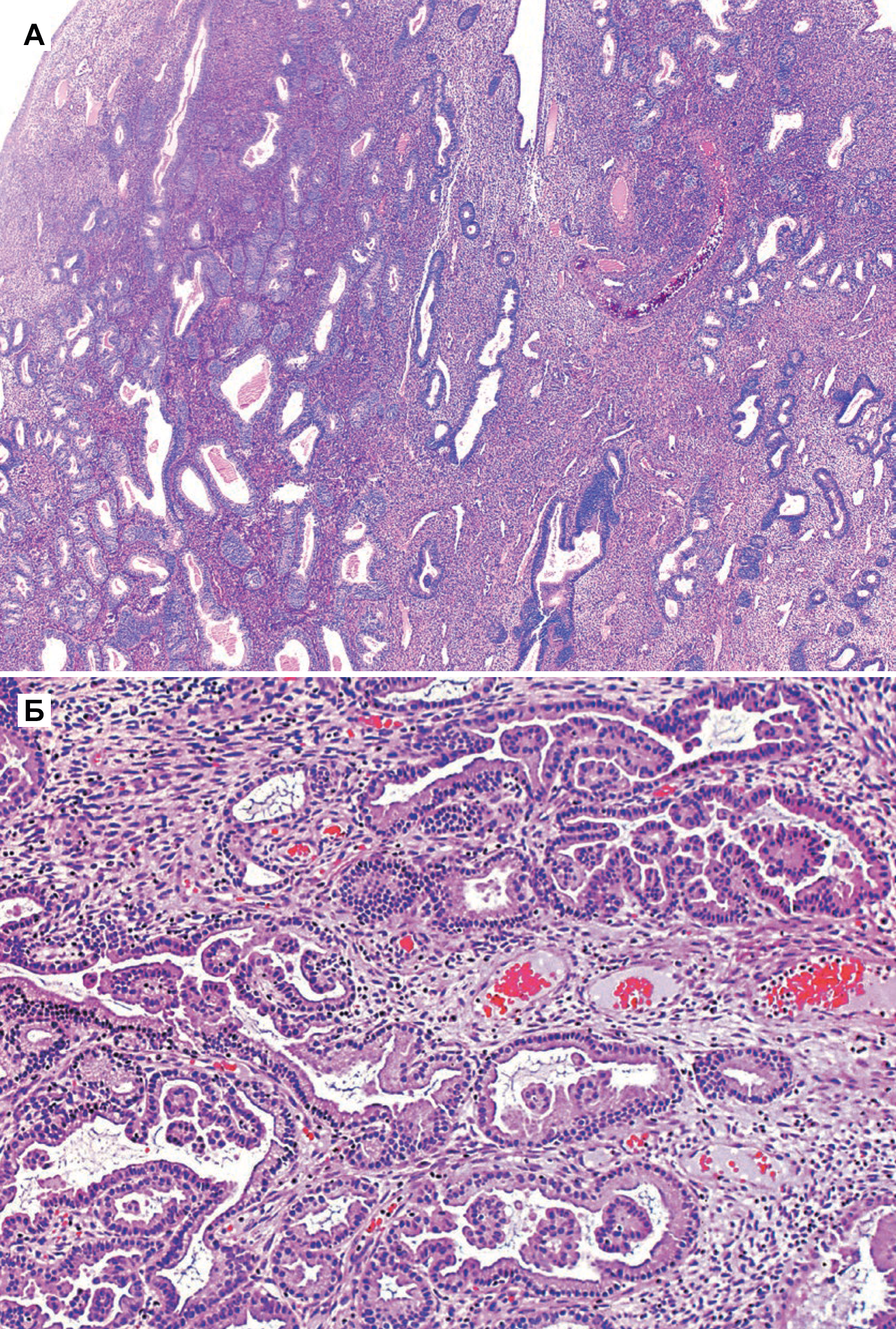
Гиперплазия эндометрия без атипии — это пролиферация с изменением строения желез и клеток, но без клеточной атипии. Изменения в строении обычно видны при малом увеличении, но важной особенностью, которая определяет прогноз и возможность малигнизации — это клеточная атипия. Все типы гиперплазии характеризуются увеличением отношения железы к строме, неравномерностью формы железы и изменением размера железы (рис. 1 а и б). При гиперплазии без атипии железистый эпителий напоминает пролиферирующий эндометрий (рис. 1 б). Клетки столбчатые с амфофильной цитоплазмой и имеют псевдостратифицированные ядра, ориентированы к базальной мембране и имеют овальную форму с гладкими контурами, равномерно распределенный хроматин и небольшие незаметные ядрышки. Митотическая активность может быть переменной и может быть меньше, чем в пролиферирующем эндометрии. Частота митоза не влияет на диагноз [5].
Как правило, гиперплазия диффузная, но может быть очаговой из-за локальных различий в содержании рецепторов эстрогена и прогестерона в эндометрии. При простой гиперплазии присутствует строма в значительном объеме. Строение стромы напоминает нормальное, характерное для пролиферативной фазы, строма состоит из маленьких овальных клеток со скудной цитоплазмой. Как и в железах, в строме отмечена митотическая активность. Когда гиперплазия является полипоидной, строма может содержать артерии с толстой стенкой, подобные тем, которые наблюдаются в полипах. По мере прогрессирования гиперплазии железы располагаются более тесно. Обычно железы плотно прилегают друг к другу, хотя всегда присутствует небольшое количество стромы между ними [5].
К предраковым заболеваниям эндометрия относятся [2]:
Эндометрий — мишень половых гормонов, так как эта ткань имеет специфические рецепторы. Клетки эндометрия обновляются ежемесячно под влиянием гормональной регуляции. Нарушение гормонального статуса женщины может изменять рост и дифференцировку клеток. Поэтому могут возникнуть гиперпластические процессы [2].
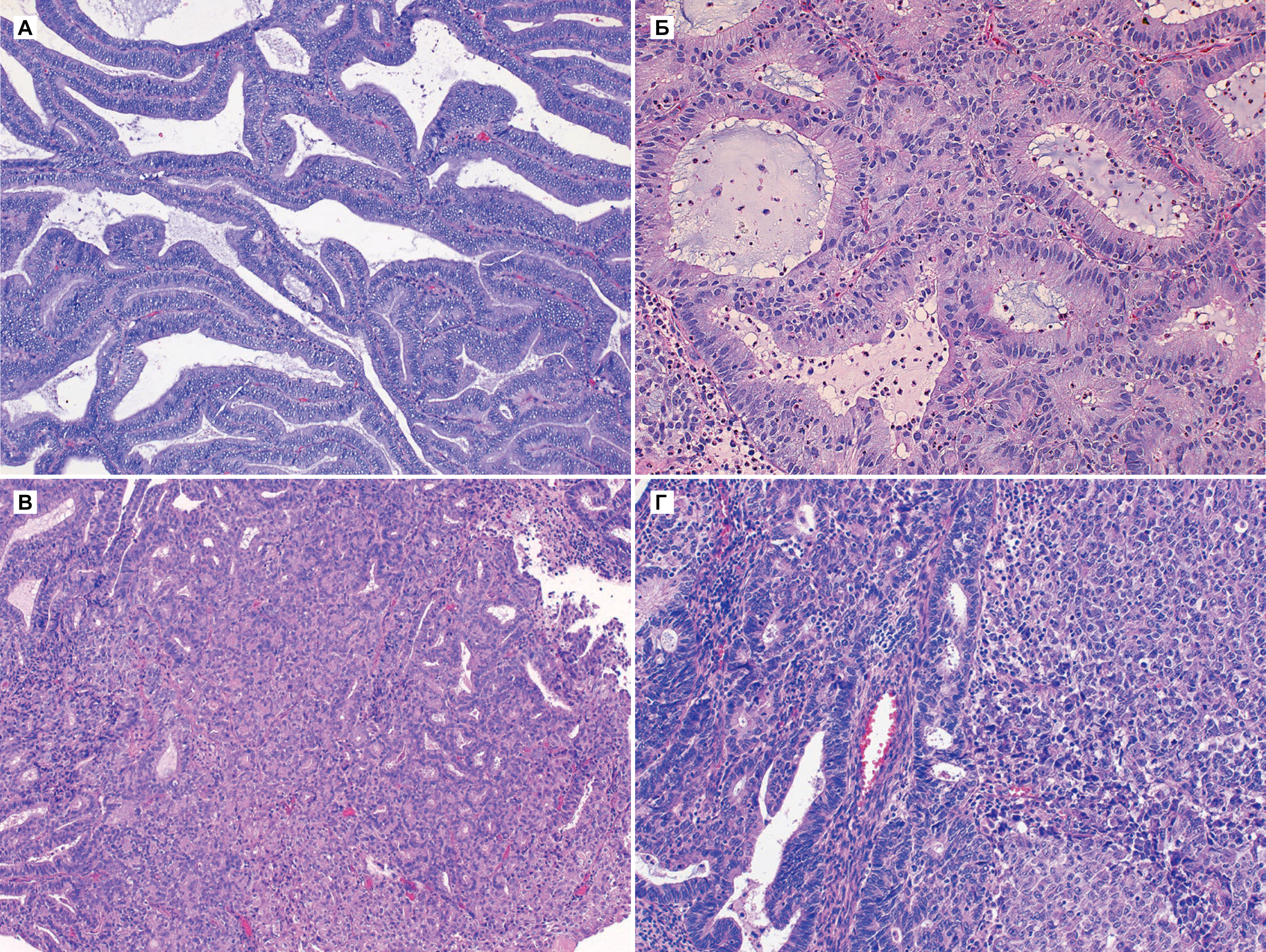
Атипичная гиперплазия отличается наличием ядерной атипии и сложным строением с тесно расположенными железами. Железы обычно неправильной формы и размера. Каждая железа имеет базальную мембрану, окруженную тонким слоем стромы, отделяющей его от соседних желез. Однако в некоторых случаях железы расположены далеко друг от друга. Встречаются как железы без клеточной атипии, так и атипичные [5].
Специфические особенности при атипичной гиперплазии включают: стратификацию, увеличение размера ядер с измененным хроматином и ядрышками. В ядрах отмечена истинная стратификация (2–4 слоя), и потеря ориентирования к базальной мембране [5].
На фоне гиперпластических процессов в эндометрии, возникающих при длительной пролиферации желез эндометрия без перехода их в секреторную фазу, может развиваться рак тела матки (РТМ) — это злокачественная опухоль, происходящая из слизистой оболочки тела матки (эндометрия). Чаще всего РТМ носит спорадический характер, и в 5 % случаев РТМ ассоциирован с наследственными синдромами, например, с синдромом Линча. Среди факторов риска: гиперэстрогения, ранние менархе, отсутствие родов в анамнезе, поздняя менопауза, возраст старше 55 лет, применение тамоксифена [3].
Эпидемиология РТМ
РТМ — самая частая злокачественная опухоль женских половых органов в развитых странах и вторая по частоте после рака шейки матки злокачественная опухоль женских половых органов в мире. В США в 2015 г. зарегистрировано более 54800 новых случаев заболевания РТМ, и более 10150 смертей от этого заболевания. В России ежегодно регистрируется более 21 тысячи больных РТМ. В структуре заболеваемости женского населения в России в 2016 г. РТМ занимал 3-е ранговое место (7,7 %). Средний возраст заболевших РТМ в России составляет 62,6 года [3,4].
Патогенез
Развитие РТМ обусловлено гиперэстрогенией, основной причиной которой является нарушение овуляции. Клиническое изучение метаболических нарушений у больных раком тела матки и морфологические особенности рака эндометрия позволили обосновать концепцию о двух основных патогенетических вариантах заболевания [2].
I тип (более частый). Опухоль развивается в более молодом возрасте, в отличие от пациенток II патогенетического варианта, на фоне длительной гиперэстрогении и гиперплазии эндометрия. У больных РТМ I патогенетического типа часто наблюдаются ожирение, сахарный диабет и гипертоническая болезнь, возможны эстрогенсекретирующие опухоли яичников или синдром склерокистозных яичников. Опухоли I патогенетического варианта, как правило, высокодифференцированные, имеют более благоприятный прогноз [2].
II тип. Опухоли эндометрия обычно низкодифференцированные, имеют менее благоприятный прогноз. Опухоли II патогенетического типа возникают в более старшем возрасте, в отсутствие гиперэстрогении, на фоне атрофии эндометрия. Примерно у 80% больных РТМ диагностируют эндометриоидную аденокарциному [2].
Выделяют три степени дифференцировки аденокарциномы эндометрия [2]:
G1 — высоко дифференцированная;
G2 — умеренно дифференцированная;
G3 — низко дифференцированная или недифференцированная.
Клиника
Ранний симптом прогрессирования рака эндометрия — появление жидких водянистых белей, нередко с примесью крови, и зуда наружных половых органов. Кровянистые выделения из половых путей бывают в виде мажущих серозно-кровянистых выделений, которые становятся порой обильными. Кровотечение, как правило, контактное или появляется после физической нагрузки [2].
Возможны боли внизу живота, которые на ранних стадиях рака носят схваткообразный характер. Это связано с сокращениями эндометрия и опорожнением матки от скопившейся в ней крови или гноевидной жидкости (гематометра, пиометра), отток которой в результате обтурации внутреннего зева затруднен. После таких схваткообразных болей появляются обильные выделения из матки — гной и кровь. При поздних стадиях боли постоянные, особенно интенсивные по ночам, связаны со сдавлением раковым инфильтратом нервных сплетений в малом тазу. При переходе процесса на мочевой пузырь и прямую кишку появляются симптомы нарушения функционирования этих органов [2].
Хирургическое вмешательство рекомендуется как наиболее эффективный метод лечения РТМ независимо от стадии как самостоятельно, так и в комбинации с другими методами [6].
Список литературы:
Митозы и митотический индекс
Дата создания: Октябрь 27, 2017
Дата изменения: Ноябрь 28, 2017
Митозы и митотический индекс
Новый показатель в гистологическом исследовании
Американский Объединенный комитет по онкологии добавил показатель частоты митозов в протокол клинической диагностики. Показатель митозов заменил другой индекс — уровень проникновения по Кларку для меланом, стадия T1.
Американские ученые (Dermatol Surg. 2011 Aug;37(8):1080-8) поставили задачу оценить необходимость биопсии сторожевых лимфоузлов на основании показателя митотической активности тонких (до 1 мм) меланом.
Что означает митотическая активность при меланоме?
Митоз — процесс деления (размножения клеток). Если в гистологическом препарате удаленной родинки (опухоли) определяются делящиеся клетки, находящиеся в процессе деления (митоза). Митотическая активность (митотический индекс) определяется под микроскопом, как процент делящихся клеток от 1000 клеток препарата (опухоли).
Наличие митозов демонстрирует рост и активность опухоли, а также дает определенный прогноз развития заболевания. Важно применить агрессивное лечение, в случаях, когда в гистологическом препарате определяются митозы. Вовремя проведенное правильное лечение спасает жизнь.
Одним из эффективных способов лечения и предотвращения метастазирования является биопсия сторожевого лимфоузла
Биопсия сторожевого лимфоузла
эффективное лечение и точный прогноз
В исследовании установлена необходимость выполнения биопсии сторожевого лимфоузла при митотическом индексе более 1, при толщине опухоли менее 1 мм. Также необходима биопсия сторожевого лимфоузла в случае изъязвления опухоли, при толщине опухоли менее 1 мм.
Митотический индекс оказался более четким прогностическим критерием, чем глубина проникновения по Кларку, в случае тонких меланом (до 1 мм). Самым точным методом, в этом случае, является биопсия сигнального лимфоузла.
При обнаружении микрометастазов в лимфоузле выполняется удалении регионарных лимфоузлов, что примерно на 20% повышает шанс на полное излечение.
Диагноз — меланома. Что делать?
Немедленно обращайтесь в клинику онкодерматологии Меланома Юнит
Вам будет составлен четкий план действий, в зависимости от предоставленных меддокументов и данных о заболевании
В данном случае промедление может привести к крайне неблагоприятным последствиям, даже в случае если Вам сказали только наблюдаться. На данный момент, в России биопсия сигнальных лимфоузлов при меланоме еще не выполняется
В большинстве случаев меланома поддается правильному лечению, на ранних стадиях практически гарантированно полное выздоровление.
Митозы в эпителии что это
Опухолевые клетки отличаются от нормальных нарушениями прочной сопряженности между процессами роста и дифференцировки [9]. Увеличение темпа воспроизводства озлокачествленных клеток обеспечивается не столько через укорочение митотического цикла, сколько за счет возрастания количества тех элементов, которые вместо достижения терминальной степени дифференцировки остаются во фракции роста [6, 11, 13]. В качестве еще одного механизма немалую роль играет «карикатурная» сигнальная связь, то есть нарушенная интеграция между малигнизированными клетками, проходящими через этапы дифференцировки, и микроокружением [2, 4]. Достигнут значительный прогресс в области изучения морфофункциональных особенностей слизистой оболочки желудка при предраке и раке, отчасти связанный с развитием высокочувствительных способов выявления в гистологических срезах отдельных тканевых и клеточных компонентов [1, 3]. Однако многие аспекты структурно-метаболической перестройки слизистой оболочки желудка при ее малигнизации остаются предметом дискуссий, и поиск изменений, предшествующих возникновению опухоли, по-прежнему актуален [5, 10].
Материал и методы исследования
Срезы окрашивали гематоксилином и эозином в комбинации с реакцией Перлса, по ван Гизону с окраской эластических волокон резорцин-фуксином Вейгерта, ставили ШИК-реакцию. Полутонкие срезы окрашивали реактивом Шиффа и азуром II. Исследования проводили в универсальном микроскопе Leica DM 4000B (Германия). Ультратонкие срезы, контрастированные уранилацетатом и цитратом свинца, исследовали в электронном микроскопе JEM 1010 при ускоряющем напряжении 80 кВт.
Результаты исследования и их обсуждение
Светооптическое исследование первичных опухолей пациентов 1-й группы выявило превалирование зрелых форм аденокарцином, характеризующихся формированием папиллярных и тубулярных железистых структур, умеренно выраженной тканевой и клеточной атипией, появлением патологических митозов, в разной степени выраженными фиброзными изменениями стромы. В низкодифференцированной аденокарциноме среди обширных скоплений опухолевых клеток или фиброзных полей с трудом обнаруживались мелкие железы, степень анаплазии опухолевых клеток возрастала. Перстневидно-клеточный рак отличался диффузным распределением клеток типичной перстневидной формы и, как правило, отсутствием десмопластической реакции стромы.
Особый интерес представляло изучение состояния слизистой оболочки желудка в отдаленных от опухоли участках. При кишечном типе рака светооптическое исследование фрагментов пилорического отдела желудка во всех наблюдениях выявило наличие распространенной неполной кишечной метаплазии. Обращала на себя внимание атрофия слизистой оболочки, иногда выраженная, с заметным истончением собственной пластинки, дистрофическими изменениями покровно-ямочного эпителия и уменьшением количества желез [7]. Диспластические изменения эпителия от слабой до тяжелой степени (увеличение ядерно-цитоплазматического соотношения, снижение секреции мукоида, псевдомногорядность, повышение митотической активности) обнаружены в большинстве исследованных фрагментов. Характерна многофокусность диспластических изменений, нарастающих по направлению к опухолевому очагу.
В фундальном отделе желудка очаговая кишечная метаплазия эпителиоцитов отмечена у 25% пациентов. Диспластические изменения энтеролизованного и интактного эпителия выявлены в половине наблюдений. Мононуклеарная инфильтрация отличалась слабой интенсивностью и поверхностной локализацией. В целом, патологические изменения в фундальном отделе желудка носили менее выраженный характер по сравнению с пилорическим отделом.
При изучении регионарных лимфатических узлов обращали внимание на наличие, размер и множественность метастазов. У пациентов с аденокарциномами метастазы в лимфатических узлах обнаружили у 37% больных.
Таким образом, светооптическое исследование первичных опухолей желудка пациентов 1-й группы выявило преобладание зрелых форм аденокарцином, характеризующихся формированием капиллярных и тубулярных железистых структур, умеренно выраженной тканевой и клеточной атипией. В большинстве случаев зрелых аденокарцином опухолевый очаг хорошо отграничен от окружающих тканей стенки желудка. Перстневидно-клеточный рак отличался диффузным распределением изолированных округлой формы клеток, содержащих в цитоплазме большое количество слизи. Опухоль характеризовалась инфильтративным ростом и была плохо отграничена от окружающих тканей [8, 12].
Новообразования у пациентов 2-й группы состояли из полиморфных либо мономорфных по составу анапластических клеток, располагающихся в виде тяжей, комплексов, или изолированно друг от друга. Клеточные ядра различались по основным светооптическим характеристикам: форме, размерам, окраске. Наиболее часто в клетках недифференцированного рака желудка встречались крупные гиперхромные угловатой формы ядра, а также небольшие светлые пузырьковые ядра. Цитоплазма была, как правило, скудная и плохо различима. Анализ частоты и выраженности патологических изменений нетрансформированной слизистой оболочки обнаружил их сходство с перифокальными процессами при диффузном типе карцином в первой группе наблюдений, что свидетельствует об определенном гистогенетическом единстве этих вариантов рака желудка. Ведущим патологическим изменением являлась дисплазия генеративных зон желудочного эпителия на фоне атрофически-склеротических процессов. Метастазы в регионарных лимфатических узлах обнаружены у 38% пациентов, что соответствует аналогичному показателю в первой группе.
Таким образом, светооптическое исследование опухолей желудка пациентов 2-й группы выявило наличие недифференцированного рака с солидным или скиррозным характером роста. Опухолевый очаг был плохо отграничен от окружающих тканей стенки желудка, отличался инфильтративным ростом и латеральным распространением опухоли по подслизистому слою.
Смешанные формы (3-я группа) сочетали в одном опухолевом очаге участки аденокарцином с различной степенью дифференцировки (часто с перстневидными клетками) либо разные патогистологические варианты рака желудка. Морфологическая картина отражала направление «дедифференцировки» клеточных популяций от центра к периферии опухоли. Практически во всех исследованных случаях карцинома распространялась в глубь желудочной стенки, инвазируя подслизистый, мышечный, иногда серозный слои, в ряде наблюдений комплексы раковых клеток выявлялись в большом сальнике или брыжейке поперечной ободочной кишки.
В слизистой оболочке вне опухолевого очага у 60% пациентов имелась кишечная метаплазия, ограниченная пилорическим отделом желудка; с такой же частотой встречались атрофия, склероз и густая полиморфно-клеточная инфильтрация. Наличие метастазов в регионарных лимфатических узлах выявлено у 60% оперированных больных этой группы, что значительно превышало данные первых двух анализируемых групп.
Таким образом, светооптический анализ перифокальных процессов в слизистой оболочке при различных патогистологических формах рака желудка показал, что при высоко- и умереннодифференцированных аденокарциномах наиболее типичными изменениями являются распространенная неполная кишечная метаплазия и ассоциированная с этими участками дисплазия на фоне диффузной атрофии эпителия. При низкодифференцированной и перстневидно-клеточной аденокарциномах, а также при недифференцированном раке желудка на первый план выходят атрофические изменения слизистой оболочки и дисплазия генеративных зон эпителия [14].
Электронно-микроскопический анализ аденокарциномы желудка выявил множественные патологические изменения ультраструктуры малигнизированных клеток: большие, неправильной формы ядра с изрезанными контурами и неравномерным распределением крупноглыбчатого гетерохроматина в кариоплазме, увеличенным количеством ядрышек, иногда атипичными митозами.
При перстневидно-клеточном раке желудка преобладали опухолевые клетки с переполненной секреторными гранулами цитоплазмой и эксцентрически расположенным ядром аномальной формы. Слизистая оболочка желудка вне опухолевого очага отличалась мозаичностью ультраструктурной картины. В очагах кишечной метаплазии, кроме типичных покровно-ямочных эпителиоцитов, обнаружены также каемчатые и бокаловидные клетки, цитоплазма которых была переполнена крупными электронно-прозрачными глобулами слизи, а уплощенные ядра оттеснены к базальному полюсу клеток. На апикальной поверхности каемчатых эпителиоцитов выявлялись высокие, нерегулярно расположенные микроворсинки. В цитоплазматическом матриксе большое число митохондрий и развитая гранулярная цитоплазматическая сеть. Отражением атрофических процессов в слизистой оболочке желудка было наличие большого числа эпителиоцитов, почти лишенных микроворсинок, имеющих электронно-плотную цитоплазму с едва различимыми органеллами. В дистрофически измененных клетках покровно-ямочного эпителия наблюдалось уменьшение количества секреторных мукоидных гранул, среди которых преобладали незрелые, с плотным содержимым и неровными контурами. Диспластические изменения эпителиоцитов выражались в увеличении размеров ядер, появлении крупных ядрышек, значительном снижении содержания внутриклеточного муцина.
При недифференцированном раке желудка преобладали атипичные клетки с гладкими, лишенными микроворсинок контурами. Клеточные ядра отличались большими размерами, с глубокими инвагинациями в нуклеолемме, придающими ядру причудливую двухлопастную или трехлопастную форму. Изучение желудка при недифференцированном раке на отдалении от первичной опухоли показало высокую степень развития атрофически-склеротических процессов слизистой оболочки и наличие диспластических изменений эпителия, ассоциированных с генеративными зонами (желудочные ямки, верхние отделы шеек желез). Неполная кишечная метаплазия носила очаговый характер и была ограничена, как правило, пилорическим отделом желудка. Анализ частоты и выраженности патологических изменений нетрансформированной слизистой оболочки при недифференцированном раке выявил их сходство с перифокальными процессами при диффузном типе карцином в первой группе наблюдений, что свидетельствует об определенном гистогенетическом единстве этих вариантов рака желудка.
Ультраструктурный анализ карцином желудка со смешанным типом строения подтвердил полиморфизм тканей и клеточную атипию, обнаруженные при светооптическом исследовании. В участках опухоли обнаружили злокачественные клетки с признаками секреции слизи в виде различных по размеру гранул, содержащих муцин. При снижении уровня дифференцировки по направлению к периферии опухоли наблюдалось прогрессирующее изменение ядерно-цитоплазматического соотношения в сторону увеличения размеров ядер. В слизистой оболочке желудка на отдалении от опухолевого очага в ряде случаев отсутствовали патологические изменения покровно-ямочного эпителия. По мере приближения к опухолевому очагу нарастала выраженность и гетерогенность изменений эпителиальных структур слизистой оболочки желудка. Анализ перифокальных процессов в окружающей слизистой оболочке желудка выявил меньшую распространенность и частоту предраковых изменений (дисплазии, неполные кишечные метаплазии и атрофии эпителия), чем в других исследованных группах пациентов. В целом, это свидетельствует о более высоких темпах опухолевой прогрессии смешанных форм карцином желудка.
Проведен комплексный морфологический анализ, включающий световую и электронную микроскопию опухолевых очагов, нетрансформированной слизистой оболочки, и регионарных лимфатических узлов при раке желудка. По результатам микроскопического исследования слизистой оболочки желудка на отдалении от опухолевого очага у пациентов с высоко- и умереннодифференцированными карциномами желудка установлено, что наиболее типичными изменениями являются распространенная неполная кишечная метаплазия и ассоциированная с этими участками дисплазия. В прилежащих к опухоли участках слизистой оболочки нередко обнаруживалась неравномерная гиперплазия эпителия. При низкодифференцированной и перстневидно-клеточной карциномах, а также при недифференцированном раке желудка на первый план выходит дисплазия генеративных зон эпителия; неполная кишечная метаплазия носит очаговый характер.
Цитологическая диагностика заболеваний щитовидной железы
Полный текст:
Аннотация
Цитологическая диагностика различных заболеваний человека широко применяется в современной медицине, особенно для ранней дооперационной диагностики новообразований разных органов и тканей. Тонкоигольная аспирационная пункционная биопсия с последующим микроскопическим исследованием ее цитограммы — одна из интегральных частей диагностической цитологии, в том числе при диагностике заболеваний щитовидной железы (ЩЖ). Методы, используемые для верификации различных вариантов тиреоидной патологии (пальпация, ультразвуковое исследование — УЗИ, сцинтиграфия, биохимические и иммунологические тесты и др.), далеко не всегда позволяют уточнить характер патологических изменений в ЩЖ. Например, холодные узлы (по данным сканирования) лишь в части случаев оказываются злокачественными новообразованиями ЩЖ, как и основная масса узловых зобов у больных из регионов, эндемичных по зобу; в большинстве случаев нет нужды в их оперативном удалении. И только микроскопическое исследование пунктатов ЩЖ, особенно ее узловых образований, позволяет уточнить диагноз и принять адекватное решение о характере лечебных мер. Тонкоигольная аспирационная пункционная биопсия ЩЖ относится к неинвазивным морфологическим диагностическим средствам, позволяющим практически со 100 % долей вероятности поставить правильный диагноз. Вместе с тем, поскольку ЩЖ является эпителиальным органом, в структурах которого клетки тесно «спаяны» между собой, клеточные связи рвутся с трудом, что крайне затрудняет получение информативного материала для последующего микроскопического исследования. Для облегчения процесса получения материала на иглу, которой производят пункционную биопсию, в Эндокринологическом научном центре РАМН стали наносить насечки на расстоянии примерно 0,5—0,7 см от острого конца иглы (канд. мед. наук А. В. Антонов), что позволяет брать материал, как гарпуном, без аспирации и получать обильный пунктат. При ишемизации пунктируемого участка железы удается получить обильный пунктат практически без примеси периферической крови (канд. мед. наук И. В. Пантелеев). Полученный таким образом материал наносят на обезжиренное предметное стекло и с помощью шлифованного предметного стекла получают мазок (аналогично мазку крови). Высушенные на воздухе мазки окрашивают по Маю—Грюнвальду— Гимзе. Ежегодно мы исследуем от 1,5 до 2,5 тыс. пункционных биопсий от больных с различной патологией. Информативность полученного материала во многом зависит от опыта и умения хирурга. Скудные пунктаты, как правило, малоинформативны и позволяют лишь описать пунктат без заключения о характере патологических изменений в ЩЖ. Обильные клеточные пунктаты из разных точек железы, особенно при подозрении на диффузную и (или) сочетанную патологию, дают возможность поставить окончательный диагноз.
Ключевые слова
Для цитирования:
Бронштейн M.Э. Цитологическая диагностика заболеваний щитовидной железы. Проблемы Эндокринологии. 1997;43(3):30-38. https://doi.org/10.14341/probl10393
For citation:
Bronstein M.E. Cytological diagnosis of thyroid disease. Problems of Endocrinology. 1997;43(3):30-38. (In Russ.) https://doi.org/10.14341/probl10393
Цитологическая диагностика различных заболеваний человека широко применяется в современной медицине, особенно для ранней дооперационной диагностики новообразований разных органов и тканей. Тонкоигольная аспирационная пункционная биопсия с последующим микроскопическим исследованием ее цитограммы — одна из интегральных частей диагностической цитологии, в том числе при диагностике заболеваний щитовидной железы (ЩЖ). Методы, используемые для верификации различных вариантов тиреоидной патологии (пальпация, ультразвуковое исследование — УЗИ, сцинтиграфия, биохимические и иммунологические тесты и др.), далеко не всегда позволяют уточнить характер патологических изменений в ЩЖ. Например, холодные узлы (по данным сканирования) лишь в части случаев оказываются злокачественными новообразованиями ЩЖ, как и основная масса узловых зобов у больных из регионов, эндемичных по зобу; в большинстве случаев нет нужды в их оперативном удалении. И только микроскопическое исследование пунктатов ЩЖ, особенно ее узловых образований, позволяет уточнить диагноз и принять адекватное решение о характере лечебных мер. Тонкоигольная аспирационная пункционная биопсия ЩЖ относится к неинвазивным морфологическим диагностическим средствам, позволяющим практически со 100 % долей вероятности поставить правильный диагноз. Вместе с тем, поскольку ЩЖ является эпителиальным органом, в структурах которого клетки тесно «спаяны» между собой, клеточные связи рвутся с трудом, что крайне затрудняет получение информативного материала для последующего микроскопического исследования. Для облегчения процесса получения материала на иглу, которой производят пункционную биопсию, в Эндокринологическом научном центре РАМН стали наносить насечки на расстоянии примерно 0,5—0,7 см от острого конца иглы (канд. мед. наук А. В. Антонов), что позволяет брать материал, как гарпуном, без аспирации и получать обильный пунктат. При ишемизации пунктируемого участка железы удается получить обильный пунктат практически без примеси периферической крови (канд. мед. наук И. В. Пантелеев). Полученный таким образом материал наносят на обезжиренное предметное стекло и с помощью шлифованного предметного стекла получают мазок (аналогично мазку крови). Высушенные на воздухе мазки окрашивают по Маю—Грюнвальду— Гимзе. Ежегодно мы исследуем от 1,5 до 2,5 тыс. пункционных биопсий от больных с различной патологией. Информативность полученного материала во многом зависит от опыта и умения хирурга. Скудные пунктаты, как правило, малоинформативны и позволяют лишь описать пунктат без заключения о характере патологических изменений в ЩЖ. Обильные клеточные пунктаты из разных точек железы, особенно при подозрении на диффузную и (или) сочетанную патологию, дают возможность поставить окончательный диагноз.
Наш многолетний опыт исследования пунктатов ЩЖ в сопоставлении в значительной части случаев с результатами последующего гистологического исследования операционного материала у тех же больных, а также с данными литературы позволяет нам описать подходы к оценке исследуемого пунктата и микроскопические критерии, в том числе цитологические, для диагностики известных заболеваний ЩЖ.
При микроскопическом исследовании окрашенных мазков пунктатов ЩЖ следует учитывать количество полученного материала, его клеточный состав, наличие коллоида, его состояние (плотность — густой, жидкий). При оценке паренхиматозного компонента пунктата — тиреоцитов (фолликулярных, или так называемых А-кле- ток) — следует учитывать их форму и размеры; моно- или полиморфность; изолированные они или формируют агрегаты; количество клеток в агрегате, отражающее пролиферативную активность клеток; особенности агрегатов и скоплений; наличие тяжей, клеточных шаров. Исследуя тиреоциты, нужно обращать внимание на текстуру цитоплазмы, ее окрашиваемость, наличие включений (их особенности и окрашиваемость), на признаки, отражающие функциональную активность клетки, в том числе на число, размеры и форму ядер, их положение в клетке; характер хроматина, распределение и окрашиваемость его частиц; наличие ядрышек, цитоплазматических включений, вакуолей, фигур митоза и признаков амитотического деления и оценивать ядерно-плазменное отношение. Особое внимание следует обращать на признаки, отражающие реакцию организма на патологический процесс: наличие транссудата, экссудата, фибрина, некротических масс, детрита, признака дистрофических изменений клеток; на присутствие крови в пунктате и ее происхождение — из кровеносных сосудов железы или из очагов кровоизлияний в ней. При правильном проведении пункционной биопсии и ишемизации пунктируемого участка периферическую кровь, как правило, берут только при диффузном токсическом зобе (ДТЗ), когда железа необычайно богато васкуляризирована. Наличие периферической крови в пунктате ЩЖ при ДТЗ — важный критерий в цитологической диагностике этого заболевания. Напротив, присутствие крови из очага кровоизлияния (измененные эритроциты, отсутствие среди них лейкоцитов, наличие макрофагов, в том числе гемосидерофагов) является, хотя и косвенным, но все же достоверным признаком наличия узла в железе, чаще всего — узлового зоба, реже — аденомы и еще реже — рака, хотя во всех этих случаях кровоизлияния могут иметь место. Реже всего они возникают при диффузных изменениях в железе, причем только в просвете кистозно-расширенного фолликула.
При обнаружении патологических (атипичных) клеток следует прежде всего определить их тип (тканевую принадлежность), изолированные они или формируют комплексы, взаимосвязь клеток в комплексах, в частности наличие признаков разобщения (дискомплексации) клеток; типы формируемых комплексов и структур, форму и размеры клеток и их ядер, ядерно-плазменное отношение, особенности цитоплазмы и ее тинкториальные свойства, наличие включений в цитоплазме, их число, размеры и тинкториальные свойства, характер распределения в цитоплазме; особенности ядер (форма, размеры, локализация); характер окрашивания хроматина, наличие ядрышек и их особенности, наличие цитоплазматических включений в ядрах, фигур митоза и другие особенности, способные дать информацию для решения вопроса о характере патологических изменений в железе, по крайней мере в пропунктированном образовании или фокусе.
Цитологическая диагностика заболеваний ЩЖ должна базироваться на данных макро- и микроскопического исследования пунктатов в сопоставлении с результатами клинического обследования, УЗИ и гормональными проявлениями заболевания. Цитологический и морфологический диагнозы по сути являются клинико-патологическим диагнозом. Несовпадение же клинического и цитологического диагнозов является результатом либо неадекватной оценки клинических и лабораторных проявлений заболевания, либо неадекватной оценки цитограммы пунктата, либо (что чаще всего имеет место) того, что патология ЩЖ сочетанная, оказывающая взаимное влияние друг на друга, в связи с чем клинические и лабораторные проявления оказываются как бы ’’смазанными», не отражающими истинный характер патологических изменений в железе. Так, аутоиммунный тиреоидит (АИТ), особенно атрофический вариант, на фоне которого имеются узловой токсический зоб или токсическая аденома, как правило, не сопровождается признаками нарушения функции ЩЖ (дефицит гормонов ЩЖ вследствие АИТ нивелируется избытком гормонов, вырабатываемых гиперфункцио- нирующим узлом), вследствие чего на периферии отсутствуют проявления нарушения гормонального статуса. В таких ситуациях только при сканировании в ЩЖ обнаруживают горячий (токсический) узел на фоне непоглощающей радиофармпрепарат тиреоидной ткани. УЗИ ЩЖ у таких больных выявит наличие узлового зоба или аденомы на фоне АИТ, но не объяснит отсутствия каких-либо клинических и лабораторных признаков нарушения функции ЩЖ. И только цитологическое исследование пунктатов обеих долей ЩЖ и пальпируемого узлового образования позволит поставить окончательный диагноз: АИТ в сочетании с узловым токсическим зобом (или токсической аденомой).
Цитологическая верификация заболеваний ЩЖ должна базироваться прежде всего на современной общепринятой классификации тиреоидной патологии, в соответствии с которой различают следующие ее варианты.
а) узловой зоб: солитарный, многоузловой или конгломератный, когда узлы интимно спаяны между собой; б) диффузный зоб;
г) смешанный зоб (диффузно-узловой или многоузловой).
а) болезнь Грейвса (ДТЗ, базедова болезнь);
б) АИТ (разнообразные клинические и морфологические варианты).
а) эмбрионального строения (солидного, трабекулярного, тубулярного);
б) микрофолликулярного строения;
в) фетального строения (характеризуется наличием участков, образованных микрофолликулами, разбросанными по рыхлой строме, чаще в центре узла; по периферии — фолликулы с коллоидом нормального диаметра);
г) фолликулярного строения (только из В-клеток);
д) папиллярного строения, в том числе папиллярные цистаденомы.
а) папиллярные раки;
б) фолликулярные раки;
в) смешанные папиллярно-фолликулярные раки;
г) низкодифференцированные, недифференцированные или анапластические раки.
а) С-клеточные аденокарциномы разнообразного строения;
б) медуллярный рак, нередко с амилоидозом стромы.
Зобная болезнь, возникающая вследствие дефицита йода, характеризуется прежде всего гипертрофией ЩЖ за счет как ее диффузного увеличения, так и формирования в ней узлов. Известны 2 основных механизма гипертрофии ЩЖ при дефиците йода — накопление коллоида в фолликулах и пролиферация фолликулярных клеток, степень выраженности которой зависит от уровня тиреотропного гормона в крови. Накопление коллоида приводит к растяжению фолликулов и уплощению фолликулярных клеток; при преобладании такого процесса развивается так называемый коллоидный зоб. При гиперстимуляции фолликулярных клеток тиреотропным гормоном усиливается пролиферация тиреоцитов; дифференцировки фолликулов не происходит или формируются мелкие фолликулы без коллоида, в результате развивается так называемый паренхиматозный зоб. Чаше всего мы сталкиваемся со смешанными вариантами зобов — коллоидными, в разной степени пролиферирующими. При пунктировании ЩЖ с такими зобами получают коллоид разной плотности (чаще густой) и тиреоциты. Соотношение этих компонентов отражает морфологический тип зоба: при преобладании коллоида говорят о коллоидном зобе, а при наличии значительного количества тиреоцитов, особенно с признаками пролиферации, — о пролиферирующем коллоидном зобе. При этом степень выраженности пролиферации весьма разнообразна — от частичной до резко выраженной. Подобное строение могут иметь как диффузные, так и узловые зобы. Цитологическими признаками пролиферации тиреоцитов являются обилие клеток, наличие укрупненных фолликулярных клеток с достаточно крупными молодыми ядрами; наличие 2 ядерных клеток и более; формирование такими клетками папиллярных и микрофолликулярных структур. Фигуры митоза никогда не встречаются.
Рис. I. Кистозный коллоидный узловой зоб. В пунктате — геморрагическая кистозная жидкость с примесью коллоида (в ячейках «сети» кистозной жидкости).
Отличительной особенностью узловых зобов является наличие собственной капсулы, отсутствующей в случае фокальных зобных изменений в ЩЖ. Цитологически верифицировать клетки, принадлежащие капсуле узла, невозможно. Поэтому цитологическая диагностика узлового зоба базируется на наличии признаков регрессивных изменений, которые часто возникают в них и крайне редко — в диффузных зобах. При пункти- ровании узлового зоба с регрессивными изменениями обычно получают кистозную жидкость с примесью коллоида (рис. 1). Микроскопически она выглядит по-разному: она может не окрашиваться, о ее присутствии судят по «сети» из складов, возникающих в результате денатурации белков при фиксации мазков; в складках обычно располагаются измененные эритроциты и гемоси- дерофаги. Примесь коллоида обусловливает окрашивание кистозной жидкости, причем тем интенсивнее, чем гуще коллоид. Геморрагическая кистозная жидкость характеризуется обилием измененных и (или) лизированных эритроцитов и ге- мосидерофагов (см. рис. 1). По соотношению сохранившихся, измененных и лизированных эритроцитов можно судить о давности кровоизлияния.
Цитологически, как и гистологически, удается верифицировать узловые зобы разнообразного строения: коллоидные, в пунктате которых преобладает густой коллоид, а эпителиальный компонент представлен небольшим количеством уплощенных и (или) мелких кубических тиреоцитов без признаков пролиферации; коллоидные, частично пролиферирующие узловые зобы, в которых эпителиальный компонент выражен в большей степени, чем в предыдущем варианте, часть клеток — с признаками пролиферации; пролиферирующий коллоидный зоб (эпителиальные клетки многочисленные, основная их часть или все они с признаками пролиферации). Во всех этих случаях могут иметь место выраженные в разной степени регрессивные изменения, приводящие к кистозной дегенерации узлов. Подобные морфологические варианты характерны и для диффузных зобов, которые верифицируются по сходству цитограмм пунктатов из обеих долей и отсутствию выраженных регрессивных изменений в сопоставлении с данными пальпации и УЗИ ШЖ.
Рис. 2. ДТЗ. В пунктате — секретирующий эпителий (капли секрета в апикальной части отдельных клеток и внеклеточно).
Ув. 200.
При различных вариантах зобной болезни в ЩЖ нередко наблюдаются морфологические признаки аутоиммунного процесса. Сводятся они обычно к очаговой лимфоидной инфильтрации стромы железы и реже — узловых зобов без признаков повреждения их паренхимы. Эти инфильтраты, как правило, немногочисленные, небольшие, представлены в основном зрелыми лимфоцитами. В этих случаях следует отмечать лишь факт лимфоидной инфильтрации стромы доли и (или) узла.
Цитологически удается разграничивать и известные морфологические варианты АИТ: классический (зоб Хашимото, хронический АИТ), хронический лимфоматозный тиреоидит, фиброзный тиреоидит и хронический лимфоматозный и(или) фиброзный струмит (аутоиммунный процесс, возникающий на фоне предсушествуюшей струмы). Классический вариант (рис. 4) характеризуется обильным клеточным пунктатом практически без примеси коллоида, представленным лимфоидными элементами различной степени зрелости с примесыо иммунобластов, плазматических клеток; фагоцитирующими гистиоцитами (макрофагами), в цитоплазме которых обнаруживаются остатки клеток, ядер и т. д.; единичными многоядерными гигантскими клетками типа клеток инородных тел; стромальными клетками или их ядрами; немногочисленными гистиоцитами и разнообразным, чаще небольшим, количеством тиреоцитов, основную массу которых могут представлять клетки Ашкенази (синонимы: клетки Гюртле, онкоциты, эозинофильные клетки, оксифильные клетки). Во всех случаях наблюдается преобладание лимфоидных элементов над эпителиальным компонентом.
Рис. 3. ДТЗ с явлениями хронического лимфоматозного струмита. В пунктате — обилие тиреоцитов и примесь лимфоидных элементов и стромальных клеток.
Рис. 4. АИТ, классический вариант. Пунктат обильный, представлен иммунобластами, лимфоцитами разной степени зрелости и плазматическими клетками.
В отличие от классического варианта АИТ хронический лимфоматозный тиреоидит (другой морфологический вариант АИТ) характеризуется более скудным пунктатом, представленным в основном зрелыми лимфоцитами с небольшой примесью клеток светлых центров лимфоидных фолликулов, большим количеством стромальных клеток и числом тиреоцитов, примерно равным числу элементов, основная масса которых уплощена и с признаками дистрофических изменений или трансформирована в клетки Ашкенази. В пунктате встречаются различного размера глыбки плохо окрашивающегося коллоида.
Для фиброзного варианта АИТ характерен прежде всего скудный пунктат, представленный небольшим количеством лимфоидных клеток, большей частью зрелых лимфоцитов, плазматических клеток, таким же количеством стромальных клеток или их ядер и еще меньшим числом эпителиальных клеток (тиреоцитов) — плоских, кубических или низких цилиндрических; коллоид встречается редко.
Хронический лимфоматозный струмит — вариант АИТ на фоне предсуществующего зоба, прежде всего диффузного или смешанного. Лимфоидная инфильтрация выражена в меньшей степени, чем при классическом варианте АИТ, но представлена теми же структурами и, следовательно, соответствующими лимфоидными стромальными клетками, а паренхиматозный компонент представлен разнообразными тиреоцитами, в том числе пролиферирующими, и разнообразным количеством коллоида разной плотности, отражающими наличие зобных изменений в железе в сочетании с аутоиммунным процессом (рис. 5). Последний может иметь место и в узловых зобах при диффузно-узловых вариантах зоба.
Цитологическая диагностика новообразований ЩЖ (доброкачественных и злокачественных) сложна и ставит перед собой по крайней мере 2 задачи: 1) дифференциальный диагноз с узловым зобом, поскольку любая опухоль подлежит обязательному хирургическому удалению в отличие от узловых зобов; 2) дифференциальный диагноз между доброкачественной и злокачественной опухолью, поскольку объем оперативного вмешательства на ЩЖ зависит от характера роста опухоли.
Рис. 5. Аденома эмбрионального строения (тубулярно-солидного). Пунктат обильный, опухолевые клетки мономорфные с гипертрофированными ядрами.
Рис. 6. Аденома микрофолликулярного строения. Пунктат обильный, опухолевые клетки мономорфные с гипертрофированными ядрами, формируют микрофолликулярные структуры.
Рис. 7. Аденома из клеток Ашкенази с кистозными изменениями. В пунктате на фоне кистозной жидкости с измененными эритроцитами — скопления из клеток Ашкенази — округло-полигональных с округлыми ядрами и мелкозернистой цитоплазмой.
Рис. 8. Папиллярно-фолликулярная аденокарцинома. Пунктат обильный, основная часть клеток изолированные (выраженная дискомплексация), в части ядер — цитоплазматические включения, вакуоли.
По существующим в настоящее время представлениям доброкачественные опухоли из С-кле- ток ЩЖ не формируются.
Злокачественные новообразования ЩЖ представлены в основном раками разной степени дифференцировки из всех типов тиреоидных клеток — А, В и С. Наиболее часто встречаемыми в эндокринологической практике являются раки из А- клеток папиллярного, фолликулярного или смешанного строения, а также фолликулярно-солидные раки. Все они, за исключением папиллярных раков, растущих в кисте, представляют собой фокусы опухолевого роста, лишенные собственной капсулы. При пунктировании этих новообразований получают обильный клеточный материал, цитограмма которого характеризуется большим количеством изолированных клеток или комплексов опухолевых клеток (рис. 8) — гипертрофированных атипичных тиреоцитов с четко выраженными клеточными границами, резко базофильной цитоплазмой, гипертрофированными ядрами, нередко содержащими ядрышки. Ядра молодые, пузыревидые, с нежной хроматиновой сетью, располагаются центрально или эксцентрично в зависимости от формы клетки. В части ядер имеются цитоплазматические включения и структуры, напоминающие спилы ствола дерева (рис. 9), а также вакуоли. В комплексах, представляющих собой обрывки стенок фолликулов, мелкие фолликулы, солидные опухолевые структуры, отмечается выраженная дискомплексация клеток, приводящая к их разобщению, в результате чего в пунктате имеется значительное количество изолированных клеток. Дискомплексация клеток и наличие в ядрах цитоплазматических включений — цитологические признаки, патогномоничные для А-клеточных раков ЩЖ. Для цитограмм пунктатов папиллярных раков характерно также присутствие папиллярных структур и наличие в ядрах, помимо цитоплазматических включений, складок или бороздок вдоль длинной оси ядра. Если опухоль представляет собой склерозирующую аденокарциному, в пунктате встречаются и стромальные клетки, а если опухоль растет в кисте (основная масса папиллярных раков), в пунктате имеется кистозная жидкость с примесью плохо окрашивающегося коллоида. В случае папиллярной цистаденокарциномы — редкого варианта папиллярного рака ЩЖ — диагноз ставят на основании присутствия в пунктате, помимо обрывков опухолевых сосочков с массивной рыхлой стромой, покрытых большей частью одним слоем относительно мелких округло-полигональных опухолевых клеток со всеми описанными выше признаками и подобных изолированных клеток, также кистозной жидкости, содержащей макрофаги, детрит, дистрофически-измененные опухолевые клетки и т. д.
Рис. 9. Фолликулярно-солидная аденокарцинома. Комплекс опухолевых клеток. В одном из ядер — включение в виде спила ствола дерева.
Рис. 10. С-клеточный рак. Основная масса опухолевых клеток с зернистой цитоплазмой. В части из них наблюдается вакуолизация цитоплазмы.
Раки из В-клеток по структуре мало отличаются от раков из А-клеток, вместе с тем цитологически они труднее диагностируются из-за отсутствия выраженных цитологических признаков, отличающих их от доброкачественных новообразований из В-клеток. Окончательный диагноз ставится лишь при гистологическом исследовании удаленной опухоли. Цитологически же по описанным ранее признакам можно лишь верифицировать опухоль из В-клеток без уточнения характера ее роста.
Наиболее сложно цитологически дифференцировать опухоли из С-клеток из-за полиморфно- сти опухолевых клеток как в пределах одной опухоли, так и в разных опухолях в связи с разнообразием структур, формируемых этими клетками (железистые, папиллярные, перицитарные и т. д.). Эти опухоли возникают как спорадические варианты и как часть синдромов множественных эндокринных опухолей. Как и большинство раков из А- и В-клеток, раки из С-клеток не имеют собственной капсулы. Пунктаты С-клеточных опухолей обильные клеточные. Большинство опухолевых клеток изолированные, морфология их варьирует от опухоли к опухоли, от веретеновидных до округло-полигональных, иногда они напоминают плазматические клетки с четкими клеточными границами или без таковых, с центрально или эксцентрично расположенными вытянутыми или округлыми ядрами, с обильной или скудной, гомогенной или мелковакуолизированной, светлой или темной цитоплазмой, богатой мелкими метахроматически окрашивающимися гранулами (так называемые зернистые клетки; рис. 10). Все эти клетки независимо от формы и размеров объединяют нерезко выраженная базофилия цитоплазмы, наличие в ядрах 1—2 мелках ядрышек. Встречаются варианты с многоядерными опухолевыми клетками. В умеренно-дифференцированных С- клеточных раках, наиболее типичным представителем которых является медуллярный рак, опухолевые клетки четких структур не формируют, они ’’собираются» в пласты, гроздья, тяжи, войлокоподобные структуры; патогномичным для них следует считать наличие амилоида в виде гранул или глыбок различного размера, располагающихся внутри- или внеклеточно и окрашивающихся метахроматически в ярко-малиновый цвет (при окраске основными красителями типа азура II). В более высокодифференцированных раках из С- клеток опухолевые клетки могут формировать и описанные выше структуры, что позволяет относить их к аденокарциномам. И в таких опухолях может иметь место отложение амилоида в строму, но в значительно меньшем количестве, чем в медуллярных раках.
Острый тиреоидит цитологически диагностируется по тем же признакам, что и острое воспаление любой другой локализации. Гранулематозные процессы в ЩЖ могут быть как первичными (подострый тиреоидит де Кервена вирусной этиологии), так и вторичными при генерализации специфического процесса с вовлечением ЩЖ в патологический процесс (туберкулезный, сифилитический и т. д.). Цитологическая диагностика подострого тиреоидита базируется на наличии в пунктате клеточного детрита, излившегося коллоида, немногочисленных дистрофически-измененных тиреоцитов и (или) тиреоцитов с признаками пролиферации в сочетании с многоядерными гигантскими клетками инородных тел, многочисленными гистиоцитами, клетками типа эпителиоидных и немногочисленных фагоцитирующих макрофагов, а также лимфоидных элементов (рис. 11). Специфические тиреоидиты характеризуются теми же цитологическими особенностями, что и соответствующие процессы в других органах и тканях.
Рис. 11. Подострый тиреоидит де Кервена. Фон мазка — клеточный детрит, коллоид. Имеются скопления тиреоцитов (пролиферирующих или с дистрофическими изменениями); много гистиоцитов и стромальных клеток.
Тиреоидит Риделя — редкая патология ЩЖ, его приходится прежде всего дифференцировать с фиброзным вариантом АИТ. В отличие от последнего при тиреоидите Риделя в пунктате редко встречаются тиреоциты, отсутствуют клетки Ашкенази и клетки центров размножения лимфоидных фолликулов.
Резюмируя изложенное, следует подчеркнуть, что цитологическая диагностика различных заболеваний ЩЖ возможна, поскольку каждый вариант тиреоидной патологии имеет характерные микроскопические, в том числе цитологические, особенности, отражающие патологические изменения в ЩЖ при соответствующих ее заболеваниях. Вместе с тем она возможна и достоверна при условии получения во время проведения пункционной биопсии информативного материала, достаточно обильного, в котором представлены все возможные структуры и типы клеток, а также содержимое полостей. Трудности цитологической диагностики заболеваний ЩЖ обусловлены прежде всего тем, что в большинстве случаев мы сталкиваемся с сочетанными вариантами тиреоидной патологии. Однако если цитолог располагает хорошими пунктатами (из обеих долей, раздельно из образований и прилежащей к ним ткани соответствующей доли), микроскопическое исследование таких пунктатов позволяет достоверно оценить практически весь спектр патологических изменений, возникающих в железе, и поставить окончательный диагноз. Скудные пунктаты, особенно из одного патологического очага, позволяют цитологу лишь описать особенности полученного материала без уточнения характера патологических изменений в железе. Поэтому следует стремиться к получению обильных и информативных пунктатов без примеси или с минимальной примесью периферической крови, из-за которой клетки из железы нередко деформируются, что крайне затрудняет их микроскопическую идентификацию и исследование. Данные цитологического исследования пунктатов ЩЖ следует сопоставлять прежде всего с данными клинического обследования и УЗИ больных, поскольку это может позволить, с одной стороны, оценить результаты микроскопического исследования пунктатов с клинических позиций, а с другой — понять и объяснить часто несовпадающие результаты клинических и цитологических исследований, что в конечном счете позволяет уточнить диагноз и выбрать адекватную терапию.