Метаболизм азотистых оснований
Статья будет посвящена базовому, но крайне интересному разделу биохимии — метаболизму азотистых оснований. Сегодня мы рассмотрим то, как из аминокислот и глюкозы получается материал, кодирующий нашу биологическую сущность, — нуклеиновые кислоты (ДНК и РНК). Это понадобится нам для понимания очень важных вещей. Например, как одна мутация в метаболизме нуклеотидов способна подарить ребенку тяжелейший иммунодефицит или сделать из него глубокого инвалида. Почему не живут долго и счастливо многие из тех, кто злоупотребляет вином, красным мясом, шоколадом и прочими радостями. Почему иногда умирают (во всяком случае, часто умирали раньше) при проведении противоопухолевой химиотерапии. В статье, посвященной нарушению метаболизма азотистых оснований, ты узнаешь и о редких заболеваниях, о которых забывают 90 % врачей, принимая их за другие, более известные и очевидные. Но для начала надо постичь базу, ведь без понимания метаболизма азотистых оснований перечисленные мною факты и заболевания будет крайне сложно понять. Приступим.
Немного терминологии
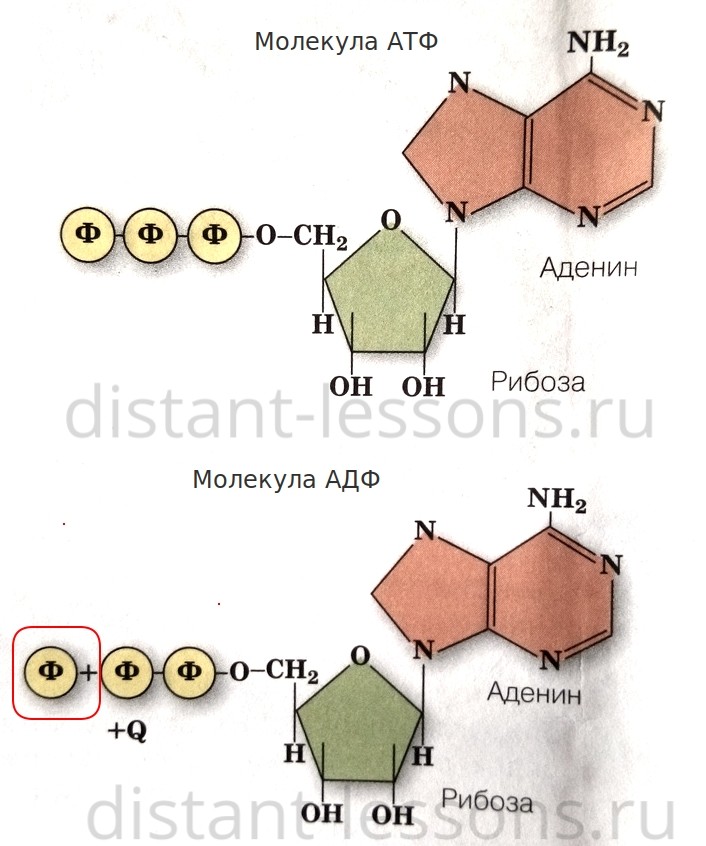
Нуклеотидом мы будем называть соединение, представляющее собой совокупность трех частей [3]:
Уберем фосфат — получим нуклеозид. Уберем еще и рибозу и получим азотистое основание — пуриновое или пиримидиновое «кольцо». Эта терминология необходима для понимания названий целого ряда ферментов, которыми сегодня мы будем развлекать наш мозг.
Попадая в твой ЖКТ, в 12-перстную кишку, нуклеиновые кислоты, содержащиеся в пище, расщепляются рибонуклеазами, нуклеотидазами и прочими ферментами поджелудочной железы. Продукты расщепления в виде нуклеотидов и нуклеозидов (иногда и вовсе азотистых оснований) попадают в энтероциты (клетки слизистой оболочки тонкой кишки).
В энтероцитах есть ксантиноксидаза, которая переводит пурины (аденин, гуанин) в мочевую кислоту. Мочевая кислота, как правило, стремится всосаться в кровь и выйти с мочой через почки. Может также пропустить себя в просвет кишки и выйти с калом (кстати, это бывает и весьма ощутимо, если имеется декомпенсированная патология почек).
Пиримидины утилизируются своим путем [1, 3], о котором мы поговорим позже. Но главное, что ты должен понять: экзогенных источников нуклеотидов для организма нет. Нуклеотиды, попадающие с пищей, не усваиваются, а лишь дают некоторое количество уратов — солей мочевой кислоты. Не перевелись еще люди, которые ведут активную пропаганду «Нет ГМО» и осуществляют на этом нехилую спекуляцию при продаже пищевых продуктов. Пусть в пище будет хоть трижды перекрещенная и модифицированная ДНК, твоя кишка все равно превратит все в кусок химуса и уратов, и ты даже не поймешь, что съел шедевр генной инженерии…
Образование пуринов. «Откуда же тогда взять мономеры для нуклеиновых кислот? Как и откуда берутся нуклеотиды? Как они используются дальше?» — и еще тысяча вопросов, которые добровольно не пришли бы в твою голову, если бы не предстоящий зачет по биохимии. Именно на них мы будем искать ответ.
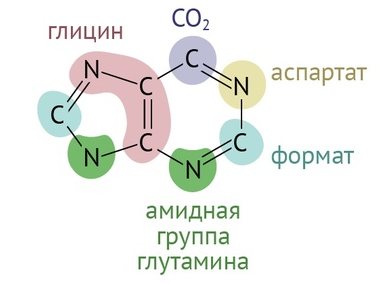
Пурины — гуанин и аденин — формируются буквально из ничего. Все, что нам нужно для создания пуринового кольца — глюкоза (поступающая в пентозо-фосфатный цикл), глицин, две молекулы глутамина, одна молекула аспартата, пара молекул активной метилированной формы фолиевой кислоты + немного терпения и приправы в виде пяти молекул АТФ [1].
Я не хочу грузить тебя серией реакций синтеза пуринов, ее на экзамене полностью никто не спросит, и, скорее всего, для принятия решений в своей работе она тебе тоже не нужна. Но кое-что ты знать должен.
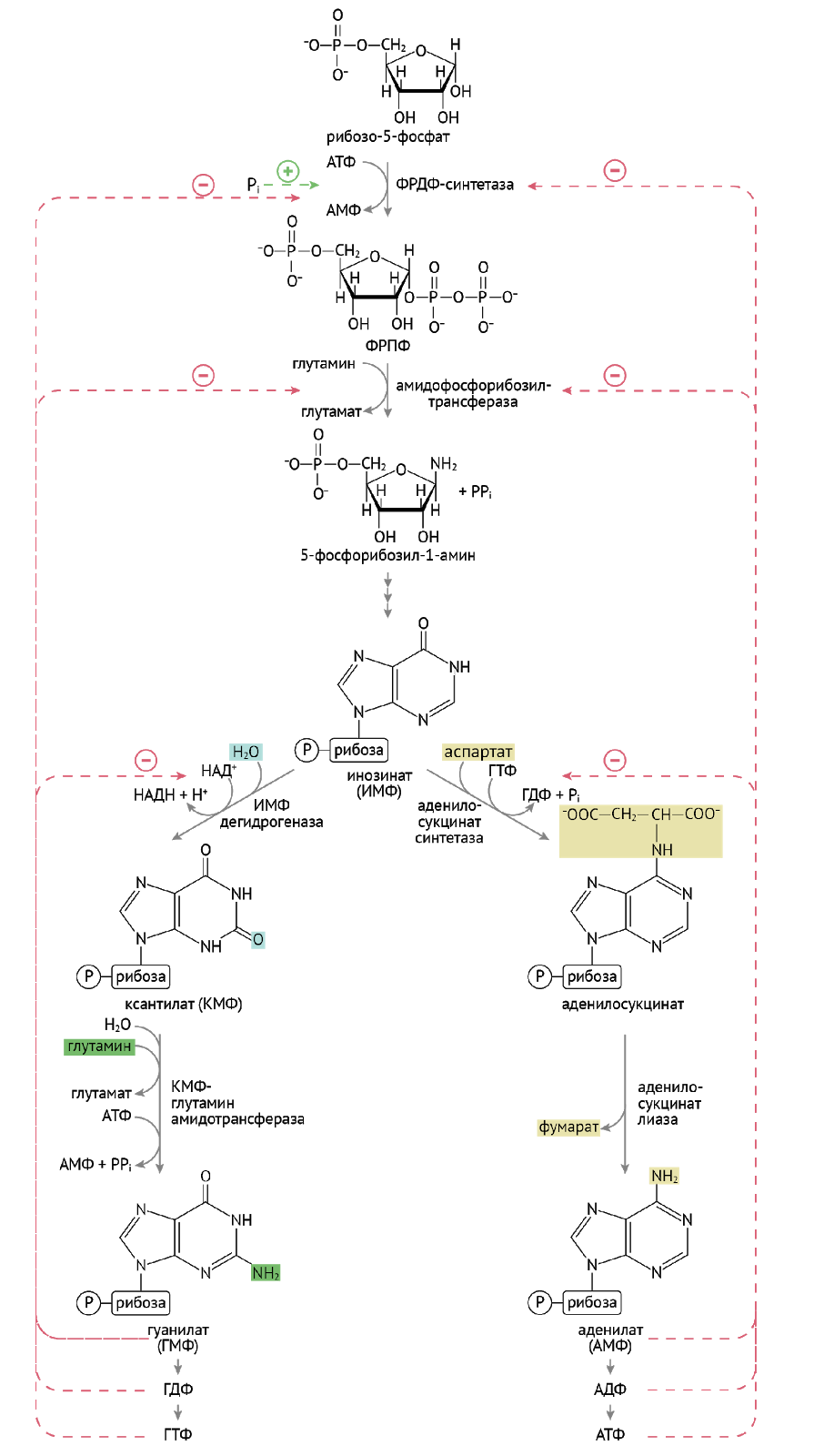
Синтез пуринов проходит два основных этапа: формирование инозинмонофосфата (ИМФ) и получение из ИМФ таких нуклеотидов, как ГМФ и АМФ.
Необходимо знать ключевые моменты этого синтеза.
Первый из них — лимитирующая реакция синтеза пуринов — формирование фосфорибозилпирофосфата (ФРПФ).
(Для тех, кто не понял: лимитирующая реакция — это та реакция, скорость которой определяет скорость всего процесса, а также та, что подвергается наиболее жесткой и сложной регуляции).
Далее следует еще порядка девяти реакций, которые из 5-фосфорибозил-1-амина сделают инозинмонофосфат (ИМФ). На этом закончится первый этап синтеза. Для экзамена и последующей работы тебе нужно знать, какие молекулы участвуют в формировании пуринового кольца, и эти две реакции. Для жизни — и того меньше.
2 этап. Чрезвычайно важен и интересен. Два брата, два параллельно идущих, как ты со своим другом, ̶п̶о̶ ̶н̶а̶к̶л̶о̶н̶н̶о̶й̶ к синтезу АМФ и ГМФ.
Что интересно: конечные продукты этого чрезвычайно интересного (никому) синтеза — ГТФ и АТФ — помогают дружественному параллельному циклу, даруя энергию для синтеза нуклеотида. Несколько ниже приведена иллюстрация вышеописанных биохимических событий.
Распад пуринов и дальнейшая судьба одиноких азотистых оснований
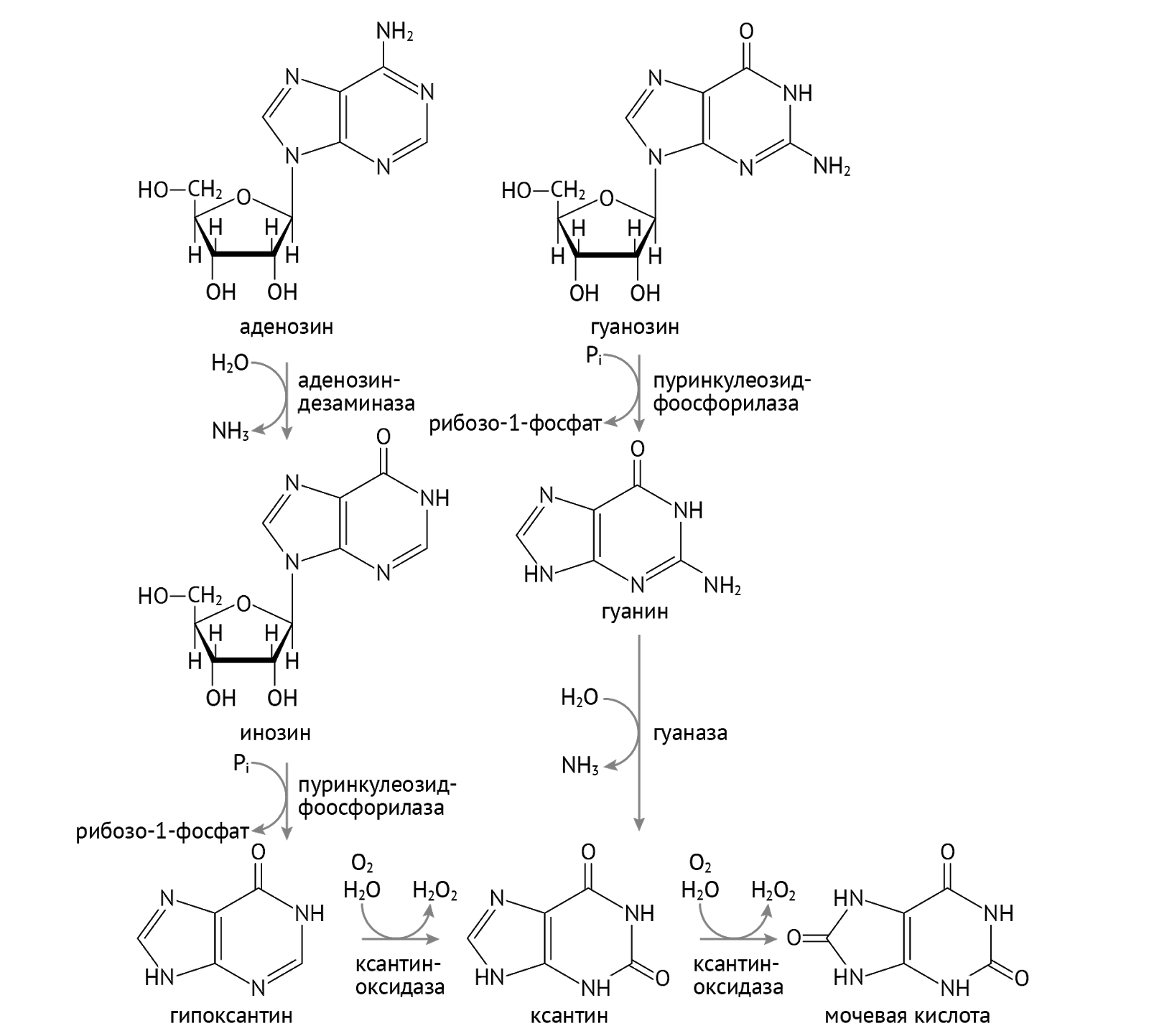
Катаболизм пуринов не менее важная и интересная серия процессов, потому что так же, как и синтез пуринов, их катаболизм является ключевым моментом для понимания патогенеза ряда заболеваний. Большинство нуклеотидов подвергаются повторному использованию (отдать некому, выкинуть жалко), заново включаясь в синтез нуклеотидов. Проследим путь их катаболизма.
Как мы видим, аденозин (аденин + рибоза) стремится стать гипоксантином. Но на пути к этому ему нужно перевоплотиться назад в инозинмонофосфат. В этом ему поможет аденозиндезаминаза. Хорошо запомни этот фермент, мы к нему не раз еще вернемся. Гипоксантин, кстати, может стать просто ксантином, чем обязан ксантиноксидазе.
Гуанозин считает стадию гипоксантина для себя недостойным (не может смириться с тем, что именно АТФ, а не ГТФ, является основным источником энергии в клетке, старые обиды несчастной молекулы). В силу этого ГТФ не церемонится и становится ксантином, минуя стадию образования гипоксантина. И здесь перед ним встает выбор из двух путей. Путь 1: гипоксантин и ксантин станут мочевой кислотой и оставят после себя лишь воспоминания, удалившись в мочу (или в суставы и почечные канальцы в виде уратов). Путь 2: камбэкнуться в ИМФ (а затем в АМФ) и ГМФ. В этом им поможет братан, которого во дворе прозвали гипоксантингуанинфосфорибозил-трансферазой (ГГФРТ).
Получившиеся вновь ГМФ и ИМФ (🡪 АМФ) превращаются в ГТФ и АТФ путем присоединения фосфорных остатков. Здесь все просто.
Резюме: для нас клиническое значение будут иметь нижеперечисленные ферменты:
Их значение для реализации той или иной патологии будет обсуждаться в соответствующей статье.
Синтез пиримидинов
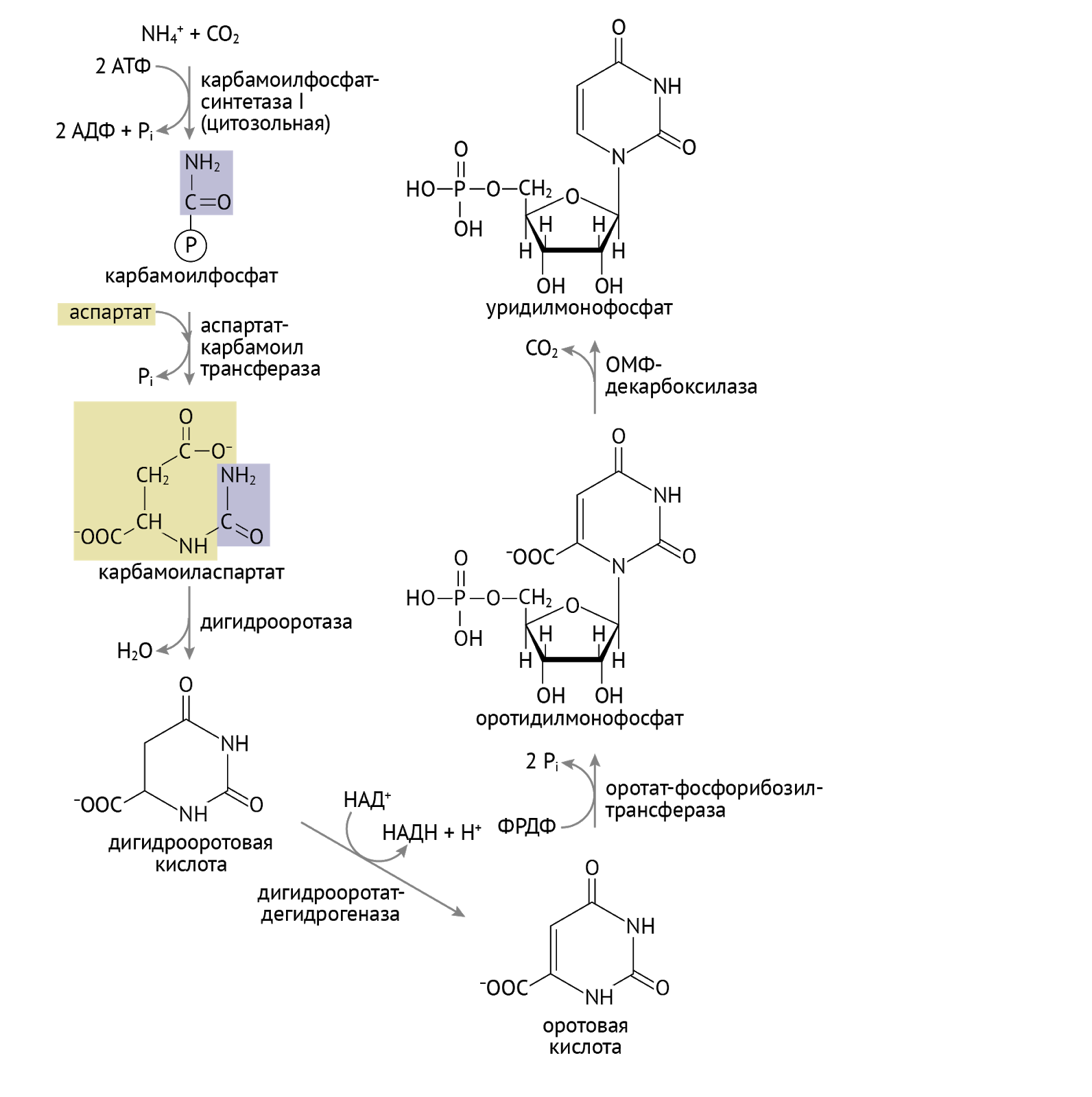
Здесь все проще и сложнее одновременно. Реакций здесь меньше, они понятнее, а значит, тебя могут спросить их на экзамене. Не пугайся, а просто смотри и запоминай.
С карбомоилфосфатом мы еще встретимся. Забегая далеко вперед (дальше, чем твое отчисление) сообщу тебе, что это соединение – исходный продукт для синтеза мочевины в печени. Той самой мочевины, в которую превращается весь «вредный» азот в организме. Советую отнестись внимательнее к следующим ферментам: оротатфосфорибозил-трасфераза и оротатмонофосфат (ОМФ)-декарбоксилаза. Нарушение их функции — ключевой момент в реализации такого патологического состояния, как оротовая ацидурия.
Взглянув на схему, мы видим, что конечным продуктом этого этапа является уридинмонофосфат (УМФ). С обостренным чувством собственной важности УМФ дает начало:
Все образованные соединения — АТФ, ГТФ, ЦТФ, УТФ — используются для синтеза рибонуклеиновых кислот, функцию которых ты должен был помнить не давеча как с третьего класса средней школы. Они имеют важное значение в матричных биосинтезах: в транскрипции ДНК, синтезе белка.
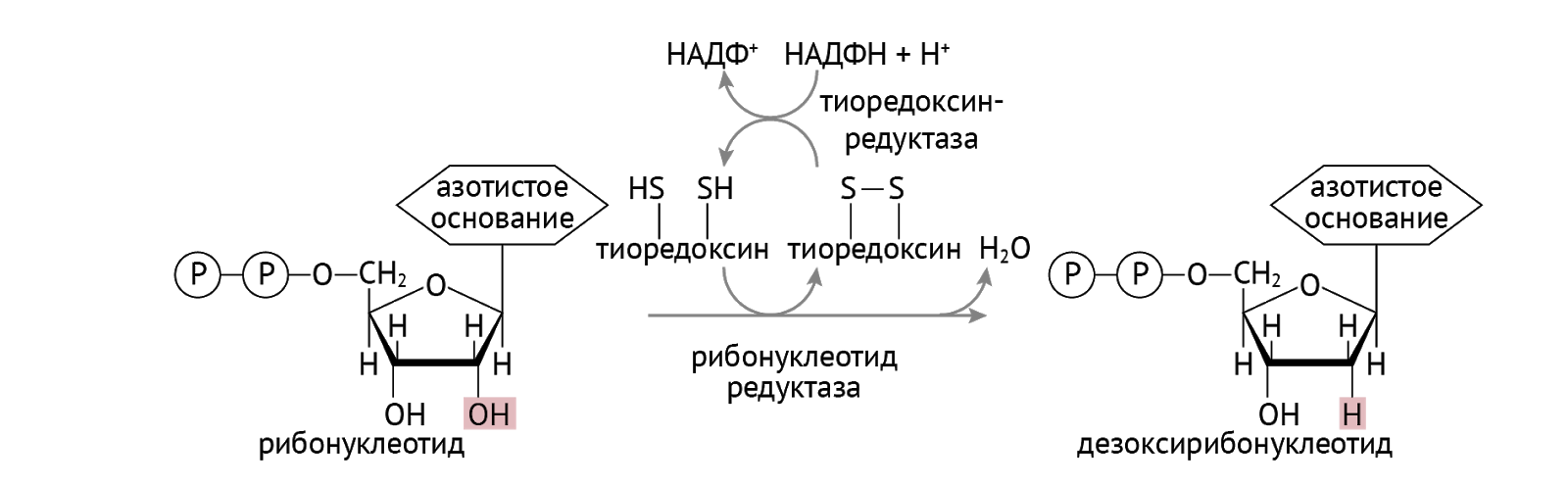
Но у нас есть еще и ДНК. Та штука, которая определяет твой фенотип и все, что из него вытекает. ДНК-полимераза установила фейс-контроль для синтеза ДНК. Он заключается в том, что все субстраты должны быть дезоксирибонуклеотидом [1, 3].
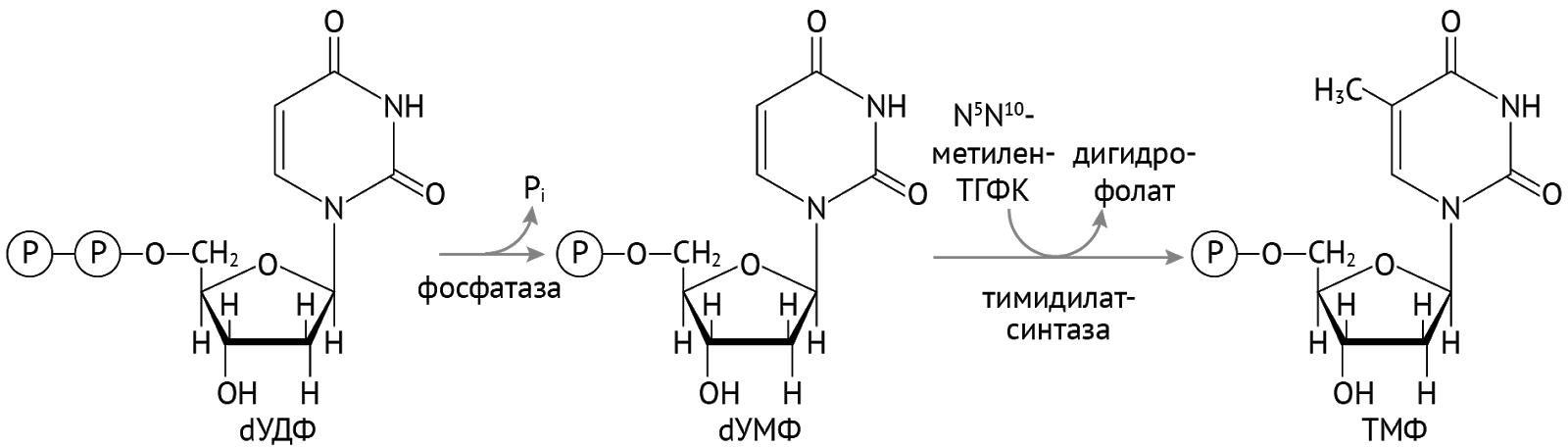
Есть исключение из правил. Это касается УТФ. Чтобы попасть в ДНК, ему нужно притвориться не просто дезоксирибонуклеотидом. Ему нужно притвориться ТТФ (тимидинтрифосфат). Что он и делает:
Далее остается присоединить остатки фосфорной кислоты и получить тимидинтрифосфат [1].
Важно отметить, что тимидилатсинтаза и реакция образования ТМФ являются чрезвычайно важными в отношении синтеза ДНК. Также здесь можно заметить, что необходимым кофактором является тетрагидрофолиевая кислота.
Именно данная реакция является мишенью метотрексата — цитостатического противоопухолевого препарата, являющегося антиметаболитом — структурным аналогом фолиевой кислоты, который проявляет к тимидилатсинтазе недвусмысленное сродство. Связываясь с ней, метотрексат останавливает реакцию образования ТМФ, тем самым обрывая синтез ДНК в самом зародыше — на этапе образования ее структурных компонентов. Метотрексат нашел применения в онкологии (преимущественно при гемобластозах) и в ревматологии (ревматоидный артрит [5]).
Распад пиримидинов
В нашей жизни ничего не вечно. Пиримидины тоже гибнут, но распадаясь, оставляют после себя ряд предшественников, которые участвуют в метаболизме, но уже другими путями.
Комментируя сложную схему распада пиримидинов, я акцентирую внимание на двух важных вещах:
Биологическое значение нуклеотидов в клетках. Функции, выходящие за рамки синтеза нуклеиновых кислот
Обсудив с тобой предметы сложной и высокой материи, мы переходим к самому интересному и «вкусному» (только не блевани) разделу настоящей статьи.
Нуклеотиды являются кирпичами для нуклеиновых кислот, что важно для реализации генетической информации и превращения ее в реальный фенотип со своими уникальными морфологическими особенностями. Этот процесс заслуживает отдельной лекции (спойлер — она следующая).
Но этим не исчерпывается значение нуклеотидов.
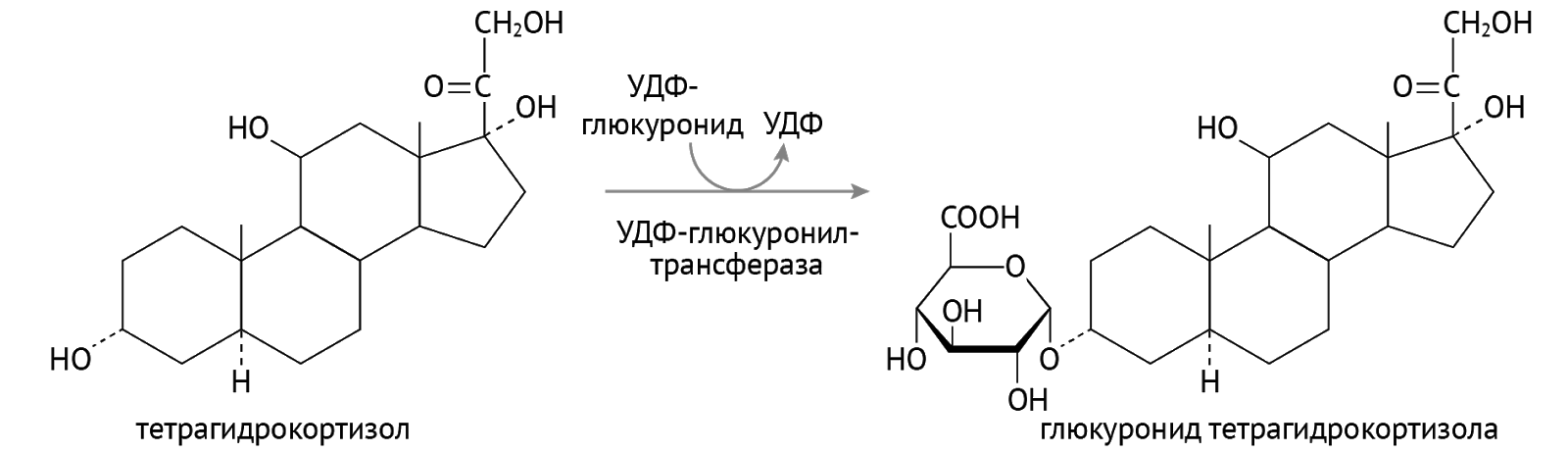
Детоксикация. Кое-кто из них используется в организме для детоксикации ксенобиотиков — лекарств, токсинов и иных химикатов, поступающих в организм, а также для детоксикации липофильных (т. е. растворимых в липидах и нерастворимых в воде) соединений: гормонов, билирубина. Суть детоксикации (обезвреживания) — перевести плохо растворимое в воде вещество в хорошо растворимое, что необходимо для последующего выведения через почки с мочой из организма. Достигается это присоединением полярной химической группы к исходному хулигану. Сначала формируется гидроксильная группа (если таковой нет, это этап образования более полярных соединений). А затем наступает этап конъюгации… Посмотрим, как это выходит на примере тетрагидрокортизола (рис. 11) [2].
А вот схема для менее дотошных, чем автор данной лекции.
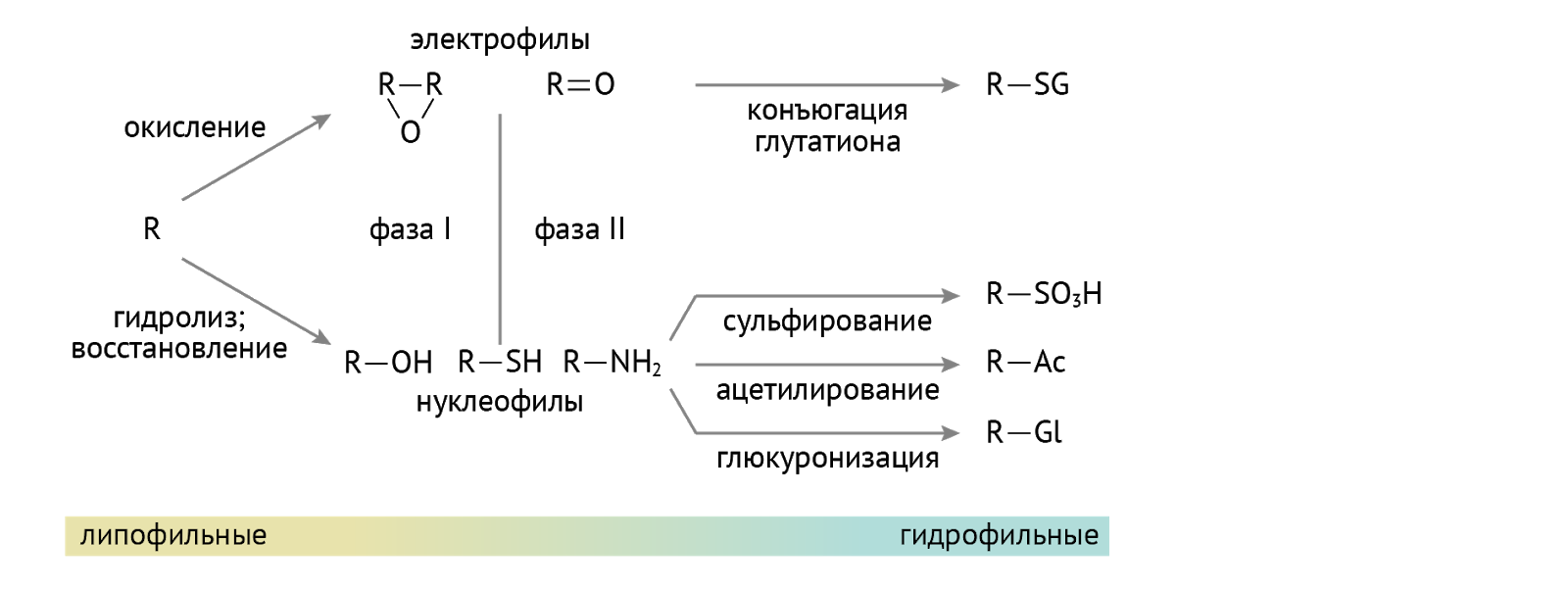
Никто: «Ух ты, классно и понятно».
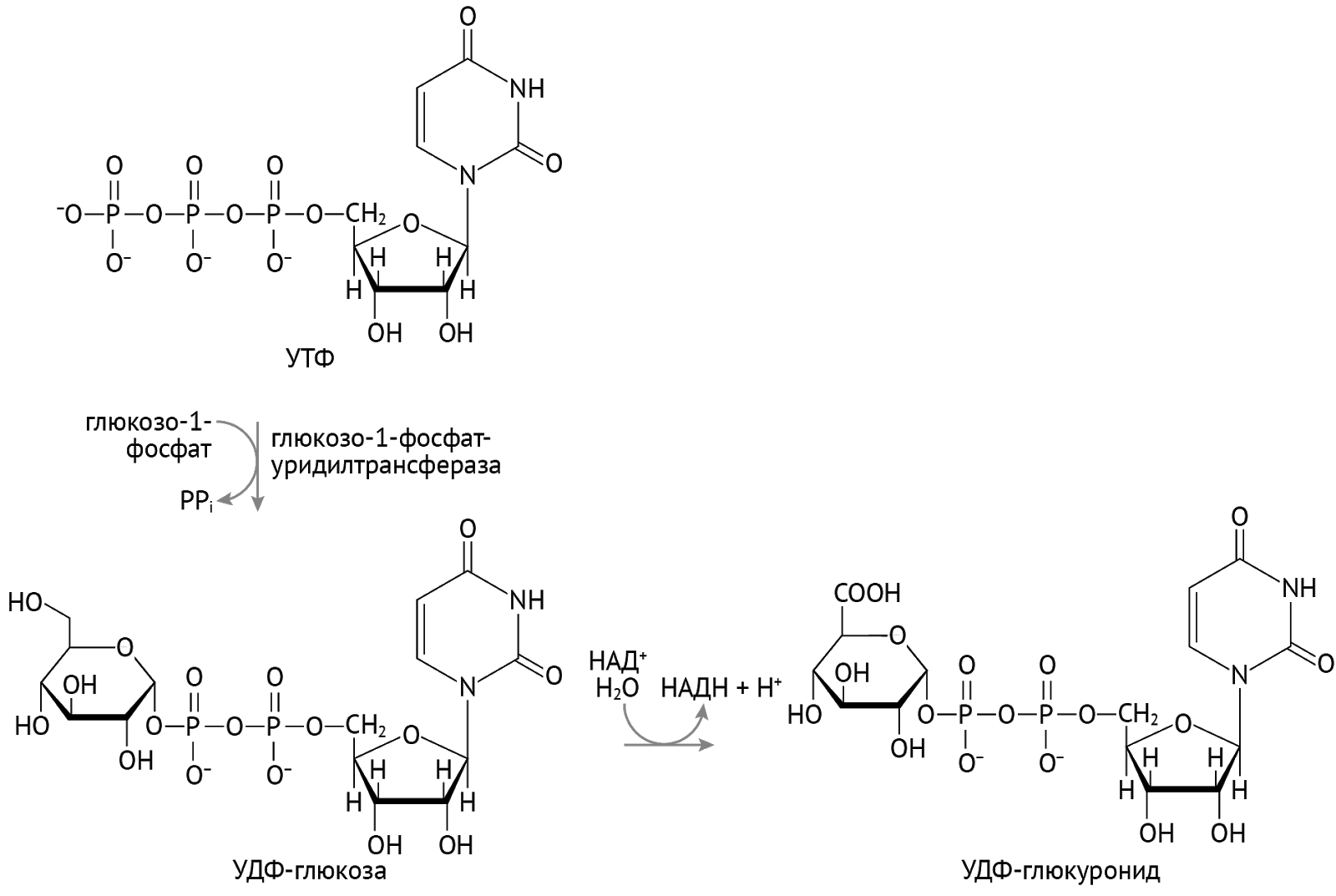
Твой экзаменатор: «А откуда ты возьмешь такую форму нуклеотида, которая будет способна конъюгировать с ксенобиотиками?».
Ты:
Важное значение эта форма УДФ имеет и для метаболизма билирубина: благодаря УДФ-диглюкурониду токсичный липофильный билирубин становится полярным, растворимым в крови и моче, конъюгированным билирубином [1, 2].
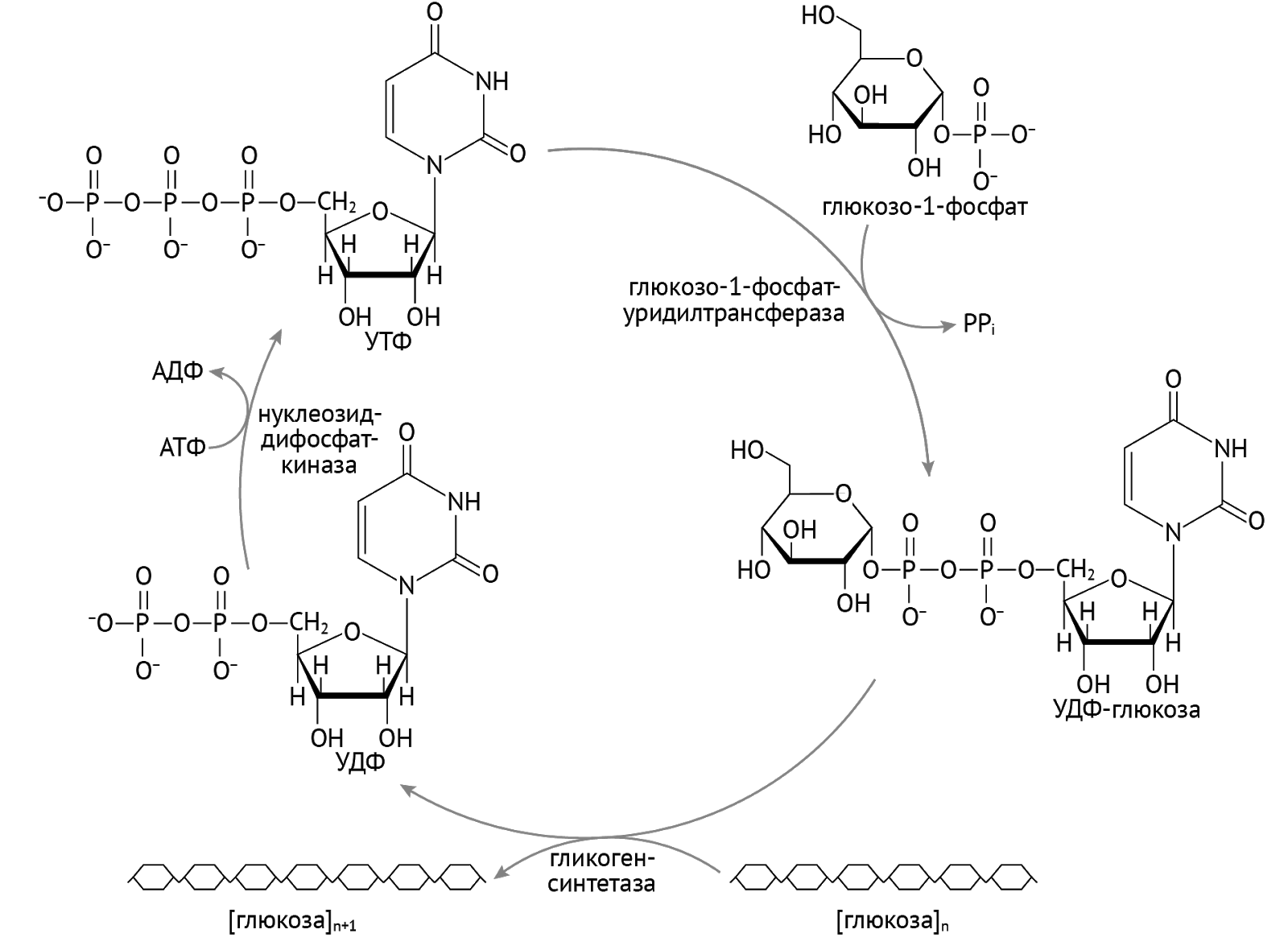
Гликоген. Неоценимое значение УДФ имеет и для образования гликогена.
Гликоген — это сравнительно инертная макромолекула, которая является резервуаром источника энергии в печени и мышцах. Через восприятия сигнала от инсулина глюкоза посредством активации (в виде присоединения фосфорного остатка и изомеризации) прыгает на гликоген благодаря посредничеству УТФ [1].
Вторичные сигнальные молекулы. Нуклеотиды, в частности, цАМФ и цГМФ, играют важную роль в процессе реализации клеточных функций и межклеточного взаимодействия. Клетка, будучи кирпичом биологического коммунизма, воспринимает сигналы от вышестоящих регуляторных систем, которые контролируют ее деятельность.
Это может выражаться в:
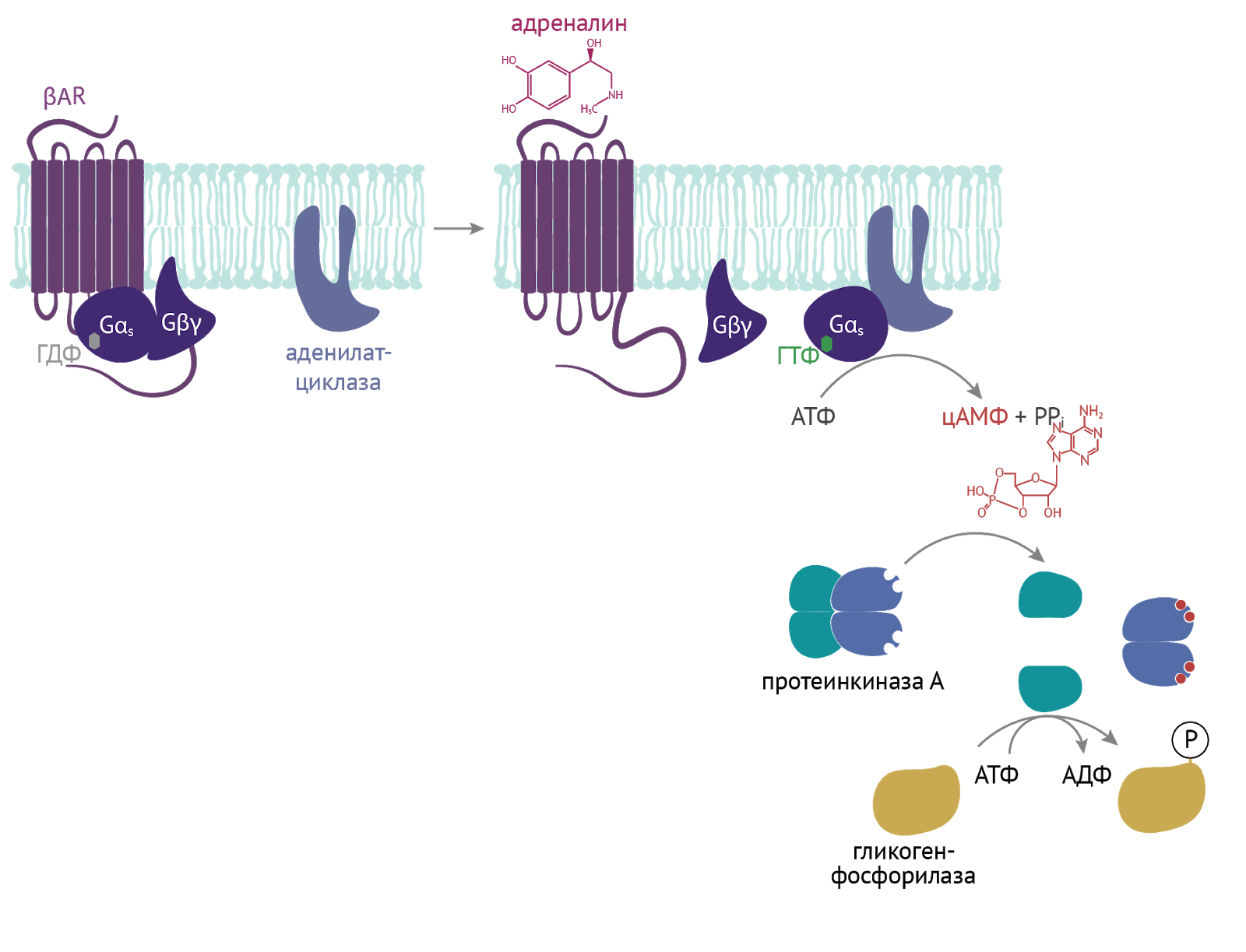
Такие молекулы, как цАМФ и цГМФ, являются одними из важных вторичных мессенджеров. Клетка, воспринимая сигнал извне (будь то гормон, нейромедиатор или любой другой разбойник), изменяет внутри себя концентрацию этих мессенджеров. Те вмешиваются в серию внутриклеточных последовательных реакций и тем самым усиливают первоначальный сигнал [4].
Здесь пример воздействия адреналина на метаболизм гликогена. Концентрация цАМФ растет, что приводит к активации протеинкиназы А. Та активирует гликогенфосфорилазу, что приводит к высвобождению из гликогена глюкозы и получению дополнительного источника энергии для выполнения различных нужд организма [4].
Примеров, когда нуклеотиды играют важную роль в организме, чрезвычайно много. Вспомнить хотя бы о том, кто в клетках является главным источником энергии (АТФ). Нуклеотиды в ходе своего метаболизма могут становиться источником иных метаболитов, которые могут принимать участие в энергетическом метаболизме (α-кетоглутарат, пировиноградная кислота 🡪 ацетил-Коа) и так до бесконечности. Придет время, и мы обсудим те случаи, когда метаболизм пуринов и пиримидинов в силу тех или иных причин нарушается [1].
Иногда это имеет очень серьезные последствия…
Химия, Биология, подготовка к ГИА и ЕГЭ

Состав молекулы:
Связи между остатками фосфорных кислот называются макроэнергетическими, т.к. при их расщеплении высделяется энергия:
АДФ — аденозиндифосфат ( 2 остатка фосфорной кислоты)
АМФ — аденозинмонофосфат ( 1 остаток фосфорной кислоты)
Энергия такой связи — от 40 до 60 кДж\моль, в то время как обычной — около 10 кДж\моль ( в 4-6 раз больше!)
Синтез молекулы АТФ происходит в полуавтономных органойдах клетки — митохондриях и хлоропластах, а выделившаяся энергия запасается в результате реакций распада — дыхания, брожения и фотосинтеза.
В реакциях синтеза (пластического обмена) АТФ расходуется, в реакциях энергетического обмена — наоборот, выделяется.
В ЕГЭ очень часто встречаются вопросы преобразования АТФ в ходе фотосинтеза или синтеза белка. Давайте четко определимя, где молекула расходуется, а где образуется:
происходит синтез АТФ
( фосфорилирование АДФ до АТФ)
используется энергия АТФ
идет цикл реакций, в которых через ряд
промежуточных продуктов образуется глюкоза:
АТФ в реакции синтеза белка:
Активация аминокислоты специфичным ферментом в присутствии АТФ
Присоединение активированной аминокислоты к специфичной тРНК с высвобождением аденозинмонофосфата (АМФ)
Связывание аминоацил-тРНК (тРНК, нагруженной аминокислотой) с рибосомами, включение аминокислоты в белок с высвобождением тРНК (здесь АТФ уже не участвует)
§ 8. Строение и функции РНК. АТФ
1. Какие слова пропущены в предложении и заменены буквами (а—г)? В состав молекулы АТФ входит азотистое основание (а), пятиуглеродный моносахарид (б) и (в) остатка (г) кислоты.
а – аденин
б – рибоза
в – три
г – фосфорной
2. Выявите сходство и различия в строении аденилового нуклеотида и молекулы АТФ.
Сходство: в состав молекул обоих веществ входит азотистое основание аденин и пятиуглеродный сахар рибоза.
Различия: в составе аденилового нуклеотида (как и в составе любого другого нуклеотида) есть только один остаток фосфорной кислоты, и отсутствуют макроэргические (высокоэнергетические) связи. Молекула же АТФ содержит три остатка фосфорной кислоты, между которыми имеются две макроэргические связи.
3. Какие связи называются макроэргическими? Что представляет собой процесс гидролиза АТФ? Синтеза АТФ? В чем заключается биологическая роль АТФ?
Макроэргическими (высокоэнергетическими) называются ковалентные связи между остатками фосфорной кислоты, при разрыве которых выделяется большое количество энергии — около 40 кДж/моль (для сравнения: при разрыве обычных ковалентных связей высвобождается примерно 12 кДж/моль).
На первом этапе гидролиза от АТФ отщепляется остаток фосфорной кислоты. При этом выделяется 40 кДж/моль энергии и АТФ превращается в АДФ — аденозиндифосфорную кислоту:
Второй этап гидролитического расщепления наблюдается сравнительно редко. При этом происходит отщепление еще одной фосфатной группы, высвобождение второй «порции» энергии и превращение АДФ в АМФ — аденозинмонофосфорную кислоту:
Наряду с гидролизом АТФ необходим ее непрерывный синтез. Для того чтобы присоединить остаток фосфорной кислоты к АДФ, нужно затратить не менее 40 кДж энергии:
Биологическая роль АТФ в том, что в живых организмах она выполняет функцию аккумулятора и переносчика энергии.
4. Сравните по различным признакам ДНК и РНК. Выявите черты их сходства и различия.
● Это органические вещества, биополимеры, относятся к нуклеиновым кислотам.
● Построены из нуклеотидов, в состав каждого из них входит азотистое основание, пентоза и остаток фосфорной кислоты. Азотистые основания (аденин (А), гуанин (Г) и цитозин (Ц)) входят как в состав нуклеотидов ДНК, так и в состав нуклеотидов РНК.
● Молекулы образованы атомами углерода (С), водорода (Н), кислорода (О), азота (N) и фосфора (Р).
● Содержатся в клетках всех живых организмов.
● Являются носителями генетической (наследственной) информации.
● В состав нуклеотидов ДНК входит остаток пятиуглеродного сахара дезоксирибозы, а в состав нуклеотидов РНК — остаток рибозы.
● Азотистое основание тимин (Т) может входить только в состав нуклеотидов ДНК, а урацил (У) — только в состав нуклеотидов РНК.
● Молекула ДНК двухцепочечная, имеет вид двойной спирали. Молекулы РНК обычно одноцепочечные, могут иметь различную пространственную конфигурацию.
● Полинуклеотидные цепи РНК значительно короче цепей ДНК.
● В клетках эукариот основная часть ДНК содержится в ядре. Молекулы РНК находятся не только в ядре, но и в цитоплазме клеток.
● ДНК обеспечивает хранение наследственной информации и её передачу дочерним клеткам в процессе деления. РНК обеспечивает реализацию наследственной информации, участвуя в процессе биосинтеза белков на рибосомах.
5. Какие виды РНК содержатся в клетке? Сравните их по выполняемым функциям, особенностям строения и процентному содержанию от общего количества РНК в клетке.
В клетке содержатся три вида РНК: рибосомные (рРНК), транспортные (тРНК) и матричные, или информационные (мРНК, иРНК).
Молекулы рРНК выполняют структурную функцию. В комплексе с особыми белками они приобретают определённую пространственную конфигурацию и образуют рибосомы (а точнее, субъединицы рибосом), на которых происходит синтез белков из аминокислот. Рибосомные РНК составляют около 80% всех РНК клетки.
Транспортные РНК осуществляют перенос аминокислот к рибосомам и участвуют в процессе синтеза белка. Молекулы тРНК сравнительно небольшие (в среднем состоят из 80 нуклеотидов), благодаря внутримолекулярным водородным связям они имеют специфическую пространственную структуру, напоминающую лист клевера. Транспортные РНК составляют около 15% всех РНК клетки.
Матричные, или информационные, РНК (мРНК, иРНК) наиболее разнородны по размерам и структуре. Они содержат информацию о структуре определённых белков и служат матрицами в ходе синтеза этих белков на рибосомах. Информационные РНК составляют около 3-5% всех РНК клетки.
6. В одну клетку ввели молекулы АТФ, меченные радиоактивным фосфором 32Р по последнему (третьему) остатку фосфорной кислоты, а в другую — молекулы АТФ, меченные 32Р по первому (ближайшему к рибозе) остатку. Через 5 мин в обеих клетках измерили содержание неорганического фосфат-иона, меченного 32Р. Где оно оказалось выше и почему?
Последний (третий) остаток фосфорной кислоты легко отщепляется в процессе гидролиза АТФ, а первый (ближайший к рибозе) – не отщепляется даже при двухступенчатом гидролизе АТФ до АМФ. Поэтому содержание неорганического фосфат-иона, меченного 32 Р, будет выше в той клетке, в которую ввели АТФ, меченную по последнему (третьему) остатку фосфорной кислоты.
Биология. 11 класс
§ 8. Строение и функции РНК. АТФ
Строение и функции РНК. РНК, так же как и ДНК, представляет собой биополимер, построенный из нуклеотидов. Однако молекулы РНК имеют ряд особенностей. Вы знаете, что в состав нуклеотидов РНК вместо дезоксирибозы входит рибоза, а вместо тимина (Т) — урацил (У). Кроме того, молекулы РНК значительно короче ДНК и представлены одной полинуклеотидной цепью, а не двумя.
Лишь некоторые вирусы имеют двухцепочечные молекулы РНК, представляющие собой генетический материал этих неклеточных форм.
*Количество нуклеотидов в молекулах ДНК, как правило, исчисляется миллионами, в то время как полинуклеотидные цепи РНК обычно состоят из 75—3000 мономерных звеньев. Известно, что некоторые РНК могут включать десятки тысяч нуклеотидов, но это является не правилом, а исключением.*
Молекулы РНК могут принимать различную пространственную конфигурацию, прежде всего за счет образования водородных связей. Но, в отличие от ДНК, эти связи формируются не между двумя разными цепями, а между отдельными участками одной и той же цепи, комплементарными друг другу.
*Содержание ДНК в клетках организма сравнительно постоянно, а количество РНК сильно варьирует. Молекулы РНК обеспечивают синтез белков, поэтому наибольшее их содержание характерно для клеток, активно вырабатывающих белки. Это, например, секреторные клетки пищеварительных и эндокринных желез, синтезирующие ферменты и белковые гормоны, лейкоциты, продуцирующие антитела, и т. д.*
Существует несколько видов РНК, различающихся по строению молекул, содержанию в клетке и выполняемым функциям. Все виды РНК синтезируются на определенных участках одной из цепей ДНК. Такой синтез называется матричным, поскольку молекула ДНК является матрицей (т. е. образцом, моделью) для построения молекул РНК.
Рибосомные РНК (рРНК) составляют более 80 % всех РНК клетки. Молекулы рРНК соединяются с особыми белками и образуют рибосомы — органоиды, в которых происходит синтез белков из аминокислот.
*Молекулы рРНК составляют более 50 % массы рибосомы и имеют сложную объемную структуру. Бóльшую часть цепи рРНК составляют комплементарные участки. Они соединяются водородными связями и приобретают спиральную конфигурацию. Взаимодействуя с рибосомными белками, одна или несколько молекул рРНК компактно укладываются в пространстве. Так формируются субъединицы рибосом — структурные компоненты этих органоидов.
Установлено, что рРНК в составе рибосомы выполняют не только структурную функцию, но и каталитическую. В процессе синтеза белка они ускоряют образование пептидных связей между аминокислотами, т. е. действуют подобно ферментам. Такие молекулы РНК, обладающие каталитическим действием, были названы рибозимами (сокращение от «рибонуклеиновая кислота» и «энзим»). Кроме рРНК, известны и другие рибозимы. Они могут катализировать расщепление самих себя или других молекул РНК, а также соединять фрагменты РНК друг с другом.
До открытия рибозимов единственными биологическими катализаторами считались ферменты. За исследование каталитических свойств рибонуклеиновых кислот американские молекулярные биологи С. Олтмен и Т. Чек в 1989 г. были награждены Нобелевской премией.*
Транспортные РНК (тРНК) — самые маленькие из молекул РНК, участвующих в синтезе белков. В среднем они состоят из 80 нуклеотидов. тРНК связывают аминокислоты, доставляют их в рибосомы и обеспечивают правильное включение этих аминокислот в полипептидную цепь. Для каждой из 20 белокобразующих аминокислот существует как минимум одна особая разновидность тРНК, а для некоторых аминокислот — несколько. Содержание тРНК составляет около 15 % от общего количества клеточных РНК.
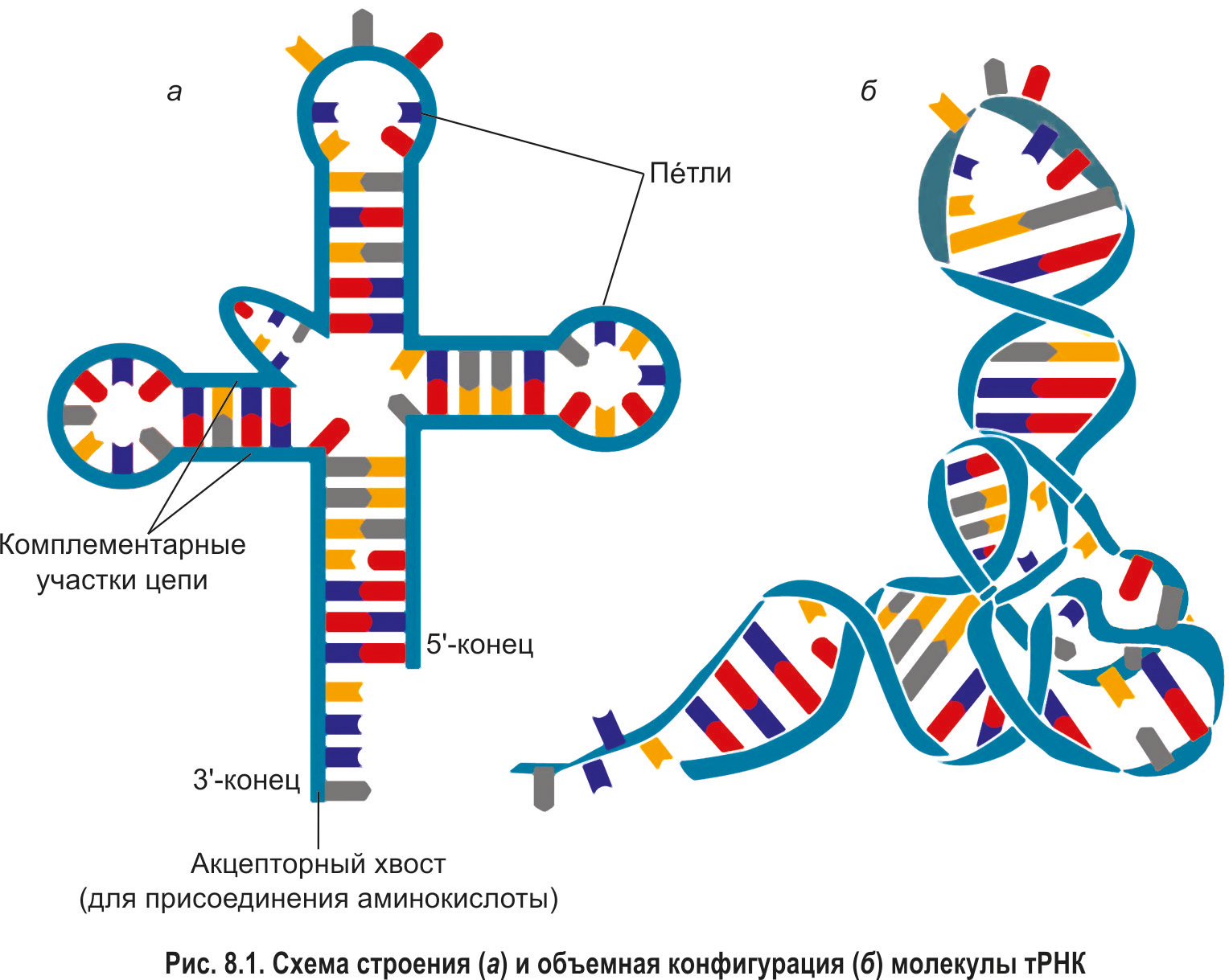
Все тРНК имеют сходное строение. Благодаря образованию внутримолекулярных водородных связей молекулы тРНК приобретают особую структуру, в которой комплементарно связанные участки чередуются с петлями (рис. 8.1). Такая пространственная конфигурация была названа клеверным листом.
*Как и любая другая полинуклеотидная цепь, молекула тРНК имеет 5′- и 3′-концы. У всех тРНК на 5′-конце находится гуаниловый нуклеотид, а 3′-конец завершается последовательностью ЦЦА. Присоединение аминокислоты происходит именно к 3′-концу молекулы тРНК, поэтому он называется акцепторным хвостом.*
Матричные, или информационные, РНК (мРНК, иРНК) наиболее разнообразны по строению и длине цепей. Молекулы мРНК содержат информацию о первичной структуре определенных белков. Во время синтеза белков в рибосомах они служат матрицами, определяющими порядок расположения аминокислот в белковых молекулах. Поэтому биосинтез белка, так же как и синтез РНК, относится к матричным процессам. Количество мРНК не превышает 3—5 % всех РНК, содержащихся в клетке.
*У ядерных организмов каждая молекула мРНК, как правило, содержит закодированную информацию о структуре одного белка. Для бактерий и вирусов характерны мРНК, кодирующие несколько разных белков.*
Функции рассмотренных видов РНК связаны с процессами синтеза белка. Следовательно, рРНК, тРНК и мРНК обеспечивают реализацию наследственной информации, хранящейся в молекулах ДНК.