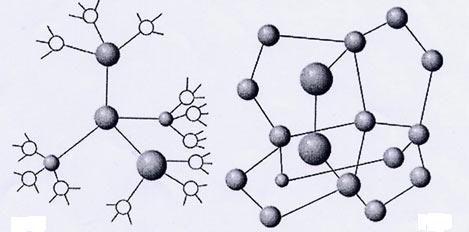
Связь строения воды с ее функциями
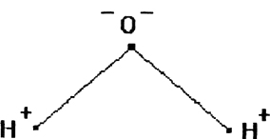
1. Один атом кислорода в воде соединен ковалентными связями с парой атомов водорода. Поэтому каждый атом водорода приобретает частично положительный заряд, а атом кислорода частично отрицательный.
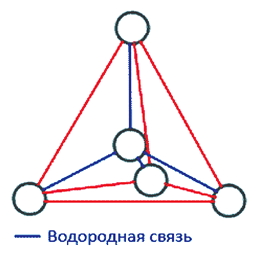
2. Между отрицательно заряженным атомом кислорода одной молекулы воды и положительно заряженным атомом водорода другой молекулы имеется водородная связь. Потому молекулы воды и связаны друг с другом.
3. Водородные связи легко разрушаются — они в 20 раз слабее ковалентных связей. Поэтому молекулы воды подвижны в клетке и организме.
4. Водородные связи также обусловливают высокую температуру кипения воды, теплоемкость (способность поглощать тепло при минимальном колебании собственной температуры).
Роль воды в живой системе — клетке
1. Молекула воды — это диполь, так как в области атомов водорода преобладает заряд положительный, а в области атома кислорода выше плотность отрицательного заряда.
2. Угол связи H-O-H в молекуле воды составляет 104,5 градуса, поэтому положительный и отрицательный заряды сосредоточены на разных концах молекулы. И именно поэтому вода — прекрасный растворитель полярных веществ.
3. Вода вообще является универсальным растворителем благодаря своей способности образовывать гидраты.
4. Вода способна на ориентирование в электрическом поле, она может присоединиться к различным молекулам и участкам молекул, несущим заряд, — при этом образуются гидраты. Если силы притяжения внутри молекулы воды меньше, чем силы притяжения молекул воды к молекулам иного вещества, это вещество растворятся в воде.
5. Поэтому выделяют гидрофильные вещества — они хорошо растворимы в воде: соли, щелочи, кислоты. Данные вещества диссоциируют на заряженные частицы — катионы и анионы. Молекулы воды взаимодействуют с ними.
6. Кроме полярных соединений к гидрофильным веществам относятся также сахара, аминокислоты, спирты — неполярные соединения, в составе которых имеются полярные группы (OH, различные радикалы).
7. Гидрофобные вещества — с трудом или вовсе не растворяются в воде. К ним относятся жиры, жироподобные вещества, бензин, парафин, каучук. Жироподобные вещества находятся, например, внутри клеточных мембран, ограничивая исход растворенных веществ из клетки в окружающую среду и проникновение обратно.
8. Вода — участник многих реакций в клетке, ведь большинство реакций идут как раз в водном растворе. Белки, липиды, углеводы и другие органические вещества расщепляются в результате работы ферментов и взаимодействия с водой до более простых веществ в результате реакций гидролиза.
9. В связи с высокой теплоемкостью вода отлично поддерживает тепловое равновесие в клетке, и при сильном повышении температуры среды вода нагревается медленно, но долго сохраняет тепло. Организмы защищены водой от резких колебаний температуры окружающей среды, поэтому процессы обмена веществ могут происходить в стабильных условиях.
10. Вода имеет относительно высокую для жидкостей теплопроводность. Тепло равномерно распределяется по всему объему воды в клетке, препятствуя перегреванию в отдельных точках.
11. Испарение воды обеспечивает охлаждение именно всей поверхности клетки, так как на разрыв водородных связей тратится энергия. Таким образом, вода участвует в терморегуляции.
12. Вода — источник кислорода, который растения выделяют в атмосферу.
13. Вода — источник водорода, который используется для синтеза органических веществ растениями.
14. Вода — среда для транспорта веществ в организме. Она обеспечивает ток лимфы и крови, восходящие и нисходящие токи растворов по древесине и лубу у растений. В клетках вещества, растворенные в воде, транспортируются через клеточные мембраны. Транспортные функции воды обеспечиваются ее низкой вязкостью и высокой подвижностью.
15. В клетке различают воду свободную (ее 90 процентов) и связанную (10 процентов). Связанная вода участвует в образовании макромолекул и никогда не теряется живой клеткой. Вода определяет объем и тургор клеток и тканей. Тургор — напряженное состояние плазматической мембраны, вызванное давлением воды внутри клетки.
16. Вода характеризуется высоким поверхностным натяжением — этим обеспечивается сцепление ее молекул. Благодаря такому свойству молекулы воды передвигаются по проводящим тканям растений, а также некоторые животные двигаются по поверхности воды. Например, клоп-водомерка при передвижении использует именно поверхностное натяжение воды. На первой и третьей паре ног у него есть специальные волоски, которые не продавливают слой воды, а держат жука на поверхности.
17. При замерзании воды ее объем возрастает, а плотность уменьшается, поэтому вода в виде льда всплывает на поверхность водоема. Максимальную плотность вода имеет при температуре 4 градуса, а при 0 она имеет меньшую плотность. Зимой часть воды в реках превращается в более легкий лед, который всплывает на поверхность и создает защиту для речных обитателей, препятствуя промерзанию толщи воды. При этом более теплая и плотная вода (с температурой не ниже 4 градусов) концентрируется под покровом льда, создавая условия для выживания водных животных. Поздней осенью, при понижении температуры ниже 4 градусов в клетках растений образуются кристаллы льда и они погибают. Чтобы выжить, многие растения накапливают в тканях белки и сахара, благодаря чему вода с растворенными в ней органическими веществами не замерзает, и растения благополучно переносят холода.
Структура молекул воды и их ассоциатов
Вода начинается с молекулы
Итак, молекула воды ( 1 H2 16 O) состоит из двух атомов водорода ( 1 H) и одного атома кислорода ( 16 O). Оказывается, что едва ли не все многообразие свойств воды и необычность их проявления определяется, в конечном счете, физической природой этих атомов, способом их объединения в молекулу и группировкой образовавшихся молекул.
В отдельно рассматриваемой молекуле воды атомы водорода и кислорода, точнее их ядра, расположены так, что образуют равнобедренный треугольник. В вершине его – сравнительно крупное кислородное ядро, в углах, прилегающих к основанию, – по одному ядру водорода. Модель молекулы воды, предложенная Нильсом Бором, показана на рис. 1.5.
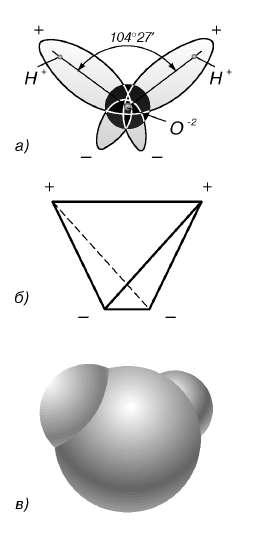
Рис. 1.5. Строение молекулы воды
а – угол между связями O-H;
б – расположение полюсов заряда;
в – внешний вид электронного облака молекулы воды.
Электронное строение молекулы воды
Таким образом, в молекуле воды различают четыре полюса зарядов: два отрицательных (избыток электронной плотности в области кислородного ядра) и два положительных (недостаток электронной плотности у двух водородных ядер). Для большей наглядности можно представить, что полюса занимают вершины деформированного тетраэдра, в центре которого находится ядро кислорода (рис. 1.5б).
Общий вид электронного облака молекулы воды показан на рис. 1.5в.
Вода растворяет все!
Во многом благодаря диэлектрической проницаемости, вода проявляет себя как универсальный растворитель. Ее растворяющему действию в той или иной мере подвластны и твердые тела, и жидкости, и газы.
Постоянно соприкасаясь со всевозможными веществами, вода фактически всегда представляет собой раствор различного, зачастую очень сложного состава.
Даже из свежевыпавшей дождевой воды можно выделить различные минеральные и органические вещества, растворенные в ней (до нескольких десятков миллиграммов на литр).
Минеральный состав воды
В пресных природных водах – речных, озерных – содержание растворенных веществ обычно не превышает 1 г/л. От нескольких единиц до десятков граммов на литр колеблется содержание солей в морской воде: например, в Балтийском море их не более 5 г/л, в Черном – 18, а в Красном море – около 40 г/л. В среднем в 1 л океанской воды растворено 34. 35 г солей. Общее количество их настолько велико, что, выделенные из воды, они покрыли бы поверхность земного шара слоем стометровой толщины.
Солевой состав речных и морских вод различен не только количественно, но и качественно. На 89% морские соли состоят из хлоридов (преимущественно – натрия и кальция), на 10% – из сульфатов (натрия, калия и магния), на 1% – из карбонатов (натрия и кальция), а также незначительных количеств других солей. В пресных водах набор минеральных примесей выглядит иначе. Больше всего здесь карбонатов (натрия и кальция) – до 80%. Сульфатов (натрия, кальция и магния) – около 13%. Остальные 7% приходятся на хлориды (натрия и кальция) и другие соли.
Из газов в пресных и морских водах наиболее широко представлены кислород, азот, углекислый газ, сероводород. В чистых холодных истоках горных рек содержание кислорода может достигать 6 мг/л. В глубинных слоях Черного моря высока концентрация сероводорода – до 100 мг/л. Этот ядовитый газ присутствует и в нижних слоях некоторых озер.
В пресных и морских водах в небольших количествах имеются и разнообразные органические компоненты – растворимые соединения типа белков, сахаров, спиртов, углеводородов и т.п. Это продукты жизнедеятельности и распада животных и растительных организмов, населяющих водоемы и их берега, а также отходы промышленности и сельского хозяйства.
Формирование кластеров воды
Полярность молекул воды, наличие в них частично нескомпенсированных электрических зарядов порождает склонность к группировке молекул в укрупненные «сообщества» – ассоциаты. Оказывается, полностью соответствует формуле Н2O лишь вода, находящаяся в парообразном состоянии. Это показали результаты определения молекулярной массы водяного пара. В температурном интервале от 0 до 100°С концентрация отдельных (мономерных молекул) жидкой воды не превышает 1%. Все остальные молекулы воды объединены в ассоциаты различной степени сложности, и их состав описывается общей формулой (H2O)x
Непосредственной причиной образования ассоциатов являются водородные связи. Они возникают между ядрами водорода одних молекул и электронными «сгущениями» у ядер кислорода других молекул воды. Правда, эти связи в десятки раз слабее, чем «стандартные» внутримолекулярные химические связи, и достаточно обычных движений молекул, чтобы разрушить их. Но под влиянием тепловых колебаний так же легко возникают и новые связи этого типа. Возникновение и распад ассоциатов можно выразить схемой:
Поскольку электронные орбитали в каждой молекуле воды образуют тетраэдричес-кую структуру, водородные связи могут упорядочить расположение молекул воды в виде тетраэдрических координированных ассоциатов
Исследователи раскрывают все более тонкие и сложные механизмы «внутренней организации» водной массы. Кроме льдоподобной структуры, жидкой воды и мономерных молекул, описан и третий элемент структуры – нететраэдрической.
Определенная часть молекул воды ассоциирована не в трехмерные каркасы, а в линейные кольцевые объединения. Кольца, группируясь, образуют еще более сложные комплексы ассоциатов.
Изучение структуры жидкой воды еще не закончено; оно дает все новые факты, углубляя и усложняя наши представления об окружающем мире. Развитие этих представлений помогает нам понять многие аномальные свойства воды и особенности взаимодействия ее, как растворителя, с другими веществами.
Научная электронная библиотека
Шишелова Т И, Корзун Н Л, Толстой М Ю,
1.1. Физические свойства воды
Физические свойства в полной мере изложены во многих работах. Вода (Н2O) – простейшее устойчивое химическое соединение водорода с кислородом, бесцветная жидкость с температурой кипения 100 °С. Химическая формула воды такая простая: Н2О; Н–О–Н [1–8]. Размер одной молекулы воды составляет около 3 Å (ангстрем) или примерно 0,28 нм (нанометра).
Рис. 1. Схема строения
молекулы воды
Рис. 2. Тетраэдрическая структура молекулы воды
Вода состоит из одного относительно большого атома кислорода и двух небольших атомов водорода, вокруг которого вращается облачко общих отрицательно заряженных электронов (рис. 1). Угол H–O–H молекулы H2O в газообразном и жидком виде колеблется от 104,5 до 109°
Во льду все молекулы связаны между собой водородными связями. При этом четыре связи каждой молекулы локально организованы в тетраэдрическую структуру, четыре близлежащие молекулы располагаются в вершинах трехгранной пирамиды, в центре которой находится пятая молекула
воды (рис. 2).
Положительно заряженное ядро атома кислорода, ввиду своей большой массы и заряда, сильнее притягивает к себе электронное облачко, оголяя при этом ядра водорода.
Три ядра в молекуле воды образуют равнобедренный треугольник с двумя протонами водорода в основании и кислородом в вершине. Расстояние O–H 0,9568 Å (0,1 нм); H–H – 1,54 Å (0,15 нм). Модель молекулы воды, предложенная Нильсом Бором [9], показана на рис. 3.
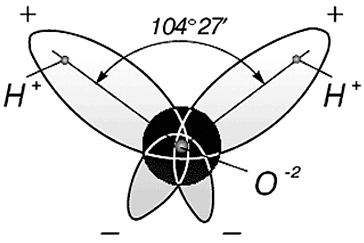
Рис. 3. Строение молекулы воды, предложенное Н. Бором [9]:
а – угол между связями H–H;
б – внешний вид электронного облака молекулы воды
Свойства воды в основном зависят от водородных связей. Из-за большой разности электроотрицательности атомов водорода и кислорода электронные облака сильно смещены в сторону кислорода. По причине этого, а также того, что ион водорода не имеет внутренних электронных слоев и обладает малыми размерами, он может проникать в электронную оболочку отрицательно поляризованного атома соседней молекулы. Благодаря этому каждый атом кислорода притягивается к атомам водорода других молекул и наоборот.
Каждая молекула воды может участвовать максимум в четырех водородных связях: два атома водорода – каждый в одной, а атом кислорода – в двух; в таком состоянии молекулы находятся в кристалле льда. При таянии льда часть связей рвется, что позволяет уложить молекулы воды плотнее; при нагревании воды связи продолжают рваться, и плотность ее растет, но при температуре выше 4 °С этот эффект становится слабее. При испарении рвутся все оставшиеся связи. Разрыв связей требует много энергии, отсюда высокая температура и удельная
теплота плавления и кипения и высокая теплоемкость. Вязкость воды обусловлена тем, что водородные связи мешают молекулам воды двигаться с разными скоростями. Строение электронного облака молекулы воды таково, что во льду каждая молекула связана четырьмя водородными связями с ближайшими к ней молекулами, координационное число молекул в структуре льда равно четырем. О размере молекулы можно судить по величине расстояния между ближайшими молекулами во льду, составляющего 2,67 Å (0,267 нм). Соответственно молекуле воды можно приписать радиус равный 1,38 Å (0,138 нм). Дипольный момент воды равен 1,87 Дебая. Электрический дипольный момент – векторная физическая величина, характеризующая, наряду с суммарным зарядом электрические свойства системы заряженных частиц (распределения зарядов) в смысле создаваемого ею поля и действия на нее внешних полей.
Исследования показали, что в воде сохраняется ближняя упорядоченность, свойственная структуре льда. Следовательно, тенденция каждой молекулы воды к окружению четырьмя ближайшими молекулами и к образованию с ними водородных связей свойственна как жидкому, так и твердому состоянию. Расстояние между ближайшими молекулами при плавлении льда изменяется от 2,76 Å (0,276 нм) до 2,90 Å (0,29 нм). Свойственное среднее расположение ближайших молекул ведет к очень рыхлой, ажурной структуре. Именно с этим связаны аномальные свойства воды.
Почти шарообразная молекула воды имеет заметно выраженную полярность, так как электрические заряды в ней расположены асимметрично. Каждая молекула является миниатюрным диполем с высоким дипольным моментом.
Полярность молекул, наличие в них частично некомпенсированных электрических зарядов создает группировки молекул – ассоциаты. Полностью соответствует формуле Н2O лишь вода, находящаяся в парообразном состоянии. В температурном интервале от 0 до 100 °С концентрация отдельных (мономерных молекул) жидкой воды не превышает 1 %. Все остальные молекулы воды объединены в ассоциаты различной степени сложности, и их состав описывается общей формулой
[Н2O]Х. Причиной образования ассоциатов являются водородные связи. Они возникают между ядрами водорода одних молекул и электронными «сгущениями» у ядер кислорода других молекул воды.
Неравномерное распределение электрических зарядов приводит к тому, что молекула воды поляризуется, становится маленьким магнитиком.
В магнитном поле Земли молекулы воды, находящейся в жидком состоянии, собираются в некие нестабильные конструкции под действием притяжения разноименно заряженных полюсов. Нестабильность таких конструкций определяется слабостью водородных связей между молекулами воды, называемых иногда водородными мостиками.
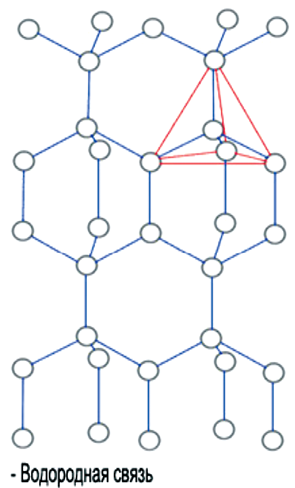
Тетраэдрическая форма отдельной молекулы повторяется в кристаллической структуре льда. Возможно, определенную роль здесь играет то, что угол H–O–H молекулы H2O почти равен идеальному тетраэдрическому углу 109°, а молекулы воды, как мы знаем, объединяются с помощью водородных связей, которые они образуют именно в направлении O–H. Эти трехгранные пирамиды могут также объединяться в некую сверхструктуру. Во льду такая сложная трехмерная сверхструктура из тетраэдров простирается на весь объем (рис. 4).
Рис. 4. Структура Н2О льда
Льдообразная молекула воды содержит как простые молекулы воды, так и кластера льдообразных структур (рис. 5).
Молекулы воды называют диполями потому что
Итак, рассмотрим наиболее весомые понятия о строении молекул воды!
Благодаря наличию водородных связей каждая молекула воды образует водородную связь с 4-мя соседними молекулами, образуя ажурный сетчатый каркас в молекуле льда. Именно такое упорядоченное состояние молекул воды можно назвать «структурой». Каждая молекула может одновременно образовывать четыре водородные связи с другими молекулами под строго определенными углами, равными 109°28′, направленных к вершинам тетраэдра, которые не позволяют при замерзании создавать плотную структуру.
На моём сайте имеются, и будут появляться статьи, которые, на первый взгляд «отдельные» и не имеют никакого отношения к другим статьям. На самом деле, большинство статей сайта имеет взаимосвязь в одно целое. В данном случае, описывая свойства дистиллированной воды, я использую Дипольную теорию электрического тока, это альтернативное понятие об электрическом токе, которое подтверждается и наукой и практикой лучше, чем классическое понятие.
При воздействии энергии источника электрического тока, все диполи атомов воды (как проводника) поворачиваются, ориентируясь своими одноимёнными полюсами в одном направлении. Если молекулы воды до появления внешнего электрического поля создавали кластерную (взаимно ориентированную) структуру, то для ориентации во внешнем электрическом поле потребуется минимальное количество энергии источника электрического тока. Если же структура была не организованной (как у дистиллированной воды), то потребуется большое количество энергии.
Заметьте, «в народе» бытует мнение, что дистиллированная вода и талая вода должны обладать одинаковыми электропроводными свойствами, ведь что у одной, что у другой отсутствуют химические примеси (как правило – соли), их химический состав одинаков, да и строение молекул воды что в талой воде, что в дистиллированной одинаково.
На самом деле всё выглядит наоборот, отсутствие примесей совсем не говорит о свойствах электропроводности воды. Не понимая этого, некоторые люди, «убивают» аккумуляторные батареи ещё на этапе их заправки электролитом, подменяя дистиллированную воду на талую, или просто очищенную через угольный фильтр. Как правило, заправленный аккумулятор, который куплен на автомобильном рынке служит меньше, чем тот, который вы купили сухозаряженным и разбавив серную кислоту дистиллированной водой, заправили его сами. Это лишь потому, что «готовый» электролит, или заправленный аккумулятор – это в наше время средство заработка, а чтобы определить какая вода использовалась, надо провести дорогую экспертизу, никто этим не заморачивается. Торгашу не важно, сколько прослужит аккумулятор на твоём авто, а Вам тоже, возиться с кислотой не очень хочется. Зато, я Вас уверяю, аккумулятор, над которым попотеете Вы, при минусовых температурах будет намного бодрее, чем заправленный из уже готового бутылочного электролита.
Кластеры воды на границах раздела фаз (жидкость-воздух) выстраиваются в определенном порядке, при этом все кластеры колеблются с одинаковой частотой, приобретая одну общую частоту. При таком движении кластеров, учитывая, что входящие в кластер молекулы воды являются полярными, то есть, имеют большой дипольный момент, следует ожидать появления электромагнитного излучения. Это излучение отличается от излучения свободных диполей, так как диполи являются связанными и колеблются совместно в кластерной структуре.
Частота колебаний кластеров воды и соответственно, частота электромагнитных колебаний может быть определена по следующей формуле:
Изучение движения молекулы воды в электрическом и магнитном полях
ИЗУЧЕНИЕ ДВИЖЕНИЯ
МОЛЕКУЛЫ ВОДЫ В ЭЛЕКТРИЧЕСКОМ И МАГНИТНОМ ПОЛЯХ
Оглавление
Характеристики воды 3
Электрические свойства молекул и дипольный момент 4
Движение молекулы воды в электрическом поле 5
Магнитный дипольный момент 7
Движение молекулы воды в магнитном поле 8
Список литературных источников 9
Введение
Вода – одно из самых распространенных веществ на нашей планете, она имеет огромное значение в эволюции как живой, так и неживой природы. Спектр применения воды необычайно широк: быт, промышленность, сельское хозяйство – этот список можно продолжать сколь угодно долго. Именно поэтому изучением воды, ее физических и химических свойств, до сих пор занимаются ученые всего мира. Вода, казалось бы, самое обыкновенное вещество, но имеет столько неразгаданных тайн и неизученных свойств.
Тема данной исследовательской работы – «Изучение движения молекулы воды в электрическом и магнитном полях». Чтобы больше понять о веществе, нужно рассмотреть его мельчайшую частицу – атом либо молекулу. В этой работе будут рассмотрены некие свойства молекулы воды.
Изучение движения молекулы представляет практический интерес. Как влияет на молекулу однородное, неоднородное электрическое поле? Каким образом молекула движется в магнитном поле?
Характеристики воды
Вода (оксид водорода) – бинарное неорганическое соединение, химическая формула – 
При нормальных условиях вода – прозрачная жидкость, не имеющая ни цвета (в малом объеме), ни запаха, ни вкуса. В твёрдом состоянии называется льдом (кристаллы льда могут образовывать снег или иней), а в газообразном – водяным паром. При атмосферном давлении вода замерзает (превращается в лёд) при температуре в 0°C и кипит (превращается в водяной пар) при температуре 100°C.
Плотность воды – 0,9982 г/куб. см., ее динамическая вязкость (ст. усл.) – 0,00101 Па•с (при 20°C), ее кинематическая вязкость (ст. усл.) – 0,01012 кв. см/с (при 20°C), температура плавления – 0°C, температура кипения – 99,974°C, молярная теплоёмкость (ст. усл.) – 75,37 Дж/(моль•К), теплопроводность (ст. усл.) – 0,56 Вт/(м•K).
При давлении в 611,73 Па температура кипения и плавления совпадает и становится равной 0,01°C. Такое давление и температура называются тройной точкой воды. [3]
При более низком давлении вода не может находиться в жидком состоянии, и лёд превращается непосредственно в пар. Температура возгонки льда падает со снижением давления.
При температуре 374°C (647 K) и давлении 22,064 МПа вода проходит критическую точку. В этой точке плотность и другие свойства жидкой и газообразной воды совпадают. [4]
При более высоком давлении нет разницы между жидкой водой и водяным паром, следовательно, нет и кипения или испарения.
При таянии льда, его плотность увеличивается (с 0,9 до 1 г/куб. см). Почти у всех остальных веществ при плавлении плотность уменьшается. При нагревании от 0°C до 4°C (точнее 3,98°C), вода сжимается. Благодаря этому могут жить рыбы в замерзающих водоёмах: когда температура падает ниже 4°C, более холодная вода, как менее плотная остаётся на поверхности и замерзает, а под льдом сохраняется положительная температура. Высокая температура и удельная теплота плавления (0°C и 333,55 кДж/кг), температура кипения (100°C) и удельная теплота парообразования (2250 КДж/кг), по сравнению с соединениями водорода с похожим молекулярным весом. Высокая теплоёмкость жидкой воды. Высокая вязкость. Высокое поверхностное натяжение.
Это свойство воды используется живыми существами. В живой клетке и в межклеточном пространстве вступают во взаимодействие растворы различных веществ в воде. Вода необходима для жизни всех без исключения одноклеточных и многоклеточных живых существ на Земле.
Вода имеет показатель преломления n=1,33 в оптическом диапазоне. [4] Однако она сильно поглощает инфракрасное излучение, и поэтому водяной пар является основным естественным парниковым газом. Он отвечает более чем за 60% парникового эффекта. [4] Благодаря большому дипольному моменту молекул, вода также поглощает микроволновое излучение, на чём основан принцип действия микроволновой печи. [4]
Электрические свойства молекул и дипольный момент
Электрические свойства молекул – важные характеристики строения молекул. Изучение таких свойств устанавливает закономерности связи свойств со строение молекул. Знание электрических свойств поможет при описании явлений, происходящих при помещении молекулы в электрическое поле, в чем и состоит цель данной работы.
Молекулы всех веществ делятся на полярные (дипольные) и неполярные. В дипольных молекулах центры отрицательных и положительных зарядов не совпадают, к таким молекулам относится молекула воды.
Атомы в молекуле воды расположены под углом, вершина которого – атом кислорода, он является центром распределения отрицательного заряда, а между атомами водорода – центр распределения положительного заряда. Заряды создают молекулярные силовые поля. [2] Количественная характеристика полярности определяется электрическим моментом диполя, который равен произведению величины положительного заряда на расстояние между зарядами и направлен от отрицательного заряда к положительному:

где q – величина положительного заряда, I – вектор с началом в отрицательном заряде и концом в положительном.
Для системы из N частиц электрический дипольный момент равен

где 



Для воды дипольный момент равен: 

Движение молекулы воды в электрическом поле
Итак, будет ли электрическое поле действовать на помещенную в него молекулу воды? Каково это действие? Каким будет движение молекулы, поступательным или вращательным? Какова будет скорость молекулы, ее перемещение, ускорение?
Прежде всего, необходимо рассмотреть движение заряженных частиц в электрическом поле. На заряженную частицу в электростатическом поле действует кулоновская сила, которую можно найти по следующей формуле:

Кулоновская сила сообщает ускорение:

где m – масса заряженной частицы [1].
Но вода – диэлектрик, то есть молекула воды нейтральна. Действует ли на нее электрическое поле?
Так как молекула воды – диполь, то действие электрического поля направлено на ее разноименные полюса. На положительные полюса действует сила, направленная по линиям напряженности поля, а на отрицательный полюс – сила, направленная против линий напряженности. Электрическое поле окажет на молекулу воды ориентирующее действие вдоль направления поля. Этому препятствует хаотическое тепловое движение молекул, стремящееся произвольно «разбросать» диполи. В итоге совместного действия поля и теплового движения возникает преимущественная ориентация дипольных электрических моментов вдоль поля, возрастающая с увеличением напряженности электрического поля и с уменьшением температуры [2].
В однородном внешнем электрическом поле с напряженностью Е на заряды диполя будут действовать силы F1 = F2 = qE. Разложим их на составляющие 








Рис.1.3. Диполь в однородном электрическом поле





Вращающий момент (момент сил), действующий на молекулу во внешнем поле в скалярной и векторной формах:

Вектор момента направлен перпендикулярно плоскости рисунка, то есть при помещении диполя в электрическое поле 


Молекула приобретает угловое ускорение 




Момент инерции молекулы воды может быть выполнен по формуле классической механики:

где K – общее число химических элементов, образующих исследуемую молекулу; 



Момент инерции служит мерой инертности тела при вращении, а следовательно, играет ту же роль, что и масса при поступательном движении.
В однородном электрическом поле молекула воды будет поворачиваться вокруг своего центра масс вдоль силовых линий поля, но вращательного движения происходить не будет, движение молекулы будет колебательным.
В неоднородном электрическом поле на положительный и отрицательный заряды молекулы будут действовать неодинаковые силы, их значения будут различны по модулю.
Рис. 1.4. Диполь в неоднородном электрическом поле








В неоднородном электрическом поле молекула воды не просто будет поворачиваться, но еще и начнет притягиваться к области усиления поля, то есть туда, где гуще силовые линии. Таким образом, движение молекулы относительно электрического поля можно считать поступательным.
Магнитный дипольный момент
Исследование взаимодействий полюсов постоянных магнитов привело к представлению о существовании магнитных зарядов, аналогичных электрическим зарядам. Пара таких магнитных зарядов, равных по модулю и противоположных по знаку, рассматривались как магнитный диполь. Позднее было установлено, что магнитных зарядов не существует, что магнитные поля создаются движущимися электрическими зарядами, то есть электрическими токами. Однако понятие о магнитном дипольном моменте сохранили, поскольку на больших расстояниях от замкнутых проводников, по которым протекают токи, магнитные поля оказываются такими же, как если бы их порождали магнитные диполи.
Магнитный момент (магнитный дипольный момент) – основная величина, характеризующая магнитные свойства вещества. Магнитным моментом обладают элементарные частицы, атомные ядра, электронные оболочки атомов и молекул. Магнитный момент элементарных частиц (электронов, протонов, нейтронов и других), как показывает квантовая механика, обусловлен существованием у них механического момента – спина. [8] Спин имеет квантовую природу и не связан с перемещением частицы как единого целого.

где h – постоянная Планка, равная 
Экспериментально установлено, что в этих единицах (в соответствии с правилами квантовой механики) наблюдаемые проекции всех спинов на заданное направление принимают либо целое, либо полуцелое значение (либо 1, 2, 3… либо 


Магнитный дипольный момент атома или ядра аналогичен характеристике стрелки компаса. Он представляет собой вращающий момент, действующий на атом или ядро в магнитном поле. Дипольный момент – векторная величина. Магнитный момент атома высчитывается:

где q – заряд электрона, h – постоянная Планка, c – скорость света, 




Намагничивание магнетиков (любого класса) характеризуется намагниченностью, которая определяется как векторная сумма магнитных моментов атомов магнетика в единице объема:


Где J – намагниченность, 

Физическая величина, коэффициент, характеризующий связь между магнитной индукцией 




Магнитная восприимчивость — физическая величина, характеризующая связь между магнитным моментом (намагниченностью) вещества и магнитным полем в этом веществе.

где J – намагниченность веществ под действием магнитного поля, 

Движение молекулы воды в магнитном поле
Будет ли действовать магнитное поле на молекулу воды? Вода – диамагнетик, то есть вещество, результирующий магнитный момент атомов которого равен нулю. Атомы воды не имеют собственных магнитных полей. Но, электроны атома, помещенного во внешнее магнитное поле, приобретают дополнительное вращение, обусловленное полем. В магнитном поле диамагнитный атом приобретает магнитный момент, следовательно, он создает собственное магнитное поле.
При наличии внешнего магнитного поля все атомы диамагнетика (воды) приобретают магнитные моменты одного направления, противоположного внешнему полю. Поля магнитных диполей-атомов усиливают друг друга, и магнетик приобретает собственное магнитное поле направления, противоположного внешнему магнитному полю. Внутри магнетика магнитное поле ослабляется. Однако намагничивание диамагнетика имеет место лишь в присутствии внешнего поля. При снятии поля диамагнитный эффект немедленно исчезает.
Что происходит при помещении молекулы воды в магнитное поле? Когда диполь воды помещается в магнитное поле, на него действует сила Лоренца, заставляющая молекулу совершать колебательные движения.
Сила Лоренца – сила действия электромагнитного поля согласно классической (неквантовой) электродинамике на точечную заряженную частицу. Выражается:

Где q – заряженная частица,