Мутация протромбина что это такое
Маркер связан с изменением уровня фактора II (протромбина) системы свертываемости крови. Исследуется для выявления генетической предрасположенности к тромбоэмболии, тромбозам, инфаркту миокарда, ишемической болезни сердца, тромбоэмболическим осложнениям во время беременности. Имеет прогностическое значение при приеме оральных контрацептивов и гормональной заместительной терапии.
Полимеразная цепная реакция в режиме реального времени.
Какой биоматериал можно использовать для исследования?
Венозную кровь, буккальный (щечный) эпителий.
Как правильно подготовиться к исследованию?
Специальной подготовки не требуется.
Генетический маркер F2 G20210А
Мутация гена F2 проявляется в замене гуанина (G) на аденин (А) в позиции 20210 регуляторной области гена и обозначается как генетический маркер G20210А.
Возможные генотипы
Встречаемость в популяции
Встречаемость аллеля А в европейской популяции составляет от 1,7 до 3 %.
Ассоциация маркера с заболеваниями
Общая информация об исследовании
Система гемостаза представляет собой совокупность биохимических процессов, обеспечивающих жидкое состояние крови, поддержание ее нормальных реологических свойств (вязкости), предупреждение и остановку кровотечений. В нее входят факторы свертывающей, естественной противосвертывающей и фибринолитической систем крови. В норме процессы в ней уравновешены, что обеспечивает жидкое состояние крови. Смещение этого равновесия вследствие внутренних или внешних факторов может повышать риск кровотечений или тромбообразования.
Наследственная тромбофилия (патология, обуславливающая повышенную склонность к тромбообразованию) – одно из самых распространенных генетических нарушений. Она часто остается недиагностированной и проявляется обычно в форме тромбоза глубоких вен и венозной тромбоэмболии. Нарушение свертываемости крови при наследственной тромбофилии в большинстве случаев вызывается изменениями в генах факторов свертывания крови II и V, связанными с известными генетическими маркерами (F2 G20210A, F5 G1691A). Именно они играют главную роль в развитии тромбофилии и ассоциированных с ней заболеваний.
Протромбин (фактор II) – витамин-К-зависимый гликопротеин, синтезируемый в печени и циркулирующий в крови в неактивной форме. При недостатке витамина К уровень протромбина в крови уменьшается, что может приводить к кровотечениям.
Протромбин, или коагуляционный фактор II, является одним из главных компонентов свертывающей системы крови. При мутации гена протромбина повышается экспрессия гена, что в свою очередь приводит к повышению уровня протромбина в плазме. Мутация гена F2 проявляется в замене гуанина (G) на аденин (А) в позиции 20210 и обозначается как генетический маркер G20210А. Изменение происходит в регуляторном участке гена, поэтому нарушения структуры белка не происходит, но это влияет на регуляцию синтеза белка. У носителей аллеля А в крови обнаруживается повышенный уровень протромбина. Соответственно, риск образования тромбов возрастает.
Мутация в гене F2 наследуется по аутосомно-доминантному типу, поэтому патологический эффект реализуется даже при наличии одной копии поврежденного гена (генотип G/A).
Сочетание мутации гена протромбина и мутации Лейден увеличивает риск тромбофилии с ранним началом. Наряду с повышенным риском тромбозов наличие наследственной тромбофилии может быть связано с повышенным риском развития акушерских и гинекологических осложнений (привычное невынашивание, задержка внутриутробного развития плода, гестозы и др.).
Например, спонтанные аборты в первом триместре беременности чаще наблюдаются у пациенток с генотипом G/A. Поэтому для безопасного течения беременности необходимо своевременно выявить генетическую составляющую риска тромбоэмболических осложнений и начать их профилактику.
Проявление носительства тромбофилических генетических мутаций зависит также от возраста, факторов окружающей среды и наличия других мутаций. Носители аллеля, предрасполагающего к тромбофилии, могут не иметь никакой клинической симптоматики заболевания до появления внешних провоцирующих факторов. Негенетические факторы, такие как беременность, прием оральных контрацептивов, гормональная заместительная терапия, длительная иммобилизация, курение и другие, могут значительно увеличивать риск.
Особенно важна генетическая диагностика при наличии наследственной тромбофилии. Наследственный дефект коагуляции следует предполагать при отсутствии тромбоза в возрасте до 45 лет при отсутствии дополнительных факторов риска, например хирургического вмешательства или иммобилизации, при частых тромбозах у взрослых или тромбозе в детском возрасте. Генетическое исследование будет иметь профилактическое значение для человека в случае, если у его кровных родственников имелись тромботические заболевания в молодом возрасте.
Своевременная диагностика генетической предрасположенности к повышенной свертываемости крови поможет избежать серьезных последствий для сердечно-сосудистой системы и развития ассоциированных тяжелых заболеваний при проведении ранних профилактических и/или лечебных мероприятий.
Интерпретация результатов исследования должна проводиться врачом в комплексе с другими генетическими, анамнестическими, клиническими и лабораторными данными.
Исследование рекомендуется проводить в комплексах:
Фактор коагуляции II (тромбин) F2: G20210A в Москве
Генетическое исследование, направленное на выявление мутации гена F2. Мутация ассоциирована с повышенной свертываемостью крови, в результате чего возможно развитие ряда патологий со стороны сердечно-сосудистой системы и тромбоэмболических осложнений беременности.
Приём и исследование биоматериала
Когда нужно сдавать анализ Фактор коагуляции II (тромбин) F2: G20210A?
Подробное описание исследования
Исследование генетической мутации в гене протромбина (F2) используется в диагностике наследственной тромбофилии, которая проявляется тромбозами глубоких вен и легочной артерии, а также рядом акушерских осложнений. Исследование также используется в диагностике заболеваний сердечно-сосудистой системы.
Ген F2 кодирует фактор свертывания крови II (протромбин). Мутация G20210A связана с заменой гуанина на аденин в положении 20210. В результате мутации изменяется синтез протромбина. Люди с А-аллелем имеют увеличенный синтез протромбина, в результате чего риск формирования тромбов повышается.
При повреждении сосудистой стенки в организме человека запускается процесс свертывания крови, называемый гемостазом. Гемостаз включает в себя серию последовательных химических реакций (каскад коагуляции). В этом каскаде участвуют факторы свертывания крови, которые активируются один за другим и приводят к формированию кровяного сгустка, который препятствует излишней кровопотере.
Для обеспечения нормального процесса свертывания в крови должно быть достаточное количество всех факторов, каждый из которых должен быть функционально активным.
Недостаточная активность может привести к обильной кровопотере, излишняя активность — к чрезмерному свертыванию.
Протромбин, или фактор II свертывающей системы крови, выступает предшественником тромбина — важнейшего компонента образования кровяного сгустка. Он постоянно находится в плазме крови и активируется в момент повреждения ткани или органа. Как часть свертывающей системы крови он участвует в формировании тромба, который препятствует излишней кровопотере при травме.
Наследственная тромбофилия — распространенная наследственно обусловленная предрасположенность к гиперкоагуляции. Тромбофилия проявляется образованием глубоких венозных тромбозов, тромбоэмболией легочной артерии.
Тромбоз глубоких вен, как правило, поражает бедренную вену и проявляется болью в месте образования тромба (также может наблюдаться судорога или онемение), покраснением кожи на этом участке, а также отеком. Боль усиливается во время ходьбы или физических нагрузок.
Тромбоз легочных артерий приводит к тромбоэмболии легочной артерии, симптомами которой являются одышка, боли в грудной клетке, кашель (иногда с примесью крови), частый слабый пульс, бледность кожи.
Наследственная тромбофилия наследуется по аутосомно-доминантному типу, т.е. для проявления патологии человеку достаточно унаследовать «дефектный» ген от одного из родителей. При наследовании мутации от обоих родителей клинические проявления будут более выраженными. Риск наследования мутации, ведущей к тромбофилии, составляет 50%.
Предрасположенность к тромбофилии может никак не проявляться у человека в обычной жизни, но во время беременности, особенно в третьем триместре, изменение свертываемости крови опасно развитием серьезных осложнений.
При беременности формируется дополнительный маточно-плацентарный круг кровообращения, благодаря которому кровь матери вместе с питательными веществами поступает к плоду. Повышение активности свертывающей системы крови (гиперкоагуляция) в третьем триместре беременности — физиологический процесс, направленный на подготовку к родам и предупреждение массивного кровотечения. При наличии предрасположенности к гиперкоагуляции, риск осложнений беременности возрастает в 10 раз.
Ряд негенетических факторов увеличивают риск формирования осложнений, связанных с гиперкоагуляцией, к ним относят:
Данное генетическое исследование рекомендовано отдельным группам пациентов:
Генодиагностика на наличие мутаций гена F2 у пациентов из групп риска позволяет вовремя начать профилактику тромбозов и избежать развития патологий со стороны сердечно-сосудистой системы (ишемический инсульт, инфаркт миокарда), а также осложнений беременности.
Генетика комплекс протромбин в Москве
Лабораторное исследование по выявлению мутации гена протромбина (фактора II свертываемости крови). Исследование проводится для диагностики предрасположенности к тромбоэмболии, тромбозам, инфаркту миокарда и некоторым тромбоэмболическим осложнениям (послеоперационным и при беременности).
Что входит в комплекс
Приём и исследование биоматериала
Когда нужно сдавать анализ Генетика комплекс протромбин?
Подробное описание исследования
Тромбоз-ассоциированные заболевания или заболевания, связанные с аномальным образованием тромбов в кровеносных сосудах, занимают одну из лидирующих позиций в структуре заболеваемости и смертности населения всего мира.
Тромбофилия (предрасположенность к повышенному образованию тромбов) проявляется рецидивирующими венозными и артериальными тромбозами различной локализации, эмболиями (закупоркой) легочной артерии и других сосудов, инфарктов органов (легких, миокарда, мозга, почек и др.).
Тромбозы относятся к мультифакторным заболеваниям, в основе которых лежит взаимодействие как внешних, так и внутренних генетических (наследственных) факторов риска. Особый интерес представляют полиморфизмы (мутации) генов, продукты которых принимают участие в процессах тромбообразования.
Протромбин – витамин К-зависимый гликопротеин, который под воздействием активированного фактора Х свертывания превращается в тромбин. Мутация гена протромбина G20210A характеризуется заменой нуклеотида гуанина (G) нуклеотидом аденин (A) в позиции 20210. В ходе этого процесса уровень протромбина может быть увеличен в 1,5–2 раза выше нормы.
Данную точечную мутацию считают второй по распространенности мутацией, связанной с наследственной тромбофилией. Частота мутации FII G20210A в европеоидной популяции составляет от 1 до 5%, а у пациентов с венозными тромбоэмболиями – от 4 до 18%.
Характерные проявлениями полиморфизма фактора II – это ранние тромбозы (до 45 лет), инфаркт миокарда, инсульт, тромбоэмболические осложнения при беременности, некоторые патологии течения беременности (гестозы, преэклампсия, отслойка плаценты и др.).
Носители мутированного гена протромбина могут не знать об этом и не иметь никакой клинической симптоматики тромбофилии, но в определенных ситуациях (беременность, прием КОК, гормональная терапия, курение) риск значительно повышается. Особенно важно своевременно определить данную генетическую мутацию в тех случаях, когда у близких родственников была диагнострирована тромбофилия, потому как полиморфизм передается с вероятностью до 50%.
Если диагностирована мутация в гене протромбина рекомендуется: замена КОК другими способами контрацепции; возможно, пожизненная или временная терапия антикоагулянтами при сложных хирургических вмешательствах, а также при осложненной беременности. Также важно определить предрасположенность к тромбоэмболиям при назначении лекарственных препаратов онкобольным.
F2 Thr165Met. Ген протромбина (ген F2).
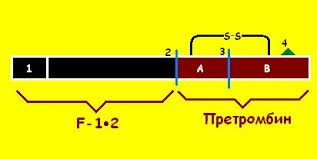
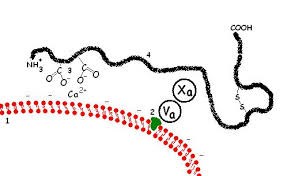
В организме механизм свертывания крови имеет каскадный характер: каждый участник, переходя в активное состояние, приобретает способность активировать другие факторы свертывания. Активация протромбина осуществляется протромбиназой, представляющей комплекс фосфолипида и ионов Ca2+ с факторами свертывания Va и Xa. В результате чего протромбин разлагается до трех пептидов: тромбин, фрагмент F1 и фрагмент F2, Тромбин включается в состав сгустка крови, фрагмент F2 слабо взаимодействует с кальцием. Согласно современным представлениям фрагмент F1 протромбина блокирует образование почечных камней.
Рис.1. Строение протромбина.
Рис.2. Протромбиназный комплекс
Ген протромбина локализован на 11 хромосоме человека в позиции 11p11-q12. Размер гена протромбина составляет 20210 пар оснований, разделяется на 14 экзонов 13 интронами.
Классической и достаточно изученной является мутация протромбина F2 G20210A (20210G>A, rs1799963). Мутацию связывают с наличием ряда мультифакториальных заболеваний: венозный тромбоз, тромбофилия, инфаркт миокарда, атеросклероз, диабет. Проявление генотипа с аллелями «риска» (G/A, A/A): мутация является фактором риска невынашивания беременности, фетоплацентарной недостаточности, внутриутробной гибели плода в I триместре, гестоза (преэклампсии), задержки развития плода, отслойки плаценты. Сдать анализ на мутацию гена F2 G20210A можно у нас в лаборатории ЦИР. Анализ включает выявление двух наиболее распространенных полиморфизмов, связанных с тромбофилией: F2 G20210A и FV 1691 G>A (мутация Лейдена).
Существует еще один вариант мутации гена протромбина – F2 Thr165Met (T165M, 494С>T, rs5896), однако в литературе имеется мало данных о наличии связи данной мутации T165M с возникновением тромбофилии в отличие от классической мутации F2 G20210A.
Однако доказана связь полиморфизма T165M с образованием мочекаменной болезни. Фрагмент протромбина 1 является одним из самых сильных белковых ингибиторов кристаллизации оксалата кальция. За счет значительного количества групп гамма-карбоксиглутаминовой кислоты в составе его молекулы фрагмент связывается с областями кристаллов оксалата кальция, образуя вокруг них протеинового «покрывала», которое препятствует сцеплению кристаллического материала. Считается, что генотип СС и присутствие аллеля С являются защитным фактором в развитии мочекаменной болезни. Есть данные, что полиморфизм 494С>T, который приводит к замене аминокислот треонина на метионин в положении 165 (Thr165Met), изменяет формирование Н-связи. В отличие от треонина метионин в 165 положении не способен образовывать Н-связь с глутаминовой кислотой из 180 положения, тем самым изменяя структуру и функцию белка фрагмента F1 мочевого протромбина (UPTF1). В связи с этим угнетается ингибирующее действие образования камней, приводящее к болезни. Отметим, что эта закономерность в исследовании была характерна для женской группы пациентов.
Также есть литературные данные о связи полиморфизма Т165М с развитием синдрома Ушера – генетического заболевания, характеризующегося сочетанием врожденной нейросенсорной тугоухости и потери зрения (пигментный ретинит). Наиболее частой причиной развития синдрома являются мутации в генах миозина VIIA (MY07A) и ушерина (USH2A), белковые продукты которых играют чрезвычайно важную роль в функционировании сетчатки и внутреннего уха. Известно, что различные мутации в гене MY07A также могут вызывать другие заболевания потери слуха. Есть данные, что полиморфизм Thr165Met имеет способность изменять третичную структуру белка, кодируемого геном MYO7A, тем самым увеличивая риск развития синдрома Ушера.
Тромбофилические и аутоиммунные нарушения.
При наличии репродуктивных проблем, подготовке к беременности, при наступлении беременности, планировании гормональной контрацепции, спектр анализов, связанных с тромбофилическими и аутоиммунными нарушениями гораздо шире.
Мутация протромбина что это такое
Несмотря на значительные достижения в области клинической практики и фармакологии, тромботические события любой локализации остаются ведущей причиной смертности и инвалидизации населения в развитых странах и представляют глобальную медико-социальную проблему [1—3]. Определено, что 6—20% верифицированных тромботических событий обусловлено носительством мутации гена протромбина F2 (20210)GA [4—6], которая характеризуется аутосомно-доминантным типом наследования и заключается в замене нуклеотида гуанин (G) нуклеотидом аденин (A) в позиции 20210. Из-за увеличения экспрессии минорного гена уровень и активность кодируемого геном протромбина могут быть в 1,5—2 раза выше, чем в норме [4]. Протромбин, или фактор II, относится к витамин K-зависимым факторам свертывания крови, являясь предшественником ключевого фермента гемокоагуляции — тромбина [7, 8].
Мутация гена протромбина F2 (20210)GA встречается в 1—6% популяции [9, 10], увеличивая риск развития венозного тромбоза в 2—4 раза [11].
Гомозиготную форму мутации гена протромбина F2 (20210)AA выявляют достаточно редко, с распространенностью приблизительно 1 на 100 000 человек, в связи с чем тромботические риски, связанные с носительством генотипа F2 (20210)AA, изучены мало. В обзоре D. Bosler и соавт. [12] сообщается о 70 случаях гомозиготного носительства F2 (20210)AA. Описанные гомозиготы демонстрируют широкую фенотипическую гетерогенность: от отсутствия эпизодов тромбоза на протяжении всей жизни, несмотря на возможные дополнительные факторы риска (беременность, онкопатология, травма), до страдающих от тромботических эпизодов начиная с неонатального периода. Необходимо отметить, что большинство исследователей согласны с тем, что редкий гомозиготный генотип F2 (20210)AA определяет тяжелое течение и частые рецидивы венозных тромбозов [13—16].
В отличие от этого гетерозиготное носительство мутации протромбина F2 (20210)GA чаще рассматривают как фактор «низкого риска» развития венозных тромбоэмболических осложнений (ВТЭО) [17—19] с отношением шансов на уровне 2—3 [20, 21]. Тем не менее на фоне дополнительных факторов риск может увеличиваться. Сообщается, что при приеме комбинированных гормональных контрацептивов (КГК) для носителей генотипа F2 (20210)GА риск ВТЭО возрастает в 16 раз [22—25], а менопаузальная гормональная терапия увеличивает риск тромбоза глубоких вен (ТГВ) в 2—4 раза [24, 26—28]. Наряду с этим рядом авторов показано, что относительный риск развития ВТЭО во время беременности и послеродовом периоде у пациенток с генотипом F2 (20210)GA составляет 3—15 по сравнению со временем вне беременности [29, 30].
Таким образом, можно предположить, что риск развития тромбозов у носителей мутации гена протромбина F2 (20210)GA кумулятивен и зависит от временно действующих (условно управляемых) факторов, таких как беременность, прием эстрогенсодержащих препаратов [31, 32].
Между тем, несмотря на наличие ассоциативной статистически значимой связи между носительством мутации гена протромбина, генотип F2 (20210)GA, и риском развития тромбоза при действии дополнительных факторов риска, предсказать степень вероятности тромбоза не представляется возможным.
Ранее нами было проведено исследование, направленное на изучение ассоциативной связи лабораторного фенотипа мутации Лейден, генотип F5L(1691)GA, с риском развития тромбозов у женщин репродуктивного возраста. По его результатам установлено, что именно выраженность резистентности фактора Va к активированному протеину С (АРС-R) играет определяющую роль в реализации тромботического события [33, 34]. В то же время данных о фенотипических проявлениях мутации гена протромбина F2 (20210)GA с риском развития тромботических событий нет, что и определило цель настоящей работы.
Цель исследования — определить связь активности протромбина (фактора II) при носительстве мутации гена протромбина, генотип F2 (20210)GA, с тромботическим эпизодами.
Материал и методы
Согласно поставленной цели, на базе клинических подразделений ФГБОУ ВО АГМУ Минздрава России проведено проспективное клиническое когортное исследование. На этапе формирования групп (2008—2011) выделены две когорты. В основную группу (n=146) включили пациенток с мутацией гена протромбина, генотип F2 (20210)GA, выявленной при обращении в Алтайский филиал ФГБУ «Национальный медицинский исследовательский центр гематологии» Минздрава России. Группа контроля (n=160) сформирована путем использования генератора случайных чисел на основе базы данных пациентов женского пола, обращавшихся в клинические подразделения ФГБОУ ВО АГМУ Минздрава России с целью прохождения диспансеризации для выбора метода контрацепции на этапе прегравидарной подготовки. Случайно выбранные пациентки были приглашены к исследованию и в случае получения от них информированного согласия, а также при соответствии критериям включения вошли в контрольную группу.
Критерии включения в основную группу:
— носительство мутации гена протромбина, генотип F2 (20210)GA;
— возраст от 18 до 45 лет.
В контрольную группу включили женщин той же возрастной группы, не являющихся носителями мутации гена протромбина F2 (20210)GA.
Критерии исключения из исследования:
— аутоиммунные заболевания, включая антифосфолипидный синдром;
— снижение функциональной активности антитромбина III, протеинов С или S.
Проведение исследования одобрено локальным этическим комитетом ФГБОУ ВО АГМУ Минздрава России (протокол № 5 от 25.06.12).
Наличие мутации гена F2 (21210)GA методом ПЦР определяли с использованием реактивов фирмы НПО «Литех» (Москва). Материалом для исследования была геномная ДНК человека, выделенная из лейкоцитов периферической крови. У всех пациенток определяли активность протромбина с использованием фактор-II-дефицитной плазмы, реагента Тромборель S и автоматического коагулометра BCS XP («Siеmens», Германия). Следует отметить, что у носительниц F2 (20210)GA активность этого фактора оценивали вне проведения гепаринопрофилактики.
Статистическую обработку данных проводили с использованием пакета статистического программного обеспечения MedCalc Version 17.9.7 (лицензия BU556-P12YT-BBS55-YAH5M-UBE51). Проверку вариационных рядов на нормальность распределения проводили с помощью теста Шапиро—Уилкоксона. Данные лабораторных показателей представлены в виде медианы (Ме), 95% доверительного интервала (95%CI) и интерквартильного размаха (25-й и 75-й перцентили). Сравнение рядов выполняли с использованием непараметрических методов. Для показателей, характеризующих качественные признаки, указывали абсолютное значение и относительную величину в процентах, проверку статистических гипотез о совпадении наблюдаемых и ожидаемых частот осуществляли с использованием критерия χ 2 и точного критерия Фишера. Для бинарных признаков вычисляли относительный риск (ОР) и 95% CI. Критический уровень значимости различий (p) определен как p 0,05) и этнической принадлежности: основная группа на 93,2% представлена европеоидной расой, группа контроля — на 91,9% (р>0,05). Время наблюдения в обеих группах составило не менее 6 лет.
В основной группе тромботические события за 6-летний период наблюдения зарегистрированы у 32 (22,8%) пациенток, в то время как в контрольной — у 2 (1,3%) (ОР 17,1; 95%Cl: 4,2—70,1; р 
Примечательно, что в 66,7% (26 из 39) наблюдений тромбозы имели венозную локализацию (средний возраст пациенток 30,7±4,3 года). Артериальные тромбозы в виде острого инфаркта миокарда и ишемического инсульта диагностированы в 33,3% (13 из 39) случаев (средний возраст пациенток 31,8±3,8 года). Таким образом, можно заключить, что возраст реализации тромботического события при носительстве мутации гена протромбина, генотип F2 (20210)GA, сопоставим (р>0,05) для тромбозов как артериальной, так и венозной локализации.
При более детальном рассмотрении структуры тромбозов (см. таблицу) 
Из 13 эпизодов острого тромбоза, возникших на фоне приема КГК у носительниц мутации гена F2 (20210)GA, в 1 случае диагностирован острый инфаркт миокарда (возраст 39 лет), в 2 случаях развился ишемический инсульт (возраст 24 и 33 года). У 8 пациенток на фоне приема КГК развился тромбоз глубоких вен голени (средний возраст 31,0±2,4 года), в 2 случаях диагностирована ТЭЛА (25 и 39 лет). Трем пациенткам был имплантирован кава-фильтр. Необходимо отметить, что КГК назначали исключительно с целью контрацепции. Принимая во внимание, что эстрогенсодержащие лекарственные средства широко используются в практике гинеколога (контрацепция, менопаузальная гормональная терапия, циклы стимуляции овуляции и т. п.), нами рассчитан риск развития тромбозов на фоне приема КГК у пациенток — носительниц мутации F2 (20210)GA, который составил 13,9 (95% CI: 1,8—105,1; р 
Принимая во внимание полученные данные, мы провели ROC-анализ с целью определения критического порога активности протромбина (в процентах) для прогнозирования развития тромбозов вне зависимости от локализации у носительниц мутации гена протромбина, генотип F2 (20210)GA (рис. 3). 
Площадь под кривой (AUC) у показателя активности протромбина 174,8% определена как 0,904 (95%CI: 0,825—0,955) при уровне значимости р