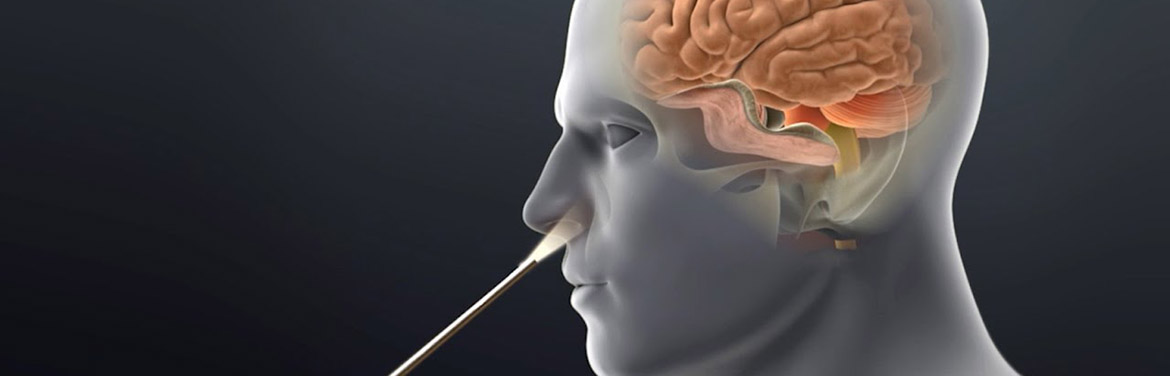
Удаление опухолей гипофиза через нос
Опухоли гипофиза — одно из частых новообразований центральной нервной системы. Чаще всего встречаются доброкачественные опухоли этой одной из важнейших желез внутренней секреции — аденомы. Симптоматика аденом гипофиза может зависеть как от размеров и локализации опухоли, так и от того, какой отдел гипофиза поражен, и какой гормон она продуцирует. В зависимости от размера аденомы гипофиза различают микроаденомы и макроаденомы. Макроаденома имеет размер более 1 см. Она может приводить к симптоматике двумя способами: путем сдавления окружающих структур головного мозга и путем синтезирования определенных гормонов.
Диагностика аденом гипофиза включает лучевые методы — КТ и МРТ, а также рентгенографию черепа.
Лечение опухолей гипофиза может быть как оперативным, так и неинвазивным, в частности, с использованием стереотаксической лучевой терапии.
На сегодня наиболее эффективным и безопасным методом лечения опухолей гипофиза считается малоинвазивное хирургическое вмешательство. Такая операция проводится без вскрытия черепной коробки и всё вмешательство осуществляется трансназально, то есть, через носовой ход эндоскопическим доступом. Такой метод возможен благодаря анатомической особенности расположения гипофиза.
Трансназальный метод удаления опухолей гипофиза сегодня считается наиболее распространенным. По своей сути это так называемый транссфеноидальный метод, так как вмешательство выполняется клиновидную пазуху, пустое пространство в черепе за носовыми проходами, непосредственно под головным мозгом. Задняя стенка этой пазухи покрывает гипофиз.
Еще не так давно трансназальный, или транссфеноидальный доступ для удаления опухолей гипофиза проводится через разрез перегородки носа, при этом хирург был вынужден вскрывать костную стенку клиновидной пазухи специальными инструментами.
В настоящее время такой подход ушел в прошлое и практически всегда для удаления опухолей гипофиза применяется эндоскопический метод. При этом используется специальный инструмент, на конце которого имеется видеокамера и источник света. Перед тем, как такой эндоскоп вводится в полость черепа, в задней части носовой перегородки проделывается отверстие. После этого вскрывается клиновидная пазуха черепа. Для того, чтобы достичь гипофиза, в задней стенки этой пазухи делается отверстие, через которое и вводится эндоскоп.
Трансфеноидальный доступ при удалении опухолей гипофиза имеет ряд преимуществ. Во-первых, он позволяет не затрагивать какие-либо другие области головного мозга, что сводит к минимуму риск повреждения его. Отсутствие необходимости вскрытия черепной коробки — краниотомии — также снижает риск хирургических осложнений. Недостатками данного метода удаления опухолей гипофиза является большая длительность операции при таком доступе и затруднение при опухолях большого размера.
Наиболее эффективно такое вмешательство при микроаденомах, когда размер опухоли менее 1 см. при макроаденомах гипофиза, когда опухоль уже прорастает в близлежащие структуры (нервы, ткань мозга или мозговые оболочки), шансы на адекватное удаление опухоли ниже, а вероятность повреждения соседних тканей мозга — выше.
Удаление опухолей гипофиза через трансназальный транссфеноидальный доступ занимает в среднем до 3 часов, и в большинстве случаев пациент может быть выписан домой через несколько дней. Операция проводится под общим наркозом.
В первые недели после операции может ощущаться усталость, головные боли и заложенность носа, но эти симптомы постепенно проходят. Через 2 недели пациент обычно может вернуться к привычной активности, в том числе к работе.
Удаление опухоли гипофиза может привести к изменению уровня гормонов в крови. Это связано с тем, что после операции гипофиз начинает продуцировать мало гормонов, например, ТТГ. В таких случаях пациенту приходится проводить заместительную гормональную терапию.
Сегодня в ведущих нейрохирургических клиниках стран Западной Европы, США, Израиля, Чехии, Индии, Турции и Южной Кореи, трансназальный метод удаления опухолей гипофиза считается стандартом. Оснащенность клиник современным эндоскопическим оборудование, высокая квалификация и большой опыт зарубежных нейрохирургов, а также комфортные условия пребывания — все это привлекает многих российских пациентов для лечения опухолей гипофиза.
Эндоскопическое транссфеноидальное удаление опухолей селлярной области (аденом гипофиза и краниофарингиом)
Данная операция выполняется при лечении опухолей головного мозга
По наиболее современным методикам удаление большинства аденом гипофиза и других опухолей, расположенных в области турецкого седла, выполняется трансназальным транссфеноидальным способом, т.е. через естественный носовой ход. Эти операции выполняются с помощью эндоскопической стойки малоинвазивным путем. Раньше удаление аденом гипофиза производилось с помощью большой травмирующей операции, сопровождающейся трепанацией черепа.
Суть операции по эндоскопическому удалению аденомы гипофиза
Через правый носовой ход осуществляется доступ к основанию передней черепной ямки. Для этого делается небольшое отверстие, позволяющее подойти к дну турецкого седла. Затем с помощью эндоскопов с различным углом обзора (0, 30 и 45 град.) осуществляется удаление аденомы гипофиза. После чего отверстие закрывается при помощи специальных синтетических метериалов: укладывается небольшой фрагмент косточки и заклеивается специальным клеем. Согласно существующим современным методам какие-либо тампоны в нос не устанавливаются, чтобы пациент мог свободно дышать.
Период реабилитации
Активизация пациента рекомендована на первые сутки после операции. В некоторых случаях возникает необходимость в последующей коррекции гормонального фона. Т.е. после удаления аденомы гипофиза подбирается гормональная терапия, чтобы устранить те клинические проявления, которые были у пациента. При нормальном течении заболевания выписка из стационара возможна на четвертые сутки после операции.
Анализы, требуемые для консультации нейрохирурга
Прежде, чем записаться на консультацию к нейрохирургу относительно аденомы гипофиза, необходимо пройти ряд исследований:
«Бомбу замедленного действия» представляют собой аневризмы сосудов головного мозга, а именно выпячивание истонченного участка стенки кровеносного сосуда. Разрыв аневризмы представляет угрозу для жизни в виде геморрагического инсульта или субарахноидального кровоизлияния. Проявляется резкой, внезапно начавшейся, головной болью (кинжальной), так проявляется спазм сосудов реагирующих на излившуюся кровь
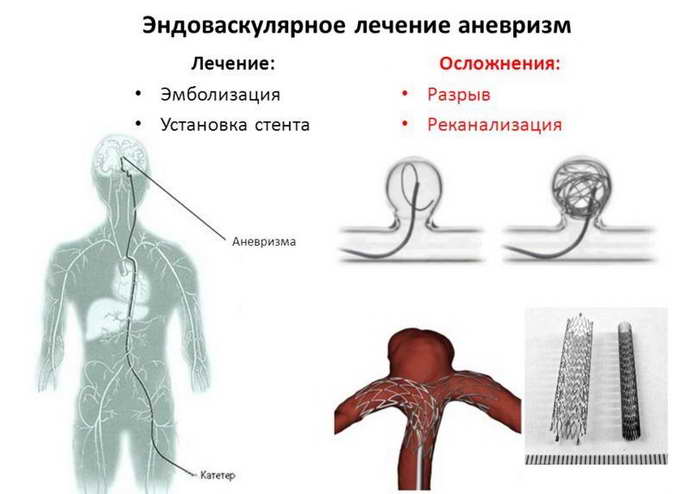
Хирургическая операция является единственным эффективным методом лечения аневризмы сосудов головного мозга. Получив результаты обследований пациента, врач принимает решение о тактике проведения операции. Так как, последствия разрыва аневризмы сосудов головного мозга часто носят летальный характер, проведение оперативного вмешательства может сохранить жизнь пациенту. Оперативное лечение возможно провести как «открытым», так и малоинвазивным способом в зависимости от показаний. «Открытые» операции требуют трепанации черепа, долгой микрохирургической операции и клипирования аневризмы – исключения ее из кровотока.
«Современные технологии эндоваскулярной нейрохирургии дают возможность делать эти операции без трепанации черепа. Через бедренную артерию по всему организму мы проводим специальные катетеры, заходим в аневризму и устанавливаем в нее специальные спирали, после чего аневризма «выключается» (атрофируется) из кровотока и таким образом исчезает риск кровоизлияния», – поясняет заведующая отделением рентгенхирургических методов диагностики и лечения Татьяна Леонидовна Дашибалова.
Бескровные операции – не новинка для бурятских нейрохирургов и рентгенхирургов, в Республиканской клинической больнице им. Н.А.Семашко их выполняют около 8 лет. Однако существуют аневризмы, которые невозможно оперировать открытым методом, в этом случае приходит на помощь метод эндоваскулярной окклюзии (эмболизации). Для передачи бесценного практического опыта в РКБ на один день из Новосибирска приехал один самых известных нейрохирургов России, к.м.н., Виталий Сергеевич Киселев, работающий в ФГБУ «Федеральный центр нейрохирургии». Врачи-рентгенхирурги Арюна Цыденова и Зоригто Балханов с участием Виталия Киселева успешно выполнили эндоваскулярные операции у 5 пациентов со сложными аневризмами. Одному из пациентов был установлен специальный поток перенаправляющий стент с эмболизацией полости аневризмы.
С раннего утра и до позднего вечера в операционной кипела работа. Пристально вглядываясь в мониторы, команда врачей и медсестер устраняла опасные аневризмы. Все манипуляции проводятся под рентген-телевизионным контролем под большим увеличением. Сначала хирург делает прокол в области передней поверхности бедра вблизи паховой связки для доступа к бедренной артерии, в артерию устанавливается интродьюсер – небольшая эластичная трубочка с клапаном, через которую затем проводятся все остальные инструменты, не травмируя стенку артерии. После этого вводится специальный катетер – более длинная и узкая трубочка со специфической конфигурацией её кончика – проводится при помощи проводника в интересующие артерии, через катетер доставляют контрастное вещество, которое хорошо визуализируется под рентгеновским излучением, проводится трехмерная ангиография с компьютерной реконструкцией изображения в объеме, находится аневризма. Далее в полость аневризмы также с помощью проводника вводят микрокатетер.
На втором шаге, как только кончик микрокатетера окажется в полости аневризмы, из микрокатетера высвобождается микроспираль, которая изменяет свою форму, и в виде беспорядочного мотка проволоки занимает собой полость аневризмы. При больших размерах аневризмы может понадобиться несколько спиралей. Заполненная проволочной спиралью аневризма выключается из кровотока и постепенно зарастает соединительной тканью, то есть, исключается возможность ее разрыва.
На заключительном этапе инструменты последовательно извлекаются из сосудистого русла, область пункции бедренной артерии ушивается специальным устройством. Сутки после вмешательства пациент наблюдается в реанимации.
Ежегодно в России примерно у 15 человек из каждых 100 тысяч происходит разрыв аневризмы (выпячивания стенки сосудов мозга), и около 15% таких больных погибает, не успевая доехать до больницы. У половины пациентов кровоизлияние повторяется в течение последующих шести месяцев — в этом случае смертность достигает 70%. И хотя частота таких аномалий высока — их можно диагностировать с помощью МРТ в сосудистом режиме, КТ с контрастированием, а благодаря современным технологиям пациент возвращается домой уже через пару дней после операции.
Операция на мозг через нос
Покорители гипофиза: как и зачем нейрохирурги проникают в мозг через нос
Лоботомия когда-то считалась успешной операцией и якобы излечивала больных от психических расстройств. Ей подверглись тысячи людей, пока сомнительный метод лечения не был запрещен. Методом тыка врачи пытались выяснить, какая область мозга за что отвечает, и безжалостно рассекали вещество головного мозга, иногда даже получая положительный эффект от процедуры. Но недолгий…
Совершенствовались доступы к мозгу: для лоботомии, например, появился специальный инструмент «орбитокласт», который вбивался в череп через глазницу. Советский нейрохирург Борис Егоров, практиковавший данный метод, предложил другой вариант: костно-пластическую трепанацию для лучшего обзора. В общем и целом оперативных доступов в нейрохирургии не счесть; и названия красивые – «арбалетный разрез по Кушингу», например. Трепанация — это только начало.
Археологические находки доказывают, что в нашей стране трепанацию черепа проводили еще в Киевской Руси. Но лечение в те времена заканчивалось сепсисом и смертью. Главная проблема — отсутствие адекватного обезболивания и предупреждение инфекций.
С годами росло мастерство во всех медицинских специальностях, на помощь пришли новые технологии. Слава Рентгену и его лучам: уже в 1907 году австрийский хирург Герман Шлоффер с их помощью подтвердил у пациента аденому гипофиза. И совершил настоящий прорыв: впервые удалил опухоль транссфеноидальным путем — сквозь клиновидную кость черепа.
Это значит, что, разрезав кожу слева от носа, Шлоффер отодвинул в сторону весь носовой лоскут и через клиновидную кость с помощью долота пробился к гипофизу. Все это происходило под рентгенологическим контролем. Потом нос был пришит обратно на место. Пациент перенес операцию хорошо, временно пошел на поправку, но, тем не менее, скончался: опухоль была удалена не до конца и возобновила свой рост. В любом случае Шлоффер уверился — опухоли гипофиза можно и нужно удалять через носовые пути. Другие нейрохирурги вняли ему.
Руки, как у Валуева
– Способ Шлоффера, конечно, не отличается косметической привлекательностью, но для того времени эта техника была прорывной, – комментирует нейрохирург Саратовской областной больницы Евгений Селиванов. – Когда наступила эра эндоскопической хирургии (примерно с начала 90-х годов) аденомы гипофиза и некоторые другие опухоли мозга стали удаляться трансназально — то есть, через нос. С помощью видеоэндоскопической техники доступ осуществляется через общий носовой ход, сам нос остается на месте.
Несколько слов об аденоме гипофиза. Это доброкачественная опухоль, которая может развиваться бессимптомно. Она имеет несколько подвидов и дает в зависимости от них разнообразную клиническую картину. Учитывая, что гипофиз — центральная эндокринная железа, аденомы гипофиза классифицируются в зависимости от гормональной продукции. Из гормонально активных выделяют чаще всего пролактиному.
– Если у женщины нарушается менструальный цикл, появляются выделения из молочных желез, не связанные с беременностью — это повод обратиться к врачу, – говорит Евгений Селиванов. – Так же, как и снижение либидо, появление лишнего веса у представителей обоих полов.
Еще одна разновидность аденомы гипофиза — соматотропинома. Ее появление приводит к акромегалии — патологическому увеличению частей тела под действием гормона роста. Типичный представитель пациентов с этим заболеванием — боксер и депутат Госдумы Николай Валуев.
– Опухоль может появиться в любом возрасте, – рассказывает врач-нейрохирург Селиванов. – Укрупняются черты лица, увеличивается нижняя челюсть, заметно вырастают стопы и кисти рук. Размер обуви может увеличиться в несколько раз. Иногда люди не обращают на это внимания, считая за возрастные изменения. Но акромегалия опасна тем, что увеличиваются так же внутренние органы. Растет нагрузка на сердце, легкие, возникает сердечная недостаточность. Страдают суставы. Инсулиноподобный фактор роста может провоцировать развитие злокачественной опухоли.
Главные признаки кортикотропиномы: ожирение, особенно в области лица и туловища, стрии, истончение и ранимость кожи, повышенное артериальное давление, остеопороз. О развитие тиреотропиномы могут свидетельствовать симптомы гипертиреоза: раздражительность, тремор пальцев рук, учащенное сердцебиение, нарушения сна и т.д. Это если речь идет о гормонально активных аденомах гипофиза.
– Гормонально неактивные аденомы гипофиза чаще всего проявляются нарушением зрения, – продолжает врач. – В целом, любая из них— как гормонально активная, так и нет, – может проявляться хиазмальным синдромом: выпадением полей зрения. Проблема в том, что это происходит, когда опухоль достигла уже значительных размеров. Известны случаи, когда человек лечился у врача-офтальмолога, перенес операцию по удалению катаракты, а у него оказалась аденома гипофиза.
Не все аденомы гипофиза требуют хирургического лечения, некоторые хорошо отзываются на медикаментозное лечение. Диагноз устанавливается на основании клинической картины заболевания, данных МРТ головного мозга и исследования гормонального профиля пациента.
– Если показано хирургическое лечение, то приблизительно 90% аденом гипофиза могут быть удалены трансназальным доступом, – говорит Евгений Селиванов. – Пластика турецкого седла, в котором лежит гипофиз, выполняется аутожиром и фасцией, взятыми с бедра пациента. Реабилитационный период короткий. Пациенты, как правило, выписываются на 5-й день с определенными рекомендациями, одна из которых — постараться исключить сморкание, кашель, чихание. Либо не зажимать нос в этот момент во избежание повышения черепного давления. Не болейте!
Операция на мозг через нос
ВСА — внутренняя сонная артерия
ЖКТ — желудочно-кишечный тракт
САК — субарахноидальное кровоизлияние
ТЭЛА — тромбоэмболия легочной артерии
ХСО — хиазмально-селлярная область
SIADH — синдром неадекватной секреции антидиуретического гормона
Трансназальные операции при аденомах гипофиза активно применяются с 60-х годов XX века [1, 2]. Однако в то время они проводились лишь микрохирургическим методом. С середины 90-х годов при транссфеноидальных операциях начали использовать эндоскопическую технику. Применение эндоскопа позволяет обеспечить широкий обзор зоны вмешательства в условиях хорошей освещенности. При этом создается возможность удаления опухоли из труднодоступных мест под непосредственным визуальным контролем, что повышает радикальность операции и снижает риск повреждения важных анатомических образований [3].
Использование эндоскопической техники расширило показания к операциям, выполняемым транссфеноидальным доступом. В настоящее время более 90% больных аденомами гипофиза оперируют транссфеноидально [4—6]. Стало возможно трансназальное удаление опухолей, которые ранее оперировались только транскраниально. Все чаще трансназально оперируют пожилых и соматически отягощенных больных. Все это привело к тому, что при транссфеноидальном удалении аденом гипофиза изменились частота и структура послеоперационных осложнений [3]. К таким осложнениям следует отнести осложнения доступа (носовые кровотечения, перфорация носовой перегородки, нарушение обонятельной функции, атрофический ринит, синехии, некроз мукопериостального лоскута, внешние деформации носа), инфекционные осложнения (менингит, интракраниальные абсцессы), нарушение мозгового кровообращения (субарахноидальное кровоизлияние, церебральный вазоспазм, ранение крупных сосудов, интракраниальные гематомы), нейроофтальмологические осложнения (зрительные и глазодвигательные нарушения), эндокринные осложнения (гипопитуитаризм, несахарный диабет, гипонатриемия), соматические осложнения и назальную ликворею.
Осложнения доступа
Послеоперационные носовые кровотечения
Носовое кровотечение является серьезным осложнением после транссфеноидального удаления аденом гипофиза и встречается в 0,7—7,1% случаев [6—11] (табл. 1). 
Использование мукопериостального лоскута и прием антитромботических препаратов не являются статистически значимыми факторами риска развития послеоперационного носового кровотечения [7].
Для уменьшения риска развития послеоперационных носовых кровотечений рекомендуется избегать повреждений и профилактически коагулировать клиновидно-небную артерию при доступе в случае ее обнажения. Также необходимо уделять особое внимание контролю артериального давления в послеоперационном периоде [7].
Атрофический ринит
Основными причинами послеоперационного атрофического ринита считаются массивное повреждение слизистой во время доступа, а также интра- и послеоперационные носовые кровотечения, которые требуют более активной коагуляции слизистой оболочки и интраназальных сосудов. Кроме того, причиной послеоперационной атрофии слизистой может послужить длительная послеоперационная тампонада полости носа [12]. Частота встречаемости атрофического ринита составляет 1,6% [12].
Нарушение обонятельной функции
Гипоосмия либо аносмия встречается в 1,4—12% случаев [8, 9, 12—15]. Это осложнение возникает при повреждении слизистой обонятельной области (стенок верхнего носового хода; верхних носовых раковин и верхнего отдела носовой перегородки) полости носа. Риск нарушения обонятельной функции после использования мукопериостального лоскута увеличивается до 26%. В 1-й месяц после операции это может быть связано с большим количеством корок в полости носа [16].
Синехии
После эндоскопических эндоназальных доступов они встречаются в 8,8—21,4% случаев и приводят к нарушениям носового дыхания [11, 17]. Оголенный хрящ носовой перегородки является источником синехий в послеоперационном периоде. Обычно новая слизистая на перегородке образуется через 10—14 нед [18]. Частота образования синехий возрастает до 20% после использования мукопериостального лоскута [16].
Перфорация носовой перегородки
В 2,3—3,7% случаев эндоскопическая хирургия основания черепа осложняется перфорацией носовой перегородки [12—17]. При использовании мукопериостального лоскута это случается почти в 4 раза чаще (14,4%) [18]. Это осложнение может проявляться головной болью, сухостью и заложенностью носа. Зачастую для восстановления адекватного носового дыхания требуется септопластика [12].
Некроз мукопериостального лоскута
Некроз мукопериостального лоскута происходит в связи с нарушением его кровоснабжения и возникает в 1,3% случаев [18]. Это состояние в первую очередь опасно инфекционными осложнениями. Так, в исследовании D. Joseph и соавт. у всех 8 больных с некрозом лоскута развился менингит. У 4 из них также обнаружена эпидуральная эмпиема. Использование эластичных тампонов и баллон-катетеров для тампонады полости носа не увеличивает риска развития некроза лоскута. Единственным статистически значимым фактором некроза лоскута оказалось использование жировой ткани для пластики послеоперационного дефекта основания черепа. Однако причины такой зависимости не описаны [18].
Внешние деформации носа
Деформация спинки носа может появиться исключительно после использования мукопериостального лоскута (в 5,8% случаев) [19]. Одновременное применение расширенного транссфеноидального доступа и мукопериостального лоскута увеличивает риск возникновения внешних деформаций. Причиной этого, вероятно, является использование лоскутов большого размера, за счет чего раневая поверхность носовой перегородки увеличивается [19].
Существуют предположения, что ишемия после выкраивания лоскута в сочетании с работой через оба носовых хода может привести к разрушению каркаса спинки носа (латеральных хрящей и носовой перегородки) и послужить причиной ее деформации [19].
Одной из причин деформации спинки носа является чрезмерно высокий забор пластического материала в виде костных и хрящевых структур.
Назальная ликворея
C развитием эндоскопической эндоназальной хирургии стали широко применяться расширенные трансназальные доступы. Для хирургических манипуляций стала доступна зона от ольфакторной ямки до краниоцервикального сочленения, т. е. почти все костное основание черепа [20]. Формируемый дефект основания черепа может иметь большую площадь, что значительно увеличивает риск развития назальной ликвореи, которая чревата опасными последствиями в виде менингита [20]. Частота развития назальной ликвореи после удаления аденом гипофиза составляет 0,6—16,7% (табл. 2) 
К предоперационным факторам, повышающим риск развития ликвореи после операции, относится недостаточная или избыточная масса тела. В норме индекс массы тела составляет 18,5—24,99 и рассчитывается по формуле
где m — масса тела в килограммах, h — рост в метрах [22].
Также фактором высокого риска послеоперационной ликвореи считаются отсутствие опухолевой капсулы, наличие в ней дефектов и значительные дефекты костей основания черепа [20].
В настоящее время в повседневную практику вошла послойная пластика послеоперационного дефекта основания черепа различными алло- и аутотканями, что значительно снизило частоту ликвореи [20]. Стоит отметить, что использование кровоснабжаемых лоскутов для пластики дефекта основания черепа статистически значимо снижает риск послеоперационной назальной ликвореи [22].
Инфекционные осложнения
Больные с аденомами гипофиза имеют повышенный риск инфекционных осложнений в послеоперационном периоде. Это связано прежде всего с нарушением функций гипоталамуса, который является центральным звеном нервной регуляции гомеостаза, в том числе иммунного. Существует большое количество как экспериментальных данных, так и клинических наблюдений, показывающих наличие иммунодефицита в случае повреждения гипоталамических структур. В частности, обнаружено снижение иммунного ответа, в том числе вторичного, на микробные и немикробные антигены [23].
Также риск инфекционных осложнений связан с самой техникой транссфеноидальных операций. При возникновении интраоперационной ликвореи создается прямое сообщение между бактериально загрязненной полостью носа и стерильной полостью черепа, что может привести к попаданию патогенов интракраниально.
Менингит
Менингит является наиболее частым инфекционным осложнением после транссфеноидального удаления аденом гипофиза. Обычно он проявляется фебрильной лихорадкой, менингеальными знаками. В анализе крови появляются неспецифические признаки воспаления, а в ликворе — увеличение цитоза, лактата, белка и потребления глюкозы.
Основными возбудителями послеоперационных менингитов являются Streptococcus pneumoniae, Staphylococcus epidermidis, Haemophilus influenzae, Corynebacterium spp., Streptococcus viridans, Serratia spp., Enterococcus spp., Klebsiella pneumoniae, Stenotrophomonas maltophilia, Acinetobacter baumannii, Candida albicans [24].
Причины развития послеоперационного менингита различны, но преимущественно связаны с нарушением правил асептики и антисептики. Из них наиболее важными являются характер санитарной обработки операционной, продолжительность операций, их техника, контингент и численность присутствующих на операции [1].
Высокий риск развития менингита ассоциирован с интра- и послеоперационной ликвореей, продолжительностью операции более 60 мин, проведением наружного люмбального дренирования и выполнением повторных операций, направленных на герметизацию полости черепа [15]. В среднем менингит проявляется в течение 14 сут после операции [24].
Несмотря на необходимость проходить нейрохирургическими инструментами через узкий условно загрязненный коридор носовой полости при трансназальных операциях, частота развития менингита после таких операций, по данным некоторых авторов [15, 25], не выше, чем после транскраниальных, и составляет 0,6—7,1% (в среднем 2%).
Интракраниальные абсцессы
Одним из наиболее опасных и потенциально летальных осложнений после эндоскопической хирургии аденом гипофиза является интракраниальный абсцесс. По данным литературы [26], частота встречаемости таких абсцессов составляет 0,2—0,6%. Наиболее частой этиологической причиной интракраниального абсцесса служат стафилококки и стрептококки, обнаруживающиеся в 30% случаев. В ряде случаев высеиваются Neisseria, Micrococcus, Citrobacter, Escherichia coli, Brucella, Salmonella, Corynebacterium и Mycobacterium. Из-за отсутствия специфических клинических симптомов и рентгенологических признаков постановка правильного диагноза осложнена. Зачастую интракраниальный абсцесс, возникший после транссфеноидального удаления аденомы гипофиза, становится интраоперационной находкой. Некоторые авторы [27] считают транссфеноидальное опорожнение методом выбора лечения питуитарных абсцессов, возникших после трансназального удаления аденом гипофиза. Транссфеноидальный доступ позволяет избежать интракраниального распространения инфекции. Во время операции ключевыми моментами являются удаление гноя и широкая трепанация передней стенки пазухи и дна турецкого седла для обеспечения аэрации и дренирования полости абсцесса [27]. Также описаны случаи транскраниального удаления питуитарных абсцессов. Течение послеоперационного периода после таких операций тяжелее, чем после трансназальных, частота развития менингита — выше [27].
Нарушение мозгового кровообращения
Повреждение крупных артерий
Повреждение крупных сосудов виллизиева круга — одно из наиболее грозных осложнений при удалении аденом гипофиза [1]. Фактором высокого риска повреждения сосудов является вариабельность анатомии интракавернозного сегмента внутренней сонной артерии (ВСА), который может значительно смещаться у пациентов с аденомами гипофиза [28]. При акромегалии и болезни Иценко—Кушинга стенки артерий становятся более хрупкими вследствие артериальной гипертензии и атеросклеротических изменений, а также изменяется анатомия полости носа, клиновидной пазухи, турецкого седла, что затрудняет ориентацию хирурга в операционной ране и повышает риск ранения артериальных сосудов [28].
В работе А. Romero и соавт. [28] проанализированы материалы по 7336 пациентам из изученной литературы и 800 пациентам собственной выборки, которым было выполнено эндоназальное эндоскопическое удаление опухоли основания черепа. Повреждение крупных интракраниальных артерий произошло в 29 (0,36%) случаях. Наиболее частой первичной патологией у пациентов, перенесших ранение артерии, оказалась аденома гипофиза — 13 случаев, из которых 11 случаев представлены повреждением ВСА и по одному случаю — передней соединительной и глазной артерии [28].
Последствия повреждения сосудов варьируют по тяжести вплоть до летального исхода. Травма сосуда может привести к формированию интракраниальной гематомы, каротидной окклюзии, стенозу, формированию псевдоаневризмы, каротидно-кавернозному соустью, субарахноидальному кровоизлиянию, вазоспазму или дистальной эмболии с ишемией мозгового вещества [28]. Окклюзия или стеноз сонных артерий может возникнуть вторично при длительной тампонаде во время остановки артериального кровотечения [28].
Основной причиной, приводящей к повреждению ВСА, выступают неправильная ориентация хирурга в операционной ране либо чрезмерно агрессивные действия в кавернозном синусе. Частота поражения ВСА обратно пропорциональна опыту хирурга [29].
Субарахноидальное кровоизлияние
Субарахноидальное кровоизлияние (САК) — редкое осложнение после транссфеноидальной хирургии аденом гипофиза и составляет 0,09—3,6% (табл. 3) 
Церебральный вазоспазм
В мировой литературе описаны единичные случаи симптоматического вазоспазма после транссфеноидальных операций. Его патофизиология после транссфеноидальных операций пока окончательно не ясна. Наиболее вероятной причиной являются интраоперационная травма артерий и субарахноидальное кровоизлияние. Еще одной причиной может стать менингит. Вазоспазм часто приводит к ишемическим изменениям в мозге и требует интенсивной терапии [30].
В работу A. Puri и соавт. [31] вошли 9 случаев симптоматического вазоспазма, описанных в мировой литературе с 1980 г. Из 9 случаев лишь 2 закончились выздоровлением, 3 случая — инвалидностью (пациенты были выписаны с гемипарезом, односторонним амаврозом и афазией) и 4 — летальным исходом. Фактором риска развития ангиоспазма предположительно является большой размер опухоли [31].
Интракраниальные гематомы
Опасным осложнением после удаления аденом гипофиза являются интракраниальные гематомы (0,68—3,7%) [6, 21]. Они могут приводить к зрительным нарушениям и грубому неврологическому дефициту вследствие компрессии черепно-мозговых нервов и окружающих нервных структур.
N. Sudhakar и соавт. [32] описывают собственный опыт транссфеноидальной хирургии, частота интракраниальных гематом после которой составила 0,8%. По данным обзора литературы, выполненного E. Laws [33], частота таких гематом достигает 3%. В статье T. Origitano и соавт. [34] неврологический дефицит из-за послеоперационных гематом либо компрессии нервных структур компонентами пластики послеоперационного дефекта основания черепа составил 7,4% случаев. F. Wang и соавт. [13] описывают 8 (0,69%) случаев из 1166, когда в ложе удаленной опухоли образовались гематомы, 7 из них потребовали эндоскопического эндоназального удаления в связи с возникшими зрительными нарушениями. Лишь у 3 из 7 пациентов зрение восстановилось до прежнего уровня.
Некоторые авторы [35] наблюдали возникновение субдуральных гематом после эндоскопической транссфеноидальной хирургии. В работах, описывающих осложнения после эндоскопической хирургии основания черепа, нет отдельного подробного описания интра- и экстракапсулярных гематом, кровоизлияний в неудаленную часть опухоли.
Нейроофтальмологические осложнения
Зрительные нарушения
Основными причинами зрительных нарушений после транссфеноидальных операций являются интраоперационная травма зрительного нерва, его ишемия либо компрессия зрительных путей гематомой или фрагментами пластики основания черепа.
В мировой литературе [13, 15] крайне скудно представлена тема зрительных нарушений. В основном информация сводится к указанию частоты зрительных нарушений: ухудшение зрительных функций после транссфеноидальных аденомэктомий возникает в 0,43—2,4% случаев.
Глазодвигательные нарушения
Послеоперационное нарушение функций глазодвигательных нервов (III, IV, VI) чаще всего отмечается при аденомах, врастающих в кавернозный синус [23]. Их причиной, так же как и зрительных, считаются интраоперационное повреждение нервов и гематома в ложе удаленной опухоли [36]. G. Frank и соавт. [36] считают наиболее уязвимым VI нерв ввиду его свободного расположения в кавернозном синусе. В свою очередь M. Koutourousiou и соавт. [21] описывают наиболее частое поражение глазодвигательного нерва. При использовании эндоскопического эндоназального доступа глазодвигательные осложнения встречаются в 0,68—11,1% случаев [6, 21].
Эндокринные осложнения
Гипопитуитаризм
Гипопитуитаризм — заболевание, проявляющееся полным или частичным выпадением секреции тропных гормонов гипофиза и, как следствие, недостаточностью функции соответствующих органов периферической эндокринной системы [23]. Переднедолевая гипофизарная недостаточность после удаления аденом гипофиза является следствием интраоперационной травмы аденогипофиза и называется вторичной [23]. Наиболее часто послеоперационный гипопитуитаризм имеет транзиторный характер (до 16,7% случаев) (табл. 4), 
При макроаденомах гипофиз в полости турецкого седла значительно сдавлен и трудно различим интраоперационно, что может приводить к его повреждению во время удаления опухоли и, как следствие, к гипопитуитаризму [13].
По мнению ряда авторов [8, 13], гипопитуитарные нарушения возникают из-за активной работы аспиратором и электрокоагуляции в полости турецкого седла. Поэтому они рекомендуют по возможности заменить электрокоагуляцию на химические средства гемостаза при удалении опухоли (Surgicel и др.) [8, 13].
Несахарный диабет
Несахарный диабет — синдром, проявляющийся выраженной жаждой и выделением большого количества неконцентрированной мочи [23]. У нейрохирургических больных его основной причиной является дефицит или нарушение секреции антидиуретического гормона. Это может происходить в результате компрессии гипоталамуса, стебля гипофиза или нейрогипофиза опухолью либо во время хирургических манипуляций в хиазмально-селлярной области (ХСО). Реже причиной несахарного диабета становится воспалительный процесс (менингит, энцефалит). Так, несахарный диабет транзиторного характера наблюдается в среднем у 30% пациентов после удаления аденом гипофиза. Однако в 3—5% случаев оперированных аденом гипофиза транзиторная форма переходит в постоянную [37]. Факторы риска возникновения несахарного диабета аналогичны факторам риска гипопитуитаризма [8].
Гипонатриемия
Гипонатриемия — одно из наиболее грозных нарушений гомеостаза у больных с аденомами гипофиза, требующее пристального внимания. Это состояние характеризуется снижением уровня натрия в сыворотке крови менее 135 ммоль/л. При отсутствии своевременной диагностики и адекватной терапии гипонатриемия может привести к серьезным осложнениям. Так, по данным K. Asadollahi и соавт. [38], у госпитализированных пациентов с различной патологией с уровнем натрия 120—125 ммоль/л летальность достигает 23%, а менее 115 ммоль/л — 50%.
По данным метаанализа D. Cote и соавт. [39], частота возникновения гипонатриемии после транссфеноидальной хирургии составляет 4—12%. Основной причиной гипонатриемии после удаления опухолей ХСО преимущественно является синдром неадекватной секреции антидиуретического гормона (SIADH) [40]. Однако ряд авторов ведущей причиной послеоперационной гипонатриемии считают церебральный сольтеряющий синдром [40].
Наличие некомпенсированного гипопитуитаризма до операции увеличивает частоту гипонатриемии после операции [40]. У пациентов, получающих глюкокортикоидные гормоны в периоперационном периоде, исключается возможность острой надпочечниковой недостаточности в качестве причины гипонатриемии. Основным фактором неконтролируемого выброса антидиуретического гормона является механическое повреждение нейрогипофиза или стебля гипофиза [40].
Соматические осложнения
Основной причиной органных осложнений после удаления аденом гипофиза является повреждение диэнцефальных структур. Возможно развитие сердечно-сосудистой, дыхательной, почечной, печеночной дисфункции, пареза ЖКТ и тромбоцитопении. Несмотря на очевидность главенствующей роли диэнцефальных структур в регуляции функции жизненно важных органов, крайне мало работ посвящено проблеме развития органной дисфункции при повреждении промежуточного мозга [41].
Дисфункция сердечно-сосудистой системы у пациентов с опухолями ХСО (в том числе с аденомами гипофиза) и осложненным течением послеоперационного периода проявляется прежде всего артериальной гипотензией. Другие жизнеугрожающие нарушения системной гемодинамики не являются характерными для этой категории пациентов. Причинами артериальной гипотензии, развивающейся более чем у 2/3 пациентов с опухолями ХСО при осложненном течении послеоперационного периода, могут быть надпочечниковая недостаточность, тиреоидная недостаточность, пангипопитуитаризм, гиповолемия при декомпенсации несахарного диабета и непосредственное повреждение диэнцефальных структур [41].
Дыхательная дисфункция у пациентов с аденомами гипофиза и осложненным течением раннего послеоперационного периода развивается так же часто, как и артериальная гипотензия, — более чем в 2/3 наблюдений [41].
Кишечная дисфункция, определяемая как парез ЖКТ, выявляется у 70% пациентов с опухолями ХСО и осложненным течением раннего послеоперационного периода. Достоверными причинами кишечной дисфункции оказались сепсис и повреждение диэнцефальных структур [41].
Тромбоцитопения, почечная и печеночная дисфункция развиваются значительно реже — в 28,4 и 1% наблюдений соответственно [41].
Наиболее частой изолированной инфекцией, осложняющей послеоперационный период, является пневмония, а наиболее частой сочетанной инфекцией — менингит и пневмония, а также пневмонии и инфекция мочевыделительной системы [41].
В зарубежной литературе в основном описана подобная частота системных осложнений. Исключением является исследование R. Fahlbusch и соавт. [42], где в 4% случаев после операции развился тромбоз глубоких вен нижних конечностей с последующим развитием ТЭЛА. Два процента больных погибли в связи с послеоперационной пневмонией.
Авторы статей об осложнениях после транссфеноидальной хирургии сходятся во мнении, что системные осложнения значительно чаще возникают в старшей возрастной группе (6,7—32%) [43]. В работе S. Hentschel и соавт. [44] отмечено, что соматические осложнения развились у 32% пациентов старше 70 лет.
Послеоперационная летальность
Частота летальных исходов после транссфеноидальных аденомэктомий невысока и составляет 0—3,2% [8]. В мировой литературе [8, 45, 46] имеется несколько обзоров летальных исходов после транссфеноидальной хирургии аденом гипофиза.
В исследование H. Halvorsen и соавт. [45] вошло 506 транссфеноидальных аденомэктомий (268 выполнено микрохирургическим методом и 238 — эндоскопическим). Летальность в этой серии составила 0,6%. Причиной смертельных исходов были ТЭЛА и массивный отек мозга у пациента с апоплексией аденомы гипофиза.
В работе J. Gondim и соавт. [25] в серии из 301 эндоскопической аденомэктомии летальность составила 1%. Во всех случаях причиной смертельного исхода была сердечная недостаточность, которая возникала не ранее чем через 2 нед после операции.
В метаанализ А. Tabaee и соавт. [46] вошли 824 пациента после эндоскопической аденомэктомии. Летальных исходов в этом исследовании было 2 (0,24%). В обоих случаях причиной смерти стала интраоперационная травма крупных сосудов.
В работах Б.А. Кадашева и соавт. [23, 47] описывается хирургическое лечение больших и гигантских аденом гипофиза, при котором частота летальности принципиально отличалась от таковой при аденомах меньшего размера. Ранее при разных типах операций (транскраниальных и трансназальных микроскопических) она составляла 18%. Основной причиной летальных исходов являлось кровоизлияние в неудаленную часть крупной опухоли. В настоящее время при эндоскопических операциях летальность существенно ниже. Так, E. Constantino и соавт. [11] сообщают о смертности после удаления гигантских аденом в 7,1% случаев. Причинами летальных исходов в этом исследовании были массивное интравентрикулярное кровоизлияние и метаболические нарушения вследствие несахарного диабета [11]. Вместе с тем есть работы [21], описывающие удаление гигантских аденом гипофиза без летальных исходов.
Заключение
Несмотря на постоянное совершенствование методики трансназального удаления аденом гипофиза, существует риск осложнений, в том числе потенциально летальных. Таким образом, разработка эффективных методов профилактики осложнений после эндоскопического эндоназального удаления аденом гипофиза актуальна и сегодня.
Концепция и дизайн исследования — П.Л. Калинин
Сбор и обработка материала — Н.И. Михайлов
Написание текста — Н.И. Михайлов
Редактирование — П.Л. Калинин, И.А. Савин
Авторы заявляют об отсутствии конфликта интересов.