Жизнь с ДЦП. Проблемы и решения. Методы лечения. Малоинвазивные операции.
Детский церебральный паралич (ДЦП) во всех странах мира занимает одно из ведущих мест в структуре хронических болезней детей и взрослых и имеет тенденцию к увеличению распространенности.
C.В. Шишов,
зам. главного врача ООО «Центр новых медицинских технологий», врач травматолог-ортопед, к.м.н.
В результате операции сохраненные мышечные волокна увеличиваются в объеме, улучшается их сократительная способность.
Это приводит к увеличению амплитуды движений у пациента, нарастанию мышечной массы и повышению мышечной силы.
Показания к операции:
Противопоказания к операции:
Малая травматичность операций позволяет устранить до 12-14 мышечных контрактур за один этап. Часто у больных ДЦП выявляется большее количество Рубцовых контрактур, устранение которых за одно оперативное вмешательство невозможно. Тогда хирургическое лечение следует проводить в несколько этапов. Задача каждого комплекса операций — повысить уровень двигательной активности больного. Для этого перед каждым оперативным вмешательством хирург определяет ведущие в клинике контрактуры, подлежащие обязательному устранению на данном этапе. Следует подчеркнуть: хирург должен стремиться к тому, чтобы результат его операции был прогнозируемым на 100%. Для этого он должен тщательно выверить план хирургического вмешательства: во-первых, в момент наблюдения за движениями и позами пациента ортопед определяет наиболее пораженные болезнью мышцы; во-вторых, в момент осмотра и пальпации мышц он выявляет рубцовые тяжи и болевые точки; в-третьих, непосредственно перед операцией, во время наркоза при релаксации мышц (когда рубцовые тяжи выявляются наиболее отчетливо) — ортопед вновь пальпирует мышцы, проверяя намеченный план оперативного вмешательства.
Врач, как скульптор, должен предвидеть результат своей операции, наметить схему реабилитационных мероприятий с обязательным контролем достижений и спрогнозировать: через какой период времени и на каких мышцах нужно провести следующий этап хирургического лечения. Наиболее эффективными являются операции на ранней стадии мышечных контрактур до возникновения стойких контрактур и деформаций суставов. В связи с этим предпочтительно начинать оперативное лечение в возрасте 3-5 лет. Следует отметить, что своевременное хирургическое вмешательство способствует не только увеличению объёма движений ребенка, но и улучшению общего состояния организма, росту, развитию умственных способностей (вследствие увеличения подвижности ребенка и уменьшению патологической импульсации из прооперированных мышц).
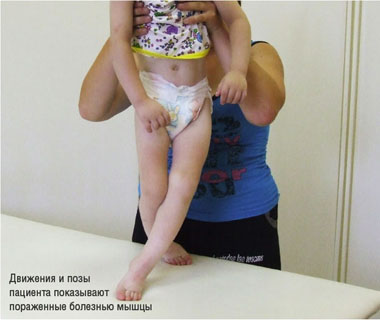
Движения и позы пациента показывают пораженные болезнью мышцы
Оптимальным жизненным режимом для больного ДЦП является такой, при котором пациент двигается каждый час хотя бы по нескольку минут.
Противопоказаны долгие занятия ЛФК с последующими длительными (более 1 часа) периодами покоя.
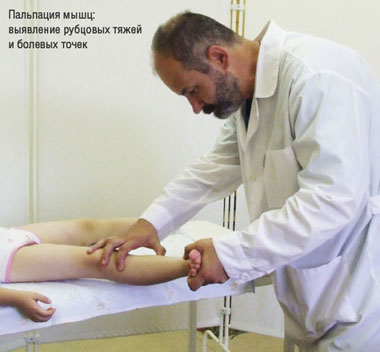
Пальпация мышц: выявление рубцовых тяжей и болевых точек
Правильно организованная послеоперационная реабилитация повышает результативность оперативного лечения и играет важную роль в улучшении двигательных возможностей больного. В течение месяца после операции пациент активизируется в домашних условиях, постепенно расширяя свой двигательный режим до уровня, имевшегося до операции. По мере исчезновения болевого синдрома рекомендуется лечебная физкультура и пассивная гимнастика. Последняя необходима пациентам, у которых объем движений в каких-либо суставах ограничен в связи с продолжительными патологическими позами. Постепенно следует переходить к пассивно-активной и активной гимнастике. Следует помнить, что главная задача лечебной физкультуры (ЛФК) — стимулировать разнообразную двигательную активность больного, не вызывая утомления. Для этого можно использовать различные комплексы физических упражнений, приспособления, тренажеры, адаптированные к возможностям больных ДЦП. Длительность занятий должна соответствовать физическому состоянию пациента: от 10 минут до 30-40 минут. Упражнения должны быть прекращены при появлении признаков утомления. После отдыха занятие следует повторить. При этом мышцы испытывают адекватную физическую нагрузку, что способствует нарастанию мышечной массы и мышечной силы пациента.
При проведении послеоперационной реабилитации не рекомендуются:
Оптимальным жизненным режимом для больного ДЦП является такой, при котором пациент двигается каждый час хотя бы по нескольку минут. Противопоказаны долгие занятия ЛФК с последующими длительными (более 1 часа) периодами покоя. Врач должен контролировать процесс реабилитации, чтобы вовремя внести соответствующие коррективы или назначить следующий этап оперативного лечения. Выполнение всех выше изложенных условий позволит малотравматичным операциям на патологически измененных мышечных волокнах внести весомый вклад в лечение больных ДЦП и поднять процесс реабилитации на качественно новый уровень. Улучшение двигательных функций при этом может и должно быть достигнуто у каждого пациента.
Функциональная нейрохирургия
Нейромодуляция — это терапевтическое изменение функций нервной системы с помощью недеструктивных электрических и медиаторных воздействий. В настоящее время нейромодуляция относится к медицине высоких технологий и активно используется для помощи больным.
Наиболее распространенным синдромом, для лечения которых используются методики нейромодуляции, является синдром спастичности.
Возникновение спастичности в раннем возрасте приводит к нарушению моторного развития и формированию миогенных, а впоследствии и фиксированных контрактур.
Клинические признаки включают:
– мышечное напряжение и ограничение движения
– затруднения в реализации повседневной деятельности (в т.ч. ходьба, прием пищи, самообслуживание)
– развитие неожиданных и болезненных мышечных спазмов
Выраженная спастичность в частности, может:
– препятствовать адекватной и комфортной жизнедеятельности
– приводит к потере самостоятельности из за невозможности самостоятельно осуществлять повседневную деятельность
– снижает качество жизни пациента и его близких, и других лиц, осуществляющих уход
– препятствует эффективному двигательному контролю
Наиболее частыми заболеваниями, при которых наблюдается синдром спастичности, являются синдром детского церебрального паралича ( ДЦП), последствия перенесенной черепно-мозговой травмы, последствия перенесенного внутричерепного кровоизлияиния.
В лечении спастичности на сегодняшний день используется комплексный подход, включающий применение консервативной терапии, реабилитационного, ортопедохирургического и нейрохирургического лечения. Задача лечения заключается в снижении спастичности, коррекции нарушений опорно-двигательного аппарата и формировании правильного двигательного стереотипа. Согласно данным международных исследований, консервативная терапия недостаточно эффективна для адекватной коррекции спастического синдрома.
Нейрохирургические медотики, используемые в лечении спастичности:
— Интратекальная баклофеновая терапия ( ITB)
— Хроническая электростимуляция спинного мозга
Интратекальная баклофеновая терапия
Метод постоянного введения баклофена непосредственно в ликворные пространства спинного мозга при помощи специального насоса ( помпы).
Программируемая инфузионная система предназначена для непрерывного введения точных доз лекарственных средств людям,нуждающимся в длительном лечении мышечной спастичности. Такая инфузионная терапия не излечит основное заболевание, но поможет справиться с его симптомами.
Этот метод позволяет снизить общую дозу препарата и тем самым уменьшить побочные явления от пероральной терапии Баклофеном.
В настоящее время интратекальная баклофеновая терапия является безальтернативным методом лечения спастических гемипарезов и тетрапарезов.
Процедура имплантации состоит из двух этапов:
1. Проведение срининг-теста
Срининг-тест заключается в однократном эндолюмбальном введении Лиорезала и оценке изменения мышечного тонуса после введения. При положительном результате следующим этапом является имплантация инфузионной системы
2. Имплантация инфузионной системы
Система состоит из :
— лекарственная помпа ( объем 20 или 40 мл в зависимости от телосложения и возраста пациента)
Имплантируемая помпа представляет собой работающее на батарейках устройство с запасом назначенного препарата, котороеполностью имплантируется под кожу. Существуют помпы 2 размеров: 20 мл и 40 мл, что соответствует количеству лекарственного средства, которое способна вместить помпа. В центре помпы имеется возвышение, называемое мембраной, через которую врач вводит лекарственное средство, чтобы наполнить помпу. Диаметр помпы составляет 7,62 см, а его толщина – 2,5 см.
— катетера, непосредственно вводимого с люмбальное простраство
Устройство управления представляет собой портативный,работающий на батарейках, компьютер, позволяющий врачу регулировать дозу лекарственного средства и контролировать работу помпы посредством беспроводной радиосвязи.
Помпа изготовлена с использованием передовых технологий, благодаря которым продолжительность работы этого устройства с точным введением препарата достигает примерно 8 лет. При разрядке батарей помпу необходимо заменить хирургическим путем.Учитывая количество препарата, оставшееся в резервуаре помпы, а также запрограммированную скорость его введения, помпа информирует вашего лечащего врача о рекомендуемой дате повторного наполнения. Кроме того, помпа сигнализирует о снижении запаса
Имплантация помпы производится во время хирургического вмешательства под общей анестезией. Данная процедура занимает от 1 до 2 часов. Помпу помещают под кожу в нижней части живота
Очень важно соблюдать график встреч с врачом, чтобы запас препарата в помпе не заканчивался. Если не получается прийти на встречу, как можно скорее свяжитесь со своим врачом, чтобы перенести встречу на другую дату.
Система для нейростимуляции состоит из дыух основных имплантируемых частей:
— нейростимулятор
— электрод
Нейростимулятор представляет собой изолированное устройств, состоящее из батареи и электроники. Он имплантируется подкожно и вырабатывает электрические импульсы, необходимые для стимуляции. Импульсы проводятся по удлинителям и электродам в спинной мозг.
Электроды – электрод представляет собой тонкий провод с контактами на кончике. Для стимуляции электроды имплантируются в эпидуральное пространство ( пространство между позвонком и твердой мозговой оболочкой).
Включенная система нейростимуляции генерирует электрические импулься, которые проводятся по удлинителям и электродам в соответствующие сегменты спинного мозга.
Неимплантируемые компоненты системы:
— программатор врача
— пульт пациента
— зарядное устройство для подзарядки батарей нейростимулятора.
Программатор врача
Используется для программирования стимулятора. Параметры вырабатываемых импульсов могут быть неинвазивно изменены. Программатор передает настройки нейростимулятору дистанционно.
Пульт управления пациента.
Портативное устройство, которое позволяет пациенту включать\выключать нейростимулятор, когда это необходимо или для проверки состояния заряда батареи.
Операция по установке нейростимулятора состоит из трех частей
— имплантация электродов
— тестовая стимуляция
— имплантация нейростимулятора.
1. Имплантация электродов
2. Тестовая стимуляция. Rg, КТ или МРТ-контроль.
3. Имплантация нейростимулятора.
Подбор программы стимуляции
Для эффективного снижения мышечного тонуса в большинстве случаев используется периодический режим стимуляции: 3–6 раз в день по 10–60 минут. Параметры электростимуляции подбираются индивидуально.
Ожидаемые результаты при хирургическом лечении спастичности:
Снижение мышечного тонуса в ногах и в отдельных группах мышц
Улучшение ухода за собой
Улучшение походки
Улучшение функциональной дееспособности и независимости
Снижение боли, связанной со спастичностью
Улучшение перемещения
Улучшение сна
Повышение участия в реабилитационных мероприятиях
Предотвращение или снижение риска спазмов и контрактур
Облегчение гигиенического ухода
Легкость в уходе за пациентами
Операция на спинном мозге при дцп
Задняя селективная ризотомия — нейрохирургическая операция, выполняемая чаще всего на поясничном уровне для снижения патологического мышечного тонуса у больных с нижним спастическим парапарезом. Наиболее часто эта операция выполняется у больных со спастическими формами детского церебрального паралича (ДЦП) [1, 2]. Спастичностью называют зависящее от скорости растяжения усиление тонического стретч-рефлекса, возникающего в результате уменьшения тормозящего влияния на мотонейроны со стороны вышележащих структур [3]. Задняя селективная ризотомия снижает избыточную активность посредством чаcтичного рассечения задних корешков спинного мозга, в которых проходят миотатические волокона — пути, через которые замыкается стретч-рефлекс и реализуется спастический синдром [4]. В 2002 г. был проведен метаанализ ранних результатов ризотомии в 3 рандомизированных исследованиях. Было доказано, что в краткосрочном периоде (от 6 мес до 1 года) задняя селективная ризотомия приводит к снижению спастичности, увеличению объема движений, а также к улучшению локомоторных функций [5—7].
Отдаленные результаты ризотомии прослежены в литературе недостаточно четко, в основном показаны осложнения: деформации позвоночного столба и болевой синдром. По результатам исследования отдаленных результатов ризотомий начиная с 2011 г. были сделаны следующие выводы:
1) невозможно достоверно оценить функциональный результат, так как динамика локомоторного статуса в разных группах по шкале GMFM различна, поэтому динамику функций нужно оценивать отдельно для каждой группы;
2) функциональный результат следует оценивать отдельно в разных возрастных группах;
3) отдаленные осложнения ризотомии, например, такие как деформации позвоночного столба, могут быть не связаны с операцией, так как вообще характерны для больных ДЦП [8].
Проведенная в 1996 г. работа на базе института по исследованию результатов задней селективной ризотомии [1] подтвердила высокую эффективность вмешательства для коррекции патологического мышечного тонуса в отдаленном периоде. Однако работа была выполнена на небольшой серии больных, в работе не применялась оценка больных по глобальным двигательным шкалам. В отдаленном периоде отмечались осложнения в виде прогрессирования деформаций позвоночного столба, что могло объясняться использованием в качестве доступа ламинэктомии.
Цель настоящего исследования — систематизация и оценка отдаленных результатов задней селективной ризотомии у больных с ДЦП, относящихся к различным функциональным группам по шкале GMFM.
Материал и методы
Материал исследования составили 47 больных с ДЦП в форме нижнего спастического парапареза и тетрапареза (см. таблицу): 32 (68%) мальчика и 15 (32%) девочек, средний возраст — 7,4±6,1 года.

Все больные до операции проходили неоднократные курсы консервативного и реабилитационного лечения с незначительным и нестойким клиническим эффектом. Во всех случаях до операции больным проводили ботулинотерапию в спазмированные мышцы нижних конечностей (2—6 инъекций). У 16 больных клинический эффект отсутствовал, у 31 пациента отмечен парциальный клинический эффект, который по мере последующих инъекций регрессировал. В 5 случаях больным уже были выполнены ортопедические вмешательства по поводу фиксированных контрактур: ахиллопластика и удлинение сухожилий мышц hamstring-группы (задней группы мышц бедра).
Отбор больных для хирургического лечения проводился на основании комплексного обследования с участием невролога, физиотерапевта, ортопеда и нейрохирурга. Протокол обследования включал оценку мышечного тонуса по шкале Ashworth, оценку объема пассивных и активных движений, видеорегистрацию ходьбы и оценку локомоторного статуса по глобальной шкале GMFM-88. Шкала Ashworth предполагает градацию мышечного тонуса от 1 до 5 баллов, где за 1 балл принимается нормальное значение мышечного тонуса, а за 5 — максимальное, когда пассивные движения полностью невозможны. Шкала GMFM состоит из 88 стандартных двигательных тестов, каждый из которых в зависимости от степени выполнения градируется по 3-балльной шкале: 0 — отсутствие выполнения движений, 1 — попытка выполнения, 2 — частичное выполнение, 3 — полное выполнение. Сумма баллов отражается в процентном соотношении. Больные, набравшие 20% и менее, относятся к 5-й категории (наиболее тяжелая форма заболевания), от 20 до 40% — к 4-й, от 40 до 60% — к 3-й, от 60 до 80% — к 2-й, от 80 до 100% — к 1-й категории.
Всем больным до операции выполнялось МРТ головного мозга для оценки гидроцефалии и исключения сопутствующей интракраниальной патологии и МРТ поясничного отдела спинного мозга для определения уровня конуса. Контрольный осмотр проводился через 3, 6 и 12 мес после операции, а далее через каждый год.
Статистическую обработку данных выполняли с использованием программы SPSS Statictics 6.0. Применялся корреляционный анализ с использованием коэффициента корреляции (r) Пирсона для оценки силы связи между объемом пересекаемых фасцикул, с одной стороны, и динамикой спастичности и функции — с другой. Для анализа значимых различий между дооперационными и послеоперационными значениями мышечного тонуса и локомоторных функций в различных группах больных применяли непараметрический критерий (Т) Вилкоксона, учитывая малый размер выборки и отсутствие нормального распределения по критерию Колмогорова—Смирнова.
Все больные были включены в исследование с 2007 по 2014 г. Больные, оперированные позже, в исследование не включались, поскольку короткий срок катамнеза не позволял адекватно оценить динамику локомоторных функций. Критериями включения в исследования служили:
1) высокий мышечный тонус (3 балла и более по шкале Ashworth);
2) неэффективность консервативной терапии;
3) неэффективность ботулинотерапии.
К противопоказаниям для проведения ризотомии относились:
1) вторичная мышечная дистония;
2) гиперкинетический синдром;
3) соматические противопоказания.
Задержка психического развития не считалась противопоказанием для хирургического лечения.

При стандартном расположении конуса производилась костнопластическая ламинотомия на уровне Th12—L1. У 2 больных с фиксированным спинным мозгом ламинотомия производилась на уровне L3—L4. После вскрытия твердой мозговой оболочки визуализировался конус спинного мозга. Задний корешок L1 визуализировался в области корешкового отверстия и выделялся до уровня отхождения от заднелатеральной борозды спинного мозга. Далее, следуя по заднелатеральной борозде вниз, последовательно выделяли задние корешки L2—S1. Каждый корешок разделяли на несколько фасцикул. Далее фасцикулы подвергали интраоперационной электростимуляции моно- или биполярным стимулятором с частотой 5 Гц, длительностью импульса 0,1—0,2 мс, амплитудой 0,5—2 мА. При этом оценивали моторные ответы в ногах. Патологическими считались ответы, возникающие в разных мышечных группах либо с противоположной стороны. Фасцикулы, дающие подобные ответы, коагулировали на протяжении и пересекали (рис. 2).

Если при стимуляции фасцикул моторные ответы не регистрировались либо были низкоамплитудными, то такие фасцикулы оставляли интактными. В том случае, если при стимуляции корешка S1 возникали ответы в сфинктере, эти фасцикулы сохраняли интактными для профилактики развития нарушения функций тазовых органов. Корешок S2 во всех случаях сохраняли интактным. В общей сложности пересекали от 50 до 75% объема корешка. При установке костного блока на место производили расщепление дужек Th12—L1, осуществляли пропил в остистых отростках на глубину 2/3 их длины, после чего дужку надламывали. За счет этого устранялся диастаз между дужками и выпиленным костным блоком.
После операции профилактически больным на сутки оставляли мочевой катетер ввиду возможной задержки мочи. Для профилактики развития болевого синдрома в послеоперационном периоде на 4 дня больным назначали трамадол внутримышечно 3 раза в сутки. Вертикализация больных начиналась на 45-е сутки. В течение 3 мес больным рекомендовалось ношение поясничного корсета в положении сидя и лежа. По истечении этого срока выполняли контрольную спондилографию. При отсутствии прогрессирующих деформаций корсет снимали. Физиотерапевтические процедуры начинали выполнять после выписки больных из стационара. Спустя 3 мес после операции оценивали объем остаточных контрактур и решали вопрос о проведении ортопедохирургического лечения.
Результаты
В раннем послеоперационном периоде во всех случаях было отмечено снижение патологического мышечного тонуса в приводящих, икроножных мышцах, hamstring-группе в среднем от 4,34±0,53 перед операцией до 1,61±0,45 после операции (p 
Динамика мышечного тонуса по шкале Ashworth в этих подгруппах была сходной: 2,64 в 3-й категории (от 4,28±0,39 до 1,64±0,24); 2,84 в 4-й (от 4,61±0,5 до 1,77±0,69); 2,59 в 5-й категории (от 4,22±0,54 до 1,63±0,51) (рис. 4).

Наилучшие функциональные результаты были получены у детей в возрастной группе до 10 лет. Суммарная динамика локомоторного статуса составила от 29±14% перед операцией до 32±17% в отдаленном периоде (p