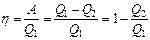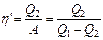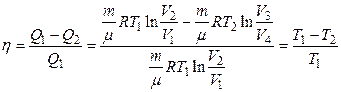Что характеризует термодинамическая вероятность
Термодинамическая вероятность



Состояние системы, определяемое термодинамическими параметрами (р, V, Т), называют макросостоянием, которое и наблюдается на опыте. В статистической физике число микросостояний, реализующих данное макросостояние системы, называют термодинамической вероятностью.
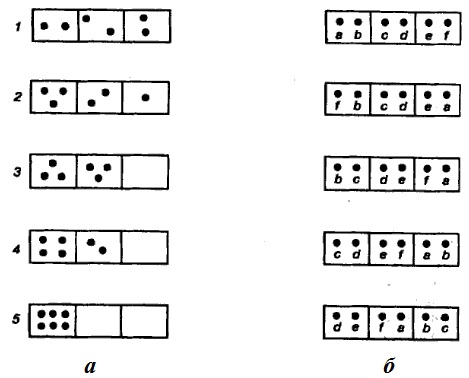
Поясним это на примере. Пусть в сосуде находятся шесть молекул газа. Мысленно разделим сосуд на три равные части.
Хаотически перемещаясь, молекулы создают определенные макрораспределения, некоторые из них показаны на рис. 43а. Любое распределение, например, первое может быть осуществлено рядом микросостояний; некоторые из возможных микросостояний, дающих первое макросостояние, приведены на рис. 43б.
В теоретической физике доказывается, что термодинамическая вероятность, т. е. количество возможных распределений N частиц по n состояниям (шесть частиц в трех частях сосуда), определяется формулой
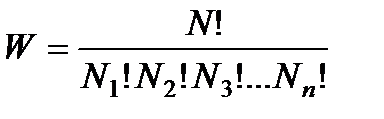
где N1 – число частиц в первом состоянии (первой части сосуда); N2 — число частиц во втором состоянии (второй части сосуда); N3 — число частиц в третьем состоянии (третьей части сосуда) и т.д.
Рис. 43. К понятию термодинамической вероятности
Вычислим термодинамические вероятности макросостояний 1, 2, 3, 4, приведенных на рис. 43а:
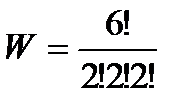
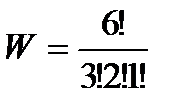
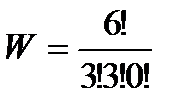
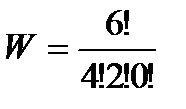
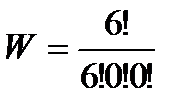
Наибольшая термодинамическая вероятность у равномерного распределения, оно может осуществляться наибольшим числом способов.
Связь энтропии с термодинамической вероятностью установил Больцман — энтропия пропорциональна логарифму термодинамической вероятности:
где k – постоянная Больцмана.
Формула (148) получила название формулы Больцмана.
Статистический смысл понятия энтропии состоит в том, что увеличение энтропии изолированной системы связано с переходом этой системы из менее вероятного состояния в более вероятное.
Одной из формулировок второго закона термодинамики, выявляющей статистический характер этого закона, является формулировка Больцмана: все процессы в природе протекают в направлении, приводящем к увеличению вероятности состояния.
Например, процесс диффузии в газах происходит потому, что равномерное распределение молекул по всему объему статистически будет более вероятным. Второй закон термодинамики является статистическим законом, выполняемым для замкнутых систем, состоящих из большого числа частиц. Второй закон неприменим для систем, состоящих из бесконечного числа частиц, так как для таких систем все состояния равновероятны.
Энтропия – аддитивная величина. Это означает, что энтропия системы равна сумме энтропий ее частей. Очевидно, уравнение Больцмана удовлетворяет этому свойству энтропии. Действительно, Вероятность сложного события, есть произведение вероятностей состояний:
При термодинамическом определении энтропии мы встретились с трудностью распространения этого понятия на случай термодинамически неравновесных состояний. Формула Больцмана (148) дает принципиальный способ преодоления указанной трудности. Надо смотреть на нее как на определение энтропии. Правда, для того чтобы это определение получило конкретное содержание, надо дополнить его способами вычисления вероятностей состояний во всех требуемых случаях. Но и без этого видно, что при таком понимании энтропии закон ее возрастания коренным образом меняет свой характер. Он утрачивает свою абсолютность и превращается в статистический закон. Энтропия замкнутой системы может не только возрастать, но и убывать.
И она действительно будет убывать, если только подождать достаточно долго. Однако процесс убывания снова сменится в дальнейшем процессом возрастания. Что же остается в таком случае от второго начала термодинамики? В чем состоит его физическое содержание? А в том, что за каким-либо заданным состоянием системы будут следовать состояния еще более вероятные, если и не с необходимостью, то в подавляющем большинстве случаев. Если система большая, а исходное состояние ее не очень близко к состоянию равновесия, то переходы системы в менее вероятные состояния будут настолько маловероятны, что на практике они совершенно не имеют никакого значении. Тогда закон возрастания энтропии оправдывается практически с абсолютной достоверностью.
Рассчитаем вероятность таких процессов. Пусть в сосуде находится всего одна молекула. Тогда, если нет внешних силовых полей, молекула с равной вероятностью может попасть либо в часть 1, либо в часть 2. Вероятности попадании ее в эти одинаковые части Р1 = Р2 = 1 /.2. Введем в сосуд вторую молекулу. Так как молекулы идеального газа не взаимодействуют между собой, то их попадания в ту или иную часть сосуда будут независимыми событиями. Вероятность того, что обе они окажутся в части 1, найдется по теореме умножения вероятностей и будет равна P1 = 1 /2 1 /2 = 1 /4.
Рассмотрим еще раз рис. 1а. Энтропия системы максимальна для 1-го состояния. Это состояние является наиболее хаотическим, или наиболее разупорядоченным. В этом состоянии система абсолютно однородна. Состояния 2, 3, 4, 5 характерны тем, что система становится неоднородной, в расположении частиц появляется упорядоченность. При движении от 1-го состояния до 5-го в расположении частиц все больше порядка (увеличивается упорядоченность, или увеличивается неоднородность системы), и при этом понижается энтропия. Наименьшей энтропией обладает вариант 5, когда все частицы расположены в одном месте. В этом случае система максимально неоднородна (или максимально упорядочена).
Термодинамическая вероятность W состояния тела или системы
— это число способов, которыми может быть реализовано данное конкретное термодинамическое состояние (макросостояние). Иначе говоря, это число всевозможных микрораспределений частиц по координатам и скоростям (микросостояний), которыми может быть осуществлено данное макросостояние.
Формула Больцмана:S = klnW
где k—постоянная Больцмана.
Энтропия системы определяется логарифмом числа микросостояний, спомощью которых может быть реализовано данное макросостояние.
Энтропия является мерой неупорядоченности системы, — чембольше число микросостояний, реализующих данное макросостояние, тем больше энтропия.
44. Принцип возрастания энтропии.
Все процессы в замкнутой системе ведут к увеличению её энтропии. В замкнутой системе идут в направлении от менее вероятных состояний к более вероятным, до тех пор, пока вероятность состояния не станет максимальной. В состоянии равновесия — наиболее вероятного состояния системы — число микросостояний максимально, при этом максимальна и энтропия.
45. Второе начало термодинамики.
| Любой необратимый процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает(закон возрастания энтропии). |
Первое начало термодинамики выражает закон сохранения и превращения энергии применительно к термодинамическим процессам.
Второе начало термодинамики определяет направление протекания термодинамических процессов, указывая, какие процессы в природе возможны, а какие — нет.
Существуют ещё две формулировки второго начала термодинамики, эквивалентных закону возрастания энтропии:
1) по Кельвину: невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу;
2) по Клаузиусу: невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к телу более нагретому.
46.Третье начало термодинамики.
| Третье начало термодинамики — теорема Нернста-Планка — постулирует поведение термодинамических систем при нуле Кельвина (абсолютном нуле): энтропия всех тел в состоянии равновесия стремится к нулю по мере приближения температуры к нулю Кельвина. | 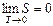 |
Теплоемкости Cv и Сp при Т = 0 К равны нулю, поскольку:
47.Тепловые двигатели и холодильные машины.
Тепловой двигатель — это периодически действующий двигатель, совершающий работу за счет полученной извне теплоты.
Термостатом называется термодинамическая система, которая может обмениваться теплотой с телами практически без изменения собственной температуры.
Рабочее тело — это тело, совершающее круговой процесс и обменивающееся энергией с другими телами.
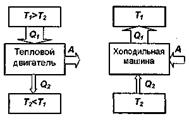
Принцип работы теплового двигателя: от термостата с более высокой температурой Т1, называемого нагревателем, за цикл отнимается количество
 |
Термический КПД двигателя:
Чтобы КПД был равен 1, необходимо, чтобы Q2=0, а это запрещено вторым началом термодинамики.
Количество теплоты Q1, отданное системой термостату Т1, больше количества теплоты Q2, полученного от термостата Т2 на величину работы, совершенной над системой.
Эффективность холодильной машины характеризует холодильный коэффициент η’ — отношение отнятой от термостата с более низкой температурой количества теплоты Q2 к работе А, которая затрачивается на приведение холодильной машины в действие:
48. Теорема Карно
| Извсех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей Т1 и холодильников Т2, наибольшим КПД обладают обратимые машины. При этом КПД обратимых машин, работающих при одинаковых температурах нагревателей и холодильников, равны друг другу и не зависят от природы рабочего тела, а определяются только температурами нагревателя и холодильника. |
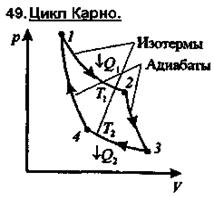 |
Наиболее экономичный обратимый круговой процесс, состоящий из двух изотерм и двух адиабат.
Рассмотрим прямой цикл Карно, в котором в качестве рабочего тела используется идеальный газ, заключенный в сосуд с подвижным поршнем.
Последовательные термодинамические процессы в цикле Карно
| Изотермическое расширение 1—2 Т = const; V2 > V1 | 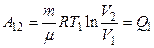 |
| Адиабатическое расширение 2—3 δQ = 0; Т2 Т2 | 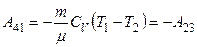 |
Работа, совершаемая в результате кругового процесса,
Для адиабат 2-3 и 4-1 уравнения Пуассона: 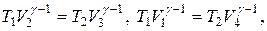
Используя это, термический КПД цикла Карно:
действительно определяется только температурами нагревателя и холодильника.
| Реальные газы, жидкости и твердые тела. |
При рассмотрении реальных газов необходимо учитывать собственный объем молекул и силы межмолекулярного взаимодействия.

Дата добавления: 2016-04-22 ; просмотров: 2130 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Вероятность в термодинамике
Вы будете перенаправлены на Автор24
Вероятность термодинамическая — количество методов, благодаря которым возможно реализовать любое состояние макроскопической физической системы.
Рисунок 1. Энтропия и вероятность. Автор24 — интернет-биржа студенческих работ
В термодинамике положение концепции характеризуется конкретными значениями плотности, температуры, давлением и другими измеряемыми величинами. Перечисленные параметры определяют дальнейшее состояние системы в целом, но при одной и той же плотности, элементарные частицы могут располагаться в различных местах её объёма и иметь совершенно разные значения импульса или энергии.
Каждое состояние термодинамической системы с определенным разделением её частиц по вероятным квантовым или классическим положениям называют в физике микросостоянием.
Вероятность термодинамическая приравнивается количеству микросостояний, которые реализуют существующее макросостояние. Такой процесс не является вероятностью в математическом аспекте, следовательно, используется в статистической физике для определения свойств концепции, находящейся в термодинамическом, постоянном равновесии.
Для точного расчёта вероятности в термодинамике существенно, считаются ли одинаковые элементы системы неразличимыми или различными. Поэтому квантовая и классическая механика приводят к абсолютно разным выражениям для термодинамической вероятности.
Особенности вероятности в термодинамике
Рисунок 2. Термодинамическая вероятность. Автор24 — интернет-биржа студенческих работ
Готовые работы на аналогичную тему
Основное достоинство термодинамики заключается в том, что она помогает рассмотреть общие свойства концепции при равновесии и общие закономерности определения плотности, получить важные сведения о самом веществе, не зная в полной мере его начальную внутреннюю структуру.
Ее законы и методы применимы к любому материальному телу, к любым системам, которые включают магнитные и электрические поля, поэтому они стали основами в таких сферах:
Исследователь Больцман считал атомистическую теорию вполне обоснованной. Бесконечное или огромное количество частиц делает невозможным механический эффект, нуждается в статистическом описании. Математическим инструментом современной статистики является исчисление и определение вероятностей. Больцман доказал, что поскольку базой термодинамических процессов выступают кинетические обратимые процессы, то необратимость в измеряемой термодинамикой энтропии, не может быть на практике абсолютной. Поэтому и энтропия должна быть непосредственно связана с возможностью осуществления данного микросостояния.
Таким образом, необратимый физический процесс есть плавный переход из менее вероятного положения в более вероятное, а логарифм изменения начального состояния с точностью до стабильного множителя полностью совпадает с перемещением энтропии. Этот эффект Больцман использовал для идеального газа.
Чем выше уровень беспорядка в скоростях и координатах частиц системы, тем больше возможность того, что концепция будет в состоянии хаоса. Формула Больцмана может рассматриваться как основное определение энтропии.
Расчет вероятности в системах
Рисунок 3. Расчет вероятности. Автор24 — интернет-биржа студенческих работ
В случае, если система очень большая, а исходное положение ее не слишком близко к состоянию равновесия, то переходы веществ в менее вероятные состояния будут практически невозможны, что на практике они не имеют совершенно никакого значении. Тогда закон увеличения энтропии оправдывается экспериментально с абсолютной достоверностью.
Рассчитаем точную вероятность таких физических процессов. Пусть в определенном сосуде находится всего одна молекула. Тогда, в случае отсутствия внешних силовых полей, элементарная частица с равной вероятностью может оказаться либо в часть 1, либо в часть 2. Вероятности такого попадании одинаковые и записываются так:
После того, как в сосуд попадает вторая молекулу, их попадания будут всегда независимыми состояниями, так как элементы идеального газа не взаимодействуют между собой. В случае, если в течение длительного времени фотографировать распределение атомов в сосуде через равные промежуточные положения, то на каждые 1000 кадров придется в среднем примерно один кадр, на котором будут зафиксированы все молекулы только в части сосуда 1. Аналогичное явление можно наблюдать в части 2.
По гипотезе сложения вероятностей, получится в среднем 2 кадра на каждую тысячу с элементарными частицами, сосредоточенными в любой части системы. Все это не только принципиально вполне возможно, но и фактически доступно обычному наблюдению. Практически нет никаких шансов зафиксировать соответствующую флуктуацию. При равном количеству Авогадро показателю температуры для соответствующей вероятности получается настолько малая величина, что с такого рода возможностями и соответствующими им условиям можно совершенно не считаться.
Различие термодинамической и математической систем
На сегодняшний день ученые разделяют две основные вероятности в термодинамике:
Термодинамической вероятностью называется определенной число микросостояний, посредством которых можно провести необходимое макросостояние концепции. Чтобы найти термодинамическую вероятность ее начального состояния, следует подсчитать количество комбинаций, которые помогут осуществить любое пространственное распределение элементарных частиц.
Этот параметр определяется числом перестановок из наличного движения частиц.
Математическая вероятность состояния равна отношению термодинамической возможности к общей величине возможных микросостояний. Математическая вероятность всегда меньше одной единицы, между тем как вероятность в термодинамике выражается большими числами. Вероятность в математике не аддитивна и непосредственно связана не с термическими особенностями системы, а с механическими, например, с движением молекул в среде и их скоростью.
Одному и тому макросостоянию может соответствовать множество второстепенных микросостояний. По Л. Больцману, чем большим числом таких положений может реализоваться конкретное макросостояние, тем оно на практике более вероятно. Термодинамической вероятностью состоянию концепции называется число микросостояний, реализующих в итоге макросостояние.
При пользовании указанных способов необходимо иметь в виду, что основанные на ней выводы считаются наиболее вероятными только в термодинамическом вопросе, и указывают только на возможность или невозможность того или иного физического процесса. В реальных условиях не исключены незначительные отклонения от сделанных выводов, и протекающие явления могут при отдельных обстоятельствах быть иными, чем те, которые действовали исходя из общих термодинамических соображений.
Термодинамическая вероятность
Вероятность термодинамическая не является вероятностью в математическом смысле. Она применяется в статистической физике для определения свойств систем, находящихся в термодинамическом равновесии (для них Вероятность термодинамическая имеет максимальное значение). Для расчёта Вероятность термодинамическая существенно, считаются ли частицы системы различимыми или неразличимыми. Поэтому классическая и квантовая механика приводят к разным выражениям для Вероятность термодинамическая
Полезное
Смотреть что такое «Термодинамическая вероятность» в других словарях:
ТЕРМОДИНАМИЧЕСКАЯ ВЕРОЯТНОСТЬ — (см. ВЕРОЯТНОСТЬ ТЕРМОДИНАМИЧЕСКАЯ). Физический энциклопедический словарь. М.: Советская энциклопедия. Главный редактор А. М. Прохоров. 1983. ТЕРМОДИНАМИЧЕСКАЯ ВЕРОЯТНОСТЬ … Физическая энциклопедия
термодинамическая вероятность — – вероятность того, что столкнувшиеся молекулы будут иметь достаточную энергию для взаимодействия. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
ТЕРМОДИНАМИЧЕСКАЯ ВЕРОЯТНОСТЬ — см. Энтропия. Геологический словарь: в 2 х томах. М.: Недра. Под редакцией К. Н. Паффенгольца и др.. 1978 … Геологическая энциклопедия
термодинамическая вероятность — termodinaminė tikimybė statusas T sritis Standartizacija ir metrologija apibrėžtis Mikrobūsenų, galinčių sudaryti sistemos makrobūseną, skaičius. atitikmenys: angl. thermodynamic probability vok. thermodynamische Wahrscheinlichkeit, f rus.… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
термодинамическая вероятность — termodinaminė tikimybė statusas T sritis chemija apibrėžtis Mikrobūsenų, galinčių sudaryti sistemos makrobūseną, skaičius. atitikmenys: angl. thermodynamic probability rus. термодинамическая вероятность … Chemijos terminų aiškinamasis žodynas
термодинамическая вероятность — termodinaminė tikimybė statusas T sritis fizika atitikmenys: angl. thermodynamic probability vok. thermodynamische Wahrscheinlichkeit, f rus. термодинамическая вероятность, f pranc. probabilité thermodynamique, f … Fizikos terminų žodynas
термодинамическая вероятность — termodinaminė tikimybė statusas T sritis Energetika apibrėžtis Makroskopinės sistemos būsenos charakteristika, lygi fiziškai skirtingų mikrobūsenų skaičiui, galinčiam užtikrinti tam tikrą makrobūseną. atitikmenys: angl. thermodynamic probability… … Aiškinamasis šiluminės ir branduolinės technikos terminų žodynas
Термодинамическая вероятность — см. Вероятность термодинамическая … Большая советская энциклопедия
ВЕРОЯТНОСТЬ ТЕРМОДИНАМИЧЕСКАЯ — число, пропорциональное количеству физически различимых микроскопических состояний, которыми может быть реализовано данное макроскопическое состояние системы. Напр., состояние газа с определенной энергией может быть реализовано множеством… … Большой Энциклопедический словарь