что называют эффектом джоуля томсона
Полезное
ДЖОУЛЯ-ТОМПСОНА ЭФФЕКТ — (Джоуля Келвина эффект), снижение температуры, имеющее место при выходе газа через небольшое отверстие в зону низкого давления. Это происходит потому, что при выходе газ должен противостоять межмолекулярным силам. На этом эффекте основан принцип… … Научно-технический энциклопедический словарь
ЭФФЕКТ ДЖОУЛЯ-ТОМПСОНА — ЭФФЕКТ ДЖОУЛЯ ТОМПСОНА, см. ДЖОУЛЯ ТОМПСОНА ЭФФЕКТ … Научно-технический энциклопедический словарь
эффект Джоуля — — [Я.Н.Лугинский, М.С.Фези Жилинская, Ю.С.Кабиров. Англо русский словарь по электротехнике и электроэнергетике, Москва, 1999 г.] Тематики электротехника, основные понятия EN Joule effect … Справочник технического переводчика
СКИН-ЭФФЕКТ — (от англ. skin кожа, оболочка) (поверхностный эффект), затухание эл. магн. волн по мере их проникновения в глубь проводящей среды, в результате к рого, напр., перем. ток по сечению проводника или перем. магн. поток по сечению магнитопровода… … Физическая энциклопедия
Скин-эффект — (от англ. skin кожа, оболочка) поверхностный эффект, затухание электромагнитных волн по мере их проникновения в глубь проводящей среды, в результате которого, например, переменный ток по сечению проводника или переменный магнитный поток… … Большая советская энциклопедия
TОMCOHA ЭФФЕКТ — доп. выделение или поглощение тепла (помимо тепла, выделяемого в соответствии с законом Джоуля Ленца) при прохождении тока через проводник, в к ром имеется перепад темп ры. Кол во тепла пропорционально току и перепаду темп ры. Предсказан У.… … Естествознание. Энциклопедический словарь
ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ — один из двух осн. законов термодинамики, представляет собой закон сохранения энергии для систем, в к рых существ. значение имеют тепловые процессы. П. н. т. было сформулировано в сер. 19 в. в результате работ нем. учёного Ю. Р. Майера, англ.… … Физическая энциклопедия
СССР. Естественные науки — Математика Научные исследования в области математики начали проводиться в России с 18 в., когда членами Петербургской АН стали Л. Эйлер, Д. Бернулли и другие западноевропейские учёные. По замыслу Петра I академики иностранцы… … Большая советская энциклопедия
Медицина — I Медицина Медицина система научных знаний и практической деятельности, целями которой являются укрепление и сохранение здоровья, продление жизни людей, предупреждение и лечение болезней человека. Для выполнения этих задач М. изучает строение и… … Медицинская энциклопедия
ФИЗИКА — (от древнегреч. physis природа). Древние называли физикой любое исследование окружающего мира и явлений природы. Такое понимание термина физика сохранилось до конца 17 в. Позднее появился ряд специальных дисциплин: химия, исследующая свойства… … Энциклопедия Кольера
Электротермия — (от Электро. и греч. thérme жар, тепло) прикладная наука о процессах преобразования электрической энергии в тепловую; отрасль электротехники, осуществляющая проектирование, изготовление и эксплуатацию электротермических установок;… … Большая советская энциклопедия
Что называют эффектом джоуля томсона
В гл. II было указано, что расширение идеального газа в пустоту не сопровождается изменением его температуры. Небольшое изменение температуры, наблюдаемое при точных измерениях, объясняется неидеальностью газа. Следующее видоизменение опыта по расширению газа, предложенное Джоулем и Томсоном, позволяет достичь заметного изменения температуры газа, в частности охлаждения, обусловленного его неидёальностью.
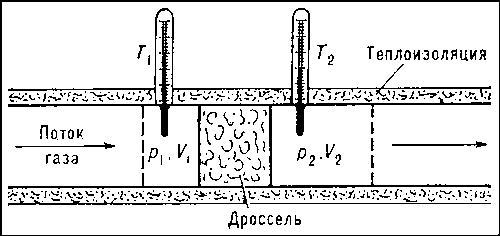
Газ при достаточно большом, но постоянном давлении вынуждают протекать через теплоизолированную пористую перегородку. Это значит, что протекание газа происходит адиабатно,
Гидродинамическое сопротивление перегородки приводит к тому, что на ней теряется часть давления газа и газ выходит из перегородки при более низком давлении. Газ, следовательно, расширяется или, как говорят в технике, дросселируется. Дросселем называется любое устройство, представляющее сопротивление для протекания газа. В технических установках для охлаждения газов вместо пористой перегородки часто используются достаточно узкие сопла.
Для того чтобы течение газа было стационарным, т. е. происходило при постоянных значениях давлений по обе Стороны дросселя, необходим какой-либо насос (компрессор), который поддерживал бы постоянными эти давления. Этот компрессор производит внешнюю работу сжатия газа, которая расходуется на преодоление сопротивления дросселя. Этим процесс дросселирования отличается от расширения газа в пустоту, при котором внешняя работа равна нулю.
Мы покажем, что для неидеального газа процесс Джоуля — Томсона, т. е. процесс дросселирования, вообще говоря, должен сопровождаться изменением его температуры. Такое же расширение идеального газа не вызывает никакого изменения температуры.
Явление изменения температуры газа при его адиабатном расширении дросселированием от одного постоянного давления к другому назьшается эффектом Джоуля — Томсона.
Изменение температуры неидеального газа в процессе Джоуля — Томсона объясняется тем, что при расширении газа увеличивается расстояние между молекулами и, следовательно, совершается внутренняя работа против сил взаимодействия между молекулами. За счет этой работы изменяется кинетическая энергия молекул, а следовательно, и температура газа. В идеальном газе, где силы взаимодействия олекул равны нулю, эффекта Джоуля — Томсона нет.
Количественно эффект Джоуля — Томсона характеризуется дифференциальным коэффициентом Джоуля — Томсона который определяется отношением изменения температуры газа, 
Вычислим коэффициент Джоуля — Томсонаг пользуясь выведенными ранее термодинамическими соотношениями. Это вычисление явится полезной иллюстрацией применения термодинамики для решения конкретных задач. Но прежде чем приступить к этим вычислениям, проанализируем детальнее процесс Джоуля — Томсона. Для этой цели несколько схематизируем этот процесс.
Представим себе, что определенная масса, например 1 моль газа, протекает слева направо через пористую перегородку 
Пусть 1 моль газа занимает объем V, между перегородкой 










Вычислим внешнюю работу, совершенную газом. При перемещении поршня 





Согласно первому началу термодинамики, работа, совершенная газом, должна быть равна изменению его внутренней энергии с обратным знаком, поскольку процесс расширения проведен адиабатно, так что 

Функция 


Для идеального газа как внутренняя энергия, так и произведение 


температуры. Равенство тепловых функций идеального газа по обе стороны перегородки одновременно означает и равенство температур. Значит, для идеального газа коэффициент Джоуля-Томсона равен нулю.
Для неидеального газа, как мы знаем, внутренняя энергия зависит не только от температуры, но и от объема V, занимаемого газом [см., например, (85.10)]. Поэтому равенство тепловых функций в случае реальных газов еще не свидетельствует о равенстве температур.
Действительно, опыт показывает, что большинство газов (азот, кислород, углекислота и др.) в процессе дросселирования при комнатной температуре охлаждаются. Но такие газы, как водород и гелий, при тех же условиях нагреваются. Это означает, что в первом случае коэффициент Джоуля-Томсона 


Заметим еще, наконец, что процесс Джоуля-Томсона является существенно необратимым, следовательно, он сопровождается увеличением энтропии,
После приведенных замечаний нетрудно вычислить коэффициент Джоуля-Томсона.
Уравнение (111.1) может быть переписано в виде:
но 
Теперь необходимо выразить изменение энтропии 


Подставив это значение 
откуда и получается интересующий нас коэффициент Джоуля — Томсона:
где 
Все величины, входящие в (111.4), могут быть определены, если известно уравнение состояния газа, и во всяком случае могут быть измерены. Следовательно, коэффициент 
Из уравнения (111.4) видно, что знак коэффициента 




Для идеальных газов
в чем мы убедились выше.
Для реальных газов 



Если состояние газа описывается уравнением Ван-дер-Ваальса, то, пользуясь (111.4), нетрудно найти и численное значение коэффициента Джоуля-Томсона. Для этого нужно вычислить производную входящую в (111.4).
Раскрыв скобки в левой части уравнения Ван-дер-Ваальса
Дифференцирование обеих частей уравнения по 

Подставив вместо 

Если давление газа не очень велико (порядка 100—200 атм), то
и в (111.5) ими можно пренебречь; тогда
Из этой формулы сразу видно, что коэффициент Джоуля-Томсона положителен, пока о, или При 

Очевидно, что температура инверсии 
Сопоставив (11.1.7) с выражением для критической температуры
получаем следующее простое соотношение между температурой инверсии и критической температурой:
Это соотношение, полученное в очень грубом приближении, довольно удовлетворительно подтверждается опытом. Во всяком случае, чем ниже критическая температура 


Тотч факт, что в опыте Джоуля и Томсона, который ставился при комнатной температуре, водород при расширении нагревался, в то время как другие газы охлаждались, не является, конечно, особым свойством водорода. Любой газ обнаружит такое же свойство, если ставить опыт при температуре более высокой, чем температура инверсии. Как мы увидим ниже, эффект Джоуля — Томсона используется именно для охлаждения водорода и гелия при их сжижении.
Рассмотрим теперь второй способ охлаждения газов, также применяемый для их сжижения.
Эффект Джоуля – Томсона
Адиабатическое (тепло не обменены) расширение газа может быть осуществлено в нескольких формах. Изменение температуры газа во время расширения зависит не только от начального и конечного давления, но и от того, как происходит расширение.
См. Вывод коэффициента Джоуля – Томсона ниже для доказательства этого соотношения. Значение μ J Т <\ displaystyle \ mu _ <\ mathrm 
Для идеального газа μ J Т <\ displaystyle \ mu _ <\ mathrm 
На практике эффект Джоуля-Томсона достигается за счет расширения газа через дросселирующее устройство (обычно клапан ), которое должно быть очень хорошо изолировано, чтобы предотвратить передачу тепла к газу или от него. Во время расширения из газа не извлекается никакая внешняя работа (например, газ не должен расширяться через турбину ).
В процессе Джоуля – Томсона газ изолирован, поэтому тепло не поглощается. Это значит, что
где h 1 и h 2 обозначают удельные энтальпии количества газа в областях 1 и 2 соответственно.
а) T = 300 K, p = 200 бар, s = 5,16 кДж / (кг · K), h = 430 кДж / кг; б) T = 270 K, p = 1 бар, s = 6,79 кДж / (кг · K), h = 430 кДж / кг; в) T = 133 K, p = 200 бар, s = 3,75 кДж / (кг · K), h = 150 кДж / кг; г) T = 77,2 K, p = 1 бар, s = 4,40 кДж / (кг · K), h = 150 кДж / кг; д) T = 77,2 K, p = 1 бар, s = 2,83 кДж / (кг · K), h = 28 кДж / кг (насыщенная жидкость при 1 бар); f) T = 77,2 K, p = 1 бар, s = 5,41 кДж / (кг · K), h = 230 кДж / кг (насыщенный газ при 1 бар).
Сложно физически представить, что такое коэффициент Джоуля – Томсона, μ J Т <\ displaystyle \ mu _ <\ mathrm 


C п знак равно ( ∂ ЧАС ∂ Т ) п <\ displaystyle C _ <\ mathrm
> = \ left ( <\ frac <\ partial H><\ partial T>> \ right) _
>
μ Т знак равно ( ∂ ЧАС ∂ п ) Т <\ displaystyle \ mu _ <\ mathrm
Последнюю величину измерить легче, чем μ J Т <\ displaystyle \ mu _ <\ mathrm 
Это уравнение можно использовать для получения коэффициентов Джоуля – Томсона из более легко измеряемого изотермического коэффициента Джоуля – Томсона. Далее он используется для получения математического выражения для коэффициента Джоуля – Томсона с точки зрения объемных свойств жидкости.
Чтобы продолжить, отправной точкой является фундаментальное уравнение термодинамики в терминах энтальпии; это
Теперь «деление» на d P при постоянной температуре дает
Это выражение теперь можно заменить μ Т <\ displaystyle \ mu _ <\ mathrm

Это дает выражение для коэффициента Джоуля – Томсона в терминах общеизвестных свойств: теплоемкости, молярного объема и коэффициента теплового расширения. Он показывает, что температура инверсии Джоуля – Томсона, при которой μ J Т <\ displaystyle \ mu _ <\ mathrm 
Легко проверить, что для идеального газа, определенного подходящими микроскопическими постулатами, αT = 1, поэтому изменение температуры такого идеального газа при расширении Джоуля – Томсона равно нулю. Для такого идеального газа этот теоретический результат означает, что:
Внутренняя энергия фиксированной массы идеального газа зависит только от его температуры (а не от давления или объема).