Что такое электролит пример
Неэлектролиты и электролиты: характеристика и свойства
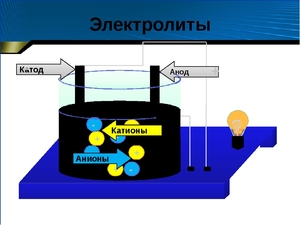
Хорошо известно, что одни вещества в растворенном или расплавленном состоянии проводят электрический ток, другие в тех же условиях ток не проводят. Это можно наблюдать с помощью простого прибора. Он состоит из угольных стержней (электродов), присоединенных проводами к электрической сети. В цепь включена электрическая лампочка, которая показывает присутствие или отсутствие тока в цепи. Если опустить электроды в раствор сахара, то лампочка не загорается. Но она ярко загорится, если их опустить в раствор хлорида натрия.
Вещества, распадающиеся на ионы в растворах или расплавах и потому проводящие электрический ток, называются электролитами.
Вещества, которые в тех же условиях на ионы не распадаются и электрический ток не проводят, называются неэлектролитами.
Неэлектролиты
Неэлектролиты находятся в растворе в виде неполярных или малополярных молекул.
Электролиты
Электролиты распадаются в растворе или расплаве на ионы, и именно наличие ионов способствует прохождению электрического тока. Процесс этот — распада на ионы — называют диссоциацией, а теория, описывающая данные процессы — теорией электролитической диссоциации. В растворе распад на ионы происходит по причине разрыва связей вещества, что является результатом взаимодействия с молекулами воды (то есть происходит гидратация электролита).
Ионы (атомы или их группы, обладающие отрицательным или положительным зарядом) под действием электрического тока начинают двигаться по направлению к одному из электродов, что и обуславливает электропроводимость.
Молекула электролита, способная диссоциировать на большее, чем два, количество ионов, будет диссоциировать постадийно. Примером может служить диссоциация многоосновной кислоты.
Подробнее познакомиться с теорией электролитической диссоциацией вы сможете, посмотрев это видео.
Степень диссоциации
Понятие, количественно характеризующее, насколько полно произошёл распад электролита на ионы, называют степенью диссоциации. Этот показатель рассчитывается как отношение количества продиссоциировавших молекул к общему числу молекул вещества в растворе и фактически показывает долю (процент) распавшихся на ионы молекул в общем количестве.
Следующие факторы могут влиять на степень электролитической диссоциации:
Температура
Зависимость от температуры достаточно сложна. Если распад на ионы экзотермический, то повышение температуры степень диссоциации будет уменьшать, а если эндотермический, повышение температуры приведёт к увеличению степени диссоциации. В целом же для каждого электролита есть определённые температурные условия, в которых он в максимальной степени будет распадаться на ионы.
Изменение показателя константы диссоциации (характеризует способность распадаться на ионы) для уксусной кислоты при изменении температуры можно привести в качестве примера:
максимальная ионизация раствора, как видно, наступает при 25 °C, а при температурах выше и ниже этого значения диссоциация происходит в меньшей степени.
Что такое степень диссоциации? Подробный ответ вы найдете в этом видео.
Природа растворителя и электролита
Стадия процесса диссоциации
Если молекула распадается на ионы постадийно, то каждая следующая стадия имеет примерно в 1000−10 000 раз меньший эффект, чем предыдущая.
Экспериментально определить степень диссоциации можно по электропроводности растворов, т. к. она прямо зависит от концентрации движущихся ионов. Истинное значение при этом получить нельзя, такое значение называют кажущимся. Оно меньше истинного, так как при движении к электродам ионы могут сталкиваться, что частично уменьшает их подвижность. При высокой концентрации может возникать притяжение между ионами, обусловленное электростатическими силами, они чаще сталкиваются, теряя свою подвижность, что влияет на показания электропроводности.
Например, в растворе соляной кислоты (1 моль/л) измерения покажут степень распада на ионы равной 0,78 (78%), но фактически раствор не будет содержать 22% недиссоциированных молекул, так как практически все молекулы диссоциированы.
Сильные и слабые проводники
По величине показателя степени диссоциации, выделяют электролиты сильные и слабые. К сильным условно относят вещества, значение степени диссоциации у которых больше 30%, если данный показатель ниже 5%, то к слабым, остальные считаются электролитами средней силы.
Сильные электролиты:
Видео
Из этого видео вы узнаете о свойствах электролитов.
Электролиты: свойства и классификации
Электролиты – растворы, имеющие в своем составе заряженные частицы, которые принимают участие в переносе зарядов между электродом и катодом. Могут быть сильными и слабыми. Процесс распада молекул на ионы называется электролитической диссоциацией. Неэлектролиты – водные растворы, в которые вещество перешло в виде молекул с сохранением первоначальной структуры. Все молекулы вещества в таких растворах окружены гидратными оболочками (молекулами воды) и не могут переносить электрический заряд.
Растворение кристалла поваренной соли
Как протекает электролитическая диссоциация
Вещества-электролиты устроены за счет ионных или ковалентных полярных связей.
Во время растворения происходит химическое воздействие вещества с молекулами воды, в результате чего оно распадается на электроны. Молекулы воды – активные диполи с двумя полюсами: положительным и отрицательным. Атомы водорода располагаются под углом 104,5°, за счет этого молекула воды приобретает угловую форму.
Вещества, имеющие ионную кристаллическую решетку, намного легче диссоциируют, они уже состоят из активных ионов, а диполи воды во время растворения только ориентируют их. Между диполями воды и ионами электролита возникают усилия взаимного притяжения, связи кристаллической решетки ослабевают и ионы покидают кристалл.
Последовательность процессов при диссоциации растворов с ионной связью
На первом этапе молекулы вещества ориентируются около диполей воды, далее происходит гидратация, а на завершающем этапе диссоциация.
Похожим образом диссоциируют электролиты, у которых молекулы строятся за счет ковалентных связей. Разница только в том, что диполи воды превращают ковалентные связи в ионные. При этом наблюдается такая последовательность процессов:
Электролитическая диссоциация полярной молекулы хлороводорода на гидратированные ионы
В растворах происходит хаотическое движение гидратированных ионов, они могут сталкиваться между собой и опять образовывать отдельные связи. Такой процесс называется ассоциацией.
Классификация электролитов
Все электролиты кроме ионов содержат молекулярные структуры, неспособные переносить разряд. Процентное содержание этих элементов оказывает прямое влияние на возможность проводить ток, параметр обозначается α и определяется по формуле:
Для вычисления берется отношение количества частиц, распавшихся на ионы к общему числу растворенных частиц. Степень распада определяется опытным путем, если она равняется нулю, то диссоциация полностью отсутствует, если равняется единице, то все вещества в электролите распались на ионы. С учетом химического состава электролиты имеют неодинаковую степень диссоциации, параметр зависит от природы и концентрации раствора, чем ниже концентрация, тем выше диссоциация. Согласно данным определениям все электролиты делятся на две группы.
Способность к диссоциации зависит от нескольких факторов, слабые электролиты во многом определяются химическими и физическими особенностями вещества. Важное значение имеет химический состав растворителя.
От каких факторов зависит степень диссоциации
График зависимости константы диссоциации от концентрации
Главные положения теории электролитической диссоциации Согласно существующей теории, электролитическая диссоциация позволяет растворам проводить электрический ток. В зависимости от этой способности они делятся на электролиты и неэлектролиты. Процесс распада веществ на ионы называется диссоциацией, положительно заряженные двигаются к катоду и называются катионами, негативно заряженные двигаются к аноду и называются анионами. Состав электролитов оказывает влияние на способность к диссоциации, технические нормы позволяют определять эту зависимость количественно.
С учетом получаемых после диссоциации ионов изменяется свойство электролитов. Вне зависимости от химического характера образуемых после диссоциации ионов, электролиты подразделяются на три большие классы:
1.Кислоты. В результате распада образуются анионы кислотного остатка и катионы водорода. Кислоты многоосновные могут преобразовываться по первой степени:
2. Основания. Электролиты, дисоциирующие на анионы гидроксогрупп и катионы металла.
3. Соли. Электролиты диссоциируют на анионы кислотного остатка и катионы металлов. Процесс происходит в одну ступень.
Химические свойства электролитов описываются при помощи химических уравнений и определяются свойствами образованных ионов. Для удаления вредных химических соединений, выделяемых в воздух во время диссоциации, используются химически нейтральные пластиковые воздуховоды.
Перспективы развития теории диссоциации На современном этапе развития теории ученые предпринимают попытки описать динамические и термодинамические свойства электролитов учитывая концепцию ионно-молекулярной структуры. Классическая теория считается примитивной, в ней ионы представляются как заряженные жесткие сферы. Главный недостаток традиционной теории – невозможность объяснить локальное снижение диэлектрической проницательности в первом приближении. Ряд растворителей поддается описанию физических свойств ступенчатой зависимостью, но протонные водные растворители имеют намного сложнее процессы релаксации.
Непримитивные модели, рассматривающие ионы в одинаковом масштабе, делятся на две группы:
Зависимость диэлектрической проницаемости от расстояния между ионами
Неравновесные явления в растворах электролитов
Неравновесный распад объясняется несколькими физическими процессами.
Контакт двух растворов с различными показателями концентрации
Принципиальная схема моста переменного тока во время измерения электропроводности
Схема определения числа переноса
Перемещение ионов в среде электрического поля по статистике является усредненным процессом, ионы делают беспорядочные перескоки, а элегическое поле оказывает только определенное влияние, точно рассчитать силу и вероятность влияния невозможно. В связи с этим, аналогия диссоциации с обыкновенным поступательным движением твердых тел весьма приближенная, но она позволяет принимать правильные качественные выводы.
Электролит, понятие, свойства и виды
Электролит, понятие, свойства и виды.
Электролит – вещество, которое проводит электрический ток вследствие диссоциации на ионы, что происходит в растворах и расплавах, или вследствие движения ионов в кристаллических решётках твёрдых электролитов.
Электролит (определение и понятие):
Электролит – вещество, которое проводит электрический ток вследствие диссоциации на ионы, что происходит в растворах и расплавах, или вследствие движения ионов в кристаллических решётках твёрдых электролитов.
Электролиты – вещества, расплавы или растворы которых проводят электрический ток.
Электролиты – вещества, подвергающиеся в растворах или расплавах электролитической диссоциации и проводящие электрический ток за счет движения ионов. Таким образом, движение электрического тока в электролитах обусловлено ионной проводимостью.
Электролиты – это проводники второго рода, вещества, электропроводность которых обусловлена подвижностью положительно или отрицательно заряженных ионов.
К электролитам относятся вещества с ионной или сильнополярной ковалентной связью. К электролитам относятся растворы солей, оснований и кислот, а также вода. Кроме того, некоторые газы ведут себя как электролиты в условиях высокой температуры или низкого давления. Некоторые кристаллы (например, иодид серебра, диоксид циркония) также являются твердыми электролитами.
Соответственно неэлектролиты – вещества, расплавы и водные растворы которых не проводят электрический ток. К неэлектролитам относятся вещества с неполярной и малополярной ковалентной связью. К неэлектролитам относятся газы (двухатомные газы, благородные газы и др.), твердые вещества и органические вещества (спирты, эфиры, бензол, бензин, сахарозу и пр.).
Способность растворов или расплавов электролитов проводить электрический ток объясняется тем, что молекулы электролитов при растворении в воде или других растворителях (например, этаноле, жидком аммиаке, жидком сернистом ангидриде) либо при расплавлении распадаются на электрически положительно и отрицательно заряженные частицы — ионы. Величина заряда иона численно равна валентности атома или группы атомов, образующих ион.
Электролитическая диссоциация (ионизация):
Процесс распада молекул в растворе или расплаве электролита на ионы называется электролитической диссоциацией (или ионизацией). Процесс диссоциации носит обратимый характер. Одновременно с процессами диссоциации в растворах или расплавах электролита протекают и процессы ассоциации ионов в молекулы. При неизменных внешних условиях (температура, концентрация и др.) устанавливается динамическое равновесие между диссоциациями (распадами) и ассоциациями. Это означает, что определенное количество молекул электролита распадается на ионы и такое же количество молекул образуется вновь из ионов. Поэтому в растворах или расплавах электролита всегда диссоциирована определённая доля молекул вещества.
Уравнение диссоциации молекулы электролита (КA) на катион (К + ) и анион (А — ) в общем виде записывается так:
Для конкретных химических соединений уравнение диссоциации выглядит следующим образом:
Число положительных и отрицательных ионов электролита в растворе или расплаве может быть разным, но суммарный заряд катионов всегда равен суммарному заряду анионов, поэтому раствор (или расплав) в целом электрически нейтрален.
Процесс диссоциации электролитов в воде легче всего происходит у соединений с ионной связью (солей, щелочей), которые при растворении образуют гидратированные ионы. Как правило, соединения с ионной связью (соли и щелочи) диссоциируют полностью. Соединения с сильнополярной ковалентной связью диссоциируют частично. При растворении вещества с сильнополярной ковалентной связью (например, хлороводород HCl) диполи воды ориентируются у соответствующих полюсов растворяемой молекулы, поляризую связь и превращая ее в ионную с последующей гидратацией ионов.
Гидратированные ионы устойчивы. Они беспорядочно передвигаются в растворе. Однако под действием электрического тока их движение приобретает направленный характер.
Растворы электролитов обладают способностью проводить электрический ток вследствие движения ионов. Если в раствор или расплав электролита опустить электроды и на электроды подать электрический ток, то под действием электрического тока ионы приобретут направленное движение: положительно заряженные ионы (катионы) будут двигаться к катоду (отрицательному электроду), отрицательно заряженные (анионы) – к аноду (положительному электроду). Направленное движение ионов происходит в результате притяжения их противоположно заряженными электродами. Направленное движение катионов и анионов в растворе или расплаве электролита в противоположных направлениях равносильно электрическому току.
Для измерения количественной характеристики электролитической диссоциации введено понятие степень диссоциации.
Степень диссоциации (α) — это отношение числа молекул, диссоциировавших на ионы (n), к общему числу молекул (N) в растворе электролита.
Степень диссоциации выражается в долях или процентах.
Степень диссоциации (т.е. полнота диссоциации) электролита зависит от многих факторов: от природы электролита, температуры, концентрации и вида растворителя. Так, один и тот же электролит при разной температуре или при одинаковой температуре, но в разных растворителях, будет диссоциирован в разной степени. Так, диссоциация происходит только в полярном растворителе, в частности, в воде. Соли и щелочи диссоциируются полностью. С увеличением концентрации ионизация электролита идет труднее, и наоборот. Повышение температуры способствует повышению степени диссоциации, и наоборот.
Мерой способности электролитов распадаться на ионы в растворах может служить константа электролитической диссоциации (константа ионизации) (Кд).
Константа диссоциации (Кд) – это отношение произведения концентрации диссоциированных ионов к концентрации недиссоциированных молекул электролита.
Константу диссоциации можно выразить уравнением:
KA – концентрация недиссоциированного соединения в растворе;
K + – концентрация катионов в растворе;
A − – концентрация анионов в растворе.
Константа диссоциации (Кд) показывает во сколько раз скорость диссоциации больше скорости ассоциации. Чем больше константа диссоциации, тем сильнее электролит. Константа диссоциации зависит от природы электролита и растворителя, температуры и не зависит от концентрации раствора.
Виды электролитов: сильные и слабые электролиты, солевые, кислотные и щелочные электролиты и пр.:
Исходя из степени диссоциации все электролиты делятся на две группы: сильные электролиты и слабые электролиты.
Сильные электролиты – электролиты, степень диссоциации которых в растворах равна единице (то есть диссоциируют полностью) и не зависит от концентрации раствора. Сюда относятся подавляющее большинство солей, щелочей, а также некоторые кислоты (сильные кислоты, такие как HCl, HBr, HI, HNO3, H2SO4).
Слабые электролиты – электролиты, степень диссоциации меньше единицы (то есть диссоциируют не полностью) и уменьшается с ростом концентрации. К ним относят воду, ряд кислот (слабые кислоты, такие как HF, HNO2, HCO3, HPO4, почти все органические кислоты), основания p-, d- и f-элементов, почти все малорастворимые в воде соли.
Необходимо иметь в виду, что между двумя указанными группами не существует чёткой границы: одно и то же вещество может в одном растворителе проявлять свойства сильного электролита, а в другом – слабого.
В зависимости от вида ионов, на которые распадается вещество при растворении в воде, различаются:
– электролиты без ионов Н + и ОН — (солевые электролиты),
– электролиты с обилием ионов Н + (кислотные электролиты),
– и электролиты с преобладанием ионов ОН — (щелочные электролиты).
В зависимости от вида растворителя электролиты делятся на водные электролиты и неводные электролиты. Отдельно выделяется особый вид электролитов – полиэлектролиты.
В зависимости от того, какое количество ионов образуется при диссоциации молекул электролита, электролиты подразделяются на:
– симметричные электролиты. Симметричные электролиты – электролиты, при диссоциации молекул которого образуется равное число положительных и отрицательных ионов. Симметричными электролитами являются NaCl – 1,1-валентный электролит, HCl – 1,1-валентный электролит и CaSO4 – 2,2-валентный электролит;
– несимметричные электролиты. Несимметричные электролиты – электролиты при диссоциации молекул которого образуется неравное число положительных и отрицательных ионов. Несимметричным электролитом является, например, H2SO4 – 1,2-валентный электролит.
В зависимости от природы электролита выделяются:
– соли. Соли, как электролиты, диссоциируют в водном растворе с образованием иона металла в качестве катиона и иона кислотного остатка в качестве аниона. Соли диссоциируют полностью.
– кислоты. Кислоты, как электролиты, диссоциируют в водном растворе с образованием иона водорода H + в качестве катиона и иона кислотного остатка в качестве аниона. Многоосновные кислоты диссоциируют ступенчато. Причем каждая последующая ступень диссоциирует сложнее, т.к. образующиеся ионы кислотных остатков являются более слабыми электролитами.
Например, фосфорная кислота диссоциирует в три ступени, потому, что имеет 3 атома водорода:
Общая формула диссоциация для фосфорной кислоты будет выглядеть так:
– основания. Основания, как электролиты, диссоциируют в водном растворе с образованием гидроксид-иона ОН — в качестве аниона и иона металла в качестве катиона.
Электролит

Всего получено оценок: 309.
Всего получено оценок: 309.
Электролиты – вещества, расплавы или растворы которых проводят электрический ток. К электролитам относятся кислоты, основания и большинство солей.
Диссоциация электролитов
К электролитам относятся вещества с ионной или сильнополярной ковалентной связью. Первые в виде ионов существуют еще до перевода их в растворенное или расплавленное состояние. К электролитам относятся соли, основания, кислоты.
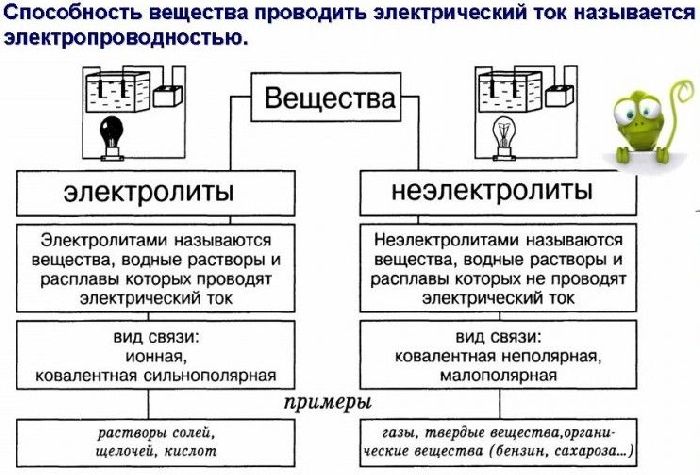
Различают сильные и слабые электролиты. Сильные электролиты при растворении в воде полностью диссоциируют на ионы. К ним относятся: почти все растворимые соли, многие неорганические кислоты (например, H2SO4, HNO3, HCl), гидроксиды щелочных и щелочноземельных металлов. Слабые электролиты при растворении в воде незначительно диссоциируют на ионы. К ним относятся почти все органические кислоты, некоторые неорганические кислоты (например, H2CO3), многие гидроксиды (кроме гидроксидов щелочных и щелочноземельных металлов).
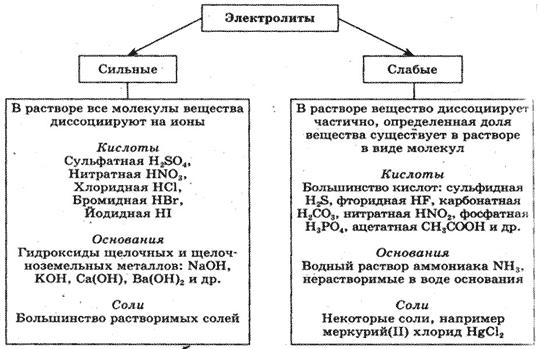
Вода также является слабым электролитом.
Как и другие химические реакции, электролитическую диссоциацию в растворах записывают в виде уравнений диссоциации. При этом для сильных электролитов рассматривают процесс как идущий необратимо, а для электролитов средней силы и слабых – как обратимый процесс.
Кислоты – это электролиты, диссоциация которых в водных растворах протекает с образованием ионов водорода в качестве катионов. Многоосновные кислоты диссоциируют ступенчато. Каждая следующая ступень идет все с большим и большим трудом, так как образующиеся ионы кислотных остатков являются более слабыми электролитами.
Основания – электролиты, диссоциирующие в водном растворе с образованием гидроксид-иона ОН- в качестве аниона. Образование гидроксид-иона является общим признаком оснований и обуславливает общие свойства сильных оснований: щелочной характер, горький вкус, мылкость на ощупь, реакцию на индикатор, нейтрализацию кислот и т. д.
Щелочи, даже малорастворимые (например, гидроксид бария Ba(OH)2) диссоциируют нацело, пример:
Соли – это электролиты, диссоциирующие в водном растворе с образованием катиона металла и кислотного остатка. Соли диссоциируют не ступенчато, а нацело:
Теория электролитической диссоциации
Электролиты – вещества, подвергающиеся в растворах или расплавах электролитической диссоциации и проводящие электрический ток за счет движения ионов.
Теория электролитической диссоциации (С. Аррениус, 1887) в современном понимании включает следующие положения:
Гидратация ионов – экзотермический процесс. Соотношение затраты и выигрыша энергии определяет возможность ионизации в растворе. При растворении вещества с полярной ковалентной связью (например, хлороводород HCl) диполи воды ориентируются у соответствующих полюсов растворяемой молекулы, поляризую связь и превращая ее в ионную с последующей гидратацией ионов. Этот процесс является обратимым и может идти как полностью, так и частично.
Что мы узнали?
Электролиты – это соли, кислоты, основания, способные проводить электрический ток. Электролиты бывают сильные и слабые. Также в статье приводится информация кратко о соединениях электролитов.