Что такое пми в медицине
Что такое пми в медицине
Понятие пациент-ориентированного подхода появилось достаточно недавно. Безусловно, данный подход произрастает из недр клиент-ориентированного подхода, только с той разницей, что в данном случае клиентом (конечным потребителем) является пациент (клиент медицинской организации), а услуга является медицинской. Это вносит в формирование подхода существенные особенности. Приравнивать клиент-ориентированный подход к пациент-ориентированному, конечно, нельзя, хотя стоит заметить, что принципы формирования их, безусловно, едины. Формируя услугу и выводя ее на рынок, необходимо понимать, что ключевым будет конгруэнтность покупательской (потребительской) способности и предлагаемой модели услуг [1]. Продукт (услуга) должен прежде всего соответствовать ожиданиям потребителя. Необходимо выстраивать гибкую систему взаимодействия (работы) с клиентами и своевременно менять условия предоставления услуг в случае изменения потребностей и желаний конечного потребителя. Создание комфортных эмоционально-психологических условий и соучастие в поиске решений для клиента – это базовые принципы наряду со стремлением постоянно совершенствоваться и изменяться к лучшему в отношении производства продукта (услуги) [2]. Особенности пациент-ориентированного подхода заключаются в том, что на основе клиент-ориентированности необходимо создать инновационный подход к планированию, проведению, оценке и контролю медицинской помощи, которая базируется на партнерских и взаимовыгодных принципах сотрудничества между пациентом и его ближайшим окружением (семья) с медицинской организацией в лице административного, врачебного, сестринского и обеспечивающего персонала [3; 4].
Принципы пациент-ориентированного подхода
1. Первый принцип пациент-ориентированности заключается в уважении потребительских ценностей, потребностей и предпочтений. Рассматривая принцип «уважительного отношения к пациенту», можно говорить, что данный аспект отражается в обеспечении прав граждан в сфере оказания медицинской помощи. Помимо этого, ставится во главу угла приоритет интересов пациента.
2. Второй принцип – целостность, логичность и преемственность лечебно-диагностического процесса. Надо понимать, что пациенты в данном аспекте являются уязвимым звеном. Болезнь, которая снижает качество жизни пациента, окрашивает в негативные краски психоэмоциональный фон настроения. Пациент, видя согласованность действий со стороны медицинских работников, вселяет в себя надежду на скорейшее выздоровление.
3. Третий принцип – информированность пациента обо всех деталях лечебно-диагностического процесса, о ходе медико-социальной реабилитации и т.д. Этот принцип достаточно широкий и охватывает много аспектов. Так, пациент по желанию должен иметь доступ к информации о своем заболевании, о клиническом состоянии, о вариантах лечения, а также о методах профилактики.
4. Четвертый принцип – создание комфортных условий пребывания пациента в процессе оказания ему медицинской помощи на всех этапах: в амбулаторно-поликлиническом учреждении, в стационаре, в отделениях реабилитации и т.д.
5. Пятый принцип – обеспечение эмоциональной поддержки в отношении пациента. В реализации данного принципа медицинский работник должен учитывать такие факторы, как обеспокоенность пациента по поводу своего состояния, а также исхода заболевания. Надо учитывать, что пациенты могут испытывать тревогу из-за возможных последствий болезни (инвалидизация, финансовая несостоятельность, потеря работы, проблемы в семье).
6. Шестой принцип – создание условий общения пациента с его ближайшим окружением. Следует уделять внимание уровню субъективного комфорта пациента, по возможности обеспечивать всестороннюю поддержку, не ограничивать его в общении с родственниками, коллегами, друзьями.
7. Седьмой принцип – обеспечение непрерывности лечебного процесса, а также оправдание ожиданий в части его видоизменения со временем. Для обеспечения этого принципа прежде всего надо доносить подробную информацию о лекарственных препаратах, ограничениях, диетах в доступной для пациента форме.
8. Восьмой принцип является базовым и формирующим все предыдущие принципы. Он заключается в надлежащем обеспечении доступности медицинской помощи для потенциального пациента. Это физическая доступность к медицинской организации, наличие общественного транспорта, возможность беспрепятственной записи на прием к врачу, возможность выбора врача, методики лечения.
Внедрение пациент-ориентированного подхода
Один из первых шагов во внедрении пациент-ориентированного подхода при оказании медицинской помощи населению – это необходимость знать мнение пациентов о качестве и доступности оказываемых им медицинских услуг [8]. Самый простой способ – это опрос пациентов «на выходе». Прежде всего, необходимо поменять модель взаимодействия в структуре взаимодействия с пациентом как конечным и ключевым потребителем медицинской услуги [9; 10]. Необходимо задавать вопрос «Что бы Вы хотели улучшить в работе медицинской организации?», а не «Что случилось у Вас при посещении медицинской организации?». При этом надо понимать, что отслеживание настроений и ожиданий пациентов ложится не на плечи медицинских работников (врачебный и/или средний медицинский персонал), а на обеспечивающий персонал по данному направлению. Медицинский персонал обеспечивает основной поток ценностей организации, и пациент-ориентированность в их отношении лежит в области этики и деонтологии медицинской деятельности, степени эмпатии и т.д. [11].
Можно говорить о трёхуровневой системе (структуре) пациент-ориентированного здравоохранения. На микроуровне ключевым является модель взаимоотношений «врач – пациент», на среднем уровне – «медицинская организация – пациент», на макроуровне – «национальная система здравоохранения – пациент». При этом в сбалансированной системе здравоохранения основой в этой структуре является модель «врач – пациент». Она является «материнской платформой» (базовым неделимым элементом) для формирования модели «медицинская организация – пациент». В свою очередь, модель «медицинская организация – пациент» является базовым элементом для модели макроуровня [12]. В несбалансированной системе здравоохранения одна из моделей может преобладать на фоне деградации других моделей. Так, например, при гипертрофии модели «врач – пациент», которая преобладает в кризисные ситуации (при разрушении национальной системы здравоохранения), формируется частный децентрализованный сектор медицинских организаций. При увеличении роли государства и централизации системы здравоохранения, бюрократизации и формализации лечебно-диагностического процесса происходит деградация модели «врач – пациент». При этом при увеличении доли государства в формировании национальной системы здравоохранения, при отсутствии эффективных инструментов управления (процессно-ориентированный подход в управлении медицинской организацией, внедрение бережливых технологий на рабочих местах) и контроля (независимые профессиональные союзы, ассоциации и т.д.), происходит монополизация рынка медицинских слуг и уничтожение конкурентных взаимоотношений [13]. Отсутствие конкуренции на рынке медицинских услуг пагубно сказывается как для медицинских работников, так в итоге и для пациентов. Для медицинского персонала в данной ситуации ключевым критерием профессиональной состоятельности становится не уровень и широта компетенций, а лояльность к работодателю. Для пациентов – это прежде всего падение качества медицинских услуг [14; 15].
Внедрению пациент-ориентированного подхода в оказании медицинских услуг могут препятствовать ряд факторов. Прежде всего, это система профессиональной организации труда медицинских работников. Здесь одним из ключевых факторов является негибкая система оплаты труда. В настоящее время, несмотря на введение эффективных критериев оценки труда сотрудников, утвержденная система, по сути, не учитывает качества оказываемых медицинских услуг (за исключением формальных критериев). Привязка количества обслуживаемых пациентов к оценке качества оказанных услуг и уровню оплаты труда является не эффективной в долгосрочной перспективе [16]. Такой подход может привести в формальной оценке труда медицинских работников без корреляции с показателями здоровья обслуживаемого населения. Зачастую врач может стремиться (если речь идет о корреляции между уровнем оплаты труда и количеством пациентов) к увеличению базы пациентов. Тем самым сокращается время, затрачиваемое на каждого пациента в отдельности. Такой подход неминуемо приведет к падению качества медицинских услуг, профессиональному выгоранию и деградации модели «врач – пациент» [17].
Одним из примеров привязки уровня оплаты врача к количеству пациентов могут служить данные социологического опроса медицинских сотрудников, проведённого Ernst&Young Russia в 20 тыс. медицинских организациях государственного и частного сектора в 2015 г. Так, более 45 % организаций сообщили о том, что уровень оплаты труда сотрудников зависит напрямую от выполнения плана по количеству пациентов. В этих организациях введена прогрессивная шкала заработной платы в зависимости от суммы выручки организации. В то же время 55 % опрошенных заявили, что их цель – это эффективное лечение пациентов, и считают привязку размера зарплаты к прибыли организации пагубной. По мнению А.З. Столпнера, привязка заработной платы врача к выручке может повлиять на необоснованные с медицинской точки зрения назначения (лечебно-диагностические процедуры и т.д.). По его мнению, практика доплаты за дополнительные назначения врачу широко распространена в настоящее время в столичных медицинских организациях. Он настаивает на том, что упор на качество лечения заставляет пациента возвращаться именно в эту клинику и приводить туда своих родственников и знакомых, тем самым повышая уровень доверия к медицинской организации. Стоит заметить, что в данном подходе главная цель – это повышение уровня доверия к бренду (brand loyalty) [14].
По мнению James Alan Robinson, профессора University of Chicago, одного из ведущих специалистов в области политики и менеджмента в сфере здравоохранения, все три существующие модели оплаты труда в системе здравоохранения (оплата за отдельно взятые услуги, подушевое финансирование, фиксированные ставки оплаты труда) не являются совершенными. Он заявляет, что «оплата за услуги поощряет оказание нецелесообразных услуг, мошенническое накручивание посещений и процедур и бесконечное перенаправление пациентов от одного специалиста к другому», «подушевая оплата поощряет отказ в предоставлении нужных услуг, отказ от хронических больных и сужение объема работы при отбрасывании пациентов, требующих много времени», «окладная система подрывает продуктивность, поощряет отдых на рабочем месте и насаждает бюрократическую ментальность, в которой любая процедура – еще чья-то проблема» [18; 19].
Комплаентность и лояльность пациентов
Ключевой базовый принцип пациент-ориентированного подхода – это повышение комплаентности (patient compliance) и лояльности пациентов (patient loyalty). В данном аспекте стоит различать эти два понятия, хотя с лингвистической точки зрения они, безусловно, являются синонимичными. Разделение этих понятий при формировании пациент-ориентированного подхода необходимо ввиду различной функциональной значимости (нагрузки) этих определений. Приверженность к следованию назначенного лечения (adherence to therapy), а также выполнению требований врача по соблюдению лечебно-охранительного режима отражает личное отношение в системе «врач – пациент». Но этот фактор определяется уровнем доверия пациента к компетенции врача, его уровню профессиональной подготовки (квалификации). По мнению I.E. Leppik, категория «приверженности» включает в себя несколько компонентов: поведенческий компонент (пациента), его нацеленность на результат, а также степень возможности (условий) выполнения назначений. На практике уровень «приверженности» обычно измеряется правильностью или неправильностью выполнения медикаментозных назначений (следование назначенным дозам, соблюдение временного интервала и т.д.). Если пациент принимает лекарственное средство в дозе, составляющей 80–120 % от назначения, то уровень «приверженности» можно расценивать как высокий. Помимо прямых оценок «приверженности», существуют и косвенные (непрямые) методы определения уровня данного показателя. К ним можно отнести количество использованных/оставшихся таблеток, анкетирование, проверку записей (дневников) пациентов и т.д. [20].
Что касается «лояльности» пациента, то целесообразнее ее рассматривать в модели «медицинская организация – пациент». Данный показатель отражает как степень доверия пациента к конкретной медицинской организации (к юридическому лицу, к учреждению), так и к системе оказания медицинской помощи в целом. Например, доверие к частной или государственной системе здравоохранения или к системе «платной» или «бесплатной» медицины. Так, согласно данным агентства BusinesStat, в 2019 г. более 27,0 % жителей Москвы и Московской области обращались за услугами частных медицинских организаций. Высокий показатель ( %) обращаемости в коммерческие клиники на фоне развитой сети государственных учреждений здравоохранения говорит прежде всего о степени доверия респондентов. Ключевыми причинами явились в 35,2 % случаев – высокая профессиональная составляющая врачей, по мнению респондентов, в 34,5 % – высокая результативность назначенных схем и процедур. При этом 56,4 % опрошенных шли на прием к конкретному врачу (фактор приверженности модели «врач – пациент»). На фактор приверженности в модели «медицинская организация – пациент», по мнению 21,4 % респондентов, повлиял хороший уровень организации медицинской помощи (оперативность, полнота охвата и т.д.). Помимо медицинских организаций, в круг субъектов мотивационной модели «медицинская организация – пациент» может быть включена и страховая компания. Но этот аспект играет роль исключительно в частном секторе. Что касается государственного сектора здравоохранения, согласно опросу, доверие к врачу (42,4 %) значительно ниже, чем доверие к медицинской организации (76,9 %) в целом (или к системе государственного здравоохранения). Это обусловлено главным образом тем, что наряду с признанием низкой квалификации врачей в госсекторе, респондентами осознается «всеобщий» охват государственных гарантий в системе ОМС и возможность «получить» дорогостоящие методы лечения и обследования при наличии показаний. Омрачает эту картину, по мнению 79,9 % респондентов, высокий уровень «бюрократизации» государственной система оказания медицинской помощи. В то же время в частном секторе доверие к врачу значительно выше, чем к коммерческой организации в целом. Это обусловлено тем, что большинство опрошенных (65,5 %) считают, что руководство таких организаций ставит цель получения прибыли на порядок выше, чем оказание качественной медицинской помощи [16].
При формировании пациент-ориентированного управления в медицинской организации необходимо руководствоваться в принятии решений прежде всего интересами пациента (клиента). Главной целью является повышение уровня доверия пациента к врачу и к медицинской организации в целом. Взаимодействие в данной системе осуществляется на взаимовыгодных условиях и партнёрских отношениях, что должно отражаться на планировании и реализации медицинских услуг населению. Для оценки деятельности медицинской организации и системы здравоохранения в целом необходимо учитывать мнение граждан о системе контроля качества медицинских услуг и результативности/эффективности менеджмента [20; 21]. Учредитель медицинской организации должен регулярно инициировать проведение независимого опроса прикрепленных пациентов, что должно стать основой для планирования объема и вида медицинских услуг. Внедрение пациент-ориентированного подхода при надлежащей имплементации ведет, прежде всего, к повышению обращаемости населения, приверженности к лечению, что, в свою очередь, отразится на показателях выявляемости заболеваний, длительности ремиссий, снижения уровня заболеваемости, а также на более широком охвате населения профилактическими мероприятиями [22].
Нарушение ритма сердца и проводимости (аритмии сердца)
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
Практически у 80% пациентов с ишемической болезнью сердца регистрируются аритмии различного характера и до 65% из них угрожают жизни. НРС могут быть самостоятельными или являться осложнением заболеваний сердечно-сосудистой системы и других органов и систем
С учетом частоты сердечных сокращений их можно подразделить на две большие группы:
1. Брадиаритмии:
2. Тахиаритмии:
Важно отличать нарушения ритма сердца, вызванные органическим (необратимым) поражением миокарда, и функциональные нарушения. Как правило, функциональные нарушения встречаются при здоровом сердце и могут быть вызваны психогенными, рефлекторными и гуморальными расстройствами. Функциональные нарушения ритма сердца встречаются достаточно часто, важно выявить и исключить вызывающие их причины, что позволит избавить человека от аритмии.
Органические нарушения возникают при: коронарной ишемии, гемодинамических пороках сердца и крупных сосудов, сердечной недостаточности, гипертонии. Они могут появляться при токсическом воздействии (медикаментозных препаратов, алкоголя и др.) или инфекционно токсическом (ревматизм, вирусные инфекции, миокардиты различной этиологии и др.), гормональных сдвигах. Аритмии бывают врожденные (синдром WPW, врожденная АВ блокада и др.) и приобретенными, вызванные внешними воздействиями (миокардит,операции и травмы сердца и др.).
Основные симптомы (проявления аритмий)
Брадиаритмии:
Тахиаритмии:
Обычно диагностика аритмий осуществляется врачом поликлиники, кардиологом или врачом скорой помощи. Имеет значение сбор анамнеза, физикальное обследование, и различные инструментально-диагностические методы. Наиболее важным является регистрация НРС на ЭКГ (для предъявления аритмологу).
На сегодняшний день в специализированных или многопрофильных клиниках пациентов консультирует врач кардиохирург-аритмолог и определяет необходимость и возможность эндоваскулярного интервенционного (малотравматичного) лечения нарушения ритма сердца. В нашей Клинике есть все необходимые ресурсы для диагностики и лечения аритмий
К методам диагностики нарушения ритма сердца относят:
Тилт-тест – проба с пассивным ортостазом. Проводится на специальном поворотном столе. Позволят выявить или исключить связь между развитием обморочных состояний и нарушениями сердечного ритма.
Лечение аритмий: хирургическая коррекция нарушений ритма сердца
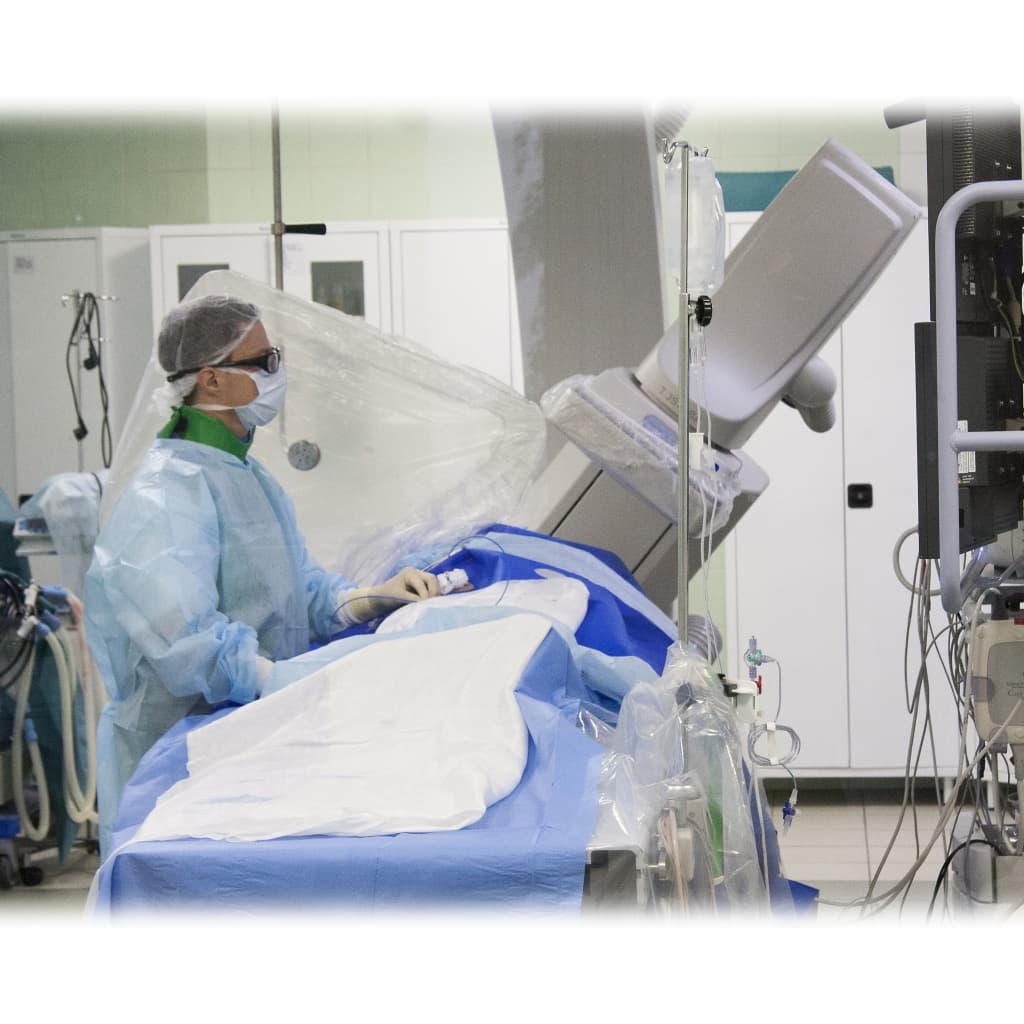
В нашей Клинике выбор способа лечения нарушения ритма сердца осуществляется специа-листом с учетом клинической картины заболевания, данных инструментально-диагностических исследований и рекомендаций Российского кардиологического обще-ства, Всероссийского научного общества аритмологов.
Самостоятельный прием препаратов, самолечение различными методами является крайне не желательным и не безопасным, если неизвестен и не учитывается характер, механизм и причина аритмии.
Существует несколько способов лечения нарушения ритма сердца:
Операция выполняется под местной анестезией в условиях рентгеноперационной длительностью до 40-55 минут.
Эффективным и радикальным методом лечения тахиаритмий является катетерная аблация (деструкция) очага аритмии. Операция, в среднем, длится не более 1 часа, и через сутки пациент может быть выписан из стационара.
О правилах регистрации программного обеспечения как медицинского изделия в России
Гусев Александр,
Директор по развитию бизнеса, к.т.н.
Обновление июнь 2021
Введение
Многие виды современного программного обеспечения, предназначенные для применения в медицине и здравоохранении, являются с нормативной точки зрения программными медицинскими изделиями (ПМИ) и подлежат, согласно закону, государственной регистрации..
Процесс регистрации программного обеспечения (ПО) как медицинского изделия является достаточно непростым. Он достаточно непросто и детально урегулирован законодательно. В последнее время Министерство здравоохранения совместно с Росздравнадзором плотно работают над точечным совершенствованием нормативно-правовых актов в области программных медицинских изделий, в особенности применяющими технологии искусственного интеллекта (ИИ).
Основными задачами регулирования этой сферы концепция называет: создание механизмов упрощенного внедрения продуктов с использованием технологий ИИ и РТ; установление юридической ответственности при применении систем ИИ и РТ, развитие страховых институтов; совершенствование режима оборота данных; создание национальной системы технического регулирования и оценки соответствия; разработка комплекса мер по стимулированию развития технологий.
Для того, чтобы помочь в упрощении прохождения процедур подготовки и регистрации программного обеспечения как медицинского изделия, специалистами компании «К-Скай» разработан данный обзорный документ.
Краткий обзор нормативно-правовых актов
По мнению многих участников рынка и разработчиков ПО, это определение является слишком широким, допускающем достаточно вольную трактовку как экспертами регулятора, так и правоохранительными органами, и судами. Тем не менее – далее все обсуждение и анализ мы будем проводить, понимая под специальным программным обеспечением (СПО) именно ПО, которое регулятор и надзорные органы могут воспринимать к медицинское изделие (МИ).
Согласно п.4 этой же 38-й статьи 323-ФЗ, «На территории Российской Федерации разрешается обращение медицинских изделий, зарегистрированных в порядке, установленном Правительством Российской Федерации, уполномоченным им федеральным органом исполнительной власти». П. 15 38-й статьи гласит «Запрещается производство: 1) медицинских изделий, не включенных в государственный реестр медицинских изделий и организаций (индивидуальных предпринимателей), осуществляющих производство и изготовление медицинских изделий, за исключением медицинских изделий, производимых для проведения испытаний и (или) исследований; 2) фальсифицированных медицинских изделий».
Таким образом, 323-й ФЗ запрещает производить МИ, если они не включены в государственный реестр медицинских изделий. Обращаем внимание на формулировку запрета – запрещается именно не реклама/продажа/применение – а непосредственно весь оборот, включая даже производство.
Есть одно исключение: постановлением Правительства РФ от 01.09.2020 N 1335 «О внесении изменения в пункт 2 Правил государственной регистрации медицинских изделий», от регистрации освобождены медицинские изделия, которые предназначены для использования на территории международного медицинского кластера (ММК) или на территориях инновационных научно-технологических центров.
Нарушение запрета на производство, а также применение незарегистрированных медизделий, карается административным и уголовным преследованием.
Статья 238.1 уголовного кодекса дает разъяснение – что же такое уголовно наказуемое деяние: «Производство, сбыт или ввоз на территорию Российской Федерации фальсифицированных лекарственных средств или медицинских изделий, либо сбыт или ввоз на территорию Российской Федерации недоброкачественных лекарственных средств или медицинских изделий, либо незаконные производство, сбыт или ввоз на территорию Российской Федерации в целях сбыта незарегистрированных лекарственных средств или медицинских изделий, либо производство, сбыт или ввоз на территорию Российской Федерации фальсифицированных биологически активных добавок, содержащих не заявленные при государственной регистрации фармацевтические субстанции, совершенные в крупном размере». Согласно п.2 этой статьи «Крупным размером в настоящей статье признается стоимость лекарственных средств, медицинских изделий или биологически активных добавок в сумме, превышающей сто тысяч рублей».
Иными словами – если разработчик МИ продал свое решение на сумму свыше 100 тыс. руб. – это уголовная ответственность. Если меньше – то административная. Уголовным кодексом предусмотрено следующее наказание:
Практика уголовного преследования за продажу незарегистрированного медицинского программного обеспечения, увы, уже есть в нашей стране, причем преследования уже после регистрации, за продажу незарегистрированного МИ ранее.
Государственный контроль за обращением медицинских изделий осуществляется Федеральной службой по надзору в сфере здравоохранения (Росздравнадзором), https://roszdravnadzor.ru/. Порядок такого контроля установлен Приказом Росздравнадзора от 09.12.2019 № 9260 «Об утверждении Административного регламента Федеральной службы по надзору в сфере здравоохранения по осуществлению государственного контроля за обращением медицинских изделий».
В данное время в нашей стране уже зарегистрировано несколько программных продуктов для здравоохранения, созданных на основе технологий ИИ:
Порядок прохождения регистрации
Процесс подготовки и регистрации программного обеспечения как медицинского изделия с т.з. разработчика (производителя) условно можно разделить на 3 основных этапа::
Этап №1. Подготовка
На первом подготовительном этапе разработчику ПО необходимо ответить на 2 основных вопроса:
Вопрос №1. Является ли ПО МИ или нет?
Критерии отнесения ПО к медицинскому изделию в настоящее время определены информационным письмом Росздравнадзора от 13.02.2020 № 02И-297/20. Согласно этому письму, ПО является МИ, если присутствуют 4 критерия:
1. ПО является программой для ЭВМ или ее модулем вне зависимости от аппаратной платформы, способов размещения ПО и предоставления к нему доступа
2. ПО не является составной частью другого МИ
3. ПО предназначено производителем для оказания медицинской помощи
4. Результат работы ПО заключается в интерпретации в автоматическом режиме, в том числе с использованием искусственного интеллекта и этот результат влияет на принятие клинических решений.
При применении этого письма и предусмотренных критериев самое важно – это понимание, что все 4 критерия должны быть справедливы для какого-то программного продукта – только в этом случае такой продукт – МИ. Если хоть один из критериев неактуален для какого-то программного решение – оно автоматически не может быть признано медицинским изделием и значит – освобождается от необходимости государственной регистрации до вывода его на рынок.
Разъяснения:
1. Первый пункт означает – что МИ может быть любое ПО и без разницы, на каком оборудовании оно работает и как доставляется до пользователя. Это, в свою очередь означает, что такие виды ПО, как облачные сервисы, микросервисы, встраиваемые компоненты (плагины и т.д.) могут быть МИ.
2. Второй – значит что ПО не разработано специально для какого-то аппаратного медицинского изделия и не является его составной частью. Оно должно быть универсальным и работать на любом оборудовании и без подключения каких-то определенных медицинских устройств. Если такое ПО предназначено для какого-то конкретного медицинского оборудования – то его не следует рассматривать как специальное ПО – оно проверяется и регистрируется вместе с аппаратным МИ.
3. Третье – означает что медицинским изделием является только то ПО, которое производитель осознано предназначил именно для применения при оказании медицинской помощи. Если производитель выпустил ПО для применения в медицинских организациях, но не в медицинских целях – это не МИ. Это, в свою очередь, означает – что все бухгалтерское ПО, решения в области медицинской статистики, администрирования МО и тд – не является МИ
4. Четвертый пункт самый важный. Его смысл в следующем: МИ не признается ПО, которое существенно не обрабатывает информацию, не изменяет ее и тем самым не создает дополнительный риск причинения здоровью пациента в случае применения такого ПО. Если ПО просто принимает, хранит и передает «как есть» медицинскую информацию – пусть даже и при оказании медицинской помощи, такое ПО не является МИ. Например – системы ведения электронных медицинских карт, системы обмена и хранения медицинских изображений и т.д. Если же ПО не просто принимает, но затем и изменяет (создает новую) медицинскую информацию – т.е. осуществляет ее машинную интерпретацию таким образом, что результаты этой интерпретации могут повлиять на клиническое решение (неважно – врача, медсестры и тд) – то это однозначно ПО. Сюда относятся все системы поддержки принятия врачебных решений, сложные лабораторные системы и тд.
Если разработчик так не считает или у него есть сомнения (что чаше всего и бывает), то в обоих случаях пока единственной более/менее надежной мерой является написание официального обращения в Росздравнадзор, в котором нужно указать, что именно за программное обеспечение вы разрабатываете, для чего оно предназначено и хотя бы в общих чертах представить его основные, наиболее важные функции. Данная норма предусмотрена п.6 решения Совета Евразийской экономической комиссии от 12.02.2016 N 46 «О Правилах регистрации и экспертизы безопасности, качества и эффективности медицинских изделий», согласно которой заявитель при необходимости «… получает предварительные консультации экспертной организации по вопросам регистрации и экспертизы медицинского изделия». В соответствии с п. 1 «Положения о Федеральной службе по надзору в сфере здравоохранения» Росздравнадзор, являясь федеральным органом исполнительной власти, осуществляющим функции по контролю и надзору в сфере, имеет право давать юридическим и физическим лицам разъяснения по вопросам, отнесенным к его компетенции.
Если есть опыт, то написание такого письма и его согласование с юристом можно сделать быстро – за 1 день и далее направить официально. Так как законодательно возможность обратиться в Росздравнадзор по электронным канала связи не предусмотрена, то поэтому письмо на бумажном носителе отправляем курьером или «Почтой России». Это – минимум 1 день, а то и 3-5 дней. И затем ждем – максимум 1 месяц.
Если вам ответили, что ваш продукт не МИ – для вас все закончилось, дальнейшие шаги можно не осуществлять. Если в ответе сказано, что ваше решение – МИ – тогда идем дальше.
Вопрос №2. Какому классу риска относится ПО?
После того как мы убедились, что наше ПО – медицинское изделие, нам надо понять, какой класс потенциального риска несет наше решение? Для этого необходимо воспользоваться приказом Минздрава №4н от 06.06.2012 г. с изменениями, внесенными приказом №686н от 07.07.2020. Согласно этому документу, для СПО предусмотрен отдельный III раздел документа, в котором определены 4 класса потенциального риска применения: 1, 2а, 2б и 3. Если ПО использует в своей работе технологии искусственного интеллекта, то такое ПО однозначно будет иметь 3й (максимальный) класс риска.
Этап №2. Испытания
Обратим внимание, что согласно п.25 раздела III Приказа Минздрава №2 от 09.01.2014, токсикологические испытания проводятся только в отношении изделий, которые согласно документации производителя контактируют с организмом человека при использовании МИ. Сейчас практически все ПО можно поставить по электронным канал связи, включая скачивание с сайтов – что позволяет избежать физического контакта человека с разными дисками, коробками, флешками и другими носителями. Поэтому для программного обеспечения подавать документы, подтверждающие результаты токсикологических исследований, не нужно.
Также не требуется подавать документы, подтверждающие результаты испытаний медицинского изделия в целях утверждения типа средств измерений – т.к. вероятнее всего ПМИ таковым не является.
Затем, на основании ТУ, необходимо разработать блок документации на программный продукт, причем она должна соответствовать большому списку ГОСТов, основная часть из которых была создана еще в прошлом веке (см. таблицу ниже). Разработчик на свой страх и риск решает – разрабатывать ли этот пакет документов самому или лучше привлечь специальную организацию для этого, чтобы сократить потери времени на исправление ошибок и сразу сделать все грамотно.
| Обозначение документа | Название документа |
| ГОСТ 21552-84 | Средства вычислительной техники. Общие технические требования, приемка, методы испытаний, маркировка, упаковка, транспортирование и хранение |
| ГОСТ Р МЭК 62304-2013 | Изделия медицинские. Программное обеспечение. Процессы жизненного цикла |
| ГОСТ Р ИСО 15223-1-2014 | Изделия медицинские. Символы, применяемые при маркировании на медицинских изделиях, этикетках и в сопроводительной документации. Часть 1. Основные требования |
| ГОСТ Р 50444-92 | Приборы, аппараты и оборудование медицинские. Общие технические условия |
| ГОСТ Р ИСО/МЭК 12119-2000 | Информационная технология. Пакеты программ. Требования к качеству и тестирование |
| ГОСТ Р ИСО/МЭК 9126-93 | Информационная технология. Оценка программной продукции. Характеристики качества и руководства по их применению |
| ГОСТ Р ИСО 9127-94 | Системы обработки информации. Документация пользователя и информация на упаковке для потребительских программных пакетов |
| ГОСТ 28195-89 | Оценка качества программных средств. Общие положения |
| ГОСТ Р 51188-98 | Защита информации. Испытания программных средств на наличие компьютерных вирусов. Типовое руководство |
| СанПиН 2.1.7.2790-10 | Санитарно-эпидемиологические требования к обращению с медицинскими отходами |
По нашему опыту и мнению коллег-разработчиков, создание пакета документов может занять от 1 до 2 месяцев.
Далее необходимо пройти технические, а затем – клинические испытания.
Согласно п.4 Правил регистрации, утвержденных постановлением №1416, технические испытания проводятся с целью определения соответствия характеристик медицинского изделия требованиям нормативной документации, технической и эксплуатационной документации производителя и принятия последующего решения о возможности проведения клинических испытаний. Производитель сам определяет, каким нормативным документам соответствует его изделие.
Клинические испытания представляют из себя разработанное и запланированное систематическое исследование, предпринятое для оценки безопасности и эффективности медицинского изделия. Провести клинические испытания можно только при условии успешного проведения технических испытаний.
Клинические испытания программных медицинских изделий допускается провести в форме анализа и оценки клинических данных. Для этого оформляется отчет, в котором должны содержаться клинические доказательства эффективности и безопасности медицинского изделия. Он должен соответствовать принятым правилам проведения клинических испытаний медицинских изделий, доказывать полноту проведенных исследований, достоверность результатов и сравнение клинических данных с имеющимися аналогами. Именно на основе такого отчета экспертное учреждение Росздравнадзора должно потом будет признать результаты исследований удовлетворительными.
Продолжительность клинических испытаний зависит от назначения и сложности медицинского изделия. Программа клинических испытаний составляется заявителем совместно с медицинской организацией, осуществляющей их проведение, в соответствии с требованиями, указанными в технической и эксплуатационной документации производителя, а также требованиями нормативной документации.
Если в ходе клинических испытаний выявляются несоответствия МПО назначению и показаниям к применению, установленным производителем в эксплуатационной документации или если установлены факты и обстоятельства, создающие по мнению эксперта угрозу жизни и здоровью граждан и медицинских работников при применении и эксплуатации программного продукта – то по такому ПО выносится решение об отрицательном результате испытаний. В остальных случаях должно быть принято положительное решение.
Результатом проведения испытаний являются акты, разработанные по образцам, утвержденным приказом Минздрава №2.
Таким образом, для проведения испытаний разработчику необходимо выбрать одну из уполномоченных организаций, заключить с ней соответствующий договор на оказание услуг, оплатить их и дождаться выполнения. Методика определения размера платы за экспертизу и испытания медицинских изделий регулируется приказом Минздрава №1386н.
Перечень подготовительных мероприятий и оценки длительности каждого из них приведены в таблице ниже.
| № | Событие | Длительность |
| 1 | Разработка комплекта технической и эксплуатационной документации | Не регламентирован, зависит полностью от разработчика. Чем менее зрелый продукт/ИТ компания будут заявляться на регистрацию – тем длительнее и сложнее этот этап. |
| 2 | Заключение соглашения между разработчиком ПМИ и организацией, осуществляющей проведение испытаний и доработку документов | Не регламентирована. По опыту – от нескольких дней до 2-3 недель. |
| 3 | Проведение технических испытаний | Не более 30 рабочих дней со дня предоставления в испытательную организацию образца МИ и документации. По согласованию с заявителем может быть продлен, но не более чем на 12 рабочих дней. П.10 раздела II приказа Минздрава №2н |
| 4 | Проведение клинических испытаний | Согласно п. 39 раздела IV приказа Минздрава №2 длительность не ограничена. По опыту – несколько месяцев. |
| 5 | Оформление заявления на государственную регистрацию и пакета сопроводительных документов | Если очень быстро – 1 день |
| 6 | Оплата государственной пошлины за регистрацию | Можно сделать параллельно с предыдущим этапом |
Таким образом, этап разработки документов и проведение испытаний может занять от 3 до 6 месяцев или даже больше. Самое сложное на данном этапе:
Этап №3. Регистрация
Процесс регистрации включает прием и проверку документов на полноту и достоверность указанных заявителем сведения, а затем – проведение экспертизы качества, эффективности и безопасности.
Для программных медицинских изделий, в т.ч. созданных с применением технологий ИИ, постановлением Правительства РФ от 31 мая 2018 года №633 «Об изменениях в порядке государственной регистрации медицинских изделий» предусмотрена упрощенная процедура регистрации, срок которой сокращён на 20 рабочих дней за счёт проведения экспертизы качества, эффективности и безопасности в один этап без необходимости предварительного получения разрешения на проведение клинических испытаний.
Порядок организации и проведения экспертизы качества, эффективности и безопасности медицинских изделий утвержден приказом Минздрава от 20.03.2020 №206н. В нем приказом Минздрава от 22.04.2021 №386н внесены дополнения, касающиеся экспертизы программных медицинских изделий. Кроме этого, действует решение Совета Евразийской экономической комиссии от 12.02.2016 №46 «О Правилах регистрации и экспертизы безопасности, качества и эффективности медицинских изделий».
Дополнительно к этим нормативным документам существуют общие методические рекомендации по проведению экспертизы качества, эффективности и безопасности, разработанные соответствующими учреждениями и утвержденные в 2016 г.
Экспертиза качества, эффективности и безопасности медицинского изделия проводится подведомственным Росздравнадзору экспертным учреждением: ФГБУ «ВНИИИМТ» или ФГБУ «ЦМИКЭЭ».
После успешного прохождения регистрации сведения о разработчике и медицинском изделии размещаются в «государственном реестре медицинских изделий и организаций (индивидуальных предпринимателей), осуществляющих производство и изготовление медицинских изделий» (далее – Государственный реестр). Правила его ведения утверждены постановлением Правительства РФ от 19.06.2012 г. N 615 «Об утверждении Правил ведения государственного реестра медицинских изделий и организаций, осуществляющих производство и изготовление медицинских изделий». Сам реестр доступен на сайте Росздравнадзора по адресу http://www.roszdravnadzor.ru/services/misearch
Перечень мероприятий по государственной регистрации и оценки длительности каждого из них приведен в таблице ниже.
Таким образом, если мы примем, что заявитель с первой попытки оформил все документы правильно, у Росздравнадзора и экспертного учреждения не было замечаний и запросов дополнительной информации, то производителю потребуется минимум 40 дней на получение регистрационного удостоверения.
Обратим особое внимание – что длительность этого этапа напрямую зависит от качества и полноты оформленных документов и проведения испытаний. Т.к. очень сложно предсказать, что должно быть написано в том или ином документе и как именно его оценивают соответствующие эксперты, невозможно гарантировать, что указанные выше сроки будут повсеместно соблюдаться. По той практике, которую накопили на данное время разработчики медицинского программного обеспечения, во время регистрации порой документы возвращаются заявителю на доработку и уточнение. Именно поэтому процесс регистрации может быть длительным. Чтобы этого избежать – необходимо очень качественно прорабатывать документы, при возможности – консультируясь у соответствующих экспертов и компаний, имеющих опыт такой регистрации.
Показанные выше сроки – это именно сроки регистрации. Не забудем про подготовительный этап проведения технических испытаний и разработки документации, который был описан нами выше.
Пострегистрационный мониторинг ПМИ
В соответствии с решением коллегии Евразийской экономической комиссии от 22.12.2015 №174, после регистрации и вывода медицинского изделия на рынок должен осуществляться мониторинг его безопасности. Порядок его проведения на территории РФ утвержден приказом Минздрава от 15.09.2020 г. №980н.
Целью мониторинга является выявление и предотвращение побочных действий и неблагоприятных событий, связанных с применением МИ и создающих угрозу жизни и здоровью граждан и медицинских работников.
Мониторинг представляет собой сбор сведений о таких событиях и их централизованную регистрацию в информационной системе «Неблагоприятные события медицинских изделий» для последующего анализа, проведения экспертизы и при необходимости контрольных мероприятий, направленные на предотвращение таких ситуаций в будущем.
Классификация неблагоприятных событий, связанных с обращением МИ, утверждена приказом Росздравнадзора №4513 от 20.05.2021.
Источником информации могут быть различные каналы, включая получение сведений из государственных информационных систем в сфере здравоохранения, информации от пользователей, данных, предоставленных самим заявителем и т.д. В соответствии с приказом №1113н от 19.10.2020 субъекты обращения медицинских изделий обязаны сообщать в Росздравнадзор о фактах и обстоятельствах, создающих угрозу жизни и здоровью граждан и медицинских работников при применении и эксплуатации медицинских изделий, в течение 20 рабочих дней.
Производитель МИ обязан предоставить отчет о неблагоприятном событии и корректирующих действиях. В случае выявления и подтверждения неблагоприятных событий или причинения вреда жизни и здоровью производитель ПМИ обязан выполнить ряд превентивных мероприятий, предусмотренных приказом Минздрава №980н, включая информирование потребителей. Если производитель не будет принимать необходимых мер по предотвращению угрозы здоровью, Росздравнадзор имеет право изъять данное ПМИ из обращения.
Выводы
Подготовка документов, испытания и регистрация – процесс сложный и длительный. Несмотря на наличие некоторых рамок сроков проведения отдельных процедур, длительность всего процесса в первую очередь зависит от самого разработчика.
Если все делать строго по «букве закона» и с первой попытки оформить все необходимые документы на высоком уровне, то в среднем на подготовку, испытания и регистрацию ПО как МИ разработчику может потребоваться от 3 до 9 месяцев.
Причина длительности и сложности государственной регистрации медицинских изделий состоит в том, что кроме работы самого Росздравнадзора, которая действительно является вполне оперативной и прозрачной с точки зрения нормативного регулирования, подготовительные и промежуточные этапы, особенно проведение клинических испытаний, выполняются специальными организациями, являются сложными и длительными. Именно они вносят основной вклад в затягивание процесса подготовки к регистрации.



