Что такое цитокины какова их роль в иммунной системе
Иммунная система Часть 5 Цитокины
Иммунная система Часть 5 Цитокины
Цитокины
Очень значительная группа крупных молекул, секретируемых клетками после их взаимодействия с антигенами и другими цитокинами. Они служат связующим звеном между врожденным и приобретенным иммунитетом, влияют на выраженность воспалительного и иммунного ответа, передают сигналы клеткам через рецепторы на их поверхности. Цитокины и их антагонисты используются в лечении онкологических, воспалительных, инфекционных, аутоиммунных заболеваний и при трансплантации органов и тканей.
Провоспалительные цитокины (ИЛ-1, ИЛ-6, ИЛ-12, ФНО-альфа, интерфероны, хемокины, ИЛ-8, и др.) стимулируют воспалительный ответ, разрушают пораженные клетки и вирусы. Высокий уровень этих цитокинов в крови отражает активность и тяжесть воспалительного процесса.
Противовоспалительные цитокины (ИЛ-4, ИЛ-10, ТФР-бета и др.) ограничивают развитие воспаления и завершают иммунный ответ.
Часть цитокинов несут дополнительные функции в активации клеточного или гуморального направления иммунного ответа.
Основные группы цитокинов:
Хемокины
Хемокины стимулируют хемотаксис – направленное движение и перемещение лейкоцитов. Производят хемокины лейкоциты, тромбоциты, эпителиальные и эндотелиальные клетки. Эти клетки расположены в местах наиболее частого проникновения возбудителей (кожа, слизистые оболочки, сосуды) и через хемокины зовут лейкоциты на помощь для быстрого обезвреживания чужеродных антигенов. Из минусов – к хемокиновым рецепторам на поверхности Т-лимфоцитов приспособился вирус иммунодефицита человека, используя их для проникновения в клетку.
Колониестимулирующие факторы
Вырабатываются эндотелиальными клетками, фибробластами, макрофагами, тучными клетками и T-хелперами. Предназначены для стимуляции гемопоэза – роста клеток крови. Выделяют:
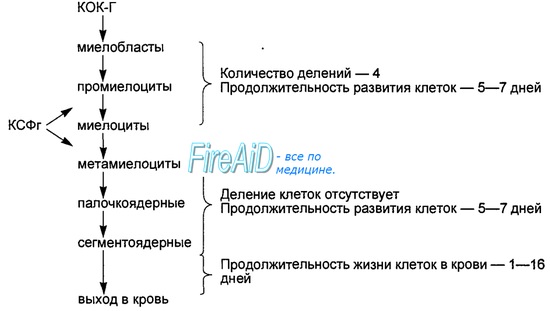
Гранулоцитарный колониестимулирующий фактор (Г-КСФ) стимулирует рост предшественников нейтрофилов.
Гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ) стимулирует рост моноцитов, нейтрофилов, эозинофилов и базофилов, активирует макрофаги.
Макрофагальный колониестимулирующий фактор (М-КСФ) стимулирует рост предшественников моноцитов.
Трансформирующие факторы роста
Трансформирующий фактор роста альфа
Макрофаги, моноциты, эпителиальные клетки, клетки костного мозга
Стимулирует рост и развитие иммунных клеток. Стимулирует выработку слизи.
Трансформирующий фактор роста бета
В-лимфоциты, макрофаги, тучные клетки
Подавляет рост лимфоцитов, отменяет эффекты многих цитокинов, переключает на синтез IgA. Способствует заживлению тканей и росту соединительной ткани в месте воспаления.
Факторы некроза опухоли
Фактор некроза опухоли – альфа
Макрофаги, лимфоциты, нейтрофилы, дендритные клетки, тучные клетки
Вызывает апоптоз, активирует макрофаги, синтез ИЛ-1, ИФН-гамма, ГМ-КСФ. Стимулирует воспаление, повреждает опухолевые клетки, повышает температуру тела.
Фактор некроза опухоли-бета
Лимфоциты, преимущественно Т-клетки
Усиливает фагоцитоз, развитие лимфоидных органов. Повреждает опухолевые клетки.
Выберите город
Годовой абонемент
Годовой абонемент входит в состав первого заказа и дает возможность год Вам и членам Вашей семьи сдавать анализы в два раза дешевле. Результаты всех анализов бессрочно будут храниться в личном кабинете. Подробнее
Что такое цитокины какова их роль в иммунной системе
Цитокинами называют белковые и полипептидные молекулы, которые продуцируются клетками иммунной системы (лимфоцитами, мононукле-арными фагоцитами, дендритными клетками), а также стромальными клетками. Цитокины действуют на клетки, соединяясь со своими поверхностными рецепторами. Связывание цитокина с рецептором служит источником сигнала активации генов, который передается в ядро клетки. Чувствительность клеток-мишеней к действию цитокинов изменяется в зависимости от количества цитокиновых рецепторов на их поверхности. Время синтеза цитокина, как правило, краткосрочно: лимитирующим фактором служит нестабильность молекул мРНК. Отдельные цитокины (например, ростовые факторы) продуцируются спонтанно.
Большинство цитокинов оказывают наиболее выраженное влияние в ближайшем микроокружении клеток-продуцентов. Местное действие цитокинов может быть как аутокринное, так и паракринное, в зависимости от того, связывается ли цитокин с рецептором на самой клетке-продуценте, или — на соседней клетке. Системное (эндокринное) влияние цитокинов возможно только в случае интенсивного накопления их в циркулирующей крови (например, при эндотоксическом шоке). Обычно в крови присутствуют следовые количества цитокинов, недостаточные для проявления системных эффектов.
В костном мозге, в тимусе и лимфоидных органах постоянно происходит спонтанный синтез цитокинов, выполняющих функции ростовых факторов, которые связываются с рецепторами на клетках-предшественницах, стимулируя процессы их пролиферации и дифференцировки.
— Вернуться в оглавление раздела «Физиология человека.»
Как работает иммунитет. Основные понятия
Механизм иммунного ответа и иммунные клетки. Основные понятия.

(краткий обзорный материал)
СОДЕРЖАНИЕ:
Цитокины
«Азбука Морзе» организма
Подробнее о цитокинах см. по кнопке-ссылке:
Упомянутая выше условность классификации означает, что цитокин, входящий в одну из перечисленных групп, при определенных условиях в организме может сыграть диаметрально противоположную роль — например, из провоспалительного превратиться в противовоспалительный.
Без налаженной связи между видами войск любая хитроумная военная операция обречена на провал, поэтому клеткам иммунной системы очень важно, принимая и отдавая приказы в виде цитокинов, правильно их интерпретировать и слаженно действовать. Если цитокиновые сигналы начинают вырабатываться в очень большом количестве, то в клеточных рядах наступает паника, что может привести к повреждению собственного организма. Это называется цитокиновым штормом: в ответ на поступающие цитокиновые сигналы клетки иммунной системы начинают продуцировать всё больше и больше собственных цитокинов, которые, в свою очередь, действуют на клетки и усиливают секрецию самих себя. Формируется замкнутый круг, который приводит к разрушению окружающих клеток, а позже и соседних тканей.
Иммунные клетки
По порядку расчитайсь!
Все клетки, относящиеся к иммунной системе и привлекаемые ею для обеспечения эффекторных реакций, в функциональном отношении условно разделяют на четыре группы.
Врожденный иммунитет
Клетки врожденного иммунитета распознают патоген по специфичным для него молекулярным маркерам — так называемым образам патогенности [4]. Эти маркеры не позволяют точно определить принадлежность патогена к тому или иному виду, а лишь сигнализируют о том, что иммунитет столкнулся с чужаками. Для нашего организма подобными маркерами могут служить фрагменты клеточной стенки и жгутиков бактерий, двухцепочечная РНК и одноцепочечная ДНК вирусов, и т.д. При помощи специальных рецепторов врожденного иммунитета, таких как TLR (Toll-like receptors, Толл-подобные рецепторы) и NLR (Nod-like receptors, Nod-подобные рецепторы), клетки взаимодействуют с образами патогенности и приступают к реализации своей защитной стратегии.
Теперь подробнее рассмотрим некоторые клетки врожденного иммунитета.
Адаптивный иммунитет
«спецподразделения вооруженных сил организма»
Видео 2. Кратковременные взаимодействия Т-клеток с дендритной клеткой ( ДК ) (обозначена зеленым ). Видео снято при помощи прижизненной двухфотонной микроскопии. →
T-лимфоциты
Видео 3. Движение Т-хелперов ( красные ) и Т-киллеров ( зеленые ) в лимфоузле. Видео снято при помощи прижизненной двухфотонной микроскопии. →
Всё вышесказанное относится к αβ-Т-лимфоцитам, однако существует еще один тип Т-клеток — γδ-T-лимфоциты (название определяет состав белковых молекул, образующих TCR) [7]. Они относительно малочисленны и в основном заселяют слизистую оболочку кишечника и другие барьерные ткани, играя важнейшую роль в регуляции состава обитающих там микробов. У γδ-T-клеток механизм распознавания антигенов отличается от αβ-Т-лимфоцитарного и не зависит от TCR [8].
B-лимфоциты
Схема иммунного ответа
Когда организм атакуют патогены, в бой в первую очередь вступают клетки врожденного иммунитета — нейтрофилы, базофилы и эозинофилы. Они выделяют вовне содержимое своих гранул, способное повредить клеточную стенку бактерий, а также, например, усилить кровоток, чтобы как можно больше клеток поспешило в очаг инфекции.
Одновременно с этим дендритная клетка, поглотившая патоген, спешит в ближайший лимфоузел, где передает информацию о нём находящимся там Т- и В-лимфоцитам. Те активируются и путешествуют до местонахождения патогена (рис. 2). Битва разгорается: Т-киллеры при контакте с зараженной клеткой убивают ее, Т-хелперы помогают макрофагам и В-лимфоцитам осуществлять их механизмы защиты. В итоге патоген гибнет, а победившие клетки отправляются на покой. Бόльшая их часть погибает, но некоторые становятся клетками памяти, которые поселяются в костном мозге и ждут, когда их помощь снова понадобится организму.
Так выглядит схема любого иммунного ответа, однако она может заметно видоизменяться в зависимости от того, какой именно патоген проник в организм. Если мы имеем дело с внеклеточными бактериями, грибами или, скажем, глистами, то основными вооруженными силами в этом случае будут эозинофилы, В-клетки, продуцирующие антитела, и Th2-лимфоциты, помогающие им в этом. Если же в организме поселились внутриклеточные бактерии, то на помощь в первую очередь спешат макрофаги, которые могут поглотить инфицированную клетку, и Th1-лимфоциты, помогающие им в этом. Ну а в случае вирусной инфекции в бой вступают NK-клетки и Т-киллеры, которые уничтожают зараженные клетки методом контактного киллинга.
Как мы видим, многообразие типов иммунный клеток и механизмов их действия неслучайно: на каждую разновидность патогена у организма припасен свой эффективный способ борьбы (рис. 3).
Рисунок 3. Основные типы патогенов и клетки, принимающие участие в их уничтожении.
А теперь все вышеописанные иммунные перипетии — в коротком видео.
Видео 5. Механизм иммунного ответа. →
Аутоиммунитет
громыхает «гражданская война».
К сожалению, ни одна война не обходится без потерь среди гражданского населения. Долгая и интенсивная защита может дорого стоить организму, если агрессивные высокоспециализированные войска выйдут из-под контроля. Повреждение собственных органов и тканей организма иммунной системой называется аутоиммунным процессом [2]. Заболеваниями этого типа страдает около 5% человечества.
Селекция Т-лимфоцитов в тимусе, а также удаление аутореактивных клеток на периферии (центральная и периферическая иммунологическая толерантность), о которых мы говорили ранее, не могут полностью избавить организм от аутореактивных Т-лимфоцитов. Что же касается В-лимфоцитов, вопрос о том, насколько строго осуществляется их селекция, до сих пор остается открытым. Поэтому в организме каждого человека обязательно присутствует множество аутореактивных лимфоцитов, которые в случае развития аутоиммунной реакции могут повреждать собственные органы и ткани в соответствии со своей специфичностью.
За аутоиммунные поражения организма могут быть ответственны как Т-, так и В-клетки. Первые осуществляют непосредственное убийство безвинных клеток, несущих на себе соответствующий антиген, а также помогают аутореактивным В-клеткам в продукции антител. Т-клеточный аутоиммунитет хорошо изучен при ревматоидном артрите, сахарном диабете первого типа, рассеянном склерозе и многих других болезнях.
В-лимфоциты действуют куда более изощренно. Во-первых, аутоантитела могут вызывать гибель клеток, активируя на их поверхности систему комплемента или же привлекая макрофаги. Во-вторых, мишенями для антител могут стать рецепторы на поверхности клетки. При связывании такого антитела с рецептором тот может или блокироваться, или же активироваться без реального гормонального сигнала. Так происходит при болезни Грейвса : В-лимфоциты производят антитела против рецептора к ТТГ (тиреотропному гормону), мимикрируя действие гормона и, соответственно, усиливая продукцию тиреоидных гормонов. При миастении гравис антитела против рецептора к ацетилхолину блокируют его действие, что приводит к нарушению нейромышечной проводимости. В-третьих, аутоантитела вместе с растворимыми антигенами могут образовывать иммунные комплексы, которые оседают в различных органах и тканях (например, в почечных клубочках, суставах, на эндотелии сосудов), нарушая их работу и вызывая воспалительные процессы.
Как правило, аутоиммунное заболевание возникает внезапно, и невозможно точно определить, что стало его причиной. Считается, что триггером для запуска может послужить практически любая стрессовая ситуация, будь то перенесенная инфекция, травма или переохлаждение. Значительный вклад в вероятность возникновения аутоиммунного заболевания вносит как образ жизни человека, так и генетическая предрасположенность — наличие определенного варианта какого-либо гена.
Кроме того, на развитие болезни может влиять уровень экспрессии аутоантигена в тимусе. Например, продукция инсулина и, соответственно, частота презентации его антигенов Т-клеткам различается от человека к человеку. Чем она выше, тем ниже риск развития сахарного диабета первого типа, так как это позволяет удалить специфичные к инсулину Т-лимфоциты.
Заключение
Как мы уже убедились, иммунитет — это сложнейшая сеть взаимодействий как на клеточном, так и на молекулярном уровнях. Создать идеальную систему, надежно защищающую организм от атак патогенов и одновременно ни при каких условиях не повреждающую собственные органы, не смогла даже природа. Аутоиммунные заболевания — побочный эффект высокой специфичности работы системы адаптивного иммунитета, те издержки, которыми нам приходится платить за возможность успешно существовать в мире, кишащем бактериями, вирусами и другими патогенами.
Гемопоэтическая стволовая клетка
Кем быть? Как гемопоэтическая стволовая клетка «выбирает профессию «
Часть ГСК находится в состоянии покоя: такие клетки неактивны и не участвуют в клеточном цикле. Но проснувшись, гемопоэтическая стволовая клетка делает очень важный выбор. Уникальным свойством всех стволовых клеток является способность к самообновлению — так называют симметричное деление с образованием идентичных копий материнской клетки. Так гемопоэтическая стволовая клетка может практически бесконечно продлять свое детство.
* — По современным данным, гемопоэтическая стволовая клетка «взрослеет», постепенно теряя способность к самообновлению и приобретая способность к дифференцировке. А решение выбрать «рабочую специальность», то есть мегакариоцитарное и эритроцитарное направление дифференцировки, клетка принимает еще до того, как рассмотрит варианты с «учебой» и «армией» (миелоидным или лимфоидным ростками) [11].
Общие лимфоидные предшественники дают начало клеткам иммунной системы — NK-клеткам, T- и B-лимфоцитам, — которые защищают организм от вторжения. NK-клетки (большие гранулярные лимфоциты) убивают чужаков, T-лимфоциты могут распознавать эпитоп (участок антигена ) врага и организовывать наступление (T-хелперы) или атаковать самостоятельно (цитотоксические лимфоциты), а B-лимфоциты, тоже после знакомства с антигеном, могут превращаться в плазматические клетки, вырабатывать специфические антитела и поражать ими врага на расстоянии.
Каким же образом гемопоэтическая стволовая клетка решает, оставаться ей вечно юной или встать на путь дифференцировки и превратиться в зрелую клетку крови? И как она выбирает свою будущую профессию? Результаты большого количества исследований доказывают, что важную роль играет окружение гемопоэтической стволовой клетки*. В первую очередь, это различные виды клеток, формирующие гемопоэтическую нишу костного мозга.
Однако выбор профессии — непростой процесс. И огромную роль в нём, помимо внешнего воздействия, играют личные предпочтения и склонности. Как и у человека, у гемопоэтической стволовой клетки богатый и сложный внутренний мир, который представлен транскрипционными факторами. Именно их взаимодействия приводят в конечном итоге к принятию решения, кем же ей быть [17, 18].
Конечно, представление работы транскрипционных факторов в виде механических блоков — чрезвычайное упрощение. Кроме того, описанные взаимодействия — лишь малая часть огромной сети транскрипционных факторов. В настоящее время ведутся масштабные исследования, чтобы составить представление о внутренних факторах, участвующих в регуляции дифференцировки гемопоэтической стволовой клетки, и об их взаимосвязи с внешними факторами, такими как влияние других клеток и растворимых факторов. Все эти знания помогут лучше понять процессы, лежащие в основе кроветворения в норме и при различных заболеваниях, разработать подходы к лечению этих заболеваний, а также научиться управлять судьбой гемопоэтических стволовых клеток in vitro и in vivo.
Дополнительная информация:
К разделу:
Дополнительно см.:
Источник (по материалам): А. Боголюбова. Иммунитет: борьба с чужими и… своими. / Спецпроект: аутоиммунные заболевания / biomolecula 26.01.2017
Литература:
Будьте здоровы!
ССЫЛКИ К РАЗДЕЛУ О ПРЕПАРАТАХ ПРОБИОТИКАХ
Роль цитокинов в процессах адаптивной интеграции иммунных и нейроэндокринных реакций организма
Полный текст:
Аннотация
Иммунная, эндокринная и нервная системы интегрированы благодаря существованию взаимных путей передачи информации об изменениях их фактического функционального состояния. Главными задачами мозга являются прием, интеграция и хранение информации, и есть убедительные доказательства, что это относится и к информации, полученной с помощью иммунных реакций организма. Доказано, что выработка цитокинов в головном мозге может быть вызвана не только периферической иммунной стимуляцией, но и собственно нервными клетками, стимулированными определенными нейросенсорными сигналами. Эволюционно сохраненные антигомеостатические механизмы, характерные для конкретных заболеваний, — предмет дальнейших исследований, результаты которых могут быть очень важны для разработки терапевтических стратегий, которые препятствовали бы нежелательным комбинированным эффектам иммунных и нейроэндокринных медиаторов.
Ключевые слова
Для цитирования:
Трошина Е.А. Роль цитокинов в процессах адаптивной интеграции иммунных и нейроэндокринных реакций организма. Проблемы Эндокринологии. 2021;67(2):4-9. https://doi.org/10.14341/probl12744
For citation:
Troshina E.A. The role of cytokines in the processes of adaptive integration of immune and neuroendocrine reactions of the human body. Problems of Endocrinology. 2021;67(2):4-9. (In Russ.) https://doi.org/10.14341/probl12744
Иммунная, эндокринная и нервная системы интегрированы благодаря существованию взаимных путей передачи информации об изменениях их фактического функционального состояния. Главными задачами мозга являются прием, интеграция и хранение информации, и есть убедительные доказательства, что это относится и к информации, полученной с помощью иммунных реакций организма.
Известно, что мозг объединяет все виды сенсорной информации, множество данных подтверждает наличие двунаправленной связи между нейроэндокринной и иммунной системами на протяжении всех этапов жизни человека. Возможность обработки и интеграции с прочими сигналами информации, сопряженной с функционированием системы иммунитета, представляет собой феномен биологической целесообразности на уровне центральной нервной системы человека. Не исключено, что он отчасти может быть сопряжен с системой цитокинового участия в формировании так называемой синаптической пластичности.
Доказано, что выработка цитокинов в головном мозге может быть вызвана не только периферической иммунной стимуляцией, но и собственно нервными клетками, стимулированными определенными нейросенсорными сигналами. Например, психосенсорный стресс индуцирует прямую церебральную продукцию цитокинов [1].
В принципе, выработка иммунорегуляторных цитокинов в головном мозге — это физиологический процесс, который имеет важнейшее значение для реализации основных функций мозга, например, памяти, обучения, адаптации. Этот процесс объясняется биологическими свойствами цитокинов, которые представляют собой молекулы, обеспечивающие взаимодействие клеток посредством множества различных механизмов, а именно:
паракринное (воздействие через растворимые медиаторы на соседние клетки); матрикринное (цитокины в неактивной форме связываются с протеогликанами межклеточного матрикса и высвобождаются под действием металлопротеиназ); юкстакринное (сигнал передается через плазматическую мембрану соседней клетки), эндокринное (системное действие цитокинов, поступающих в кровоток).
Источниками продукции цитокинов являются активированные Т- и В-лимфоциты, макрофаги, а также ( в ряде случаев) клетки, которые не имеют отношения к иммунной системе (например, интерлейкин (ИЛ)-6 вырабатывают фолликулярно-звездчатые клетки гипофиза, эндотелиальные и синовиальные клетки, хондроциты и др.)
Различают провоспалительные и противовоспалительные цитокины (ИЛ-2, ИЛ-10, ИЛ-27, ИЛ-35 и ИЛ-37), а также обладающие двоякими свойствами (например, ИЛ-6). Кроме того, выделяют регуляторные цитокины, которые обеспечивают толерантность к собственным тканям, минимизацию тканевого повреждения. Координированная выработка элементами иммунной системы различных цитокинов происходит в непосредственной близости к клеткам-мишеням.
Источники продукции и функции некоторых цитокинов представлены в таблице.
Таблица. Цитокины, источники их продукции и функции [2]
Цитокин
Источники продукции
Функции
Стимулирует ответ Th1 и Th2, ингибирует ответ Th17 и дифференцировку Tfh.
Стимулирует развитие Treg, B-клеток, моноцитов, NKT
Стимулирует развитие Th17, B-клеток
Моноциты, макрофаги, ДК
Стимулирует пролиферацию T-клеток и ЕК.
Защищает нейтрофилы от апоптоза, модулирует фагоцитоз и стимулирует секрецию ИЛ-8.
Индуцирует пролиферацию и дифференцировку В-клеток, усиливает синтез Ig плазмоцитами
Стимулирует дифференцировку B-лимфоцитов в клетки памяти, усиливает синтез Ig плазмоцитами.
Увеличивает активность макрофагов и ЕК
T-клетки, ТК, базофилы, эозинофилы
Усиливает ответ Th2, ингибирует дифференцировку Th1 и Th17.
Регулирует альтернативный путь активации макрофагов.
Активирует В-клетки и индуцирует экспрессию МНС II (главный комплекс гистосовместимости II класса) на покоящихся В-клетках
T-клетки, ТК, базофилы,
эозинофилы, NKT, моноциты,
Усиливает ответ Th2.
Стимулирует созревание и дифференцировку В-клеток.
Ингибирует продукцию провоспалительных цитокинов
Индуцирует ответ Th1 и Th17.
Стимулирует рост пре- и про-В-клеток
B- и T-клетки, моноциты
Индуцирует острофазный ответ совместно с ИЛ-1 и ФНОα.
Дифференцировка В-клеток в плазмоциты, усиление активности плазмоцитов.
Дифференцировка моноцитов и Т-клеток
Дифференцировка наивных Т-клеток в Th1, стимуляция продукции ИФНγ и ФНОα ЕK и NKT, усиление цитотоксической активности ЕК и СD8 +
Активированные ДК и фагоциты
Совместно с ИЛ-6 и TGF-β стимулирует дифференцировку наивных CD4 + в Th17
Семейство цитокинов ИЛ-1
Продуцируются многими клетками, но в особенно большом количестве — моноцитами, макрофагами, ДК
Провоспалительные: ИЛ-1А, ИЛ-1В, ИЛ-18, ИЛ-36А, ИЛ-36В, ИЛ-36G, ИЛ-33. Активируют врожденный и приобретенный иммунитет, острое и хроническое воспаление.
Противовоспалительные: ИЛ-1Ra, ИЛ-36Ra, ИЛ-37
Семейство ИЛ-17 (ИЛ-17A, ИЛ-17B, ИЛ-25, др.)
Th17, CD8 + T-клетки, ЕК, NKT, нейтрофилы
Активация транскрипционных факторов, индуцирующих экспрессию генов антибактериальных пептидов, провоспалительных хемокинов и цитокинов и металлопротеиназ
T-клетки, B-клетки, моноциты, макрофаги, ДК
Моноциты, макрофаги, нейтрофилы, лимфоциты
Хемоаттрактант для нейтрофилов, ЕК, T-клеток, базофилов и эозинофилов
Th2, активированные эозинофилы, ТК, CD8 + Т-клетки, ЕК, NKT
Дифференцировка и функционирование миелоидных клеток; усиление хемотаксической активности и способности к адгезии эозинофилов; заживление ран
Активированные макрофаги, моноциты, CD4 + Т-клетки, В-клетки, ЕК, нейтрофилы, ТК
Провоспалительный цитокин, который индуцирует острофазные белки и стимулирует ангиогенез
Th1, CD8 + Т-клетки, ЕК, В-клетки, макрофаги
Член семейства ФНО, который участвует в регуляции гомеостаза ДК и CD4 + Т-лимфоцитов, а также оказывает прямой цитотоксический эффект на опухолевые клетки
Эозинофилы, макрофаги, Treg
Иммуносупрессивное действие, влияет на генерацию Treg и толерогенных ДК, существенно снижает цитотоксическую и цитокинпродуцирующую активность моноцитов/макрофагов, снижает продукцию ими нитросоединений, реакционно-способных радикалов и провоспалительных цитокинов
Примечание. Th — Т-хелпер; Treg — регуляторные T-лимфоциты; ДК — дендритные клетки; ЕК — естественные киллеры; ТК — тучные клетки; ИФН — интерферон; ФНО — фактор некроза опухоли; АПК — антигенпрезентирующие клетки; Tfh — фолликулярные Т-хелперы; NKT — естественные Т-клетки; FoB — фолликулярные В-лимфоциты; Breg — регуляторные В-лимфоциты; СD — кластеры дифференцировки (Clusters of Differentiation); ИЛ — интерлейкин; Ig — иммуноглобулин.
На сегодняшний день выявлена продукция ряда цитокинов в центральной нервной системе (ЦНС) [3], а введение, например, ИЛ-18 индуцирует экспрессию его собственного гена в головном мозге [4]. Есть данные о том, что ИЛ-1 и ИЛ-6 вырабатываются непосредственно в гипоталамусе и гипофизе во время периферических специфических иммунных реакций. Индуцированные таким образом цитокины важны для синаптической пластичности, так, ИЛ-1 поддерживает, а ИЛ-6 ингибирует механизмы, ответственные за обучение и консолидацию памяти [3][5][6].
Существует теория, что физиологические воздействия на функции мозга тех цитокинов, которые продуцируются вслед за периферическими иммунными или центральными нейрональными сигналами, следует рассматривать в контексте общепринятой концепции тройственного синапса, включающей астроциты [7] в качестве третьей стороны. Есть данные, что астроциты как нейроиммунные клетки, взаимодействующие с клетками микроглии, могут играть центральную роль в интеграции иммунных сигналов в мозг с сохраненной или недавно полученной информацией от других высокоспециализированных сенсорных систем.
Ранее считалось, что астроциты играют лишь вспомогательную роль в нейронной активности, но сегодня известно, что благодаря своему широкому распространению и тесному контакту с нейронами эти клетки представляют собой основные компоненты нейрональной среды и микроархитектуры паренхимы головного мозга, а также хранят и обеспечивают энергетические субстраты, контролируют развитие нейронных клеток, синаптогенез и синаптическую активность. Благодаря своим иммунным функциям астроциты являются частью внутренней защитной системы мозга [8]. Следовательно, они из- за их двойственных нейронных и иммунных функций могут быть расценены как «нейроиммунные» клетки, причем их функции включают в себя выработку различных медиаторов с иммунными и нервными эффектами, таких как ИЛ-1, ИЛ-6 [9].
Трехсторонний синапс может играть центральную роль в обработке иммунных сигналов в головном мозге и в их интеграции с нейросенсорными сигналами и обеспечивает молекулярные и клеточные основы для обработки крайне изменчивого массива подобных сигналов [3].
Итоговое влияние на механизмы мозга и на нейроэндокринную иммунорегуляцию тех цитокинов, которые вырабатываются при активации тройственного синапса, будет зависеть от того, как, когда и где происходит такая стимуляция, а также от типа задействованного синапса. Например, когда активируется повышенная продукция ИЛ-1 и других цитокинов, их воздействие на тройственный синапс будет заключаться в модуляции физиологических функций мозга. Когда их продукция в головном мозге будет иммунологически инициирована, их действие будет преобладать в областях мозга, в которых эти медиаторы могут восстанавливать гомеостаз и оказывать иммунорегуляторное действие, вызывая нейроэндокринные реакции.
Когда иммунные эффекты не ведут к повреждению собственных компонентов, они обычно рассматриваются как защитные адаптивные механизмы. В целом иммунные реакции можно рассматривать как гомеостатические, обеспечивающие поддержание постоянства молекулярных и клеточных компонентов организма, для обеспечения данного эффекта нужно добиться биологической стабильности посредством физиологических или поведенческих изменений. Однако данный процесс при длительном его поддержании имеет так называемую «функциональную стоимость», или аллостатическую нагрузку, и может способствовать проявлению хронических заболеваний [10].
Понятие аллостаза обычно связывают с реакциями на стресс, следовательно, и иммунный стресс может играть определенную роль, так как активность большинства физиологических систем должна быть скорректирована для мобилизации иммунных клеток. Нейроэндокринные реакции в сочетании с иммунными опосредуют метаболические изменения и обеспечивают появление иммунорегуляторных сигналов, оказывая определенное противодействие регуляторным гомеостатическим механизмам, которые стремятся поддерживать систему на заданном уровне регуляции. В свою очередь, это является физиологически затратным, особенно при процессах, основанных на резком повышении активности иммунной системы [11]. Предполагается, что физиологически регулирование затрат энергии должно быть приведено в соответствие с новым заданным значением, причем процесс должен быть обратимым при восстановлении прежних условий. Если же такая обратимость нарушается во время длительных ситуаций, вновь заданные условия способствуют манифестации патологических состояний, в т.ч. аутоиммунных заболеваний.
Тем не менее иммунные реакции способствуют и восстановлению гомеостаза путем высвобождения цитокинов и других продуктов, которые, помимо своих собственных иммунных функций, могут также индуцировать нейроэндокринные реакции, оказывающие влияние на поддержание защитных сил организма. Важную роль в этом играет гипоталамо-гипофизарно-надпочечниковая (ГГН) система. Доказано, что ИЛ-1 и ИЛ-6, вырабатываемые воспалительными клетками, являются стимуляторами эндокринной системы посредством синтеза адренокортикотропного гормона (АКТГ). Данный импульс, по-видимому, проходит по гипоталамическим рецепторам, вследствие чего ЦНС вступает во взаимодействие с эндокринной и иммунной системами в ответ на воздействие патогенов. Более того, данная связь свидетельствует о том, что регуляция ГГН-оси цитокинами при воспалении зависит от АКТГ, но, как показано в ряде исследований, длительная стимуляция с помощью ИЛ-6 не гарантирует устойчивого повышения уровня АКТГ.
Так или иначе, в норме кортизол регулирует уровни нескольких циркулирующих в крови провоспалительных цитокинов, таких как ИЛ-2, ИЛ-3, ИЛ-6, фактор некроза опухоли альфа (ФНО-a) и интерферон-γ (ИФН-γ), и влияет на активность и жизнеспособность клеток иммунной системы, угнетает фагоцитоз антигенов и их последующую элиминацию макрофагами. Кортизол угнетает как клеточный, так гуморальный иммунный ответ, поддерживая баланс про- и противовоспалительных реакций, и вызывают инволюцию лимфоидных органов, снижает фагоцитарную активность нейтрофилов и макрофагов, подавляет активность лимфоцитов, тормозя их созревание и дифференцировку, стимулируя апоптоз. За счет иммуносупрессивного эффекта — снижает количество и активность воспалительных клеток, особенно тканевых макрофагов, и ограничивает их способность реагировать на поступающие антигены. Подавление активности иммунных клеток нарушает их дегрануляцию и высвобождение разрушающих ткани ферментов (матриксных металлопротеиназ, протеаз, нуклеаз и др.), хемоаттрактантов, адгезивных молекул.
У T-лимфоцитов кортизол снижает генетическую экспрессию ИЛ-2, подавляет работу Т-клеточного рецептора и молекул, следующих за ним по сигнальному пути (лимфоцитоспецифической протеинтирозинкиназы, инозитол-1,4,5-трифосфата), посредством мембраносвязанных рецепторов. Помимо этого, кортизол вызывает повышенную экспрессию высокоаффинного рецептора ИЛ-2 на регуляторных Т-клетках.
В целом подавление иммунного ответа под действием кортизола связано с ослаблением процессинга антигенов, снижением выработки антител, нарушением различных звеньев лимфопоэза. Под действием кортизола снижается гиперчувствительность организма к различным антигенам.
Однако иммунная система функционирует на границе между здоровьем и болезнью, следовательно, иммунный ответ может быть защитным и адаптивным. Тем не менее когда иммунная система гиперактивна в течение длительного времени, она может вызвать неадаптивные нейроэндокринно-индуцированные метаболические нарушения.
Так, хроническое воспаление у пациентов с аутоиммунными заболеваниями, по всей видимости, коррелирует с измененной функцией ГГН-оси и формированием стойких или транзиторных нарушений в реализации биологических эффектов кортизола, в т.ч. на иммунную систему. Как уже отмечалось, у ГК показана способность как усиливать, так и подавлять функции иммунной системы. Для объяснения этого феномена предложено две теории, первая состоит в том, что физиология действия ГК соответствует двухфазной кривой зависимости доза–реакция так, что ГК оказывают «разрешающие» (иммуностимулирующие) эффекты в низких концентрациях и подавляющие эффекты в высоких концентрациях. Вторая теория, по сути, продолжает первую и заключается в том, что сеть клеточных эффектов конкурентной ГК-опосредованной «up-регуляции» цитокиновых рецепторов и «down-регуляции» соответствующих цитокинов является биологическим ответом с более быстрым началом, но короткой продолжительностью. Вероятно, в отсутствие любого типа воспаления базальные уровни сигнальных путей рецепторов ГК, которые управляются циркадными ритмами продукции ГК, сенситизируют клетки к повреждающим стимулам путем усиления экспрессии рецепторов цитокинов и факторов комплемента, что позволяет быстро индуцировать воспалительный ответ на повреждение ткани. Во время воспаления, однако, вызванные стрессом концентрации ГК сдерживают иммунный ответ в первую очередь путем ограничения распространения сигналов цитокинов, сокращая таким образом продолжительность иммунного ответа [12][13].
В настоящее время доказано, что при выходе продукции цитокинов и других агентов иммунной системы из-под контроля эндогенных ингибиторов ( в том числе стероидных гормонов) эти медиаторы прямо или косвенно становятся ответственными за повреждение тканей и функциональную недостаточность органов, а также гиперкатаболизм. Некоторые медиаторы, высвобождающиеся во время иммунного ответа, а также вызванные ими нейроэндокринные и метаболические реакции могут приводить к повреждению тканей и апоптозу. Клинические и экспериментальные данные указывают на то, что иммунный ответ является защитным, когда он может быстро обезвредить патоген, а данный процесс нуждается в сильной метаболической поддержке [14] и регулировке основных гомеостатических механизмов [15]. Однако, как уже упоминалось, некоторые филогенетически старые и хорошо сохранившиеся продукты иммунных клеток могут опосредовать антигомеостатические реакции.
Антигомеостатические реакции могут наблюдаться при неинфекционных воспалительных/аутоиммунных патологиях, которые в естественных условиях и на поздних стадиях могут быть связаны, в том числе, с нарушениями питания и эндокринными расстройствами. Нейтрализация отдельных цитокинов, которые могут опосредовать такие эффекты, пока невозможна, поскольку цитокины « не работают индивидуально», как правило, вызывают длительные нейроэндокринные и метаболические нарушения. Эволюционно сохраненные антигомеостатические механизмы, характерные для конкретных заболеваний, — предмет дальнейших исследований, результаты которых могут быть очень важны для разработки терапевтических стратегий, которые препятствовали бы нежелательным комбинированным эффектам иммунных и нейроэндокринных медиаторов.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источник финансирования. Источник финансирования: «Эпидемиологические и молекулярно-клеточные характеристики опухолевых, аутоиммунных и йододефицитных тиреопатий как основа профилактики осложнений и персонализации лечения», рег. № АААА-А20-120011790180-4.
Конфликт интересов. Автор декларирует отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Автор одобрил финальную версию статьи перед публикацией, выразил согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. Deak T, Bordner KA, McElderry NK, et al. Stress-induced increases in hypothalamic IL-1: a systematic analysis of multiple stressor paradigms. Brain Research Bulletin. 2005;64:541-555. doi: https://doi.org/10.1016/j.brainresbull.2004.11.003
2. Трошина Е.А., Никонова Т.В., Свитич О.А., и др. Аутоиммунный полигландулярный синдром взрослых / Под ред. И.И. Дедова, Е.А. Трошиной. — М.: ГЭОТАР-Медиа; 2019. — 264 с.
3. Besedovsky HO, del Rey A. Central and peripheral cytokines mediate immune-brain connectivity. Neurochemical Research. 2011;36:1-6 doi: https://doi.org/10.1007/s11064-010-0252-x
4. delRey A, Roggero E, Randolf A, et al. IL-1 resets glucose homeostasis at central levels. Proceedings of the National Academy of Sciences. 2006;103:16039-16044 doi: https://doi.org/10.1073/pnas.0607076103
5. Donzis EJ, Tronson NC. Modulation of learning and memory by cytokines: signaling mechanisms and long term consequences. Neurobiology of Learning and Memory. 2014;115:68-77 doi: https://doi.org/10.1016/j.nlm.2014.08.008
6. Yirmiya R, Goshen I. Immune modulation of learning, memory, neural plasticity and neurogenesis. Brain, Behavior, and Immunity. 2011;25:181-213 doi: https://doi.org/10.1016/j.bbi.2010.10.015
7. Perea G, Navarrete M, Araque A. Tripartite synapses: astrocytes process and control synaptic information. Trends in Neurosciences. 2009;32:421-431 doi: https://doi.org/10.1016/j.tins.2009.05.001
8. Gimsa U, Mitchison NA, Brunner-Weinzierl MC, et al. Immune privilege as an intrinsic CNS property: astrocytes protect the CNS against T-cell-mediated neuroinflammation. Mediators of Inflammation. 2013;2013:320519 doi: https://doi.org/10.1155/2013/320519
9. Rothwell NJ, Luheshi GN. Interleukin 1 in the brain:biology, pathology and therapeutic target. Trends in Neuroscience and Education. 2000;23:618-625 doi: 10.1016/s0166-2236(00)01661-1
10. McEwen BS. Physiology and neurobiology of stress and adaptation:central role of the brain. Physiological Reviews. 2007;87:873-904 doi: 10.1152/physrev.00041.2006
11. Sterling P, Eyer J. Allostasis: a new paradigm to explain arousal pathology; in Fisher s, Reason J (eds): Handbook of Life stress, cognition and health. New York, Wiley, 1988, P. 629-649
12. Janeway CA Jr, Travers P, Walport M, et al. Immunobiology: The Immune System in Health and Disease. 5th edition. New York: Garland Science; 2001
13. Cain DW, Cidlowski JA. Immune regulation by glucocorticoids. Nat Rev Immunol. 2017;17(4):233-247. doi: https://doi.org/10.1038/nri.2017.1
14. Fox CJ, Hammerman PS, Thompson CB. Fuel feeds function: energy metabolism and the T-cell response. Nature Reviews Immunology. 2005;5:844-852 doi: https://doi.org/10.1038/nri1710
15. Yotamisligil GS, Erbay E. Nutrient sensing and inflammation in metabolic diseases. Nature Reviews Immunology. 2008;8:923-934 doi: https://doi.org/10.1038/nri2449
Об авторе
Трошина Екатерина Анатольевна, д.м.н., профессор, член-корреспондент РАН