мадопар и мадопар гсс в чем разница
Лекрственные формы Мадопара
ЧАСТЬ 3 Мадопар
Лекарственные формы Мадопара
| Лекарственная форма | Упаковка | Леводопа | Бенсеразид |
| Мадопар 125 | 100 капсул | 100мг | 25 мг |
| Мадопар 250 | 100 капсул | 200 мг | 50 мг |
| Мадопар 250 | 100 таблеток | 200 мг | 50 мг |
| Мадопар диспергируемый 125 (таблетки быстрого действия) | 100 таблеток | 100 мг | 25мг |
| Мадопар ГСС | 100 капсул | 100мг | 25 мг |
Мадопар Стандартный
Мадопар впервые был применен в 1974 году в стандартной форме в дозах 62.5, 125 и 250 мг и вплоть до появления в 1988 году Мадопара ГСС являлся базовой терапией БП.
Назначая больному Мадопар, многие клиницисты до сих пор начинают лечение с его наименьшей дозы, постепенно повышая ее по мере необходимости. Индивидуальный подход к больному БП означает, что врач делает выбор в пользу той лекарственной формы Мадопара, которая позволяет достичь оптимального клинического эффекта. Нередко для того, чтобы добиться адекватного контроля над симптомами паркинсонизма, приходится назначать одному больному несколько различных форм Мадопара, включая стандартную, диспергируемую и Мадопар ГСС.
Мадопар ГСС (гидродинамически сбалансированная система)
Мадопар ГСС впервые был применен в 1988 году с целью достижения более равномерного высвобождения леводопы и предотвращения симптомов, которые связаны с укорочением времени действия леводопы.
Механизм действия
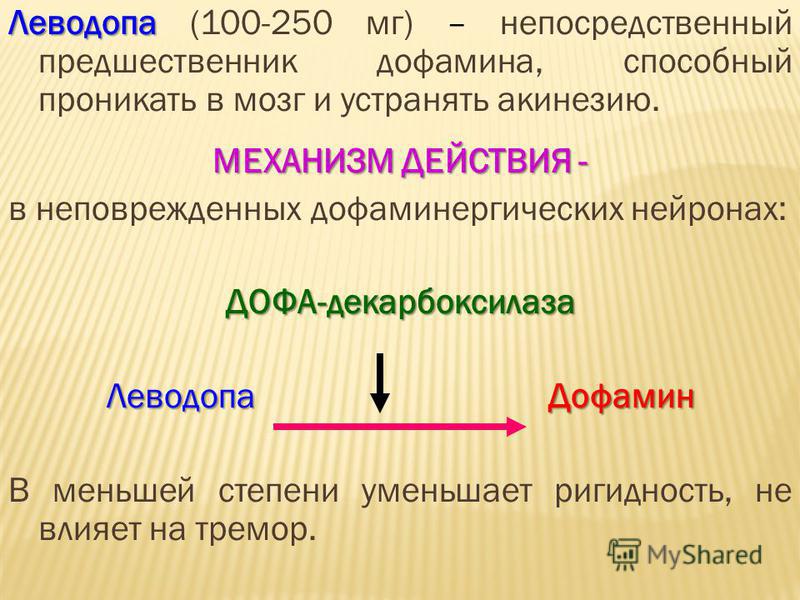
Оригинальная структура капсул Мадопара ГСС позволяет обеспечить равномерное высвобождение леводопы с течением времени. Желатиновая капсула содержит активное вещество в виде 100 мг леводопы и 25 мг бенсеразида. Активное вещество заключено в матрикс, состоящий, главным образом, из гидроколлоида, жиров, увлажняющих веществ. Плотность капсулы меньше, чем плотность желудочного сока, что позволяет ей плавать в желудке. Взаимодействие желудочного сока с матриксом капсулы приводит к формированию гидратированного пограничного слоя (коллоидной массы), через который может проникать активное вещество. Эксперименты с радиоактивно меченной леводопой показали, что капсула остается в желудке в течение 5-12 часов. Этот факт имеет важное значение, т.к. леводопа всасывается только на уровне верхней трети тонкой кишки.

Фармакокинетика
| Параметр (12 больных) | Мадопар стандартный | Мадопар ГСС | Отношение ГСС/стандартныи |
| Смакс (мг/мл) | |||
| среднее | 1,13 | 0,28 | 0,24 |
| диапазон | 0,5-4,4 | 0,1-0,6 | 0,07-0,5 |
| среднее | 1,0 | 3,0 | 2,9 |
| диапазон | 0,3-3.0 | 0,7-4,0 | 1,0-5,7 |
| AUC (мкг • час/мл) | |||
| среднее | 2,30 | 0,90 | 0,50 |
| диапазон | 0,6-4,4 | 0,3-2,2 | 0,12-0,92 |
В таблице представлены фармакокинетические параметры леводопы после однократного приема традиционной леводопы и формы с контролируемым высвобождением (125 мг).
По сравнению с традиционным Мадопаром, абсорбция леводопы из Мадопара ГСС происходит более медленно, при этом средняя максимальная концентрация в плазме (Смакс ) снижается[1]. Примерно на 2 часа увеличивается время, необходимое для достижения максимальной концентрации (tмакс). Относительная биодоступность (AUC) уменьшается до 60% от биодоступности традиционной леводопы.
Несмотря на то, что период полувыведения леводопы (45 минут) при применении Мадопара ГСС не изменяется, период полувыведения этой лекарственной формы увеличивается за счет замедленного высвобождения активной субстанции.

Роль Мадопара ГСС
Первоначально Мадопар ГСС предназначался для больных с клиническими флуктуациями симптомов паркинсонизма[2,3]. С мая 1996 года показания были расширены, и новая форма стала применяться при любых стадиях заболевания, в том числе у больных с впервые диагностированным паркинсонизмом, которым леводопа назначалась впервые[4].
Другим важным аспектом применения Мадопара ГСС является его эффективность при назначении перед сном для лечения ночных проявлений паркинсонизма[5]. По данным некоторых исследователей, 98% больных паркинсонизмом испытывают как минимум одну или более ночных проблем, в том числе трудности при поворотах в постели и подъемах с постели.
Мадопар ГСС выгодно отличается от других форм возможностью контроля над ночными проявлениями паркинсонизма. Он может быть успешно применен у впервые диагностированных больных, нуждающихся влеводопе, и у пациентов с выраженными флуктуациями симптомов.
Мадопар диспергируемый
Мадопар диспергируемый, быстрого действия, впервые был разработан в 1987 г. для удовлетворения потребности больных в жидкой форме леводопы. Показано, что приблизительно 25% больных БП имеют затруднения при глотании, и что жидкая форма является для них более удобной. Наряду с этим оказалось, что Мадопар диспергируемый обладает более быстрым эффектом по сравнению со стандартным и Мадопаром [6,7]. В результате Мадопар диспергируемый стал применяться более широко в сочетании с Мадопаром ГСС, особенно в качестве первой утренней дозы, когда необходимо быстро улучшить состояние больного и снять проявления БП.
Механизм действия
Таблетки Мадопара диспергируемого в дозе 125 мг растворяют в воде до получения молокоподобной суспензии. Ее цвет обусловлен присутствием наполнителей, в то время как леводопа и бенсеразид растворяются полностью. Обычно для приготовления суспензии достаточно 30 мл воды; суспензию необходимо принять в течение 30 минут после ее приготовления.
Фармакокинетика
Сравнение Мадопара диспергируемого со стандартным показало, что при применении Мадопара диспергируемого максимальный эффект достигается значительно быстрее[6]
Роль Мадопара диспергируемого
Мадопар диспергируемый имеет преимущества у больных паркинсонизмом с затруднениями при глотании или подвергшихся специальным процедурам, например имеющим назогастральный зонд[6,8]. Наряду с этим он может успешно применяться в сочетании с Мадопаром стандартным или Мадопаром ГСС в качестве первой утренней дозы для быстрого облегчения симптомов БП[6,7,9]. Кроме того, целесообразно использовать Мадопар диспергируемый для повышения уровня леводопы после обеда, когда многие больные испытывают акинезию, обусловленную ухудшением всасывания леводопы в связи с конкурентной абсорбцией белков в желудке[6,7].
Инструкция к применению
Дозирование и способ применения:
Мадопар стандартный и Мадопар диспергируемый
Инструкция по применению препарата Мадопар и его аналоги
Мадопар – это лекарственное средство, которое назначают для лечения паркинсонизма и синдрома беспокойных ног. Эффективных методов лечения на данный момент нет, но данное средство способно замедлять течение болезни, и улучшать самочувствие больного.
Как и любой медпрепарат, лекарство имеет свои противопоказания к применению, а также может провоцировать возникновение побочных действий. Поэтому перед приемом Мадопара необходимо внимательно ознакомиться с инструкцией по применению, а также отзывами пациентов и специалистов о препарате.
Общие сведения
Медикамент производится швейцарской компанией Ф. Хоффманн-Ля Рош Лтд, но на территории России имеется представительство. Реализуется через сеть аптек, часто медикамент заказывают через интернет.
Лекарственная группа, МНН
Комбинированный препарат, который содержит сразу два компонента – предшественник дофамина и ингибитор периферической декарбоксилазы. МНН – Леводопа + Бенсеразид. Медикамент назначают при нехватке нейромедиатора дофамина. Дефицит часто возникает у пожилых людей, когда начинается гибель нейронов центральной нервной системы, а также у людей с врожденными патологиями иммунной системы.
Лекарственные формы и стоимость
Мадопар изготавливается в нескольких лекарственных формах. Они отличаются вспомогательными компонентами, дозировкой и продолжительностью эффекта:
Цвет таблеток, капсул с разной дозировкой отличается – белый, желтый, розовый, красный, зеленый. Диспергируемые таблетки – порошок, из которого нужно приготовить суспензию путем добавления теплой воды.
Цена Мадопара в аптеках зависит от места расположения аптек и ценовой политики учреждения. Средняя стоимость препарата по Москве представлена в таблице.
| Форма выпуска | Цена (руб.) |
|---|---|
| Таблетки 250 мг 100 шт. | 1400 |
| Капсулы 125 мг 100 шт. | 600 |
Продаются во флаконе из темного стекла, картонной упаковке. Фасуются по 30, 100 штук. Срок годности таблеток 4 года с момента изготовления, капсул – 3. Хранить следует в сухом месте, подальше от солнечных лучей при температуре не выше +25°С. Лекарство отпускается по рецепту.
Состав
Активными компонентами являются леводопа и бенсеразида гидрохлорид, вспомогательные ингредиенты разных форм отличаются. Свойства основных компонентов:
Фармакодинамика, фармакокинетика
При болезни Паркинсона дофамин вырабатывается в недостаточном количестве, поэтому действующие вещества препарата повышают уровень дофамина в нейронах.
Леводопа попадает в ЦНС, превращается в дофамин в церебральных и экстрацеребральных тканях. Однако большая часть образованного вещества не достигает базальных ганглиев, что провоцирует развитие негативных реакций, низким терапевтическим результатам. Устранить данный недостаток помогает второй активный компонент – бенсеразида гидрохлорид.
Механизм действия Леводопы
Медикамент быстро всасывается тканями ЖКТ, попадает в кровь. Максимальная доза наблюдается через 60 минут после приема капсулы. Выводится из организма в течение 17 часов, но имеет свойства накапливаться в организме при регулярном употреблении. Расщепляется печенью, выводится почками с мочой, малая доля – с калом. На скорость всасывания, концентрацию, эффективность влияет прием пищи, поэтому принимают лекарство спустя 60 минут после еды.
Отличие Мадопара ГСС от Мадопара
Мадопар ГСС (гидродинамически сбалансированная система) – инновационный препарат с улучшенной формулой. Применяется как самостоятельное средство для лечения болезни Паркинсона либо в сочетании со стандартным Мадопаром. Основное отличие инновационного медикамента заключается в способности медленно всасываться, дольше действовать, вызывать меньшее количество побочных эффектов.

Изначально гидродинамически сбалансированная система применялась для терапии больных с клиническими флуктуациями симптомов паркинсонизма, немного позже сфера применения расширилась. На данный момент препарат применяется при любой форме заболевания, но под строгим контролем специалистов, в индивидуально определенной дозировке. Важным открытием стало эффективное влияние препарата на состояние организма при ночных проявлениях паркинсонизма.
Основные преимущества капсул ГСС:
Аналоги
Средства на основе идентичных действующих веществ выпускают отечественные и зарубежные компании. Вопрос замены должен обсуждаться со специалистом. Основные аналоги:
Препараты значительно отличаются по цене, но механизм действия идентичный.
Показания, ограничения
Назначают препарат при недостаточной выработке дофамина. Ведущими симптомами дефицита этого гормона являются мышечная ригидность, тремор, гипокинезия, постуральная неустойчивость. Данные проявления свойственны болезни Паркинсона либо паркинсональному синдрому. Мадопар принимают при:
Перед началом терапии требуется консультация со специалистом и обследование, так как препарат имеет множество противопоказаний:
Мадопар запрещается принимать беременным и кормящим женщинам, поскольку активные вещества проникают через плаценту и попадают в грудное молоко. В противном случае, нарушается развитие опорно-двигательного аппарата.
Не назначается лекарство детям и молодым людям до 25 лет, поскольку до этого возраста происходит формирование и укрепление скелета.
Инструкция по применению
Капсулы проглатывают целиком, таблетки допускается измельчать. Диспергируемую форму растворяют в теплой воде – 50 мл на 1 шт., выпивают в течение 30 минут. Желательно пить лекарство за 30 минут до еды либо час после.
Начинают лечение с минимальной дозировки – 1 капсула 3 р./сутки. Постепенно дозу увеличивают. Максимальный терапевтический эффект достигается при 300-800 мг леводопы, 75-200 мг бенсеразида, в зависимости от общего состояния больного и диагноза. Приближаются к необходимой дозировке постепенно в течение одного-двух месяцев.
При улучшении самочувствия дозу начинают снижать либо переходят на диспергируемые таблетки с быстрым эффектом. При поддерживающей терапии употребляют 125 г 3-6 раз в сутки, через равные промежутки времени.
Лекарственное взаимодействие
Совместное употребление других препаратов с Мадопаром может усилить либо ослабить действие таблеток. Определенные лекарственные комбинации производят следующие эффекты:
Подбор медикаментов должен осуществлять только врач. Специалист учитывает влияние медикаментов при совместном применении, корректирует при необходимости дозу.
Меры предосторожности
Чтобы избежать нежелательных последствий и добиться максимального терапевтического эффекта, нужно учитывать определенные нюансы:
При ухудшении самочувствия на фоне приема Мадопара нужно обратиться за консультацией к специалистам.
Возможные негативные реакции и передозировка
Мадопар с кровью разносится по всему организму, влияя на работу различных внутренних органов, систем. В связи со способностью лекарства накапливаться в тканях организма, существует риск развития побочных эффектов при неправильно подобранной дозировке или игнорировании хронических заболеваний органов ЖКТ:
Симптомы передозировки аналогичны, но выражены сильнее. Они проявляются мигренью, спутанностью сознания, сильной тошнотой, рвотой. Лечение симптоматическое. Предусмотрено снижение дозировки либо отмена препарата. При ухудшении самочувствия нужно проконсультироваться с лечащим врачом.
Дофаминергические препараты (мадопар) в коррекции мышечного тонуса при неврологических заболеваниях
В клинической практике невролога в контексте лечения различных неврологических заболеваний нередко возникает необходимость коррекции патологически измененного мышечного тонуса. Особенно много проблем в связи с этим приходится решать при лечении пациент
В клинической практике невролога в контексте лечения различных неврологических заболеваний нередко возникает необходимость коррекции патологически измененного мышечного тонуса. Особенно много проблем в связи с этим приходится решать при лечении пациентов с дистоническими гиперкинезами. Дистония представляет собой клинический синдром, характеризующийся неритмичными медленными насильственными движениями в различных частях тела, своеобразным изменением мышечного тонуса и формированием патологических поз [1]. Данный синдром в значительной степени гетерогенен, как клинически, так и в плане патогенеза его возникновения. По распространенности выделяют генерализованные, мультифокальные, фокальные формы; по форме гиперкинеза — тонический и клонический [1]. В настоящее время большинство исследователей предполагают, что в формировании данной патологии принимают участие холинергические, дофаминергические, и ГАМКергические (g-аминомасляная кислота) системы мозга [2, 3]. Соответственно, имеет смысл воздействовать на указанные нейротрансмиттерные системы. Более того, известно, что клинические симптомы некоторых видов дистонических гиперкинезов регрессируют при терапии препаратами леводопы. В первую очередь это касается ригидной формы торсионной дистонии, также известной как болезнь Сегавы [4], или ДОФА-зависимая дистония. Эта патология достаточно хорошо изучена, в ее основе лежат генетические дефекты (в настоящее время известны как минимум три основных дефекта, один из которых наследуется аутосомно-доминантным способом с неполной пенетрантностью, а два — аутосомно-рецессивным), в результате которых нарушается синтез ферментов дофаминового обмена и, соответственно, синтез самого дофамина. Единственным патогенетически оправданным медицинским вмешательством в данном случае является назначение препаратов леводопы, причем они практически полностью устраняют симптоматику заболевания [1, 4]. Однако в реальной клинической практике, как показывает наш опыт, достаточно редко ставится правильный диагноз, что связано с малой информированностью неврологов о данной проблеме. Немалая доля случаев ДОФА-зависимой дистонии приходится на детский возраст, и ее зачастую относят к проявлениям детского церебрального паралича (ДЦП). Соответственно больному назначают всевозможные методы лечения и реабилитации, оказывающие минимальный преходящий эффект. Фактически пациент с неверным диагнозом ДЦП, гиперкинетическая форма, обрекается на инвалидность, за исключением тех случаев, когда в лечении данной патологии используются препараты леводопы.
В Центре неврологии и нейрореабилитации (г. Красноярск) функционирует служба экстрапирамидной патологии, специализирующаяся на оказании помощи больным данного профиля. Здесь накоплен значительный опыт ведения больных с дистониями. Анализ этого опыта позволил выработать наиболее эффективные и рациональные алгоритмы лечения пациентов в условиях практического здравоохранения. Наиболее важным этапом ведения пациентов является установление правильного диагноза.
При типичной картине ригидной торсионной дистонии диагностика больших сложностей не вызывает. Терапия, исходя из патогенеза, предполагает применение препаратов леводопы с заместительной целью. Нами применяется хорошо зарекомендовавший себя препарат мадопар, содержащий леводопу и ингибитор ДОФА-декарбоксилазы бенсеразид, в дозе 125 мг 2–3 раза в день.
Однако гораздо чаще возникают определенные диагностические трудности, связанные с размытостью клинической симптоматики и поздним дебютом заболевания. Идеальным выходом было бы назначение генетического исследования всем больным, у которых существует вероятность диагноза ригидной ДОФА-зависимой дистонии. К сожалению, проведение данного исследования у большинства больных по организационно-техническим причинам невозможно. Нам представляется разумным использование более простого диагностического приема: речь идет о пробном назначении препарата леводопы. Непосредственно во время приема, в том числе амбулаторного, больной принимает растворенную в 50–100 мл воды таблетку быстрорастворимого мадопара 125 мг. Через 30–60 мин оцениваются изменения в состоянии мышечного тонуса и других проявлениях заболевания. Данный прием нашел широкое применение в нашей работе с больными, у которых подозревается развитие паркинсонизма. При ДОФА-зависимых дистониях мы также наблюдали значительный эффект с выраженным регрессом симптоматики.
При фокальных и мультифокальных, а также ДОФА-резистентных формах дистоний наиболее эффективным, по современным представлениям, является применение инъекций препарата ботулинического токсина, нарушающего нейромышечную передачу импульса и соответственно расслабляющего вовлеченные в патологический процесс мышцы. Данный эффект вариабелен по продолжительности действия, в среднем его длительность сохраняется до 4–5 мес [5]. Мы полностью согласны с данным подходом, однако существует ряд нюансов, на которых следует остановиться подробнее.
Назначение ботулинического токсина (в нашей клинике применяется препарат диспорт) оказалось весьма и весьма эффективным. Но с экономической точки зрения данный вид лечения имеет свои недостатки, как дорогостоящий и не всегда доступный лицам, не относящимся к льготной категории больных. Кроме того, длительность эффекта колеблется у разных пациентов, и значимым аспектом проблемы является пролонгирование этого эффекта. Исходя из этих целей нами были предприняты попытки комбинации инъекций диспорта и таблетированных препаратов других фармакологических групп. Наилучший эффект, с нашей точки зрения, наблюдается при применении бензодиазепинов (клоназепам) в дозе 2–3 мг в сутки либо холинолитиков (циклодол) в дозе 4–6 мг в сутки. В отдельных случаях клинический эффект инъекции можно было проследить в течение 8–18 мес.
Другой немаловажной причиной, обусловливающей правомерность назначения комбинированной терапии диспортом и миорелаксантами, являются мультифокальность дистонического гиперкинеза. Назначать больному дозы ботулотоксина, способные снять все проявления дистонического синдрома, невозможно и попросту опасно: этот препарат применяется лишь в случаях, когда имеют место наиболее инвалидизирующие проявления заболевания, а в отношении остальных симптомов ставка делается на другие препараты. В связи с этим целесообразным представляется следующее наше наблюдение: во многих случаях дистонического гиперкинеза с преобладанием тонического компонента (в первую очередь при цервикальной дистонии) нами проводилась описанная выше проба с быстрорастворимым мадопаром. При этом иногда отмечался эффект ослабления дистонии, что позволяло применять мадопар в тех же целях в дальнейшем ежедневно в дозе 125 мг 2–3 раза в день. При этом наблюдался положительный эффект. К сожалению, через несколько месяцев (в среднем 6–11) данный эффект значительно ослаблялся, что не позволяет относить данные виды дистонии к описанным выше классическим ДОФА-зависимым. Однако определенная патогенетическая общность и вовлечение дофаминергических структур в данном случае имеют место.
Таким образом, по нашему мнению, при дистоническом синдроме с преимущественным тоническим (ригидным) компонентом во всех случаях следует применять пробу с быстрорастворимым мадопаром. При наличии положительных результатов показано назначение леводопатерапии, с тщательным динамическим наблюдением за больным, а при недостаточной эффективности терапии через 1–2 мес — дополнительное подключение препаратов ботулинического токсина.
В отношении коррекции ДОФА-резистентных (первично, вторично) дистоний, а также большинства фокальных, преимущественно клонических вариантов заболевания, препаратом выбора является ботулотоксин, для усиления и продления эффекта которого целесообразно дополнительное назначение бензодиазепинов и холинолитиков.
Другой проблемой, требующей адекватного решения, является повышенный мышечный тонус у больных, перенесших острое нарушение мозгового кровообращения. Мышечный гипертонус значительно нарушает процесс восстановления нарушенных двигательных функций, а кинезиотерапия, проводимая в рамках комплексной нейрореабилитации, иногда оказывается просто неэффективной. Наш опыт позволил сформулировать удачные, с нашей точки зрения, подходы к данной проблеме.
Повышение мышечного тонуса при центральных парезах обусловлено растормаживанием спинальных нейронов, в условиях отсутствия тормозного влияния коры, что приводит к формированию спастического (пирамидного) гипертонуса. Однако, поскольку в регуляции мышечного тонуса значимую роль играет и экстрапирамидная система, ее поражение, равно как и поражение пирамидных путей, приводит к мышечной гипертонии по экстрапирамидному (пластическому) типу [6, 7]. Разумеется, на практике в процесс тем или иным образом оказываются вовлечены оба компонента, хотя, как правило, можно проследить ведущий из них. Таким образом, повышение мышечного тонуса при центральных парезах целесообразно разделить на преимущественно пирамидное, преимущественно экстрапирамидное и смешанное — когда невозможно четко определить ведущий компонент.
При ведущем пирамидном компоненте в арсенале врача имеются достаточно хорошо разработанные схемы терапии, включающей применение миорелаксантов, назначение физиотерапевтических процедур, при необходимости — проведение массажа, иглорефлексотерапии [6, 7].
Лечение мышечной гипертонии посредством инъекций ботулинического токсина нам представляется перспективным, однако до настоящего времени мы не накопили достаточного собственного опыта в отношении данного метода, что связано с экономическими и техническими трудностями.
В ходе лечения мы активно используем препараты с различными механизмами действия. Наиболее часто применяется тизанидин (сирдалуд) — миорелаксант центрального действия, стимулирующий пресинаптические α2-адренорецепторы, подавляющий высвобождение возбуждающих аминокислот, которые активизируют рецепторы к N-метил-D-аспартату (NMDA-рецепторы). Тизанидин, по нашему мнению, один из наиболее эффективных препаратов данной группы. Средние терапевтические дозы составляют от 4 до 12 мг в сутки. Наиболее распространенным побочным действием, возникающим при приеме препарата и в ряде случаев препятствующим его применению, является гипотензивный эффект.
Толперизона гидрохлорид (мидокалм) — другой миорелаксант центрального действия, активно использующийся в нашей клинике. Механизм действия препарата связан с угнетающим влиянием на каудальную часть ретикулярной формации, центральными н-холинолитическими свойствами. Средняя эффективная доза составляет 225–450 мг в сутки. Препарат, по нашему мнению, обладает несколько меньшей эффективностью, но хорошо переносится пациентами.
Также в отдельных случаях мы прибегаем к назначению баклофена — миорелаксанта центрального действия, производного γ-аминомасляной кислоты, агониста GABA β-рецепторов. Достаточно редкое использование данного препарата для снижения мышечного тонуса при центральном парезе обусловлено значительными проблемами, возникающими при титровании его дозы (начиная от 5 мг 3 раза в день и заканчивая 25 мг 3 раза в день), поскольку он способен наряду с положительным влиянием в виде снижения спастичности приводить к выраженной мышечной слабости, препятствующей проведению кинезио- и эрготерапии. Кроме того, резкое наращивание дозы (равно как и резкая отмена) способны спровоцировать развитие судорожных и психотических реакций, что также ограничивает использование данного препарата. Однако он находит себе применение при малой эффективности прочих лекарственных средств, в первую очередь у спинальных больных при грубом повышении мышечного тонуса.
Препараты группы бензодиазепинов (в первую очередь клоназепам) приводят к выраженному седативному эффекту, нередко провоцируют либо усугубляют когнитивные и вестибулярные нарушения, и потому в нашей практике для снижения мышечного тонуса у постинсультных больных не применяются.
Обращает на себя внимание тот факт, что у больных с повышением мышечного тонуса по смешанному или преимущественно экстрапирамидному типу эффективность традиционных миорелаксантов незначительна. Среди пациентов нашего Центра, перенесших инсульт, число таких случаев колеблется от 12 до 18%. Исходя из наличия пластического тонуса, а также минимальных элементов экстрапирамидной недостаточности (легкая гипомимия, брадифрения), для таких больных была предпринята попытка применения малых доз ДОФА-содержащих препаратов. На первом этапе работы с больным (после установления наличия избыточного тонуса, повышенного по смешанному либо пластическому типу) проводилась проба с быстрорастворимым мадопаром. При наличии положительного эффекта препарат мадопар назначался в дозе 62,5±125 мг ежедневно, причем на данном фоне мышечный тонус снижался и облегчалось проведение реабилитационных занятий. Так же, как и прочие миорелаксанты, мадопар назначается длительными курсами. Терапия продолжается не только в течение стационарного нейрореабилитационного курса, но и на этапе амбулаторного долечивания в течение 2–3 мес, а при необходимости и дольше. Особо хотим подчеркнуть, что в данном случае речь идет не о сосудистом паркинсонизме (который в классическом варианте имеет совершенно иную клинику — с преимущественным вовлечением нижней части тела и не поддается лечению ДОФА-содержащими препаратами), а о синдроме центрального гемипареза с комбинированным нарушением мышечного тонуса на различных этапах перенесенного инсульта.
Таким образом, мы считаем рациональным проведение пробы с быстрорастворимым мадопаром у больных после перенесенного инсульта, имеющих в неврологическом статусе, кроме ведущего синдрома центрального гемипареза, признаки экстрапирамидной недостаточности с нарушением мышечного тонуса по пластическому либо смешанному типу, а также у пациентов, резистентных к традиционным миорелаксантам. В случае положительного эффекта нам представляется целесообразным назначение мадопара с целью снижения мышечного тонуса у данной категории пациентов.
Литература
Д. В. Похабов, кандидат медицинских наук, доцент
С. В. Прокопенко, доктор медицинских наук, профессор
В. Г. Абрамов
Э. М. Аракчаа
КрасГМА, Центр неврологии и нейрореабилитации, Красноярск