маркеры остеопороза в крови что это значит
Маркеры остеопороза в крови что это значит
Современная лабораторная диагностика остеопороза.
Значимость заболевания в современном обществе и медицине определяется его распространённостью среди населения, тяжестью течения и исходов, экономическими потерями больного, семьи и общества в целом. Остеопороз (ОП) — системное метаболическое заболевание скелета, характеризующееся снижением массы костной ткани и нарушением микроархитектоники её строения, что снижает прочность кости и увеличивает риск переломов. По мнению экспертов ВОЗ, ОП сегодня — одно из наиболее распространённых заболеваний, которое наряду с инфарктом миокарда, инсультом, раком и внезапной смертью занимает ведущее место в структуре заболеваемости и смертности населения.
Результаты многочисленных исследований убедительно доказали, что костная масса является главной детерминантой механических свойств костной ткани и определяет 75-80% её крепости. Риск переломов прямо связан с абсолютными значениями минеральной плотности костной ткани (МПКТ) позвоночника и шейки бедра, а костная денситометрия — единственный достоверный метод, позволяющий установить степень снижения костной массы. Риск перелома увеличивается с возрастом, который главным образом связан у пожилых людей с низкой МПКТ. Риск перелома бедра возрастает в 2-3 раза при каждом снижении МПКТ шейки бедра на одно стандартное отклонение в соответствии с критериями ВОЗ.
Патогенез остеопороза.
ОП сегодня широко используется как модель фундаментальных исследований в изучении молекулярных механизмов межклеточного взаимодействия. ОП – многофакторное заболевание, в основе которого лежат процессы нарушения костного ремоделирования с повышением резорбции костной ткани и снижением костеобразования. Ремоделирование костной ткани начинается с резорбции, осуществляемой в процессе остеокластогенеза с образованием полости резорбции. Остеобласты (ОБ) «атакуют» полость резорбции, где строят новый костный матрикс для последующей минерализации. Оба процесса костеобразования тесно связаны. Образование кости превышает резорбцию в течение роста скелета, и наоборот, резорбция превалирует в течение последующего периода жизни человека. Оба процесса костеобразования являются результатом тесного клеточного взаимодействия ОБ иостеокластов (ОК), которые берут начало от предшественников различных клеточных линий, а именно: ОБ — из мезенхиальных стволовых клеток, ОК — из макрофагально-моноцитарных клеток крови.
Кость формируется остеобластами. Основная их функция – синтез остеоида (протеинового матрикса), который на 90-95% состоит из коллагена 1 типа, на 5% из белка остеокальцина и впоследствии минерализуется кальцием и фосфатом из внеклеточной жидкости. ОБ содержат фермент щёлочную фосфатазу, несут рецепторы к паратиреоидному гормону (ПТГ) и кальцитриолу и способны к пролиферации. Минеральная часть кости состоит из гидроксиапатита и аморфного фосфата кальция, которые нековалентно связаны с белками органического матрикса
Резорбция кости осуществляется остеокластами. Это подвижные клетки. Выделяя протеолитические ферменты и кислую фосфатазу, вызывают деградацию коллагена, разрушение гидроксиапатита и выведение минералов из матрикса. Имеется корреляция между активностью тартратрезистентной кислой фосфатазы в сыворотке крови и выраженностью резорбтивных процессов в кости.
В норме оба процесса – образование и разрушение уравновешены.
Сроки физиологического ремоделирования кости.
| Фаза резорбции кости | 14-30 дней |
| Switch-over фаза (простагландин Е2 ответственен за апоптоз остекластов) | 10 дней |
| Фаза формирования кости | 90 дней |
| Фаза отдыха | 900 дней |
Биологический смысл феномена ремоделирования кости состоит в приспособлении механических свойств кости к постоянно меняющимся условиям окружающей среды. Рост и обновление скелета сопровождается регенерацией микроповреждений и поддержанием возможности перехода минералов в кровь и обратно. У взрослых людей остеобласты продуцируют чуть меньше костной ткани, чем требуется. Следствием этого является отрицательный баланс кости, который составляет 0,5-1% ежегодно. Данный феномен известен как «ассоциированная с возрастом остеопения».
OPG-остеопротегерин – остеокластингибирующий фактор, гликопротеин, широко экспрессированный в различных тканях, является мощным ингибитором костной резорбции. OPG действует для RANKL как «мнимый» рецептор, блокирует взаимодействие с RANK и таким образом ингибирует формирование зрелых ОК, нарушает процесс остеокластогенеза и резорбцию костной ткани. Баланс между RANKL и OPG фактически определяет количество резорбированной кости.
Недавно были получены данные, что Т-клетки принимают участие в регуляции костного метаболизма. При индукции интерлейкина-17 (IL-17),который в эксперименте индуцировал экспрессию СОХ-2-зависимого простагландина Е2 и RANKL в ОБ, авторы пришли к заключению, что IL-17 — важный цитокин для остеокластной резорбции. Однако наиболее важными медиаторами для действия различных систем в процессе ремоделирования костной ткани как в норме, так и при ОП является в настоящее время система RANKL-RANK-OPG.
Факторы, играющие важную роль в патогенезе ОП и его переломов: генетические, формирование низкого пика костной массы, потеря минеральной плотности кости, ассоциированная с возрастом и постменопаузой, нарушение архитектоники строения кости, особенности геометрии кости (бедра), травмы и падения, питание с низким содержанием кальция и витамина D, белка и др., низкая двигательная активность, вредные привычки (курение, алкоголь). При вторичном ОП к перечисленным факторам присоединяются факторы заболевания, отрицательного действия лекарственных препаратов (глюкокортикостероиды, иммунодепрессанты и др.), которые вызывают потерю костной массы и ОП.
Снижение костной массы при ОП, которое является основным фактором его патогенеза, рассматривается сегодня как следствие формирования неадекватно низкого пика костной массы в молодом возрасте и интенсивной потери кости, связанной с возрастом, в пожилом возрасте. Генетические факторы — главные детерминанты пика костной массы. Вклад генетических факторов составляет 60-80% в зависимости от методов исследования (близнецы, семьи). Различные гены рассматриваются в качестве кандидатов, участвующих в сложном процессе ремоделирования, формирования и эволюции костной массы, приводящих к ОП и переломам. Многочисленные комплексные исследования различных лабораторий мира направлены на поиск конкретных генов, изучение их полиморфизма, функции и взаимодействия в процессе костного ремоделирования и ОП.
Первичный остеопороз
Остеопороз, развивающийся в периоде постменопаузы, относится к классу первичных остеопорозов. Известно, что снижение секреции половых гормонов в период климактерия оказывает прямое и опосредованное влияние на состояние костного метаболизма. Снижение содержания эстрогенов приводит к нарушению кальциевого обмена, что сопровождается уменьшением минеральной плотности костной ткани. Кроме того, имеет место подавление активности остеобластов, что приводит к преобладанию резорбции над процессами формирования костной ткани. Постменопаузальный остеопороз составляет 85% общего количества первичного остеопороза.
Сенильный остеопороз — так называемый второй тип остеопороза, в патогенезе которого важную роль играет снижение всасываемости кальция в кишечнике, чему также способствует дефицит витамина D, вызванный уменьшением поступления его с пищей, замедлением образования его в коже из провитамина D. Наибольшее значение в патогенезе сенильного остеопороза имеет дефицит активных метаболитов витамина D вследствие снижения его синтеза в почках. При сенильном остеопорозе определённую роль играет развитие резистентности к витамину D — т.е. дефицит рецепторов 1,25(ОН)2D. Указанные факторы вызывают развитие транзиторной гипокальциемии, что приводит к усилению продукции паратиреоидного гормона. В результате вторичного гиперпаратиреоза усиливается резорбция костной ткани, в то время как костеообразование к старости снижено.
Вторичный ОП
Серьёзной медицинской проблемой является и вторичный ОП, возникающий при различных заболеваниях: ревматологических, эндокринологических, онкологических, обструктивных заболеваниях лёгких и бронхиальной астмы, заболеваниях почек, щитовидной железы, органов пищеварения, при иммобилизации и длительном приёме ряда медикаментов (кортикостероиды, иммунодепрессанты, антиконвульсанты, тиреоидные гормоны и др.).
Снижение МПКТ при вторичном ОП часто достигает критериальных величин ОП (-2,5 SD и более по Т-критерию) и даёт основание поставить диагноз.
У больных ревматоидным артритом (РА) в постменопаузе развитие ОП имело место в поясничном отделе позвоночника и шейке бедра у 36%, в предплечье у 40%, а у пациентов с сохранённым менструальным циклом — у 7 и 10% соответственно. Возраст больных и длительность менопаузы, наличие факторов риска, активность и длительность заболевания, степень функциональной недостаточности суставов, проводимая терапия (особенно назначение глюкокортикоидов — ГК) оказывают влияние на величину потери МПКТ и развитие остеопении. При обследовании больных с эндогенным гиперкортицизмом (синдром и болезнь Иценко-Кушинга) ОП обнаружен у 91%, переломы тел позвонков или рёбер — у 58%. ОП у больных бронхиальной астмой значительно утяжеляет течение основного заболевания, увеличивает стоимость лечения. По данным доктора И.А.Барановой, снижение МПКТ было выявлено у 42,8% больных бронхиальной астмой 20-49 лет, ранее не получавших гормональную терапию, и потеря МПКТ увеличивалась в 5 раз при среднетяжёлом течении (53,5%) по сравнению с легким (11%). У больных молодого и среднего возраста, принимавших ГК в средней дозе 10,20±5,99 мг/сут на протяжении 8-14 лет, снижение МПКТ обнаружено у 85%, у 13% зарегистрированы переломы скелета. В качестве причины развития ОП при РА, ряде воспалительных заболеваний, бронхиальной астме обсуждается непосредственное влияние самого заболевания на костную ткань, поскольку известно большое число общих цитокинов, принимающих участие в патогенезе хронического воспалительного процесса и костного ремоделирования, а также ГК, которые наиболее эффективны для базисной терапии при ряде системных заболеваний и в то же время занимающих ведущее место в индукции вторичного ОП. Изучение переломов при вторичном ОП остаётся актуальной задачей.
Стероидный остеопороз также относится к классу вторичных остеопорозов и вызывается патологическим повышением эндогенной продукции глюкокортикоидов надпочечниками или возникает при введении синтетических аналогов кортикостероидов, применяемых для лечения ревматологических, аллергических, гематологических, глазных болезней, заболеваний кожи, желудочно-кишечного тракта (ЖКТ), почек, печени. Стероидный остеопороз возникает при заболеваниях, характеризующихся повышенной секрецией кортикостероидов надпочечниками (Иценко-Кушинга).
Биохимические маркеры костного метаболизма
Их исследуют для оценки скорости протекания процессов костного ремоделирования и диагностики остеопороза с высоким или низким темпом костного обмена, разобщённости или дисбаланса его составляющих: костной резорбции и костеобразования. Разделение показателей на маркеры образования и резорбции кости является условным. Совместно они отражают итоговые изменения резорбции и костеобразования, направленные в ту или иную сторону.
Наиболее точными маркерами костного образования в настоящее время признают исследование содержания остеокальцина, коллагена 1 типа, остеопротегерина (OPG), Интерлейкина 17 в крови.
Исследование маркеров костного ремоделирования целесообразно для:
1. Динамической оценки костного метаболизма;
2. Прогноза потери костной массы (вторичная профилактика при выявленной остеопении);
3. Прогноза перелома костей;
4. Отбора пациентов для проведения терапии;
5. Быстрого мониторинга терапии.
Процесс костного ремоделирования регулируется многими системными гормонами, цитокинами, факторами роста, идентифицированы многие локальные факторы костного ремоделирования. При изучении ОП важна оценка параметров минерального кальций-фосфор-магниевого обмена (уровень общего и ионизированного кальция, фосфора, магния, меди, цинка, витаминов С и К), которые вовлечены в процесс костеобразования.
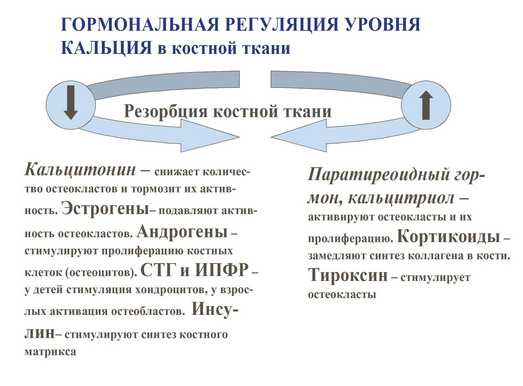
Гормональная регуляция уровня кальция в кости.
— паратиреоидный гормон – стимулирует резорбцию кости опосредованно воздействуя на остеокласты;
— кальцитонин – снижает количество остеокластов и тормозит их активность;
— эстрогены – подавляют активность остеокластов;
— андрогены – стимулируют пролиферацию остеоцитов и усиливают процессы костного синтеза;
— гормон роста и инсулинподобный фактор роста 1 (соматомедин-С) – активируют процесс синтеза кости за счёт стимуляции остеобластов;
— инсулин – стимулирует синтез костного матрикса;
— тироксин – стимулирует остеокласты, усиливая резорбцию костной ткани;
— кортикостероиды – замедляют синтез коллагена в костной ткани;
Из вышеперечисленного следует, что изучение уровня этих гормонов и маркеров костного ремоделирования на ранней стадии развития остеопении, особенно при вторичном ОП, позволит спрогнозировать и оценить вероятность дальнейшей резорбции костной ткани, провести профилактику ОП, назначить лечение.
Алгоритм лабораторной оценки костного ремоделирования.
Диагностика остеопороза
Описание
Остеопороз – это системное заболевание опорно-двигательного аппарата. Оно широко распространено во всем мире, и наша страна не является исключением. Заболевание характеризуется повышенным риском переломов по причине хрупкости костной ткани, снижения ее массы и плотности. Женщины подвержены остеопорозу больше, чем мужчины. К факторам риска также относится гормональный дисбаланс, низкий вес, прием некоторых лекарственных средств, курение, недостаточная или избыточная физическая активность, ранняя менопауза, злоупотребление алкоголем и кофе.
Данный комплекс исследований направлен на оценку костной резорбции и процесса костеобразования. Его результаты дают возможность выявить заболевание на ранней стадии и контролировать ход его лечения. В ходе ежегодного профилактического обследования комплекс рекомендован пациентам, состоящим в группе риска.
Бета-CrossLaps – это белковый фрагмент, который служит маркером резорбции костной ткани.
Кальций является одним из самых важных для организма минералов. Анализ используется для диагностики ряда патологических процессов, связанных с костной тканью, предварительной оценки кальциевого обмена.
P1NP – это основной показатель активности формирования костной ткани. Причиной повышения его уровня может быть, как остеопороз, так и ряд других заболеваний
Остеокальцин является маркером метаболизма костной ткани. Исследование позволяет оценить риск развития остеопороза.
Фосфор – это жизненно важный для человека микроэлемент, который участвует в формировании костной ткани.
Повышенная активность щелочной фосфатазы характерна для заболеваний, которые сопровождаются поражением костей.
Также в программу включены гормональные исследования.
β-сross laps (венозная кровь) в Москве
Бета-Crosslaps представляет собой маркер разрушения костной ткани. Данный белок является продуктом распада коллагена I типа, составляющего основу костной ткани.
Приём и исследование биоматериала
Когда нужно сдавать анализ β-сross laps?
Подробное описание исследования
В организме непрерывно происходят процессы разрушения (резорбции) костной ткани с помощью клеток-остеобластов и ее восстановления другими клетками — остеокластами. Совокупность этих процессов обозначают как ремоделирование кости. Обычно распад старых участков костной ткани уравновешен образованием новых.
Баланс образования/разрушения костной ткани регулируется гормонами, а также метаболическим процессамис участием кальция. В ремоделировании кости важную роль играют гормоны гипофизарной системы, щитовидной и паращитовидных желез, а также половых желез и надпочечников. Усиление процессов резорбции вызывает прогрессирующее снижение плотности костей — остеопению, наблюдается развитие остеопороза.
Остеопороз является наиболее распространенным заболеванием костей и характеризуется низкой костной массой, разрушением костной микроструктуры и повышенной хрупкостью костей.
Эта патология более распространена среди женщин в постменопаузальный период и связана с дефицитом гормонов эстрогенов, однако встречается и среди мужчин. Остеопороз также наблюдается у людей, длительно принимающих препараты, снижающие плотность костей (например, глюкокортикостероиды).
Остеопороз относится к числу осложнений, которые становятся все более распространенными с увеличением количества пациентов после трансплантации органов. Остеопороз, связанный с трансплантацией, является многофакторным и включает изменение костного метаболизма в предтрансплантационный период, посттрансплантационную потерю костной массы, вызванную иммуносупрессивной терапией и кортикостероидами, стойкий гиперпаратиреоз (у людей, имеющих почечный трансплантат) и дефицит витамина D.
Применение глюкокортикоидов, особенно в высоких дозах, приводит к снижению плотности костной ткани, раннему апоптозу (гибели) остеобластов, снижению скорости костеобразования и длительному времени задержки минерализации.
Вторичный гиперпаратиреоз является частым осложнением почечной недостаточности и чаще всего встречается у пациентов, находящихся на гемодиализе с метаболическими, сосудистыми, эндокринными и костными осложнениями. У пациентов, страдающих этим заболеванием, также развивается остеопороз.
Для лечения остеопороза применяют половые гормоны и бисфосфонаты. Терапия способствует замедлению или предотвращению потери костной массы. Для оценки эффективности лечения применяют как инструментальные методы (денситометрию), так и лабораторные тестирования.
Остеобласты синтезируют коллаген 1 типа — основу (90%) матрикса, или органической составляющей кости. Коллаген первого типа представляет собой специфический белок. В ходе разрушения костной ткани он распадается с отделением концевых фрагментов, содержащих в основе азот (N) или углерод (С). В составе С-фрагмента (С-телопептида) существует аспаргиновая кислота в альфа-форме, которая затем посредством химических реакций превращается в бета-форму. Другое название этой молекулы — Бета-Crosslaps, она служит маркером разрушения коллагена первого типа.
Увеличение содержания Бета-Crosslaps указывает на ускорение процессов разрушения кости, их преобладание над восстановлением костного матрикса. Подобная ситуация наиболее часто встречается при остеопорозе, но также может сопровождать патологию щитовидной и паращитовидных желез, онкологические и гематологические заболевания.
Определение уровня маркера Бета-Crosslaps дает информацию об уровне распада костной ткани, а также косвенно может указывать на тяжесть остеопороза. Снижение уровня Бета-Crosslaps отмечаются обычно спустя 3 месяца от начала лечения. Результаты анализа необходимо сопоставлять с результатами клинико-лабораторных и инструментальных данных.
Остеопороз (венозная кровь выделение днк) в Москве
Что входит в комплекс
Приём и исследование биоматериала
Подробное описание исследования
Остеопороз – одно из часто встречающихся заболеваний костной системы. Характеризуется прогрессирующим снижением массы и минеральной плотности костной ткани, а также и нарушением ее микроархитектоники. Последствие этих изменений проявляются в виде частых переломов костей, чаще всего страдают кости бедра, предплечья и позвонков. У женщин остеопороз протекает тяжелее, чем у мужчин. Из признаков остеопороза можно отметить уменьшение роста, «округление» спины, «выступающий» живот, боли в спине, связанные с неловкими движениями или с поднятием тяжестей, утомляемость и ноющие боли в спине после вынужденного пребывания в одном положении или ходьбы. Среди факторов риска развития остеопороза значительное влияние оказывает генетическая предрасположенность.
Что ещё назначают с этим исследованием?
Подготовка к исследованию
Специальной подготовки к исследованию не требуется. Необходимо следовать общим правилам подготовки к исследованиям.
ОБЩИЕ ПРАВИЛА ПОДГОТОВКИ К ИССЛЕДОВАНИЯМ:
Кровь рекомендуется сдавать утром, в период с 8 до 11 часов, натощак (между последним приемом пищи и взятием крови должно пройти не менее 8-ми часов, воду можно пить в обычном режиме), накануне исследования легкий ужин с ограничением приема жирной пищи.
Накануне исследования (в течение 24 часов) исключить алкоголь, интенсивные физические нагрузки, прием лекарственных препаратов (по согласованию с врачом).
За 1-2 часа до сдачи крови воздержаться от курения, не употреблять сок, чай, кофе, можно пить негазированную воду. Исключить физическое напряжение (бег, быстрый подъем по лестнице), эмоциональное возбуждение. За 15 минут до сдачи крови рекомендуется отдохнуть, успокоиться.
Не следует сдавать кровь для лабораторного исследования сразу после физиотерапевтических процедур, инструментального обследования, рентгенологического и ультразвукового исследований, массажа и других медицинских процедур.
Университет
Как восстановить костную плотность? Когда нужно проходить денситометрию? На эти и другие вопросы читателей во время прямой линии в пресс-центре ответил сепциалист.
Как восстановить костную плотность? Когда нужно проходить денситометрию? На эти и другие вопросы читателей во время прямой линии в пресс-центре ответила главный внештатный ревматолог Минздрава РБ, доцент кафедры кардиологии и внутренних болезней БГМУ, кандидат медицинских наук Наталья МАРТУСЕВИЧ.
— Для выбора правильной тактики вашего лечения необходимо удостовериться, что у вас именно остеопороз. Для этого необходимо оценить исходное состояние МПК методом двухэнергетической рентгеновской абсорбциометрии (денситометрии). Направление на это исследование при наличии показаний осуществляет врач. В случае если есть характерные для остеопороза изменения на рентгенограмме (переломы позвонков), значительное снижение роста, проведение денситометрии для постановки диагноза и выбора правильного лечения необязательно. Эффективность лечения остеопороза определяет врач по степени прироста МПК за год методом двухэнергетической рентгеновской абсорбциометрии. Прием препаратов кальция и витамина D в случае приема глюкокортикоидных гормонов обязателен, поскольку снижает риск потери костной массы, которая развивается на фоне приема гормональных лекарственных средств. В ряде случаев приема препаратов кальция и витамина D может быть недостаточно, тогда в схему лечения включают дополнительные лекарственные средства (определяет врач).
Оксана Валерьевна Азанович, РООБРЗ «Дорога к жизни»
‘Аргументы и факты’ в Беларуси № 06, 07 февраля 2017