маркировка прямой и обратный акцепт в чем разница
О «Маркировке» из первых рук: приемка и отпуск товара в аптеке
Текстовая версия вебинара для работников аптек — специалист Оператора «ЦРПТ» Анатолий Свечин рассказал о том, как работать с маркировкой лекарств
16 октября на сайте «Катрен-Стиль» состоялся вебинар на тему «Автоматизированное рабочее место в аптеке («Маркировка»): приемка и отпуск ЛС», запись которого можно посмотреть здесь. Для тех, кто по каким‑то причинам не успел принять участие в трансляции и не имеет возможности тратить время на просмотр видео, мы представляем краткое содержание самых важных моментов вебинара по правилам приемки товара в аптеке в системе МДЛП. Обязательная маркировка лекарственных препаратов стартует 1 января. В системе маркировки нужно регистрироваться уже сейчас, потому что реализация ЛС без внесения данных в базу МДЛП с Нового года станет нелегальной. Также маркировка скоро станет лицензионным требованием для аптек и производителей лекарств. Координатор проекта по регистрации выбытия Оператора «ЦРПТ» Анатолий Свечин рассказал читателям онлайн-журнала «Катрен-Стиль» о том, как работает система МДЛП, и ответил на ряд их вопросов.
Основные принципы регистрации действий с ЛС в системе
Сейчас в системе МДЛП присутствует в общей сложности 69 различных видов документов. 46 из них участники отправляют в систему, а получают только 23. При этом только три документа отправляются с помощью специальных устройств — касс и регистраторов выбытия. Вся остальная информация заносится в систему с помощью квалифицированной подписи. Это первый основной момент: организации нужна электронная квалифицированная подпись, хотя бы для того, чтобы зарегистрироваться в системе.
Существует 2 способа внесения информации о принятом товаре в систему МДЛП — программный и аппаратный.
Программный способ — это оформление документов на поступивший товар в аптеку через личный кабинет, который представляет собой простой сайт, в котором можно работать через браузер или интерфейс установленного в аптеке программного обеспечения, например, того, при помощи которого ведется весь учет ЛС (правда, его нужно будет доработать).
Аппаратный способ — это кассовая техника и регистратор выбытия. Стоит отметить, что никаких новых сканеров для приемки товара покупать не нужно. Только доработать программное обеспечение кассовой техники.

Приемка товара в аптеке
Начнем с правил приема лекарственных средств. Отгрузки могут проходить по прямому или обратному акцепту. Акцепт — это ответ о принятии оферты.
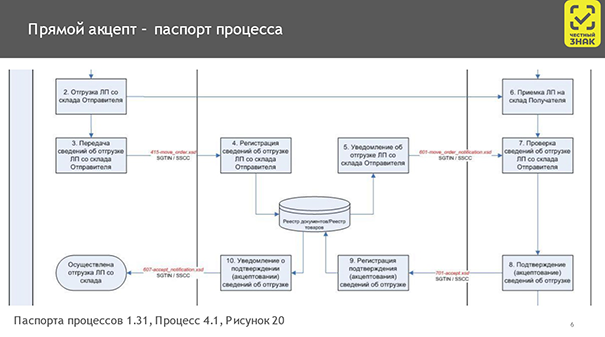
Отгрузка по прямому акцепту выполняется так: поставщик собирает заказ и отправляет в систему сообщение с полным перечнем того, что он отправил. Это могут быть агрегационные коды производителя или же коды, сгенерированные самим поставщиком. Т. е. в системе можно указать не полный перечень вторичных упаковок, а один код на весь заказ. Или несколько, в зависимости от объема.
Затем получателю приходит уведомление, что ему отгружен товар. Из уведомления копируются коды и отправляются в систему — это сигнал того, что товар принят. На схеме красным указаны коды номеров сообщения о приеме товара на складе аптеки или отправке.
После проверки товара аптеке нужно просканировать все упаковки и сравнить их со списком кодов, которые были получены от поставщика. Таким образом вы убедитесь, что вам доставлено именно то, что вы заказывали, и именно то, что отправил поставщик. Если что‑то не совпадает, то вы вправе отказаться от приемки такого товара и оформить возврат.
Нюансы приемки и проверки кодов маркировки нужно прописать с поставщиком лекарственных средств. Чтобы у вас было юридическое право вернуть товар, а у поставщика было юридическое право его принять, если при сравнении кодов маркировки вышли какие‑то неточности. Прямой акцепт защищает от пересортицы, потому что товар проверяется дважды: на стороне отправителя и на стороне получателя.
На иллюстрации ниже показано, как такие данные выглядят в «голом виде» в системе.

«Чтобы такие тексты не писать самому, как раз и нужно доработать программное обеспечение, где вы ведете учет поступления товаров в аптеку. Оно будет преобразовывать ваши данные в этот формат и отправлять их в систему МДЛП. По закону, если вы подписываете какой‑то текст электронной подписью, то программа должна дать вам возможность ознакомиться с этим текстом. Поэтому здесь и приведена такая сложная на первый взгляд таблица. Чтобы вы не пугались и знали, как это выглядит», — рассказал Анатолий Свечин.
Личный кабинет
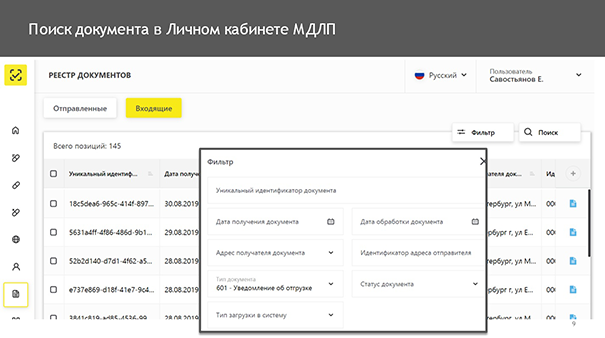
По словам представителя «ЦРПТ», найти все сопроводительные документы на лекарственные препараты на адрес аптеки очень просто. Нужно зайти в реестр документов, выбрать «Входящие» и нажать «фильтр». В фильтре указать, что вам нужен документ «601».
Обратный акцепт
Этот порядок учета поступления товаров в аптеку сложнее, чем прямая приемка.
Отправитель посылает груз, формирует ТТН, но никакие данные в систему не отправляет. Получатель тщательно проверяет товар и вносит информацию в МДЛП. После этого отправитель получает уведомление, что прием товара прошел, и соглашается со списком поставленной продукции (или не соглашается, если данные не совпадают).
Схема не защищена от пересортицы, потому что товар проверяется только один раз. Но в этом случае требуется меньше затрат (действий) от отправителя. Для использования обратного акцепта отправитель (поставщик) должен добавить получателя в «Доверенные контрагенты» в личном кабинете системы. Тогда получатель сможет делать сообщения об обратном акцепте.
Статус кода маркировки
Каждый раз, когда вы отправляете сообщение в систему любым способом, меняется статус препарата в системе. Это может быть статус «Отгружен», «Вошел в оборот» и так далее.
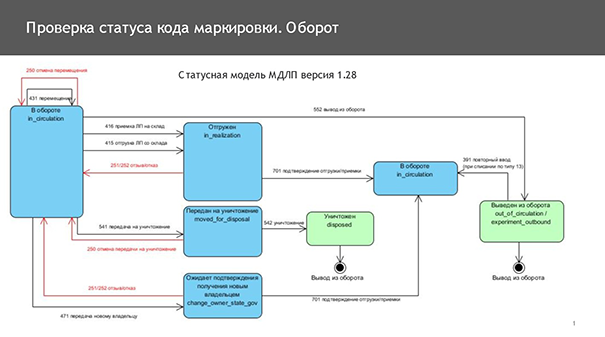
В любой момент вы сами можете узнать статус препаратов, которые вам отгружены или которые есть у вас на складе, зайдя в личный кабинет, или с помощью доработанного программного обеспечения. «Стоит сказать, что работа в личном кабинете не рекомендуется тем аптекам, у кого оборот более 10 упаковок в день. Программное обеспечение делает это всё быстрее. Всё это вначале выглядит сложно и не очень понятно. Здесь главное тестировать и снова и снова практиковаться. Как мы замеряли, приемка немаркированного товара занимает 20 минут, а у специалиста со внесением всех данных промаркированные товары принимаются за 25 минут», — уверил Анатолий Свечин.
Отказ от приемки
Отметим, что это отдельная процедура. Это — не возврат. Потому что возврат — это отгрузка по прямому акцепту, просто «в другую сторону». Ниже приведена схема оформления отказа от приемки товара.
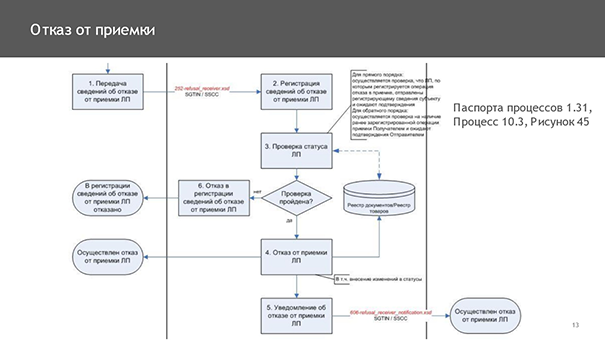
Другие варианты отказа от приемки:
Как уточнил представитель «ЦРПТ», существуют схемы взаимодействия поставщиков и аптек, при которых перепродажа товара происходит через «логистического оператора», но отгрузок по факту не происходит. Т. е. условный контрагент 1 продает условному контрагенту 2, а тот уже продает в аптеку. При этом товар остается на общем складе. В таком случае поставка оформляется от контрагента 1 в аптеку, а не от контрагента 2 в аптеку. Напомним, что в системе отражается не право собственности, а ответственность за сохранность товара.
Вывод ЛС из оборота в розницу и по льготе
Вывод ЛС из оборота происходит при помощи специальных устройств. В первую очередь это кассы.
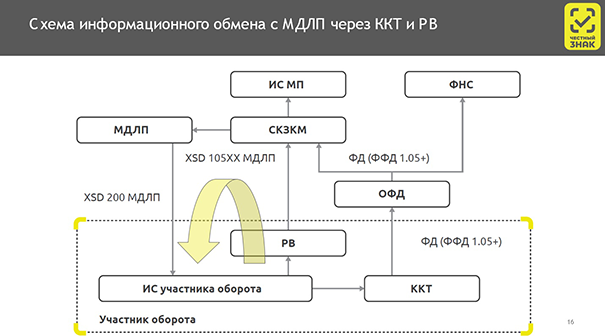
Небольшое пояснение к иллюстрации: ОФД — оператор фискальных данных. Он отправляет информацию в ФНС и на серверы криптографической защиты кодов маркировки (СКЗКМ). Оттуда информация идет в саму систему МДЛП.
Отметим, что касса не получает обратного «ответа». Удалось или не удалось вывести препарат из оборота — нужно смотреть в личном кабинете или доработанном программном обеспечении. В среднем такая операция должна занимать не более 5 секунд.
Для льготных аптек, которые занимаются 100 %-ной льготой и не используют кассовую технику, будут выданы регистраторы выбытия. Выглядят они вот так:

Прочих аптек (тем, у кого льготный отпуск не является основной и единственной сферой деятельности) законодательство пока не обязывает предоставлять регистраторы выбытия. Однако, возможно, в будущем оператор системы по собственной инициативе обеспечит регистраторами все аптеки, занимающиеся льготным отпуском, для «подстраховки». Это решение пока находится в стадии обсуждения.
По словам Анатолия Свечина, крупные производители программ, такие как «1С», «Асулон» и другие, уже представили доработанное программное обеспечение, способное работать с системой МДЛП. Также на рынке присутствует множество собственных наработок аптек для программного обеспечения касс. Вся необходимая информация о ПО есть на сайте «Честный знак».
Вывод из оборота по различным причинам
Далее мы поговорим о выводе лекарственного препарата из оборота не через реализацию, а по иным причинам. Такой вывод оформляется не через кассы или регистратор выбытия, а программным методом (через личный кабинет или доработанное аптечное ПО).
Таким образом следует оформлять уничтожение препарата, отгрузку на незарегистрированное место действия или вывод из оборота по прочим причинам:
Памятка действий
Также в ходе вебинара Анатолий Свечин представил пошаговую инструкцию по внедрению маркировки лекарств в аптечной организации. Обратите внимание, что памятка носит общий характер, поэтому порядок действий может немного отличаться в зависимости от вида деятельности. Итак, аптеке необходимо (в хронологическом порядке):
Ответы на вопросы
В конце вебинара Анатолий Свечин дал ответы на самые частые вопросы, направляемые в адрес Оператора системы. Ответы на вопросы, заданные участниками в ходе вебинара, будут опубликованы в виде отдельной статьи — следите за обновлениями в разделе «Маркировка».
Сколько регистраторов выбытия необходимо на каждое место деятельности (МД)?
Отметим, что не все МД должны быть оснащены регистраторами. Подробнее см. «Способы вывода из оборота ЛП по типам участников оборота» в библиотеке документов по маркировке на сайте Росздравнадзора. Для тех организаций, где требуется оснащение, действует принцип: 1 место деятельности = 1 регистратор выбытия (РВ). Если льготная аптека и медицинская организация располагаются по одному адресу, устанавливается 1 РВ в аптеку и 1 РВ в медицинскую организацию.
Как протестировать выбытие в «Песочнице» МДЛП?
Для тестирования бизнес-процессов выбытия в «Песочнице» МДЛП используйте личный кабинет МДЛП или API МДЛП. Использовать РВ при этом нет необходимости, так как при его использовании меняется лишь способ передачи информации и добавляются дополнительные проверки, суть процесса не изменяется. Для тестирования выбытия на промышленном контуре МДЛП с использованием РВ предусмотрена функция «Тестовое выбытие». Вы также можете протестировать использование РВ на кодах маркировки, выпущенных в рамках эксперимента, а также на упаковках уже отгруженных вам, но еще не акцептованных вашей организацией.
Не тестируйте РВ на упаковках ЛП, уже выведенных вами из оборота, это будет расценено системой как попытка использования фальсифицированных ЛП.
Когда можно получить РВ?
Установка РВ для отпуска препаратов из программы высокозатратных нозологий сейчас завершается. Анкеты на получение РВ другим участникам оборота станут доступны в октябре 2019 года.
Не удается долгое время поймать сигнал ГЛОНАСС, как решить данную проблему?
В сентябре вышла новая прошивка, улучшающая качество приема. Второй вариант — использовать усилитель ГЛОНАСС.
Если несколько окон для отпуска ЛП, сколько РВ необходимо?
1 регистратор выбытия на 1 место деятельности.
Сроки поставки РВ после подписания договора?
По Постановлению правительства № 1557 от 14.12.2019 — в течение 30 календарных дней.
Как понять, нужен ли РВ нашей организации?
Из документа «Способы вывода из оборота ЛП по типам участников оборота» в библиотеке документов по маркировке на сайте РЗН.
Когда появится возможность заполнить анкеты не ВЗН?
В октябре 2019 года.
Необходима ли установка дополнительных программ?
Для работы с ЛК МДЛП нужен бесплатный плагин для браузера. Остальное определяет разработчик ТУС (телематических услуг связи).
Нужно ли приобретать дополнительно сканеры для РВ? Если нужно, то в каком количестве?
Сканеры нужны только в сетевом (пассивном) режиме работы РВ. Количество — по числу рабочих мест. Это не связано в РВ, но как минимум 1 сканер нужен на приемке товара.
От редакции: Видеозапись описанного выше вебинара можно посмотреть по этой ссылке. Также приглашаем вас регистрироваться на другие вебинары цикла, которые состоятся 13 ноября и 11 декабря. Напоминаем, что вебинары бесплатные, а количество мест ограниченно.
Быстро разобраться в тонкостях системы МДЛП неподготовленному человеку не так‑то просто — отправляйте свои уточняющие вопросы на адрес volkovmv@katren.ru, и мы постараемся задать их лектору вебинаров заранее, чтобы он смог подготовить ответы.
Также не забывайте заходить в специальный раздел нашего сайта, посвященный маркировке лекарственных средств в аптеке. Здесь мы публикуем все самые свежие новости по теме.
Маркировка прямой и обратный акцепт в чем разница
4.1. Прямая и обратные схемы акцептования
В рамках гражданско-правовых отношений между контрагентами допускается использование одного из следующих вариантов поставки лекарственных препаратов:
1. Прямой порядок акцептования, при котором в ФГИС МДЛП отправителем регистрируются сведения об отгрузке покупателю лекарственных препаратов, а получателем осуществляется подтверждение в ФГИС МДЛП зарегистрированных отправителем сведений об отгрузке лекарственных препаратов.
2. Обратный порядок акцептования, при котором в ФГИС МДЛП получателем регистрируются сведения о приемке лекарственных препаратов на склад, а отправителем осуществляется подтверждение сведений о приемке на склад покупателя.
Регистрация в ФГИС МДЛП сведений о приемке лекарственных препаратов может осуществляться как вручную, так и с использованием товарно-учетных систем участников, интегрированных с ФГИС МДЛП.
Субъект обращения лекарственных средств, осуществляющий приемку лекарственных препаратов от другого субъекта обращения лекарственных средств в рамках гражданско-правовых отношений, в течение 1 рабочего дня с даты приемки лекарственных препаратов и регистрации в системе мониторинга сведений об отгруженных лекарственных препаратах до представления сведений о дальнейших операциях с такими лекарственными препаратами подтверждает достоверность сведений, содержащихся в системе мониторинга, путем представления сведений в систему мониторинга.
Обязательность передачи сведений по обороту маркированных лекарственных средств в ФГИС МДЛП для случаев прямого порядка приемки лекарственных средств в установленный срок действующими нормативноправовыми актами в 1 день начинает отсчет с момента выполнения двух условий:
— даты подписания актов приема передачи товара между грузоотправителем и получателем лекарственных средств.
— поступление входящего уведомления от грузоотправителя о факте совершенной отгрузки в адрес грузополучателя
В случае выбора обратного порядка представления сведений при обороте лекарственных препаратов субъект обращения лекарственных средств, осуществляющий приемку лекарственных препаратов от другого субъекта обращения лекарственных средств в рамках гражданско-правовых отношений, в течение рабочего дня с даты приемки лекарственных препаратов представляет в систему мониторинга сведения о принятых лекарственных препаратах.
Обязательность передачи сведений по обороту маркированных лекарственных средств в ФГИС МДЛП для случаев обратного порядка приемки лекарственных средств в установленный срок действующими нормативно-правовыми актами в 1 день начинает отсчет с даты подписания актов приема передачи товара между грузоотправителем и получателем лекарственных средств.
Субъектами обращения лекарственных средств ФГИС МДЛП при внесении корректной информации в части источника финансирования в случаях выполнении операций отгрузки и приемки лекарственных средств необходимо руководствоваться следующими правилами:
— Указание вида источника «1» для случаев закупки лекарственных препаратов за собственные средства включает в том числе закупку лекарственных средств в рамках: обязательного медицинского страхования, федерального фонда обязательного медицинского страхования, родовые сертификаты.
— Указание вида источника «2» для случаев поставки лекарственных препаратов за счет средств федерального бюджета
— Указание вида источника «3» для случаев поставки лекарственных препаратов за счет средств регионального бюджета
1. Отсканировать поступившие вторичные или третичные упаковки (в случае, если вторичные упаковки вложены в третичную), при помощи 2D сканера или терминала сбора данных. В случае отсутствия сканера следует внести вручную человеко-читаемую информацию о SGTIN и серийном номере, нанесенных на упаковку лекарственного препарата и\или SSCC, нанесенный на короб или паллету, в xml-документ, и затем загрузить его в ФГИС МДЛП с использованием Личного кабинета участника оборота.
3. При отсутствии расхождений и претензий к поставленному товару, осуществить приемку лекарственных препаратов и зарегистрировать в ФГИС МДЛП сведения о принятом товаре, используя для передачи информации документ в формате xml, с помощью Личного кабинета участника оборота (схема 701 логической модели файлов обмена ФГИС МДЛП). В xml-документе необходимо указать идентификаторы мест деятельности отправителя и получателя, а также отсканированные коды SGTIN или SSCC, согласно пункту 1.
При обратном порядке акцептования получателю лекарственных препаратов в случае отсутствия ТУС необходимо:
1. Отсканировать поступившие вторичные или третичные упаковки (в случае, если вторичные упаковки вложены в третичную), при помощи 2D сканера или терминала сбора данных. В случае отсутствия сканера следует внести вручную человеко-читаемую информацию о SGTIN и серийном номере, нанесенных на упаковку лекарственного препарата и\или SSCC, нанесенный на короб или паллету, в xml-документ, и затем загрузить его в ФГИС МДЛП с использованием Личного кабинета участника оборота.
2. Пройти авторизацию в Личном кабинете участника оборота, перейти в раздел «Реестр документов» и осуществить загрузку xml-документа, содержащего сведения о SGTIN поступивших упаковок лекарственных препаратов и\или SSCC (схема 416 логической модели файлов обмена ФГИС МДЛП).
3. Дождаться от поставщика лекарственных препаратов уведомления, подтверждающего факт отгрузки лекарственных препаратов (схема 607 логической модели файлов обмена ФГИС МДЛП).
При обратном порядке акцептования грузополучатель должен быть добавлен грузоотправителем в реестр доверенных контрагентов.
При наличии товарно-учетной системы, интегрированной с ФГИС МДЛП, для выполнения операций акцептования лекарственных препаратов необходимо обратиться к руководству пользователя системы, разработанному поставщиком ИТ-услуг для субъекта обращения лекарственных средств.
В рамках оборота лекарственных препаратов между контрагентами допускается отмена следующих операций:
Для удобства пользования в ФГИС МДЛП предусмотрена возможность регистрации сведений о частичном приеме лекарственных препаратов. Для этого получателю необходимо отразить в соответствующих полях «SSCC» или «SGTIN» xml-документа только те сведения, которые соответствуют фактически принятым упаковкам лекарственных препаратов (схема 701 логической модели файлов обмена ФГИС МДЛП).
Например, в случае получения от поставщика xml-документа с указанием кодов SSCC для короба N 1 и короба N 2 (схема 415 логической модели файлов обмена ФГИС МДЛП), получатель в ответ может сформировать xml-документ, содержащий информацию о приемке короба N 1 и отказе от приемки короба N 2 (схема 252 логической модели файлов обмена ФГИС МДЛП).
Также допускаются варианты регистрации в ФГИС МДЛП сведений о частичном отказе от приемки упаковок лекарственных препаратов, в том случае если в составе поставки получены лекарственные препараты, агрегированные в короб, и лекарственные препараты, в отношение которых агрегация не применялась. В данном случае участник оборота также вправе сформировать отказ от приема части неагрегированных лекарственных препаратов, сформировав и отправив в ФГИС МДЛП соответствующий xml-документ.
Допускаются сценарии отгрузки лекарственных препаратов от поставщика получателю, при которой покупателем выступает третья сторона (т.е. данной организации (ИП) переходит право собственности). В данном случае в ФГИС МДЛП регистрируется только операция передачи от поставщика фактическому грузополучателю лекарственных препаратов. Операция передачи права собственности от грузополучателя к юридическому владельцу при этом не регистрируется.
Регистрация в ФГИС МДЛП сведений об акцептовании лекарственных препаратов осуществляется в соответствии с регламентными сроками, определенными постановлением Правительства РФ от 14 декабря 2018 г. N 1556 «Об утверждении Положения о системе мониторинга движения лекарственных препаратов для медицинского применения». Регистрация сведений об акцептовании поставки должна осуществляться субъектом обращения вне зависимости от текущего статуса подписания сопроводительных финансовых документов поставки (товарные накладные, универсальные передаточные документы) субъектами обращения лекарственных средств.
В ФГИС МДЛП фиксируется фактическая стоимость единицы потребительской упаковки лекарственного препарата, которая должна соответствовать стоимости единицы потребительской упаковки лекарственного препарата, отраженной в сопроводительной документации. При этом, ряд субъектов обращения лекарственных средств рассчитывает стоимость единицы по формуле «Общая стоимость партии с НДС / количество» с округлением до полной копейки по правилу «к ближайшему целому», что при обратном пересчете (стоимость единицы потребительской упаковки * количество) вызывает различие общей стоимости партии и общей суммы НДС приведенных поставщиком в сопроводительной документации на незначительную математическую погрешность, возникающую в связи с округлением суммы.
Также допускаются случаи, когда в ФГИС МДЛП указываются фактические стоимости единицы потребительской упаковки согласно накладной, однако указанная сумма всех цен потребительских упаковок получается меньше, чем стоимость государственного контракта менее чем на стоимость одной потребительской упаковки. В этом случае поставщиком в товарной накладной указывается, что «излишек» данной упаковки поставляется за счет средств грузоотправителя.
Необходимо обратить внимание, что указанные расхождения не являются основанием для отказа грузополучателя в приемке лекарственных препаратов к учету на основании данных, отраженных в сопроводительных документах.
Маркировка лекарств в аптеке
Впервые слово «маркировка» прозвучало и обрело свой вес для фармации еще в 2015 году. Для работников отрасли это было чем-то неизвестным и пугающим — из-за отсутствия понимания зачем, как и с помощью каких инструментов она будет реализовываться.
Чтобы разобраться, откуда появилась мысль о введении системы маркировки лекарственных препаратов, нужно начать разобраться с целями проекта.
Какими бывают некачественные лекарственные препараты?
Согласно статье 4 Федерального закона от 12.04.2010 № 61 «Об обращении лекарственных средств» предлагаются следующие определения некачественных лекарственных препаратов:
Такая продукция — фальсифицированная и контрафактная — не проходит надлежащий контроль при ее производстве и реализации. Подобные препараты могут иметь опасный для здоровья состав, в них может отсутствовать активный компонент. В случае, если они соответствуют по качеству оригинальным препаратам, их производство и распространение осуществляется без надзора соответствующих органов — а это противоречит законодательству.
Чтобы защитить свои препараты от подделки, производители используют ряд предупредительных мер: защитные голограммы, изменение упаковки, объемная печать, использование специфических шрифтов и идентификационных знаков, оригинальной формы таблетки и надписей на них, гравировка на стекле ампул.
Но этого оказывается недостаточно.
Когда и как все началось?
4 февраля 2015 года на совещании президента Российской Федерации Владимира Путина с членами Правительства было объявлено о решении создать федеральную государственную информационную систему мониторинга движения лекарственных препаратов от производителя до конечного потребителя с использованием маркировки.
Поручением президента №Пр-285 от 20 февраля 2015 года было поручено обеспечить разработку и поэтапное внедрение этой системы.
Планировались следующие этапы:
По факту получилось следующее:
Зачем нужна система маркировки отрасли?
Целями системы маркировки в фармацевтической отрасли являются противодействие незаконному производству, ввозу, обороту лекарственных препаратов на территории РФ, а также стандартизация и унификация процедур учета поставок и распределения лекарственных препаратов (в том числе закупаемых для государственных нужд).
Каждый сектор заинтересован во введении маркировки. Почему?
Введение системы мониторинга несет в себе выгоды для каждого участника.
За счет этой системы государство усилит контроль за налоговыми платежами, а также за рынком сбыта (это защитит от повторной продажи лекарственных средств и нелегального сбыта). За счет снижения доли контрафактной продукции прогнозируется увеличение ВВП.
Для производителей и импортеров система мониторинга позволит эффективнее управлять логистикой, упростить планирование производства, снизить конкуренцию со стороны производителей подделок и контрафакта,
Аптеки получат свою выгоду в защите от поступления фальсифицированной или «просроченной» продукции; в снижении пересортицы товара и четком отслеживании его сроков годности; отсутствии сбоев со штрих-кодированием.
Конечному потребителю — клиенту — система мониторинга дает возможность с помощью своего мобильного устройства проверить легальность приобретаемого лекарственного препарата, получить дополнительные гарантии, что лекарства в аптеке произведены и поставлены в продажу официально, и быть уверенным в производителе.
Кто является участниками мониторинга?
В системе мониторинга участвуют производители лекарственных препаратов (ЛП), иностранные держатели регистрационных удостоверений ЛП, представительства иностранных держателей РУ ЛП, организации оптовой торговли ЛП, организации розничной торговли ЛП, медицинские организации.
Все они так или иначе подают сведения об ЛП, участвующих в обороте.
Плюсы и минусы внедрения системы мониторинга
Внедрение обязательной маркировки лекарственных средств имеет очевидные плюсы:
Существует и ряд сложностей, связанных с нововведением: процесс внедрения технически сложен и требует финансовых вложений; может усложниться процесс приемки товара в аптеках. Несвоевременная передача информации в систему мониторинга влечет за собой штрафные санкции; может произойти вымывание нижнего ценового сегмента.
Изменение законодательства
С 1 июля 2020 вступило в силу Постановление № 687 от 15.05.2020 г. «О внесении изменений в пункт 5 Положения о лицензировании фармацевтической деятельности», в соответствии с которым внесение информации о лекарственных препаратах в систему мониторинга ЛП станет лицензионным требованием для осуществления фармацевтической деятельности.
С этого момента нарушение требований законодательства повлечет за собой штрафы:
В будущем перечень статей может расшириться: за несвоевременное внесение данных в ИС МДЛП либо внесение в нее недостоверных данных и продажу лекарственных препаратов без маркировки и (или) нанесения информации, предусмотренной законодательством РФ.
Data Matrix — что это такое?
Согласно статье 46 Федерального закона от 12.04.2010 N 61 «Об обращении лекарственных средств» на вторичную (потребительскую) упаковку лекарственного препарата наносится штриховой код.
Штрих-код — это графическая информация (последовательность полос или других геометрических фигур), которая наносится на упаковку изделий для считывания ее техническими средствами. Чаще всего используется EAN-код — линейный. Он может кодировать небольшой объем информации.
При обязательной маркировке лекарственных средств дополнительно будет использоваться код Data Matrix. Это двумерный матричный код. Выбор пал именно на него из-за его преимуществ: возможности кодирования большого количества информации, высокой степени защиты (очень низкая вероятность подделки), возможности считывать код можно при повреждении, низкой стоимости генерации одного кода.
Для работы с маркированными лекарственными препаратами необходимо использовать 2D-сканер штрих-кодов. В отличие от 1D сканеров они могут считывать двумерные коды. Такой сканер приобретается участниками оборота самостоятельно.
Информация об упаковке конкретного товара, зашифрованная в коде Data Matrix, уникальна. Считывание кода происходит на каждом этапе движения товара, вся информация поступает в систему мониторинга «Честный знак». Любой человек, отсканировав код Data Matrix в приложении «Честный знак» на своем мобильном устройстве, может отследить весь путь движения товара от производителя к конечному потребителю.
Что делать с товаром, который был произведен до внедрения системы мониторинга?
На складах производителей и аптек остался товар, который был произведен еще до внедрения системы мониторинга. На их упаковках нет кода Data Matrix. Возникает закономерный вопрос — может ли данный товар реализовываться, или это станет нарушением?
Ответ: весь товар, который был произведен или ввезен на территорию РФ до внедрения программы обязательной маркировки, легален и разрешен к обороту. Немаркированный товар может реализовываться до окончания срока его годности. Это не является нарушением.
Как может осуществляться поставка товара в аптеку?
Поставка товара в аптеку может осуществляться двумя способами.
Первый — прямой порядок акцептования («прямой акцепт»). Сведения об отгрузке товара регистрируются отправителем. Получатель подтверждает зарегистрированные в системе сведения.
Второй — обратный порядок акцептования («обратный акцепт»). Сведения об отгрузке товара регистрируются получателем. Отправитель подтверждает зарегистрированные в системе сведения.
«Прямой акцепт» более точен, так как проверка штрих-кодов производится как со стороны получателя, так и со стороны отправителя. Это уменьшает вероятность возникновения пересортицы. Но не все дистрибьюторы готовы к такой форме работы — для этого требуется дополнительные оборудование и персонал.
Поэтому «Обратный акцепт» остается самым распространенным способом взаимодействия дистрибьютора с аптечными сетями. Аптека, получив поставку, должна просканировать все упаковки товара в рамках одной накладной, сформировать документ установленного вида и отправить его в систему мониторинга движения лекарственных средств. Эта информация сверяется с данными, которые вносит дистрибьютор. Если данные совпадают — считается, что поставка состоялась. Аптека получает сообщение, что поставка принята.
С этого момента товар может поступать в продажу.
Возможные трудности приемки по «Обратному акцепту»:
Решения, которые может принять аптечная организация для облегчения внедрения системы мониторинга в работу:
Вывод лекарственных средств из оборота
Вывод из оборота ЛС — реализация, продажа и отпуск (в т.ч.по рецепту) лекарственных средств потребителю, применение, передача на уничтожение, утрата и списание ЛП, отбор образцов, вывоз ранее ввезенных в РФ ЛП или вывод по другим причинам.
В системе мониторинга реализованы следующие вида вывода ЛС из оборота:
Аптечные организации чаще всего занимаются розничной продажей. Чтобы «вывести» ЛП из оборота, в аптеке должны быть: актуальное кассовое программное обеспечение, контрольно-кассовая техника и сканер для считывания 2D-кодов.
Сведения передаются так:
Чтобы избежать ошибок при реализации товара, необходимо соблюдать следующий алгоритм действий:
Вопросы, которые могут возникнуть у сотрудника
Что делать, если упаковка продается не целиком?
В момент отпуска только части упаковки, происходит «частичное» выбытие вторичной упаковки. Она должна сохраняться до момента отпуска последней доли упаковки. Для этого необходимо ввести «долю» упаковки на кассовом ПО.
В случае обнаружения попытки осуществить вывод «излишка» система мониторинга зафиксирует нарушение!
Что делать, если покупатель отказался от покупки?
Бывает, так что покупка не состоялась (отказ по инициативе покупателя, отсутствие необходимой суммы денежных средств), а маркированный лекарственный препарат «пробит» на кассе в аптеке.
В этом случае чек не закрывается и должен быть аннулирован посредством программного обеспечения. Операция пробития чека не состоялась — информация не передалась ОФД, поэтому сведения о выбытии товара в системе мониторинга не зафиксировались.
Что делать, если поставщик не подтверждает приемку товара?
Ситуация: аптека приняла поступивший товар, а поставщик не подтвердил эти сведения в системе мониторинга.
Чтобы аптека могла отпускать полученный товар, предусмотрена функция «реестра ожиданий». Аптека может «вывести» лекарственный препарат из оборота, информация об этом серийном номере отразится в реестре ожиданий.
В течение 15 дней поставщик должен подтвердить сведения. Если сведения не будут переданы, это отразится в реестре нарушений — это повлечет разбирательства со стороны Росздравнадзора.
Вопросы, которые могут возникнуть у клиента
Почему Вы продаете немаркированный товар?
На остатках в аптеках и на складах производителей остался товара, который был произведен до запуска проекта по маркировке. По закону он может реализовываться до окончания срока годности.
Качество маркированного товара лучше, чем у немаркированного?
Нет, отличие лишь в наличии знака маркировки.
Где я могу проверить легальность маркированного товара?
В мобильном приложении «Честный знак».
Как отличить маркированный товар от немаркированного?
Маркированный товар имеет отличительный знак Data Matrix.
Почему один и тот же товар Вы продаете и как маркированный, и как немаркированный?
У данных товаров разный срок производства. Один был произведен до вступления программы маркировки, а другой уже после. Это единственное отличие.
Если на товаре нет знака Data Matrix — это подделка?
Нет, это не подделка. Данный товар был произведен до запуска программы «Маркировка».
Зачем вообще нужно маркировать товар?
Наличие знака Data Matrix дает гарантию в качестве товара. По нему Вы можете проследить весь путь от производителя до Вас в мобильном приложении «Честный знак».
Маркированный товар дороже, чем обычный? Почему цена разная?
Проект «Маркировка» не влияет на образование цены на лекарственный препарат. Все расходы на маркировку товара берут на себя производители. Эти товары из разных партий поставки, поэтому цена может отличаться.
Заключение
Введение обязательной маркировки лекарственных средств было необходимым решением для снижения доли контрафактных и поддельных лекарственных средств в обороте. Перед проектом «Маркировка» стоят масштабные цели, но их достижение обеспечит результаты, в которых заинтересованы все участники жизненного цикла препарата.
Внедрение системы мониторинга и перестройка рабочего процесса изначально могут показаться сложными и пугающими. Но стоит запастись терпением, выполнять необходимые рекомендации, и в скором времени каждый сотрудник фармацевтической отрасли сможет оценить важность этого проекта.




