морфологический вариант опухоли что это
Стадии рака: классификация онкологических заболеваний
Стадия онкологического заболевания дает информацию о том, насколько велика опухоль и распространилась ли она по организму. Это помогает врачам определять прогноз пациента и план лечения.
С помощью врача-онколога, резидента Высшей школы онкологии Сергея Югая разбираемся, как врачи устанавливают стадии рака и что каждая из них означает.
На что влияет стадия онкологического заболевания?
Стадирование нужно, чтобы спрогнозировать, какие у пациента шансы на выздоровление, а также чтобы определить, какой метод лечения будет наиболее эффективен в конкретном случае, — поясняет Сергей Югай.
Все начинается с медицинского осмотра и обследований — УЗИ, КТ, МРТ, ПЭТ-КТ и других методов в зависимости от вида рака. Затем врач берет кусочек опухоли — биопсию или удаляет опухоль целиком во время операции, а после отправляет материал на гистологический анализ, чтобы поставить диагноз.
Стадии рака по TNM-классификации
Стадии онкологического процесса описывают разными способами — это зависит от вида опухоли. Один из самых распространенных способов — стадирование с помощью TNM-классификации.
Т характеризует первичную опухоль, ее размеры и вовлечение окружающих структур в опухолевый рост, например, прорастание в стенку кишки или желудка. N говорит о наличии в лимфоузлах метастазов и количестве пораженных лимфоузлов, а М — о наличии отдаленных метастазов (во внутренних органах, костях, ЦНС или лимфоузлах, которые расположены далеко от первичной опухоли), — объясняет Сергей Югай.
Индекс Т принимает значения от 0 до 4. 0 означает, что первичная опухоль не обнаружена, 1 — опухоль маленькая, а 4 — опухоль проросла в прилегающие ткани. Таким образом, чем больше цифра рядом с Т, тем ситуация сложнее. При некоторых видах рака N принимает значение 0 или 1, при других — 0, 1 или 2, а иногда — 0, 1, 2 и 3. 0 означает, что опухоль не проникла в ближайшие лимфоузлы, а 3 — что поражено множество лимфоузлов. M0 показывает, что метастазов нет, а 1 — что метастазы есть.
Онкологи выставляют стадию по TNM клинически — до операции или когда операция не планируется и патоморфологически — при изучении удаленной во время операции опухоли, — объясняет Сергей.
Клиническая стадия обозначается буквой «c», например, cT2. Патоморфологическая — буквой «p», например, pN1.
От правильной стадии зависит тактика лечения. Например, пациент — мужчина с раком желудка и стадией cT1N0M0. Это значит, что опухоль прорастает в слизистую и подслизистый слой стенки желудка. В этом случае пациенту показана операция. Если же стадия выше (cT2N1M0, например), то есть опухоль пациента прорастает в мышечный слой, и есть метастазы в лимфоузлах, то может понадобиться химиотерапия перед операцией, которая позволит улучшить результаты лечения, — добавляет Сергей.
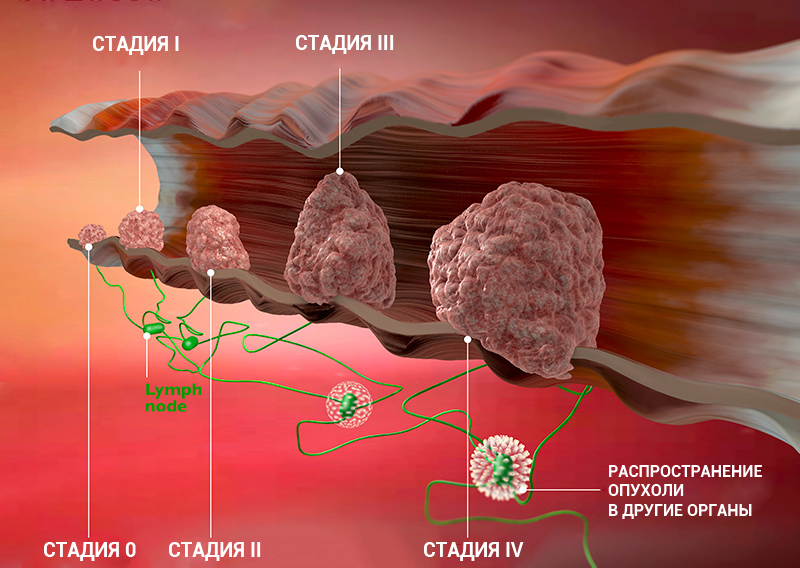
Стадию рака могут обозначать с помощью цифр — 0, I, II, III, IV. Что это значит?
Клинические стадии (0, I, II, III, IV) тесно связаны с системой TNM. Как правило, одна клиническая стадия включает в себя несколько вариантов стадирования по TNM. Эти варианты характеризуются схожими прогнозом и подходом к лечению. Например, стадии T1N3M0, T2N3M0, T3N2M0 рака легкого объединяются в IIIВ стадию, так как при любой из этих ситуаций пациент будет иметь примерно одинаковый прогноз и тактику лечения. В этом конкретном примере необходима химиолучевая терапия, а не операция, — комментирует Сергей Югай.
Меняется ли стадия после лечения, при прогрессировании заболевания?
Нет, стадия выставляется один раз. Но есть нюансы:
Например, мы хотим посмотреть, как опухоль ответила на лечение, чтобы понять, можно ли делать операцию. После лечения опухоль уменьшилась, и мы добавляем к стадии новые данные. При прогрессировании опухолевого процесса первоначальная стадия также остается прежней, но, к сожалению, прогноз будет менее благоприятный. Например, у человека II стадия рака желудка. Он прооперирован, и прогноз у него хороший. Через 2 года врачи обнаруживают у пациента метастазы в легких. Стадия остается II, но рак у пациента уже метастатический, что очень усложняет положение, — говорит Сергей.
Бывает, что люди сравнивают свою ситуацию с историями других пациентов. Если речь идет о разных онкологических заболеваниях, то такие сравнения некорректны — это заболевания с разными прогнозами и схемами лечения:
Например, с нейроэндокринным раком поджелудочной железы люди могут жить десятилетиями, а при метастатической стадии рака поджелудочной железы — полгода или год, — объясняет врач-онколог.
Что может повлиять на прогноз людей с одинаковой стадией и одним видом рака?
Сергей Югай выделяет три фактора:
Морфологическая диагностика
Морфологическая диагностика — это тип исследования, применяемый для подтверждения наличия злокачественного новообразования, выявления его этиологии и составления наиболее подходящей тактики лечения.
Акции
Оперативные вмешательства со скидкой 7%.
Онкоконсилиум может потребоваться как при лечении в «СМ-Клиника», так и пациентам других медицинских учреждений с целью получения альтернативного мнения.
«СМ-Клиника» предоставляет своим пациентам предоперационное обследование со скидкой до 72%!
Консультация врача-хирурга по поводу операции бесплатно!
Морфологические исследования позволяют диагностировать все виды злокачественных и доброкачественных опухолей различной локализации.
Морфологическая диагностика в онкологии
Морфологический анализ – изучение тканей новообразований на клеточном уровне. С его помощью подтверждают либо опровергают онкодиагноз, дифференцируют доброкачественные и злокачественные опухоли, определяют их характеристики. Никакие другие методы диагностики – УЗИ, МРТ, онкомаркеры – не дают точных и окончательных данных. Пока нет результатов морфологического анализа, рак только предполагается.
Заключение врача-патоморфолога – основа выбора лечебной стратегии и тактики. Для каждого морфологического типа опухоли разработаны протоколы лечения с доказанной эффективностью. Врач-онколог использует результаты морфологического анализа и протоколы при разработке индивидуальной терапевтической схемы.
Забор биоматериала: пункция и биопсия
Ткани для анализа получают во время пункции с помощью шприца, методом биопсии либо после их хирургической резекции. В ходе пункции можно взять образцы слюны, мочи, мокроты, жидкости из плевральной и брюшной полостей, смывы и мазки из дыхательных и половых путей, отпечатки/соскобы эрозий и язв.
Биопсия представляет собой иссечение участка опухолевой ткани – биоптата. Выполняетсямикрохирургическимиинструментами под визуальнымконтролем УЗ, КТ или другого аппарата.
Биопсия бывает наружной и внутренней (эндоскопической – через зонд, оснащенный микровидеокамерой). В ряде случаев – когда она может спровоцировать распространение опухолевых клеток по организму – новообразование сначала радикально иссекают, а потом отправляют на морфологический анализ для определения дальнейшей лечебной тактики.
Виды морфологических исследований в онкологии
Морфологическая диагностика представляет собой изучение тканей опухоли под микроскопом.
Цитологическое исследование
Оценка структурных характеристик клеток образца. Позволяет отличать злокачественные и доброкачественные опухоли, а также не опухолевые образования.
Основано на сравнении микроскопических особенностей строения клеток в норме и при патпроцессах. В отличие от гистологического анализа изучаются не срезы тканей, а клетки.
Гистологическое исследование
Позволяет определить вид опухоли и установить ее инвазивность. Для этого образцы проходят предварительную обработку. Обезвоженные ткани равномерно пропитывают парафином. Полученные блоки нарезают тончайшими пластинами, размещают их на предметных стеклах,высушивают и окрашивают. Подготовленный таким образом материал изучают под микроскопом.
По результатам анализа делают вывод о степени атипичности опухоли (предрак или рак) и ее агрессивности с точки зрения ангиогенеза (количества кровеносных сосудов). Исследование позволяет судить об инвазивности – взаимодействии опухоли с близлежащими тканями.
Иммуногистохимическое исследование
В ряде клинических случаев для определения эффективной лечебной тактики необходимо знать специфические белки опухоли. Их определяют с помощью иммуногистохимического анализа на основе специфической реакции антиген-антитело.
Исследование позволяет определять,какая ткань стала источникомзлокачественногоперерождения клеток, по метастазам выявлять первичный опухолевый очаг, прогнозировать варианты развития опухоли и ее резистентность к разным видам терапии.
Особенности морфологической диагностики в «СМ-Клиника»
Забор биоматериала для морфологического исследования производится с помощью биопсии. После забора тканей, они направляются в лабораторию, где происходит их изучение под микроскопом. Если такое изучение тканей недостаточно информативно, то проводятся дополнительные исследования.
Взятие образцов тканей проводится опытными специалистами в стерильных условиях как в условиях процедурного кабинета, так и стационара. В ходе процедуры пациенту вводится местная анестезия, поэтому процедура проходит в максимально комфортных условиях. Способ забора материала зависит от локализации новообразования.
Лаборатория медицинского центра «СМ-Клиника» располагает специальным оборудованием для обработки и хранения материала, чтобы его можно было использовать повторно для уточнения диагноза. Изучение образца производится на мощных световых и электронных микроскопах, что позволяет добиться высокой эффективности исследования.
Показания к морфологической диагностике
Данный вид исследования назначается при:
Интерпретация результатов
В результатах морфологического исследования указывают:
Морфологическое исследование опухоли делают 10 дней. В нашем центре в Санкт-Петербурге результат проходит двойную верификацию – подтверждение двумя врачами-патоморфологами. Это позволяет свести к нулю вероятность ошибочного результата. Предметные стекла и блоки сохраняем – вы можете запросить их для анализа в сторонней лаборатории.
Записаться на прием онколога в «СМ‑Клиника» вы можете круглосуточно, позвонив по телефону в Санкт-Петербурге +7 (812) 435 55 55 или заполнив форму обратной связи
Сенько Владимир Владимирович ведущий хирург онколог, зам. главврача по хирургии, руководитель хирургического стационара стаж: 21 год
Кокорина Мария Владимировна онколог, маммолог стаж: 12 лет
Бойко Александр Александрович оперирующий онколог стаж: 10 лет
Протасов Дмитрий Андреевич оперирующий гинеколог стаж: 30 лет
| Прием (осмотр, консультация) врача-онколога первичный, лечебно-диагностический, амбулаторный | 1750 |
| Прием (осмотр, консультация) врача-онколога, к.м.н. первичный, лечебно-диагностический, амбулаторный | 2500 |
Хотите мы вам перезвоним?
При подозрении на опухолевое заболевание или при наличии подтверждающих диагноз исследований вы можете обратиться к профильному онкологу нашего центра. Врачи специализируются на онкозаболеваниях мужской и женской репродуктивных систем, мочевыделительной и пищеварительной систем, болезнях крови и кожных покровов.
Морфологическая диагностика опухолей: сдвиг в сторону молекулярно-генетического анализа
Александр Иванцов, кандидат медицинских наук,
Максим Клещёв, кандидат медицинских наук,
Екатерина Кулигина, кандидат биологических наук,
НМИЦ онкологии им. Н. Н. Петрова МЗ РФ (Санкт-Петербург)
«Природа» №6, 2018
Диагностика онкологических заболеваний начинается с морфологического анализа фрагмента пораженного органа, который зафиксирован в формалине, обезвожен в спиртах восходящей плотности и заключен в парафин. Данная процедура позволяет выполнить срез толщиной 3 мкм и поместить его на стекло, затем окрасить ядра клеток и другие базофильные структуры ярко-синим щелочным красителем гематоксилином, а цитоплазму — розовым кислым красителем эозином. Окрашивание позволяет четко визуализировать основные элементы клетки. Затем сопоставляют микроскопический «пейзаж» исследуемого образца с эталонным, на котором зафиксирована характерная для конкретной анатомической области гистологическая структура. О присутствии инвазивного неопластического процесса свидетельствуют утрата типичной гистоархитектоники и клеточных молекулярных структур, наличие полиморфных неорганизованных клеток (рис. 1).
Рис. 1. Рак толстой кишки: утрата типичной гистологической структуры в ходе неопластического процесса
Помимо установления самого факта злокачественной трансформации для назначения индивидуализированной терапевтической схемы важно как можно раньше определить гистологический тип опухоли и оценить стандартные маркеры агрессивности (степень дифференцировки, митотическая активность и т. д.). В пределах одного органа патологический процесс может развиваться по совершенно разным сценариям, вовлекать разнообразные клетки и структуры. Например, среди злокачественных новообразований легкого насчитывают, по современным представлениям, более шести гистологических типов, для каждого из которых необходимы свои терапевтические подходы (рис. 2) [1]. Мелкоклеточный рак легкого отличается стремительным течением, ранним метастазированием и очень плохим прогнозом. Карциноидные опухоли, происходящие из клеток диффузной нейроэндокринной системы, имеют наилучший прогноз; это единственный тип карцином легкого, который, как ныне считается, никак не связан с курением. Саркома легких — агрессивная опухоль, развившаяся из клеток соединительнотканных структур легкого. Аденокарциномы состоят преимущественно из железистых клеток и имеют периферическую локализацию. Опухоли этого типа зачастую развиваются у некурящих людей. Они могут нести активирующие мутации в генах EGFR, ALK и ROS1, которые являются терапевтической мишенью для действия таргетных препаратов — ингибиторов тирозинкиназ.

Рис. 2. Гистологические типы рака легкого: мелкоклеточный рак (14%); плоскоклеточный (эпидермоидный) рак (20%); аденокарцинома (38%); крупноклеточный рак (3%); карциноид (5%); мезенхимальные, в том числе саркомы и лимфомы (5%); опухоли смешанных типов — плоскоклеточный и аденокарцинома, аденокарцинома и мелкоклеточный и т.д. (15%)
Чтобы безошибочно установить гистологический тип опухоли в затруднительных ситуациях, вызванных, к примеру, маленьким размером образца или утратой опухолевыми клетками способности к образованию специфических структур (низкая степень дифференцировки), или выявить некоторые специфические характеристики новообразования, морфологи используют иммуногистохимическое окрашивание (ИГХ). Этот метод сформировался еще в середине 1980-х годов [2] и сразу стал одним из наиболее востребованных в клинической онкологии (рис. 3). Появление такого диагностического теста, например, существенно изменило роль патоморфологического исследования в лечении рака молочной железы: именно от результатов ИГХ-анализа на рецепторы к эстрогенам (ER) и прогестерону (PgR), которые синтезируется опухолевыми клетками при этом заболевании, зависит назначение эндокринной терапии. В настоящее время антагонисты эстрогенов, замедляющих деление клеток рака молочной железы, принимают примерно 70% пациенток [3]. С помощью ИГХ можно также обнаружить увеличение синтеза онкобелка HER2/neu (от англ. human epidermal growth factor receptor — рецептор эпидермального фактора роста, или трансмембранная рецепторная тирозинкиназа). Опухоли, вырабатывающие HER2/neu, оказались чувствительными к терапевтическим ингибиторам этой тирозинкиназы, и назначение соответствующих лекарственных препаратов (например, трастузумаба) основано на результатах тестов, в числе которых и ИГХ-анализ [4].

Рис. 4. Низкодифференцированная аденокарцинома легкого (а, среди фиброзной ткани отдельно расположенные опухолевые клетки) и положительная ИГХ-реакция с антителом к TTF-1 в ядрах опухолевых клеток (б)
В клиническом исследовании изучали эффективность EGFR-ингибитора (гефитиниба) на самом первом этапе лечения пациентов с мутацией EGFR [6]. Чтобы включить в исследование 25 больных, нам потребовалось проанализировать образцы тканей более 500 пациентов с раком легкого, что связано с низкой частотой этой мутации, которая в общей выборке больных не превышает 6–7%. Результаты исследования поражают воображение: эффект от препарата наблюдался у всех без исключения пациентов, в то время как аналогичный показатель при назначении стандартной терапии обычно не составляет 20–30% (рис. 5).
Рис. 5. Снижение размеров опухолевых очагов (%) в ответ на применение EGFR-ингибитора (гефитиниба) у пациентов с активирующими мутациями в гене EGFR: делецией 19-го экзона (19del) и заменой в 21-м экзоне (L858R) [6]
В настоящее время патоморфология переживает фундаментальные изменения. В стройную систему знаний, накопленных десятилетиями в рамках классической цитологии, гистологии и патологической анатомии, интегрируются новейшие представления о молекулярной патологии раковых клеток. Все это дает основания говорить о появлении новой дисциплины — молекулярной патологии [7]. Многие современные алгоритмы принятия врачебных решений уже ориентируются не столько на гистологические разновидности рака, сколько на молекулярные характеристики клеток. Однако роль патолога по-прежнему остается ведущей, поскольку именно он интегрирует все полученные сведения (микроскопические и молекулярные) в общий «портрет» опухоли.
Важность молекулярной морфологии в онкологии будет возрастать в ближайшем будущем, поскольку молекулярная диагностика больше не представляет собой однократное исследование, выполняемое только на этапе постановки диагноза. Многие современные технологии лечения рака предусматривают мониторинг характеристик опухолевых клонов на протяжении всех этапов онкологической медицинской помощи. В этом десятилетии большую популярность приобрели методы «жидкой биопсии», основанные на идентификации фрагментов опухолевых клеток в периферической крови. Другой важный аспект развития морфологии — ее интеграция с различными методами компьютерного анализа, искусственного интеллекта. На наших глазах морфология опухолей превращается из относительно консервативного раздела онкологии в одну из самых динамично развивающихся дисциплин современной медицины.
Работа выполнена при поддержке Российского фонда фундаментальных исследований (проект 16-04-00921).
Литература
1. Wistuba I., Brambilla E., Noguchi M. Chapter 17: Classic Anatomic Pathology and Lung Cancer // IASLC Thoracic Oncology. Pass H. I., Ball D., Scagliotti G. V. (eds) Aurora, Colorado, 2014; 217–240.
2. Taylor C. R., Burns J. The demonstration of plasma cells and other immunoglobulin-containing cells in formalin-fixed, paraffin-embedded tissues using peroxidase-labelled antibody // J. Clin. Pathol. 1974; 27(1): 14–20.
3. Pertschuk L. P., Tobin E. H., Gaetjens E. et al. Histochemical assay of estrogen and progesterone receptors in breast cancer: correlation with biochemical assays and patients’ response to endocrine therapies // Cancer. 1980; 46(12 Suppl): 2896–2901.
4. Pegram M. D., Lipton A., Hayes D. F. et al. Phase II study of receptor-enhanced chemosensitivity using recombinant humanized anti-p185HER2/neu monoclonal antibody plus cisplatin in patients with HER2/neu-overexpressing metastatic breast cancer refractory to chemotherapy treatment // J. Clin. Oncol. 1998; 16: 2659–2671.
5. Stenhouse G., Fyfe N., King G. et al. Thyroid transcription factor 1 in pulmonary adenocarcinoma // J. Clin. Pathol. 2004; 57(4): 383–387. DOI: 10.1136/jcp.2003.007138.
6. Moiseyenko V. M., Procenko S. A., Levchenko E. V. et al. High efficacy of first-line gefitinib in non-Asian patients with EGFR-mutated lung adenocarcinoma // Onkologie. 2010; 33(5): 231–238. DOI: 10.1159/000302729.
7. Birner P., Prager G., Streubel B. Molecular pathology of cancer: how to communicate with disease // ESMO Open. 2016; 1(5): e000085. DOI: 10.1136/esmoopen-2016-000085.
Морфологический вариант опухоли что это
Московский научно-исследовательский онкологический институт им. П.А. Герцена, Москва
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
Московский научно-исследовательский онкологический институт им. П.А. Герцена — филиал ФГБУ «Национальный медицинский исследовательский радиологический центр» Минздрава России, Москва, Россия
Московский научно-исследовательский онкологический институт им. П.А. Герцена — филиал ФГБУ «Национальный медицинский исследовательский радиологический центр» Минздрава России, Москва, Россия
Московский научно-исследовательский онкологический институт им. П.А. Герцена — филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, Москва, Россия
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
Срочная морфологическая диагностика в онкологии
Журнал: Онкология. Журнал им. П.А. Герцена. 2020;9(1): 5-13
Волченко Н. Н., Борисова О. В., Мельникова В. Ю., Ермолаева А. Г., Глухова Ю. К., Славнова Е. Н. Срочная морфологическая диагностика в онкологии. Онкология. Журнал им. П.А. Герцена. 2020;9(1):5-13.
Volchenko N N, Borisova O V, Melnikova V Yu, Ermolaeva A G, Glukhova Yu K, Slavnova E N. Urgent morphological diagnosis in oncology. P.A. Herzen Journal of Oncology. 2020;9(1):5-13.
https://doi.org/10.17116/onkolog202090115
Московский научно-исследовательский онкологический институт им. П.А. Герцена, Москва
Цель исследования — показать преимущества и ограничения срочной морфологической диагностики в онкологии. Материал и методы. За период с 2017 по 2019 г. срочное интраоперационное гистологическое исследование выполнено 765 пациентам, срочное интраоперационное цитологическое исследование — 2692 пациентам (24 877 объектов исследования). Для срочного гистологического исследования применяли криостатные срезы, препараты окрашивали гематоксилином и эозином. Срочное гистологическое исследование проводили в течение 20—30 мин. Для срочной окраски цитологических препаратов применяли набор Лейкодиф-200 (Чехия). Срочное цитологическое исследование занимает 10—15 мин. Для исследования экссудатов из серозных полостей, а иногда и лимфатических узлов применяли иммунофлюоресцентное исследование (ИФИ) с антителом к эпителиальному антигену Ber-EP4 FITC (Dako). ИФИ проводили на флюоресцентном микроскопе Carl Zeiss Imager M1. В период с 2011 по 2017 г. исследовано 218 образцов EBUS-FBNA, полученных от 172 пациентов: без применения ROSE-диагностики — 178, с применением — 40 наблюдений. Результаты. Достоверность интраоперационной морфологической верификации диагноза при гистологическом исследовании составляет 98—99%, при цитологическом исследовании — 95,2%, в 5% может быть сомнительной, в 1% наблюдений нельзя было решить вопрос о злокачественности процесса. Чувствительность исследования сторожевых лимфатических узлов (СЛУ) при раке молочной железы (РМЖ) составила 95,7%, специфичность — 99,7%, достоверность — 99,1%, эффективность — 93,1%. Срочное цитологическое исследование СЛУ при раннем РМЖ в 71% случаев позволило обнаружить макрометастазы рака. Микрометастазы составляют 16% от всех гистологически выявленных метастазов, из них цитологически обнаружено только 23% из всех микрометастазов. При меланоме метастазы в СЛУ выявлены в 5% наблюдений. При адекватном взятии материала точность срочной интраоперационной диагностики с целью уточнения степени распространенности опухолевого процесса составляет 97—98%. Чувствительность ROSE-диагностики при EBUS-TBNA составила 96%, специфичность — 100%, точность — 98%. Эффективность без ROSE составила 76%, с применением ROSE — 80%. У 40% пациентов применение ROSE позволило уточнить стадию опухолевого процесса. Заключение. Важность срочной интраоперационной морфологической диагностики в онкологии несомненна, поскольку является эффективным методом, способствует адекватному проведению хирургического лечения, которое является залогом длительной безрецидивной выживаемости. В настоящее время отмечается общая тенденция к уменьшению объема резецированных тканей с соблюдением принципов онкологической безопасности, что улучшает качество жизни пациентов и не ухудшает прогноз заболевания, поэтому количество интраоперационных морфологических исследований возрастает. Особенно актуально интраоперационное исследование СЛУ при РМЖ и меланоме, а также краев резекции при РМЖ. Также чрезвычайно актуальна ROSE-диагностика для морфологической верификации труднодоступных образований минимально инвазивными методами.
Московский научно-исследовательский онкологический институт им. П.А. Герцена, Москва
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
Московский научно-исследовательский онкологический институт им. П.А. Герцена — филиал ФГБУ «Национальный медицинский исследовательский радиологический центр» Минздрава России, Москва, Россия
Московский научно-исследовательский онкологический институт им. П.А. Герцена — филиал ФГБУ «Национальный медицинский исследовательский радиологический центр» Минздрава России, Москва, Россия
Московский научно-исследовательский онкологический институт им. П.А. Герцена — филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, Москва, Россия
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
Срочная морфологическая диагностика в онкологии подразделяется на следующие два раздела: срочная интраоперационная морфологическая диагностика (СИМД) и rapid on-site evaluation (ROSE) — быстрая оценка на месте.
Цель СИМД — адекватное выполнение хирургического вмешательства. Важность СИМД остается несомненной, так как определяет тактику хирурга во время операции, позволяет избежать повторных операций или излишне обширных хирургических вмешательств.
Задачи интраоперационной морфологической диагностики:
— морфологическая верификация диагноза при невозможности дооперационной диагностики или в случае, когда морфологический диагноз не соответствует операционным находкам;
— уточнение степени распространенности опухолевого процесса путем изучения зон регионарного метастазирования, состояния органов высокого риска метастазирования, экссудатов из грудной и брюшной полостей;
— установление абластичности операционных краев резекции;
— определение состояния тканей, окружающих опухоль, при выполнении экономных операционных вмешательств;
— контроль информативности взятого материала при диагностических операциях [1—4].
Цитологическое или гистологическое исследование при СИМД имеет свои преимущества и недостатки. Основные недостатки исследования замороженных срезов — ограниченное количество используемых участков и более низкое качество гистологических препаратов, чем при плановом гистологическом исследовании после приготовления парафиновых блоков, что влияет на точность морфологического диагноза. В замороженных срезах образуются кристаллы льда, вследствие чего происходит деформация материала и искажается архитектоника ткани. Гистологическое и цитологическое исследования зависят от качества и информативности полученного материала. Совместное использование цитологического и гистологического исследований приводит к лучшей корреляции СИМД с плановым гистологическим исследованием. В некоторых случаях морфолог может отложить постановку диагноза до планового гистологического исследования, чтобы избежать ошибочного диагноза. Такой подход может привести к повторным хирургическим вмешательствам, но при неясном диагнозе и небольшом количестве полученного материала нет необходимости любой ценой добиваться интраоперационного морфологического исследования, особенно если речь идет о редких опухолях. При поражениях размером менее 1 см не следует использовать весь материал для срочного исследования, так как можно не получить категоричного заключения ни при срочном, ни при плановом исследовании.
Быстрая оценка на месте (ROSE) — это цитоморфологическая диагностическая процедура, которая позволяет в течение нескольких минут оценить адекватность полученного материала для рутинного цитологического, гистологического, иммуноморфологического и молекулярно-генетических исследований. Чаще применяется при эндобронхиальном ультразвуковом исследовании с тонкоигольной трансбронхиальной пункцией (EBUS-TBNA) или КТ-исследовании при периферических образованиях в легких, лимфаденопатии средостения, а также при образованиях в поджелудочной железе, подслизистых образованиях в полых органах, опухолях забрюшинного пространства. Применение ROSE-диагностики также оправдано при пункциях печени, щитовидной и молочной желез, подмышечных лимфатических узлов и др. Цитолог находится рядом с диагностом, проводящим манипуляцию, при получении материала проводится срочная окраска в течение 3 мин и оценка цитологом при микроскопическом исследовании адекватности полученного материала. При неинформативности материала сразу же проводится повторный забор образца. Это уменьшает число повторных процедур особенно с использованием наркоза и является эффективной и экономичной методикой. Окончательное заключение дается после планового морфологического исследования.
Появление персонализированной медицины увеличило спрос на молекулярные исследования, что делает ROSE-диагностику еще более актуальной. Точный диагноз во время ROSE может помочь эндоскопистам решить, сколько образцов опухоли необходимо взять, например, для молекулярно-генетического исследования при аденокарциноме требуется большее количество образцов, тогда как одного образца может быть достаточно при плоскоклеточной карциноме [5—9].
Для интраоперационной морфологической верификации диагноза необходимо иметь правильно оформленные сопроводительные документы с указанием анамнестических данных, стадии процесса, характера предоперационного лечения, сроков его проведения.
Цель исследования — показать преимущества и ограничения срочной морфологической диагностики в онкологии.
Материал и методы
За период с 2017 по 2019 г. срочное интраоперационное гистологическое исследование выполнено 765 пациентам, срочное интраоперационное цитологическое исследование — 2692 пациентам (24 877 объектов исследования). Для срочного гистологического исследования применяли криостатные срезы, препараты окрашивали гематоксилином и эозином. Срочное гистологическое исследование проводили в течение 20—30 мин. Для срочной окраски цитологических препаратов использовали набор Лейкодиф (Чехия). Срочное цитологическое исследование занимает 10—15 мин. Для исследования экссудатов из серозных полостей, а иногда и лимфатических узлов применяли иммунофлюоресцентное исследование (ИФИ) с антителом к эпителиальному антигену Ber-EP4 FITC (Dako). ИФИ осуществляли на флюоресцентном микроскопе Carl Zeiss Imager M1. В период с 2011 по 2017 г. исcледовано 218 образцов EBUS-FBNA, полученных от 172 пациентов: без применения ROSE-диагностики — 178, с применением — 40.
Результаты исследования
Интраоперационная морфологическая верификация опухолей различных локализаций
Периферический рак легкого. В настоящее время заболеваемость периферическим раком легкого увеличивается, особенно растет доля аденокарцином. Совершенствование радиологических методов позволяет обнаружить мелкие очаги в легких, не доступные для дооперационной морфологической диагностики, что ведет к увеличению количества интраоперационных исследований.
Гистологическое исследование. Достоверность гистологического исследования в диагностике рака легкого составляет 99%. Злокачественный процесс установлен в 44,3% наблюдений, при этом в 85% выявлена аденокарцинома легкого, а в 14,8% — метастазы аденокарциномы кишечного типа, желудка и меланомы в ткани легкого. Нейроэндокринные опухоли установлены в 8,2% наблюдений. При использовании СИМД удается избежать излишне радикальных операций при туберкулезе, саркоидозе, гамартоме, продуктивном воспалении. В настоящее время важно не только установить диагноз рака, но и его гистологическую форму. Известно, что микропапиллярный и солидный варианты аденокарциномы легкого характеризуются более агрессивным течением с более высоким риском рецидива и требуют обширных хирургических резекций, тогда как при аденокарциноме со стелющимся типом роста (lepidic тип) и микроинвазивной аденокарциноме возможны более экономные резекции. С другой стороны, точное гистологическое определение подтипа аденокарциномы является сложной задачей, поскольку часто имеется гетерогенность опухоли. Определение гистологического типа — задача планового морфологического исследования, однако при наличии в операционном образце структур с неблагоприятным прогнозом необходимо их отмечать. Возможна ошибка в определении степени инвазии в образцах замороженных тканей по сравнению с результатами, полученными при плановом гистологическом исследовании, что связано с неудачным выбором материала для срочного исследования и разрушением альвеолярных пространств в замороженных образцах.
Цитологическое исследование. Достоверность цитологического исследования при раке легкого составляет 97,2%. Цитологически определить подтип аденокарциномы трудно, что связано с нарушением структурных признаков в цитологических препаратах, а также с гетерогенностью опухоли [10—13]. Наибольшие трудности цитологического исследования возникают при дифференциальной диагностике между реактивной пролиферацией пневмоцитов и аденокарциномой со стелющимся типом роста (рис. 1),


Рак молочной железы (РМЖ). СИМД при образованиях в молочной железе в настоящее время применяют крайне редко, так как морфологический диагноз является результатом исследования дооперационных трепанобиопсий. При неуверенном дооперационном диагнозе проводится срочное морфологическое исследование.
Гистологическое исследование. Чувствительность интраоперационного гистологического диагноза составляет 97%, специфичность — 99%. Однозначно судить о характере процесса не удается в 1—2% наблюдений. Наибольшие сложности гистологического исследования возникают при склерозирующем аденозе с радиальным рубцом, когда создается ложное впечатление инвазивного роста рака. Случаи гипердиагностики возможны при пролиферирующем папилломатозе с гиперплазией эпителия протоков и формированием железистых и папиллярных структур особенно с центральным некрозом, что можно ошибочно принять за внутрипротоковый рак. Противопоказаниями к срочному интраоперационному исследованию при опухолях молочной железы являются внутрипротоковый и внутридольковый рак (cr in situ), внутрипротоковая папиллома. Высокодифференцированная папиллярная и тубулярная карциномы, инвазивный дольковый рак часто при СИМД неправильно диагностируются как доброкачественные поражения из-за отсутствия признаков клеточной атипии.
Цитологическое исследование. Интраоперационно цитологически опухоли молочной железы исследуются крайне редко: при отсутствии дооперационного морфологического диагноза или при интраоперационных находках. Цитологическая гиподиагностика составила 3,8%, что связано с морфологическими особенностями опухолевых клеток особенно при дольковом РМЖ, а также с выраженными дистрофическими изменениями опухолевых клеток. Цитологическая гипердиагностика не превысила 1% и связана с выраженными реактивными изменениями эпителия.
Опухоли яичников. Характерно отсутствие дооперационной морфологической диагностики вследствие опасности разрыва кист (опухоли яичников чаще имеют кистозную форму) и возможности диссеминации опухоли по брюшине, что приводит к 100% интраоперационной морфологической диагностике.
Гистологическое исследование. В 30% наблюдений проведено двустороннее исследование яичников. При СИМД сравнительно просто диагностируются неопухолевые поражения яичников, такие как фолликулярная, лютеиновая, эндометриоидная кисты, эндометриоз и др. СИМД опухолей яичников имеет ряд ограничений при пограничных опухолях. Около 20% серозных пограничных опухолей иногда содержит небольшие очаги серозного рака, которые могут не попасть в срез при срочном исследовании из-за ограниченного количества отбора проб [14, 15]. По нашим данным, ошибка при исследовании пограничных опухолей яичников была связана с гиподиагностикой и составила 7%, что связано в основном с наличием микроочагов рака. Возможности интраоперационного исследования муцинозных пограничных опухолей особенно ограничены из-за больших размеров опухоли и гетерогенности структуры: в одной и той же опухоли присутствуют доброкачественные, пограничные и злокачественные участки. В классификации ВОЗ (4-е издание, 2014 г.) приведены требования к вырезке материала для планового гистологического исследования: для опухолей менее 10 см в наибольшем измерении 1 блок на каждый сантиметр максимального размера; для образований более 10 см — по 2 блока на каждый сантиметр, особое внимание следует уделять участкам солидного строения, что неосуществимо в условиях СИМД [16]. Интраоперационное заключение в предположительной форме может даваться при опухолях стромы полового тяжа и герминогенных опухолях. В 14,3% случаев при СИМД выявлены метастазы в яичнике эндометриоидной аденокарциномы, аденокарциномы шейки матки, желудка, молочной железы и почки, подтвержденные плановым гистологическим исследованием. Чувствительность СИМД при опухолях яичников составляет 98,7%, специфичность — 99%.
Цитологическое исследование. Цитологически интраоперационно опухоли яичников в нашем учреждении практически не исследуются, а исследуются экссудаты из малого таза с целью уточнения распространенности опухолевого процесса.
СИМД не используется для морфологической верификации диагноза при опухолях щитовидной железы, почки, средостения. Интраоперационная морфологическая верификация диагноза не применяется для уточнения гистогенеза и степени дифференцировки опухоли, решения вопроса: первичная опухоль или метастаз, для диагностики сарком мягких тканей, злокачественных лимфом, опухолевых узлов полиморфного строения, оценки степени лечебного патоморфоза.
Достоверность интраоперационной морфологической верификации диагноза при гистологическом исследовании составляет 98—99%, при цитологическом исследовании — 95,2% (табл. 1),

Адекватная оценка лимфатического коллектора
В последнее время СИМД переживает «второе рождение» в связи с чрезвычайной актуальностью проблемы интраоперационного исследования сторожевых лимфатических узлов (СЛУ) при РМЖ, раке шейки матки и меланоме. Исследование СЛУ на наличие метастазов является предикторным фактором поражения несигнальных лимфатических узлов и определяет объем лимфодиссекции. При исследовании макроскопически неизмененных лимфатических узлов в 30—40% случаев обнаруживаются метастазы, а при микроскопическом исследовании лимфатических узлов, макроскопически похожих на метастатические, в 25—30% случаев метастазы не выявляются. Срочное интраоперационное гистологическое исследование лимфатических узлов может быть неадекватным в 25% наблюдений из-за потери опухолевых клеток при небольшом объеме поражения лимфатического узла [4].
По данным литературы [17—19], чувствительность срочного цитологического исследования лимфатических узлов колеблется от 33 до 96%.
Интраоперационную оценку состояния лимфатических узлов в нашем исследовании осуществляли с помощью цитологического исследования соскобов с поверхности разреза или серийных срезов. Определение СЛУ проводили с использованием радиоизотопного коллоида Технефит 99mTc, сцинтиграфии в режиме ОФЭКТ и ОФЭКТ-КТ. Интраоперационно для детекции СЛУ использовали портативный гамма-детектор NEO2000. Соскобы для цитологического исследования имеют ряд преимуществ: в короткие сроки можно сделать несколько препаратов с поверхности разреза, лучше серийные; лимфатический узел в дальнейшем отправляют на плановое гистологическое исследование.
При срочной интраоперационной цитологической диагностике исследовано 837 СЛУ (609 пациенток). Цитологически метастазы выявлены в 88 (10,5%) СЛУ у 68 пациенток, т. е. у каждой 9-й, в том числе у 5 при микрометастазах. При плановом гистологическом исследовании метастазы определены в 139 (16,6%) СЛУ у 116 пациенток, т. е. практически у каждой 5-й пациентки, из них в 22 (16%) наблюдениях — микрометастазы (табл. 2).


Мы проанализировали причины цитологической гиподиагностики (табл. 3).


СИМД СЛУ необходима у пациентов с меланомой кожи на ранней стадии. Первое многоцентровое исследование селективной лимфаденэктомии (MSLT-I) показало, что статус СЛУ является наиболее важным прогностическим фактором [20—22]. Анализ данных литературы показывает, что достаточно малое количество исследований посвящено срочному интраоперационному цитологическому исследованию СЛУ при меланоме. В работе N. Jonjic и соавт. [24] показано, что при исследовании 427 СЛУ от 201 пациента чувствительность цитологического метода составила 57% при 99% специфичности. V. Soo и соавт. [25] обследовали 229 пациентов: чувствительность составила 33% при 100% специфичности. Следует отметить, что, по данным A. Fahy и соавт. [26], интраоперационное гистологическое исследование замороженных срезов СЛУ позволило выявить только 47,4% метастазов меланомы, а 23% удалось обнаружить только с помощью иммуногистохимического исследования.
В нашей работе при меланоме исследовано 142 СЛУ. Метастазы выявлены в 7 (5%) наблюдениях (рис. 5).


Причины гипер- и гиподиагностики при интраоперационном морфологическом исследовании лимфатических узлов:
— исследование не всех удаленных лимфатических узлов;
— микрометастазы (для выявления необходим правильный забор материала: СЛУ должен нарезаться с интервалом 2 мм, что позволяет обнаруживать большинство макро- и микрометастазов);
— выраженные дистрофические изменения клеток опухоли;
— воспаление с наличием крупных полиморфных гистиоцитов;
— гистологический тип опухоли (например, мелкоклеточный лимфоцитоподобный рак бывает трудно отличить от гиперплазии лимфатического узла);
— пролиферация гистиоцитов и эндотелия сосудов, которая может быть принята за метастаз рака.
Данные, полученные нами при исследовании СЛУ при РМЖ и меланоме, согласуются с результатами, указанными в литературе.
Рекомендации для улучшения срочной цитологической диагностики метастатического поражения лимфатических узлов:
— Прежде всего необходимо отрабатывать технику забора материала. При размере лимфатического узла более 5 мм делать многочисленные разрезы и, соответственно, соскобы с каждой поверхности разреза. С поверхности разреза лучше брать соскоб, а не мазки-отпечатки.
— Оптимально исследовать более одного СЛУ, но не более 5 лимфатических узлов из-за ограничения временных рамок.
— Необходимо тщательно просматривать цитологические препараты, несмотря на срочность интраоперационного исследования, так как единичные опухолевые клетки можно пропустить.
— Активно внедрять в клиническую практику флюоресцентное иммуноцитохимическое исследование и молекулярно-диагностический метод исследования OSNA.
Уточнение степени распространенности опухолевого процесса
При злокачественных опухолях яичников, желудка, кишечника, мочевого пузыря, тела матки, поджелудочной железы исследуют серозу-серозную оболочку брюшной полости и малого таза, при опухолях легких — плевру.
Гистологическое исследование. При адекватном взятии материала точность срочной интраоперационной диагностики составляет 97—98%. Наибольшие сложности возникают при диссеминации перстневидно-клеточного рака из мелких клеток по брюшине, так как единичные деформированные опухолевые клетки зажаты десмопластической стромой, что требует проведения планового ИГХ-исследования.
Цитологическое исследование. Цитологически для выявления диссеминации по серозным оболочкам чаще исследуют серозные выпоты. При исследовании плевральной и асцитической жидкости проанализировано 1045 срочных интраоперационных цитологических исследований. Для диагностики характера экссудата из серозных полостей в сложных случаях при СИМД применяется ИФИ. При перстневидно-клеточном раке и пограничных опухолях яичника, когда регистрируется наибольшее число ошибочных заключений, ИФИ асцитической жидкости обязательно (рис. 7, а, б). Применение ИФИ позволило повысить эффективность цитологического выявления диссеминации по серозным оболочкам. ИФИ повышает чувствительность цитологического метода с 62 до 93%, специфичность с 95 до 99%. ИФИ в 79% случаев позволяет подтвердить диссеминацию опухоли, заподозренную при рутинном цитологическом исследовании, а в 15% определить малочисленные опухолевые комплексы, не выявленные при рутинном цитологическом исследовании, в 7% избежать гипердиагностики опухолевой диссеминации.

Цитологическое исследование мазков-отпечатков с образований серозных оболочек так же сложно, как и гистологическое, особенно при перстневидно-клеточном раке из мелких клеток, так как часто опухолевые клетки из-за выраженной плотной стромы не попадают в цитологические препараты или их сложно дифференцировать с реактивным мезотелием. Необходимо отработать методику ИФИ мазков-отпечатков с брюшины.
Контроль абластичности краев резекции
Основной целью хирурга является достижение чистых краев резекции. Положительный край резекции или близкий край (расстояние от опухоли до края резекции 2 мм и менее) оказывает существенное негативное влияние на местный рецидив, региональный рецидив, отдаленные метастазы и общую выживаемость [30].
Гистологическое исследование. При раке легкого опухолевые клетки в крае резекции гистологически выявлены в 10% случаев, что потребовало дополнительной резекции стенки бронха.
Гистологическое исследование при раке желудка: в 10% случаев в краях резекции выявлен рак, в 2% — подозрение на наличие опухолевых клеток, при раке пищевода — 3,5% (неясно). При раке желудка из-за подслизистого и внутримышечного роста опухоль распространяется далеко за пределы макроскопически определяемых границ поражения, особенно при диффузном типе рака. Следовательно, необходимо широкое иссечение на расстоянии 3—5 см от видимой границы опухоли со срочным интраоперационным исследованием краев резекции. Особое значение придается проксимальному краю резекции [31].
Цитологическое исследование. В нашем институте широко применяется цитологическое исследование краев резекции при опухолях головы и шеи. Опухолевые клетки выявлены в 6,8% наблюдений. Часто материал неинформативный или крайне скудный в 30—40% наблюдений, что не позволяет провести адекватную оценку.
В настоящее время с развитием онкопластических операций, особенно при РМЖ, имеется тенденция к проведению экономных резекций, что требует срочного интраоперационного исследования краев резекции.
Интраоперационная оценка хирургических краев при РМЖ у пациентов с экономными резекциями необходима. Однако это достаточно большая проблема, так как при срочном гистологическом исследовании отбор проб ограничен и СИМД значительно уступает плановому гистологическому исследованию. Кроме того, ткань молочной железы всегда содержит большое количество жира, который плохо поддается заморозке, что не позволяет адекватно оценить материал [32—34]. Отрицательные края резекции зависят от множества факторов, включая количество исследованных срезов и методику оценки. Изменения в понимании биологии РМЖ и широкое использование адъювантной системной терапии при ранних стадиях также повлияли на отношение к ширине поля от опухоли до края резекции. В течение многих лет считалось, что оставшиеся опухолевые клетки являются основной причиной местного рецидива, а убеждение в том, что большие отрицательные поля улучшают исход заболевания, было логическим продолжением этого взгляда. В настоящее время стало понятно, что развитие местного рецидива зависит от гормонального и HER-2-статуса опухоли: реже рецидивы развиваются при гормонозависимых и HER-2-отрицательных опухолях, чаще — у пациентов с тройным негативным молекулярным подтипом независимо от того, проводилось хирургическое или консервативное лечение. При экономных операциях важно не оставлять инвазивный компонент опухоли в оставшейся ткани, тогда как влияние на рецидив заболевания очагов cr in situ в этой ткани является спорным вопросом. Фактором риска для положительных краев резекции при РМЖ при экономных резекциях является наличие DCIS ( ductal cr in situ) по периферии опухолевого узла. Некоторыми авторами показано, что смертность в течение 10 лет от прогрессирования заболевания у пациентов с DCIS, получивших адьювантную терапию, не превышает 1%. Имеют значение размер DCIS, степень дифференцировки опухоли, наличие мультицентричных очагов, ширина поля от опухоли до края резекции. Например, обширный внутрипротоковый компонент DCIS может быть размером около 3 см и более. У пациентов с DCIS при величине отступа от опухоли до края резекции 2 мм минимизируется риск развития рецидива, но ширина поля более 2 мм не дает дополнительного преимущества [35].
В нашем институте края резекции при РМЖ исследуются цитологически. Сведений из источников литературы по цитологическому исследованию краев резекции при РМЖ практически нет. Материал забирает хирург, и в отделение доставляются цитологические препараты с маркированными краями: верхний, нижний, латеральный, медиальный, фасциальный и подсосковая зона. Для контроля абластичности краев резекции при РМЖ цитологически исследован 2 561 край резекции (1997 пациенток). Достоверность исследования составила 99%, чувствительность — 97%, специфичность — 100%, эффективность — 98%. Основная проблема заключается в том, что у молодых пациенток при отсутствии эпителия материал — только жировая ткань) образец для исследования не может считаться взятым адекватно, поскольку 80% доставленного материала составляет жировая ткань. Цитологически оценить ширину поля невозможно, поэтому хирурги опираются фактически только на макроскопические признаки опухоли, которые не всегда совпадают с ее микроскопическими границами. У 2,5% больных в крае резекции обнаружены опухолевые клетки. Ложноотрицательные цитологические заключения составили 1,2%. Фактором, определяющим морфологическую гиподиагностику опухолевого роста в краях резекции при СИМД особенно при цитологическом исследовании является инвазивная дольковая карцинома, характеризующаяся мелкими клетками размером с лимфоцит или немного крупнее, не образующими железистоподобных структур со слабовыраженными признаками атипии.
ROSE-диагностика
При открытой биопсии опухолей средостения, костей и мягких тканей используется ROSE-диагностика, когда цитолог оценивает наличие и количество адекватного материала для планового гистологического и иммуногистохимического исследования с целью верификации диагноза. Цитолог дает заключение о наличии или отсутствии опухолевого процесса, а о гистологической форме высказывается в предположительной форме (например, метастаз рака, вероятно, аденогенного, веретеноклеточная саркома или неходжкинская лимфома). Для точного диагноза требуются плановое гистологическое, иммуногистохимическое и молекулярно-генетическое исследования. Чувствительность EBUS-TBNA составила 96%, специфичность — 100%, точность — 98%. Эффективность без ROSE — 76%, с применением ROSE — 80%. Оценка информативности цитологических препаратов при EBUS-TBNA с использованием ROSE показала, что без ROSE неинформативный материал составляет 24%, а с применением ROSE — 17%. У 40% пациентов с помощью ROSE-диагностики удалось уточнить стадию опухолевого процесса.
Заключение
СИМД в онкологии, несомненно, играет важную роль и является эффективным методом диагностики, способствует адекватному проведению хирургического лечения, которое является залогом длительной безрецидивной выживаемости. В настоящее время отмечается общая тенденция к уменьшению объема резецированных тканей с соблюдением принципов онкологической безопасности, что улучшает качество жизни пациентов и не ухудшает прогноз заболевания, поэтому количество интраоперационных морфологических исследований возрастает. Особенно актуально интраоперационное исследование СЛУ при РМЖ и меланоме, а также краев резекции при РМЖ. Также чрезвычайно важна ROSE-диагностика для морфологической верификации труднодоступных образований минимально инвазивными методами.
Концепция и дизайн исследования: Н.Н.В., О.В.Б.
Сбор и обработка материала: О.В.Б., В.Ю.М., А.Г.Е., Ю.К.Г.
Статистическая обработка: Н.Н.В., О.В.Б., В.Ю.М., А.Г.Е., Ю.К.Г.
Написание текста: О.В.Б.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.