мозолистое тело интактно что это
Мозолистое тело, дисгенезия, атрофия, болезнь Маркиафавы-Биньями
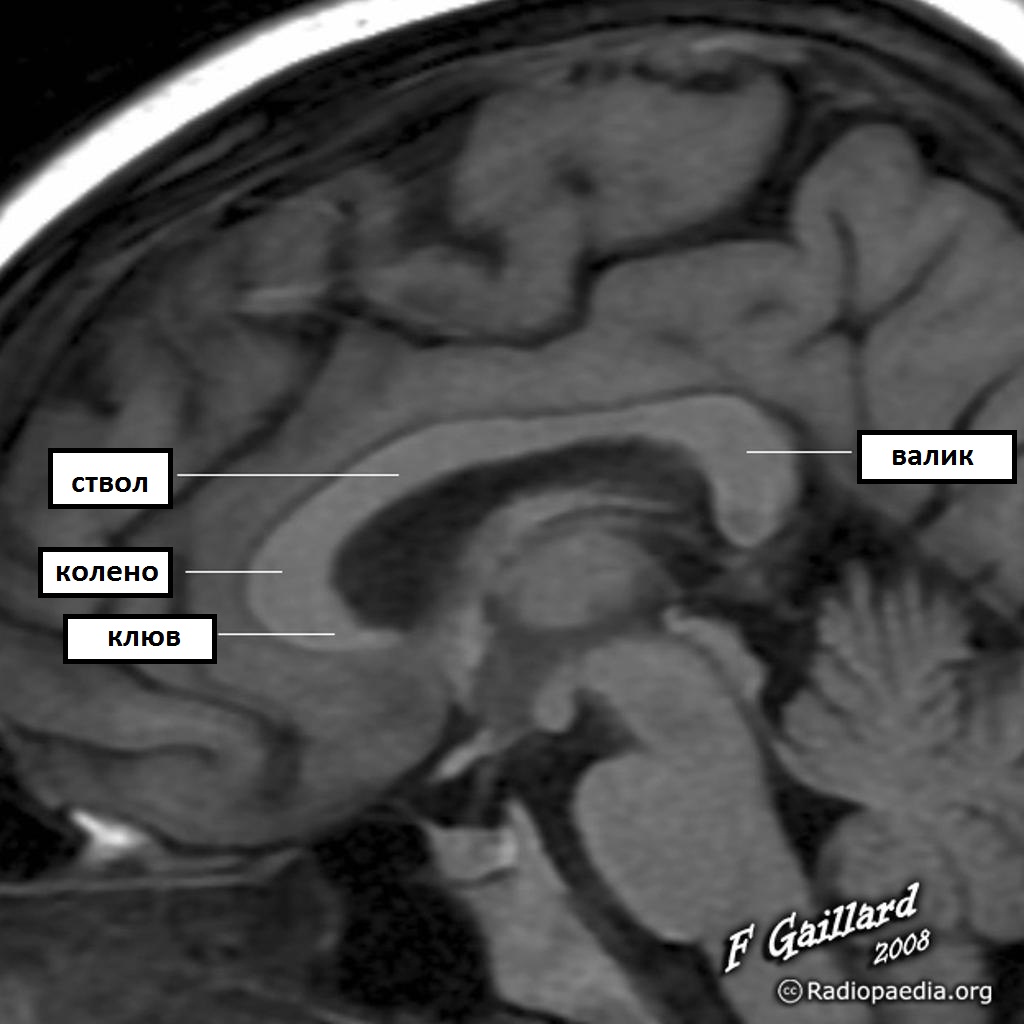
Мозолистое тело состоит:
Каждый отдел соединяет гомолатеральный отдел головного мозга.
Формирование мозолистого тела.
Мозолистое тело развивается в особом порядке:
От колена, затем тела, валик и в конце развивается клюв.
Миелинизация мозолистого тела идет от задних отделов к передним отделам.
Данные знания помогают сузить дифференциальный диагноз при патологиях мозолистого тела.
Дисгенезия vs Атрофия
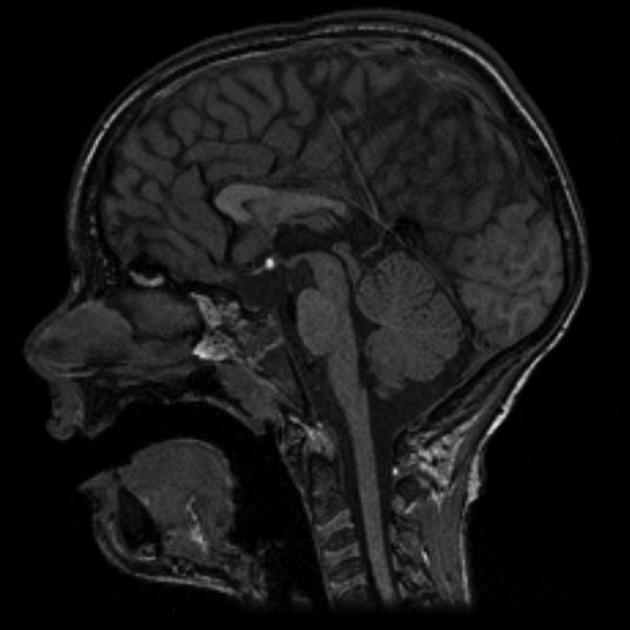
При дисгенезии мозолистого тела хорошо сформировано колено и передние отделы мозолистого тела, но отсутствует валик и клюв. Данная патология является врожденной. Патология представлена слева.
При атрофии мозолистого тела хорошо сформированы задние отделы мозолистого тела (задний отдел тела и валик), но при этом уменьшены в размерах клюв, колено и передний отдел тела. Данные изменения являются приобретенными.
Многие заболевания поражают мозолистое тело, поэтому наличие очагов не являются патогномоничным для определенного заболевания.
Болезнь Маркиафавы-Биньями (центральная дегенерация мозолистого тела, Маркиафавы синдром, экстрапонтинный миелинолиз).
Встречается у лиц злоупотребляющих алкоголем. У данных лиц на МРТ выявляется поражение валика и задних отделов ствола (тела) мозолистого тела.
На хронических стадиях болезни Маркиафавы-Биньями визуализируется мозолистое тело в виде сэндвича, при котором сохраняется верхних и нижних слоев мозолистого тела, но с некрозом средних слоев.
Гродненская областная детская клиническая больница
Под агенезией (гипо-дисгенезией) понимают отсутствие мозолистых спаек, соединяющих полушария головного мозга, как частично, так и полностью.
Формирование мозолистого тела, прозрачной перегородки и свода начинается в 11 недель внутриутробной жизни и заканчивается к 16 неделе. В зависимости от этого степень дефекта мозолистого тела связана со стадией развития плода.
Первичная агенезия встречается до 12 недели жизни плода как следствие сосудистого либо воспалительного повреждения, и может быть изолированной или связанной с другими мальформациям (например: агенезия прозрачной перегородки, голопрозэнцефалия ( нарушение формирования мозга, при котором характерно полное или частичное отсутствие разделения на полушария, в сочетании с другими пороками развития ).
Вторичная дисгенезия — частичная или полная деструкция мозолистого тела —развивается уже после формирования мозолистого тела (травматические, токсические повреждения, аноксия в системе передней мозговой артерии).
Агенезия мозолистого тела чаще обнаруживается у детей с гидроцефалией, также в сочетании с другими мальформациями мозга.
Нарушение развития мозолистого тела не имеет характерной клинической картины, а неврологическая симптоматика чаще всего представлена неспецифическими интеллектуальными и неврологическими нарушениями, вплоть до полного асимптоматического течения. При сочетании агенезии мозолистого тела с другими пороками развития мозга и черепа на первый план могут выступать именно проявления последних.
КТ-признаки агенезии мозолистого тела: широко расставленные передние рога и тела боковых желудочков, высокое стояние III желудочка между ними; медиальные стенки боковых желудочков приобретают параллельный ход, а задние рога их обычно расширены (кольпоцефалия). МРТ, выполненная в 3-х плоскостях, дает полное представление о степени недоразвития мозолистого тела: частичной — гипогенезии, полной — агенезии или частичном дефекте формирования его — дисгенезии. Наиболее показательны сагиттальные срезы, позволяющие дифференцировать формирование всех его отделов. Агенезия (гипогенезия) мозолистого тела часто сочетается с отсутствием или недоразвитием гиппокампа, миндалевидного ядра, гетеротопией серого вещества или с другими мальформациями мозга.
В качестве первичного метода диагностики используют УЗИ. К сожалению, проведение процедуры эхографии в пренатальный период имеет много трудностей, в том числе из-за особенностей предлежания плода, что приводит к учащению случаев пропуска данной патологии. А при дисгенезии, гипогенезии, обнаружить дефект еще более c ложно. Затрудняет интерпретацию заболевания то, что агенезия часто сочетается с множественными пороками развития, с различными генетическими симптомами.
Мозолистое тело
СТРУКТУРА МОЗОЛИСТОГО ТЕЛА
Основная функция мозолистого тела – осуществление коммуникации между левым и правым полушариями мозга, и эту часть мозга обычно разделяют на 4 принципиальных компонента:
НАРУШЕНИЯ РАБОТЫ МОЗОЛИСТОГО ТЕЛА
Психиатры и другие медицинские специалисты изучали функции мозолистого тела на протяжении нескольких десятилетий. Неправильное формирование этой части мозга и пороки ее развития могут привести к появлению приступов и других проблем в функционировании. Однако при наличии подобных нарушений развития функционирование человека по большей части остается нормальным, и лечение представляет собой в основном управление симптомами.
Ампутация части мозолистого тела – каллозотомия или операция по разделению полушарий – исторически использовалась как крайняя мера лечения эпилепсии. После разделения мозолистого тела сигналы, вызывающие приступы, перестают передаваться от одного полушария к другому, и это позволяет значительно снизить интенсивность приступов и сократить их продолжительность. Хирургическое разделение мозолистого тела может привести к возникновению трудностей с речью и памятью – и все же во многих случаях длительных побочных эффектов не наблюдается. Роль полушарий мозга и эффекты каллозотомии изучалась многими психиатрами в рамках исследований, которые в разговорной речи называются «исследованиями разделения мозга».
Анализ микроструктурных изменений мозолистого тела при помощи МР-трактографии у пациентов с эпилепсией
1 – ГУ «РНПЦ онкологии и медицинской радиологии им. Н.Н. Александрова» г. Минска, Беларусь
2 – ГУО «Белорусская медицинская академия последипломного образования» г. Минск, Беларусь.
В статье приведены результаты оценки МР-трактографии мозолистого тела в диагностике структурных повреждений головного мозга у пациентов с эпилепсией.
Ключевые слова: МР-трактография, эпилепсия, мозолистое тело.
Роль мозолистого тела (далее – МТ) в функционировании головного мозга сложно переоценить. Современные подходы к диагностике и технологическое развитие методов нейровизуализации открывает новые возможности в выявлении микроструктурных изменений головного мозга в целом и МТ в частности. По мнению ряда исследователей, оценка состояния МТ приобретает особое значение в анализе развития различных патологических состояний головного мозга.
МР-трактография, как методика оценки микроструктурных изменений, получила применение в диагностике аксональных повреждений, хронической ишемии головного мозга, болезни мотонейрона, острого диссеминированного энцефаломиелита, опухолей головного мозга и аномалиях развития ЦНС, кортикальных инфарктов, неопухолевых заболеваний (рассеянный склероз, болезнь Альцгеймера).
Несмотря на разнообразные клинические исследования, дифференцированные подходы к диагностике, использование различных дизайнов и протоколов нейровизуализации, в настоящее время нет четкого и однозначного понимания влияния различных отделов МТ на развитие и распространение эпилептической активности, вклад составных частей МТ в эпилептогенез, особенно при наличии сопутствующих патологических состояний головного мозга.
Кроме того, отсутствуют данные о взаимосвязи вовлечения МТ в патологический процесс с выраженностью клинических проявлений при опухолях, инсультах, воспалительных процессах, не уточнены критерии каллозальной атрофии из-за недостаточной определенности параметров главной мозговой спайки в популяции у здоровых лиц.
Многие исследователи отмечают, что диагностическая значимость МР-трактографии напрямую зависит от уровня компетенции исследователя (знания анатомии проводящих путей и умения соотнести их с МР-изображениями), а также может быть подвержена ошибкам, связанным с эффектом частичного объемного усреднения, шумом, некорректным выделением области интереса и т.п.
В рамках детального изучения микроструктурных изменений МТ современными методиками нейровизуализации (включая DTI), с учетом недостаточного количества и несистематизированности полученных сведений, требуются проведение оценки показателей FA и ADC МТ при различных патологических процессах, а также параметров транскаллезных и афферентных трактов МТ по данным МР-трактографии для сопоставления этих результатов с оценкой общего состояния проводящих путей головного мозга и определения прогнозов в отношении течения процесса, в частности – у пациентов с эпилепсией.
Показания к проведению МР-трактографии головного мозга:
Противопоказания к проведению МР-трактографии сводятся к противопоказаниям при проведении МРТ:
Ограничением при проведении МРТ является неадекватное состояние пациента и невозможность выполнения им требований к проведению МРТ. Дополнительной подготовки перед проведением МР-трактографии не требуется.
Цель исследования. Оценка данных рутинной МР-томографии и МР-трактографии в диагностике структурных повреждений головного мозга у пациентов с эпилепсией, выявление закономерностей изменения трактографической картины в зависимости от длительности приема противоэпилептических препаратов, тяжести течения заболевания. Показаниями к проведению МР-трактографии головного мозга в ходе исследования (критерии включения) считалось оценка поражений трактов при эпилепсии, измерение фракционной анизотропии (FA) и измеряемого коэффициента диффузии (ADC) для оценки микроструктурных изменений и определения дальнейшей тактики ведения пациента.
Материал и методы исследования. Нами обследовано 67 пациентов с эпилепсией, с использованием набора мультипланарных импульсных последовательностей и пакета диффузионной тензорной магнитно-резонансной томографии. Произведено сопоставление проведенных данных с контрольной группой (n=64). Средний возраст в группе пациентов с эпилепсией составил 29,1±3,2 лет.
Результаты и обсуждение. Структурные изменения при МРТ головного мозга у пациентов с эпилепсией были выявлены в 69,9% случаях: неокортикальные поражения у 21,9%, мезиальный темпоральный склероз – у 24,6%, их сочетание – у 30,1% обследованных; отсутствие визуальных морфологических изменений головного мозга было отмечено – у 23,4%. При этом у 71% пациентов было обнаружено расширение субарахноидальных пространств, в 24% случаев имела место их асимметрия с преобладанием патологических изменений на стороне очага, у 74% пациентов с эпилепсией наблюдалось расширение боковых желудочков, из них в 80% случаев – расширение височного рога бокового желудочка на стороне эпилептогенного очага.
Были получены следующие значения FA: для передних отделов мозга – 0,52 (0,5÷0,55), для задних – 0,53 (0,52÷0,54). Межполушарная асимметрия по данному параметру выявлена лишь для задних квадрантов, основная область которых представлена височными долями. Средняя диффузионная способность для передних отделов мозга составила 0,88 (0,86÷0,9), для задних – 0,89 (0,87÷0,91) без значимой асимметрии (р>0,05). Длина трактов в передних квадрантах составила 26,1 (23,8÷28,7) мм, в задних – 44,95 (41,5÷50,8) мм. При визуальной оценке симметричности трактов выявлено, что уменьшение их представленности на стороне очага характерно для пациентов с кортикальной дисплазией или экстрагиппокампальным расположением визуализируемых очагов поражения. В случае наличия мезиального темпорального склероза имело место «обеднение» трактографической картины в противоположном полушарии, что может объясняться феноменом гиппокампальной деафферентации. Наличие асимметрии трактов также было взаимосвязано со значениями FA и ADC – на стороне визуальных нарушений, где количество линий трактов (lines) было меньшим, отмечалось снижение фракционной анизотропии и увеличение средней диффузионной способности.
Было отмечено, что микроструктурные изменения в МТ коррелируют с когнитивной дисфункцией у пациентов с эпилепсией. Отмечается уменьшение количества афферентных трансколлозальных трактов у пациентов с выраженными когнитивными нарушениями. Для детальной оценки микроструктурных изменений в белом веществе с помощью DTI можно предположить формирующуюся потерю аксонов у пациентов с когнитивными нарушениями, что находит свое отражение в изменений трактографической картины. Когнитивные изменения коррелируют с DTI параметрами, отражая повреждение соединений МТ ведущее к ухудшению нервной проводимости. Таким образом, констатируется связь когнитивных нарушений с каллозальных повреждениями у пациентов с эпилепсией.
В ходе анализа в группе пациентов с эпилепсией отмечается снижение FA и повышение ADC МТ в сравнении с пациентами контрольной группы. При этом выявленное снижение FA МТ коррелировало с длительностью приема противоэпилептических препаратов (ПЭП). В литературе отмечается также снижение FA клюва и тела МТ, которое коррелирует с продолжительностью эпилепсии и отражает связь эпилепсии с микроструктурными изменения МТ. Полученные результаты позволяют предполагать, что ПЭП-терапия может привести к дополнительному повреждению и вторичной дегенерации МТ, напрямую связанных с эффектами лечения.
Заключение.
МР-трактография головного мозга у пациентов с эпилепсией позволяет получить детальную информацию о проводящих путях головного мозга, выявить их микроструктурные изменения, оценить выраженность сосудистых поражений, демиелинизации, глиоза (как сопутствующих состояний) на основе количественной оценки FA и ADC структур головного мозга, вовлекаемого в патологический процесс.
Комплексная оценка полученных результатов предполагает, что использование DTI в рутинной практике может с течением трансформироваться из «просто используемой», «рекомендуемой к применению» методики нейровизуализации в анализе микроструктурных изменений головного мозга и его структур, в «обязательно включенную» в пакет стандартных импульсных последовательностей, в особенности – в специализированных неврологических и нейрохирургических стационарах. Необходима более детальная оценка вклада DTI в понимание характера патоморфологических изменений проводящих путей головного мозга на макро- и микроструктурном уровне при различных патологических процессах и выработка оптимального алгоритма интерпретации полученных данных.
Особенности развития мозолистого тела мозга детей по данным МРТ
Полный текст
Аннотация
По мере внедрения магнитно-резонансной томографии (МРТ) в практику исследований мозга все чаще обращают на себя внимание гипоплазии мозолистого тела при разных заболеваниях центральной нервной системы. В данной работе была исследована возрастная динамика развития мозолистого тела на МРТ мозга детей без неврологической патологии и их ровесников с детским церебральным параличом (ДЦП). На срединно-сагиттальных изображениях сравнивали площадь всего мозолистого тела и его отдельных сегментов. Для анализа использовали оригинальную формулу соотношения площадей передних и задних сегментов комиссуры — коэффициент мозолистого тела (kCC). Обнаружено, что у детей группы контроля площадь мозолистого тела увеличивается, наиболее интенсивно растет валик комиссуры. У детей с ДЦП площадь мозолистого тела хотя и увеличивается с возрастом, но остается достоверно меньше, чем у здоровых детей, а относительная площадь валика почти не меняется. При этом kCC у детей с ДЦП достоверно ниже, чем в группе контроля. Известно, что группой риска по ДЦП являются недоношенные дети. Было проведено сравнительное морфометрическое исследование мозолистого тела и kCC на томограммах мозга доношенных и недоношенных детей раннего грудного возраста. Установлено, что у детей с неполным сроком гестации на момент рождения площадь комиссуры меньше, чем у доношенных сверстников, а kCC достоверно ниже. Таким образом, были получены показатели, которые позволили как охарактеризовать возрастную динамику развития мозолистого тела, так и с высокой степенью достоверности различать мозг детей из группы контроля и с ДЦП, а также определять вероятную группу риска по ДЦП среди детей младшего грудного возраста.
Ключевые слова
Полный текст
Мозолистое тело (corpus callosum, CC) — самый крупный тракт конечного мозга, который объединяет новую кору обоих полушарий и с которым традиционно связывают представления о латерализации функций, особенностях поведения человека и его когнитивных способностях. С широким внедрением в клиническую практику методов магнитно-резонансной томографии (МРТ) стали обращать внимание на гипо- и дисплазии СС у детей с заболеваниями ЦНС различного генеза: с детским церебральным параличом (ДЦП), с фетальным алкогольным синдромом, у детей, рожденных женщинами с гипотиреозом, и т. д. — всего около 50 заболеваний [12, 26, 35, 39].
ДЦП — ведущая причина детской инвалидности во всем мире, формирует группу непрогрессирующих поражений головного мозга, которые в подавляющем большинстве случаев возникают пренатально и частота встречаемости которых постоянно растет, достигая в среднем 2,11 случая на 1000 новорожденных в год [6, 31]. Неоднократно отмечена положительная корреляция роста заболеваемости ДЦП и численности новорожденных с низкой и экстремально низкой массой тела, но адекватного объяснения этому не найдено [31]. В то же время по данным МРТ в структуре мозга детей с ДЦП, кроме типичных отклонений, таких как кистозные лейкомаляции, локальные очаги демиелинизации, вентрикуломегалия [11, 13], отмечают дефицит кортикоспинального, сенсомоторных трактов мозга, а также гипоплазии СС [32, 38]. Одна из возможных причин развития гипоплазий СС — валлеровская дегенерация аксонов. Это явление было открыто более 100 лет назад и представляет собой антероградное перерождение аксонов, их миелиновой оболочки после гибели нейронов и/или отделения аксона от тела клетки. Гистологически такие аксоны визуализируются на протяжении первых двух недель после травмы, по результатам структурной МРТ изменения белого вещества той же природы обнаруживают через три недели после инсульта [16, 22]. У новорожденных методом диффузионно-тензорной томографии нарушения целостности нисходящих трактов и СС визуализируют уже в первые сутки после инсульта, это так называемая преваллеровская дегенерация [10, 19]. На более поздних сроках судить о причине гипоплазии трактов можно по уменьшению плотности инициальных нейронов и истончению коры. Так, в модельных экспериментах на животных наблюдают прямую корреляцию уменьшения количества транскаллозальных волокон, плотности нейронов и толщины коры полушарий [7, 36]. В то же время у взрослых пациентов с агенезиями СС сниженную толщину коры описывают только в первичных сенсорных и моторном полях коры [9].
Анализируя причины гипоплазий СС у детей с ДЦП и иными заболеваниями пренатального генеза, необходимо учитывать известный факт гетерохронного развития коры и периоды ее повышенной уязвимости. Во второй половине гестации критический период развития коры связан с постмиграционной дифференцировкой нейронов, когда клетки уязвимы по отношению к тератогенным факторам. Разные корковые территории проходят этот период гетерохронно. В качестве маркеров таких периодов чаще всего используют белки пре-, постсинапсов и цитоскелета. К последним относится белок микротрубочек МАР2, который позволяет идентифицировать морфотип клетки и период активного синаптогенеза, то есть критический период постмиграционной дифференцировки с высокой уязвимостью нейронов [37]. Во втором и начале третьего триместра гестации кора предцентральной, постцентральной, перисильвиевой и префронтальной областей полушарий демонстрирует опережающую постмиграционную дифференцировку, о чем свидетельствует сравнительно большая ее толщина по результатам плодной МРТ [15, 34] и МАР2-позитивные пирамидные клетки в слоях III и V [5, 44]. Эти нейроны инициируют как нисходящие, так и корково-корковые связи, в том числе транскаллозальные. Таким образом, можно обоснованно полагать, что в зависимости от временного совпадения критического периода развития клеток, неблагополучного периода беременности или преждевременного рождения нейродегенеративный процесс затронет разные области коры и скажется на организации проводящих трактов. Принимая во внимание строгую топографию каллозальных волокон, локальные гипоплазии СС можно рассматривать как следствие избирательной гибели нейронов, последующей валлеровской дегенерации транскаллозальных аксонов. Опираясь на эту гипотезу, был разработан количественный метод диагностики ДЦП по морфометрическим параметрам СС на срединных сагиттальных томограммах мозга [4]. Диагностическая значимость такого метода может быть существенно повышена его адаптацией к анализу томограмм детей младшего грудного возраста.
Цель настоящего исследования заключается в сравнительной морфометрической оценке состояния мозолистого тела по результатам МРТ мозга детей разного возраста без патологий ЦНС и с ДЦП, а также доношенных и недоношенных детей раннего грудного возраста.
Материал и методы исследования
В исследование включены результаты обследования детей, выполненных на отделении лучевой диагностики Санкт-Петербургского государственного педиатрического медицинского университета (СПбГПМУ). Все дети проходили обследование по назначению врача-невролога в период с 2008 по 2013 г. Новорожденные дети проходили МРТ-обследования в 2011 г. в ходе стационарного лечения в отделении патологии новорожденных СПбГПМУ. По результатам обследования во всех случаях имелось заключение врача-радиолога. Родители или опекуны детей подписывали информированное согласие на использование результатов обследования в открытых публикациях, исследование одобрено этическим комитетом СПбГПМУ.
В первой части работы был осуществлен сравнительный анализ МР-томограмм мозга детей обоих полов в возрасте от 2 до 11 лет без неврологических заболеваний (n = 50; 24 мальчика, 26 девочек) и их сверстников с диагнозом ДЦП (n = 60; 27 мальчиков, 33 девочки). Дети группы контроля проходили диагностическое обследование по поводу таких заболеваний, как отит, синусит, ушиб головы. Изображения были получены на томографе General Electric Signa HDx с напряженностью поля 1,5 T с использованием 8-канальной катушки приема сигнала в режимах T1 и T2 fl3d с шагом в 2 мм и толщиной среза 2,5 мм в сагиттальной и аксиальной проекциях.
Для исследования были отобраны МР-то мограммы удовлетворительного контраста и без выраженных структурных патологий мозга. По заключению врача-радиолога у всех детей с ДЦП обнаружена перивентрикулярная лейкомаляция. Во всех 110 случаях мозолистое тело мозга было полностью сформировано. Сравнительный анализ развития СС мозга детей с ДЦП и группы контроля осуществляли с учетом возраста пациентов. Принимая во внимание индивидуальную вариабельность онтогенетических преобразований мозга и психомоторного развития детей, были выделены 8 возрастных подгрупп сравнения (табл. 1). Пол детей не учитывали ввиду малочисленности этих подгрупп.
Таблица 1 (Table 1). Численный состав возрастных подгрупп сравнения детей с детским церебральным параличом и контроля
The number of cases in each age subgroups for groups with cerebral palsy and control