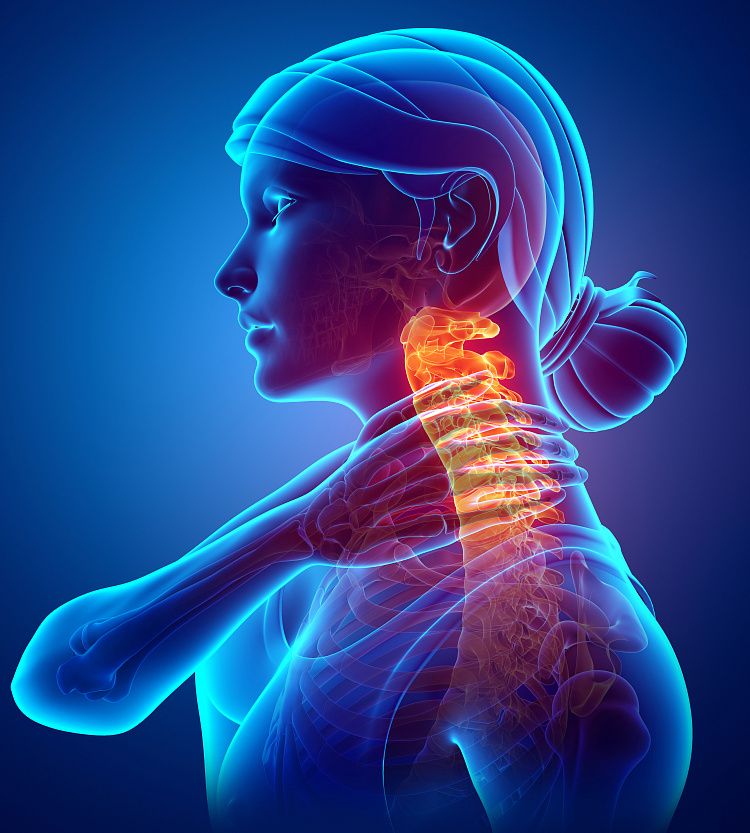
очаг в шейном отделе спинного мозга
Шейная миелопатия
Некоторые заболевания позвоночника, сосудистые нарушения и даже эндокринные патологии способны провоцировать возникновение такого неприятного и весьма снижающего качество жизни состояния, как шейная миелопатия. Она сопровождается нарушениями чувствительности и подвижности, а также может приводить к тяжелым осложнениям. Поэтому важно ее диагностировать на ранних сроках развития, установить причину возникновения и эффективно воздействовать на нее, чтобы избежать усугубления состояния.
Что такое шейная миелопатия и причины ее возникновения
Шейной миелопатией называют хорошо изученный клинический синдром, возникновение которого обусловлено поражением спинного мозга в результате воздействия различных факторов, в том числе травм, дегенеративных изменений в шейном отделе позвоночника, образования опухолей, развития инфекционных, неврологических и сосудистых заболеваний. Другими словами, шейная миелопатия и сопровождающий ее комплекс симптомов не является самостоятельным заболеванием, а выступает лишь следствием сужения позвоночного канала, нарушения питания спинного мозга, воспалительного процесса в нем, обусловленных теми или иными причинами.
В позвоночном канале проходит окруженный собственными оболочками спинной мозг с его нервными корешками и кровеносными сосудами. Поэтому его сужение, особенно прогрессирующее, рано или поздно отразится на состоянии этой ответственной за правильную работу практически всех органов и тканей человеческого тела нервной структуре, что приведет к соответствующим неврологическим нарушениям, а при поражении кровеносных сосудов – ишемии (острому нарушению питания) и другим нежелательным последствиям. Поэтому развитие симптомов шейной миелопатии требует скорейшего обращения к неврологу, комплексной диагностики и назначения лечения, которое может заключаться в проведении декомпрессионной операции.
Основными причинами развития шейной миелопатии являются:
Наиболее частой причиной развития шейной миелопатии являются осложнения остеохондроза шейного отдела позвоночника.
Нарушение может возникать в любом возрасте, хотя наиболее характерно для пожилых людей с тяжелыми дегенеративными изменениями в позвоночнике. Но если рассматривать каждую возрастную группу отдельно, то у детей наиболее часто патология становится следствием перенесения энтеровирусной инфекции, у людей молодого возраста – травмы спины и позвоночника в частности. В средней возрастной категории шейная миелопатия обусловлена новообразованиями, травмами.
В целом можно выделить 2 типа шейной миелопатии:
Миелопатия может поражать любой отдел позвоночника, включая грудной и поясничный, хотя шейный отдел в силу анатомических особенностей страдает чаще всего. В каждом случае к ее развитию приводит стеноз спинного мозга или его сосудов. Но проявления патологии напрямую зависят от локализации пораженного участка и могут кардинально различаться.
Врожденная узость позвоночного канала существенно увеличивает риск развития шейной миелопатии. Таким образом, при его диаметре менее 12 мм вероятность возникновения данного нарушения крайне высока.
Предпосылками для развития патологии могут выступать:
В отдельных случаях шейная миелопатия развивается после проведения хирургических вмешательств на шейном отделе позвоночника. В таких ситуациях иногда наблюдается перерождение тканей с формированием участков, лишенных функциональной активности. В результате они препятствуют свободному поступлению к спинному мозгу кислорода и питательных веществ. Но в подавляющем большинстве случаев шейная миелопатия становится следствием естественного старения организма.
В зависимости от причин развития различают довольно много видов шейной миелопатии. Определение конкретного из них позволяет разработать наиболее эффективную тактику лечения и добиться лучшего исхода.
Вертеброгенная
Именно эта форма шейной миелопатии, которую еще называют спондилогенной, диагностируется в подавляющем большинстве случаев. Она развивается в результате возникновения нарушений в состоянии позвоночника на фоне врожденных особенностей, например, врожденной узости спинномозгового канала, или приобретенных в течение жизни заболеваний.
В качестве основной причины развития вертеброгенной шейной миелопатии выступает остеохондроз. При этом заболевании в межпозвоночных дисках постепенно происходят дегенеративно-дистрофические изменения, что со временем приводит к образованию протрузии, а затем и межпозвоночной грыжи. В таких случаях пораженный диск выпячивается и, как правило, это происходит в сторону спинномозгового канала. При отсутствии лечения грыжа склонна постепенно увеличиваться в размерах и тем самым приводить к компрессии проходящих вблизи нее анатомических структур: спинномозговых корешков, позвоночных артерий, спинного мозга. Это и становится следствием развития так называемой дискогенной миелопатии.
Также следствием остеохондроза может становиться разрастание костной ткани тел позвонков с образованием на их поверхности костных выступов, которые называют остеофитами. Они также могут сдавливать нервные корешки, сосуды и влиять на качество работы спинного мозга.
Другим следствием дегенеративных изменений в позвоночнике становится утолщение желтых связок, гипертрофия фасеток, т. е. осложнения остеоартрита, которые также способны провоцировать развитие шейной миелопатии.
Наиболее часто вертеброгенная шейная миелопатия диагностируется у людей старше 50 лет.
Также шейная миелопатия может стать результатом искривления позвоночного столба, в частности кифоза или сколиоза, или же болезни Бехтерева, постепенно поражающей все суставы тела.
Для патологии характерно хроническое течение с постепенным нарастанием выраженности симптомов и моментами обострения. Чаще всего пациенты жалуются на снижение силы мышц шеи, плеч и рук, болезненность в шее, нарушения чувствительности, дрожь в руках.
Сосудистая
Сосудистая или дисциркуляторная миелопатия обусловлена возникновением нарушений кровообращения и поражения кровеносных сосудов, что может быть обусловлено атеросклерозом, тромбозом, венозным застоем и другими изменениями. Повреждение артерий, ответственных за питание шейного отдела спинного мозга, провоцирует атрофию нервных волокон. При этом степень выраженности проявлений нарушения во многом зависит от того, что послужило причиной их развития и возраста больного.
Именно в шейном отделе наиболее высок риск развития сосудистой миелопатии. Основным ее проявлением считается возникновение так называемого феномена Лермитта, сопровождающегося дрожью в шее, способной распространяться до запястья и стоп, во время наклонов головы или отведения ее назад. После окончания приступа дрожи наблюдается слабость. Иногда сосудистая шейная миелопатия становится причиной энцефалопатии.
Посттравматическая
Этот вид шейной миелопатии является следствием получения травм, приведших к поражению спинного мозга. Это могут быть переломы, в том числе компрессионные, вывихи, удары, которые спровоцировали смещение, компрессию, травмирование нервов, кровеносных сосудов или спинного мозга. Подобное может сопровождаться параличом, снижением чувствительности в соответствующих уровню поражения участках тела, нарушением функционирования внутренних органов.
Карциноматозная
Как следует из названия, данный вид шейной миелопатии становится результатом формирования доброкачественных или злокачественных новообразований, метастаз в позвоночнике, спинном мозге или окружающих тканях. При достижении определенных размеров они могут механически сдавливать спинной мозг, приводить к нарушению его питания и тем самым провоцировать развитие характерного для шейной миелопатии симптомокомплекса.
Наиболее часто причиной возникновения карциноматозной миелопатии являются лимфома, лейкемия, гемангиомы позвоночника и некоторые другие опухоли.
Инфекционная
Как уже говорилось, инфекционные заболевания так же могут выступать причиной развития шейной миелопатии. Она способна возникать в связи с перенесением энтеровирусных инфекций, туберкулеза, герпетической инфекции, остеомиелита позвоночника, болезни Лайма и некоторых других болезней.
Как правило, изначально больных беспокоят характерные для инфекционного заболевания симптомы, включая лихорадку, слабость и т. д. Впоследствии они сменяются признаками миелопатии, среди которых особенно часто наблюдается одышка.
При тяжелых вирусных и грибковых поражениях спинного мозга последствия могут быть необратимыми.
Токсическая
Данный вид нарушения возникает при воздействии на организм органических и неорганических нейротоксинов, способных пагубно влиять на нервные клетки. Для токсической шейной миелопатии характерно стремительное развитие, а также возникновение признаков нарушения чувствительности и подвижности. Но поражение спинного мозга в области шейного отдела встречается не так часто, как грудного.
Радиационная
Причиной развития радиационной шейной миелопатии является действие ионизирующего излучения, например, при проведении лучевой терапии при раке гортани или подавлении новообразований, локализованных в области средостения.
Симптомы миелопатии могут возникать только по прошествии 6—36 месяцев после окончания лучевой терапии. Изначально они слабые и склонны периодически исчезать, но их интенсивность постоянно возрастает. Нередко радиационная миелопатия сопровождается дополнительным образованием язв, снижением плотности костной ткани и т. д.
Метаболическая
Нарушения обмена веществ также может приводить к развитию шейной миелопатии. В частности, она может быть осложнением сахарного диабета и других эндокринных патологий.
Демиелинизирующая
Шейная миелопатия – нередкое следствие демиелинизирующих заболеваний, в том числе рассеянного склероза, болезни Бало, болезни Канавана. В таких ситуациях происходит разрушение оболочки, окружающей нервные волокна, что делает их уязвимыми и чувствительными. Это сопровождается нарушением работы соответствующих пораженному нерву органов, например, нарушением зрения, глотания и пр.
Наследственная
Некоторые наследственные заболевания могут становиться причиной развития шейной миелопатии. Одним из них является спастическая параплегия Штрюмеля. В таких случаях наблюдается усиливающаяся со временем слабость в руках, нарушения зрения, координации движений, развитие эпилепсии, задержка психического развития или деменция.
Симптомы шейной миелопатии
Характер проявлений шейной миелопатии во многом зависит от причин ее развития и степени поражения структур спинного мозга. Таким образом, у больного может присутствовать один или целый ряд симптомов следующего характера:
Но подобные нарушения характерны для запущенных, тяжелых случаев. Изначально заболевание проявляется лишь незначительным дискомфортом, который обычно люди принимают за типичную усталость после долгого рабочего дня.
Диагностика
При возникновении признаков шейной миелопатии следует обратиться к неврологу. В ряде случаев при наличии нескольких симптомов уже в ходе опроса пациента врач может заподозрить развитие этого нарушения, особенно если пациент упоминает о получении в недалеком прошлом ударов в область шеи, перенесении конкретных инфекционных заболеваний, наличии определенных хронических заболеваний. В остальных ситуациях бывает крайне сложно дифференцировать шейную миелопатию от других патологий, поскольку характерные для нее нарушения чувствительности, двигательные расстройства, боли сопровождают и ряд других распространенных заболеваний позвоночника.
Тем не менее в обоих случаях пациентам назначается комплексное обследование для оценки состояния позвоночника, спинного мозга, его корешков и сосудов. Эти данные позволят не только диагностировать шейную миелопатию, но и установить причины ее развития, а значит, и найти наиболее эффективный способ для их устранения.
На приеме врач не только проведет тщательный опрос пациента для сбора анамнеза, но и выполнит физикальное обследование, т. е. осмотр. В ходе него оценивается сила рефлексов, мышечный тонус, выраженность двигательных и чувствительных нарушений и т. д.
Далее обязательно назначается ряд инструментальных исследований:
Для получения более полных данных о состоянии здоровья пациента и причинах развития шейной миелопатии может назначаться общий анализ крови и мочи, биохимический анализ крови, анализ спинномозговой жидкости и некоторые другие лабораторные исследования. При обнаружении опухолей для точного установления природы их происхождения проводится биопсия.
После установления причины развития шейной миелопатии невролог может рекомендовать пациенту дополнительно обратиться к эндокринологу, кардиологу, ортопеду, инфекционисту, фтизиатру.
Лечение шейной миелопатии
Поскольку шейная миелопатия является только следствием развития того или иного заболевания, в первую очередь направляют усилия на устранение именно причины ее возникновения. Поэтому характер лечения напрямую зависит от того, что привело к компрессии спинномозговых структур. Оно может заключаться в применении консервативной терапии или проведении хирургического вмешательства. Также пациентам обычно назначается симптоматическая терапия, направленная на уменьшение выраженности проявлений шейной миелопатии и повышение качества жизни, пока основное лечение не даст результатов.
Таким образом, консервативная терапия обычно показана при инфекционной, сосудистой, токсической и метаболической шейной миелопатии. Она может включать:
При вертеброгенной, посттравматической миелопатии, а также отсутствии эффекта от консервативной терапии пациентам может рекомендоваться хирургическое лечение. Вескими основаниями для его проведения являются:
Задачей хирургического лечения является декомпрессия спинного мозга, т. е. устранение сдавливающего его фактора. Поэтому в зависимости от ситуации могут проводиться операции по исправлению деформации позвоночника, обусловленной переломами позвонков, а также дискэктомия и ламинэктомия. При необходимости проводится дренирование образовавшейся и оказывающей влияние на спинной мозг посттравматической кисты, замена удаленного межпозвоночного диска на эндопротез и т. д.
Дискэктомия подразумевает полное или частичное удаление межпозвоночного диска, что показано при образовании в результате прогрессирования остеохондроза или действия травмирующего фактора крупной грыжи, провоцирующей возникновение неврологических нарушений. Операция может проводиться методами с разной степенью инвазивности, но выбор конкретного осуществляется нейрохирургом на основании индивидуальных особенностей пациента. Это:
Если требуется удалить межпозвоночный диск полностью, во время операции его заменяют искусственным имплантом, которых сегодня существует достаточно много видов. Реже используют костный трансплантат, взятый из собственной кости пациента. Прооперированный и соседние сегменты позвоночника могут также фиксироваться специальными металлическими конструкциями, исключающими риск смещения позвонков и повторного развития шейной миелопатии, возможно, с более серьезными последствиями. В таких ситуациях в точки соединения отростков соседних позвонков монтируются винты, в головках которых есть отверстия. В них пропускают специальные штанги, надежно фиксирующие позвоночник. Эта методика называется транспедикулярной фиксацией.
При оскольчатых переломах и ряде других ситуаций, когда требуется получить открытый доступ к спинномозговым структурам, для устранения компрессии применяется ламинэктомия. Суть операции состоит в удалении остистого отростка, возможно, дуги, а в отдельных случаях и всего позвонка. Это позволяет создать достаточно обширное пространство для спинного мозга, устранить компрессию кровеносных сосудов и спинномозговых корешков, получить возможность удалить опухоль и т. д. В результате симптомы шейной миелопатии исчезают, а качество жизни пациента повышается. При необходимости позвонки также фиксируются посредством транспедикулярной фиксации или использования других методов.
При необходимости проведения хирургического вмешательства на шейном отделе позвоночника величина разреза имеет большое значение, поскольку не всегда доступ к участку поражения осуществляется через заднюю часть шеи. Нередко хирургу требуется «зайти» спереди, использовав передне-боковой доступ.
Таким образом, с шейной миелопатией может столкнуться каждый и эффективных профилактических мер, позволяющих снизить риск ее развития, не разработано. Поэтому во избежание ее возникновения можно порекомендовать вести здоровый образ жизни, а если нарушение уже сформировалось, следует как можно раньше обращаться за медицинской помощью. В 60% случаев при своевременно проведенном лечении, в том числе оперативном, удается добиться полного или существенного регресса неврологических нарушений. У 20% больных в таком случае состояние не изменяется, но и не ухудшается, а прогрессирование миелопатии наблюдается у 10% больных, прошедших лечение. Но при отсутствии такового заболевание обязательно будет прогрессировать и может стать причиной паралича, инвалидизации и более тяжелых осложнений.
Миелопатия причины, симптомы, методы лечения и профилактики
Миелопатия — это общая неврологическая патология, которая выражается в системном поражении различных участков спинного мозга. Чаще всего проявляется в хронической форме. Может возникнуть в шейном, грудном, поясничном и крестцовом отделах позвоночника. Развивается вследствие расстройств спинномозгового кровообращения, дегенеративных процессов в сосудистой системе, нарушений обмена веществ в разных сегментах позвоночного столба и спинного мозга. Из-за обширности причин болезни в диагнозе уточняется клинический вид миелопатии. Чтобы вылечить заболевание, необходимо обратиться к неврологу за направлением на диагностику или консультацию вертебролога, генетика, фтизиатра, онколога.
Симптомы миелопатии
Признаки болезни представляют собой целый комплекс клинических проявлений, которые одновременно характерны для других неврологических заболеваний. Наиболее точно поставить диагноз возможно только после инструментальных и лабораторных обследований. Симптомы могут быть следующими:
Статью проверил
Дата публикации: 24 Марта 2021 года
Дата проверки: 24 Марта 2021 года
Дата обновления: 03 Ноября 2021 года
Содержание статьи
Причины
Очаг поражения может локализоваться как в области спинного мозга, так и за его пределами — это становится условием для группировки причин на две категории. Причины, затрагивающие спинномозговые участки тела:
Причины, которые локализуются за пределами спинного мозга:
Стадии развития миелопатии
Ввиду общей симптоматики сразу распознать заболевание практически невозможно, поэтому его чаще всего диагностируют при появлении осложнений или нестабильности позвоночника и суставов. Обычно болезнь развивается и прогрессирует в несколько этапов:
Разновидности
Классификация миелопатии составлена, исходя из причин, формы протекания и локации болезни. Всего в медицине существует более 20 разновидностей, отличающихся по клиническим проявлениям, осложнениям и способам лечения.
Миелопатия поясничного отдела позвоночника
Локализуется в области поясницы и крестцового отдела опорно-двигательного аппарата. Симптомы:
Миелопатия шейного отдела позвоночника
Шейный тип (спондилолитический или цервикальный) возникает из-за возрастных дегенераций в позвонках и межпозвоночных дисках, чаще поражает пожилых людей. Признаки:
Формы миелопатии
Хроническая миелопатия
Выделена в отдельный вид из-за широкого распространения. Возникает вследствие заболеваний межпозвоночных дисков и позвонков, острых инфекций, рассеянного склероза, дегенерации спинномозговых корешков и дефицита витамина B12. Для определения болезни проводят соматические и неврологические исследования.
Типы миелопатии по причине развития
Диагностика
Постановка точного диагноза — залог успеха курса лечения и надёжный способ избавиться от боли. Врачи диагностируют болезнь следующими методами:
В сети клиник ЦМРТ возможно пройти обследование по таким методикам:
Очаг в шейном отделе спинного мозга

Поиск
Дифференциальная диагностика очаговых некомпрессионных поражений спинного мозга шейно-грудной локализации
Дифференциальный диагноз некомпрессионного поперечного поражения спинного мозга шейно-грудной локализации включает широкий спектр заболеваний. Диагностика требует тщательного сбора анамнеза, учета особенностей неврологической симптоматики, соматического обследования и анализа результатов магнитно-резонансной томографии. В обзоре рассмотрены особенности клинической и радиологической картины некомпрессионной миелопатии либо миелита при демиелинизирующих (рассеянный склероз, оптикомиелит Девика, идиопатический поперечный миелит), инфекционных (ВИЧ, сифилис, боррелиоз, туберкулез, вирусные миелиты), неопластических, воспалительных (системная красная волчанка, синдром Шегрена, саркоидоз) и сосудистых (инфаркт спинного мозга, артерио-венозная фистула) заболеваниях.
Differential diagnosis of focal no compression injuries of spinal cord cervical-thoracic localization
При возникновении симптомов поперечного поражения спинного мозга первоочередной задачей является исключение компрессии спинного мозга (опухоль, абсцесс, грыжа межпозвонкового диска), что достигается выполнением магнитно-резонансной томографии (МРТ) спинного мозга и позвоночника [1]. Если МРТ не выявляет компрессии спинного мозга, но обнаруживает интрамедуллярное очаговое поражение, дифференциальный диагноз проводится в пределах пяти категорий заболеваний: демиелинизирующие, сосудистые, инфекционные, воспалительные, неопластические [2].
Точных данных о распространенности тех или иных этиологических вариантов миелопатий в литературе нет. По данным C. Marsel и соавторов (неврологическая клиника г. Страсбург, Франция), которые изучили 33 случая некомпрессионной миелопатии, в 27% имел место рассеянный склероз (РС), в 18% — инфаркт спинного мозга, в 9% — параинфекционный миелит, в 6% — острый диссеминирующий энцефаломиелит (ОДЭМ), в 3% — системная красная волчанка (СКВ), в 3 % — оптикомиелит Девика, в 15% этиологию миелопатии установить не удалось [3].
В целом, наиболее часто очаговое поражение спинного мозга наблюдается при РС, распространенность которого в европейских странах достигает 30 случаев на 100 000 взрослого населения, а очаги в спинном мозге обнаруживаются в 60-90% случаев [4]. Остальные причины миелитов/миелопатий встречаются в десятки раз реже, а для некоторых форм (туберкулема спинного мозга, нейроборрелиоз, синдром Шегрена) имеются описания лишь единичных случаев [5].
Рассеянный склероз (РС) – это хроническое прогрессирующее аутоиммунное заболевание центральной нервной системы (ЦНС) с поражением белого вещества головного и спинного мозга; поперечный миелит является первым симптомом РС приблизительно в половине случаев [6]. Расстройства обычно асимметричные, негрубые, преимущественно либо двигательные, либо чувствительные, имеют ремитирующий характер; типичны нарушения функции тазовых органов. При локализации очагов в задних столбах на шейном уровне патогномоничны симптом Лермитта (парестезии, возникающие при движениях в шейном отделе и распространяющиеся вдоль позвоночника в ноги) и «синдром сенсорно бесполезной руки» (изолированная утрата проприоцептивного чувства в руках) [2].
При сканировании спинного мозга единичный или множественные очаги выявляются у большинства пациентов с РС, как правило, наряду с церебральными очагами; однако в 5–24% случаев спинальные очаги могут быть изолированными [7]. Наиболее часто очаги локализуются на шейном уровне [8]. В типичных случаях очаг занимает по длиннику менее 2-х сегментов спинного мозга, по поперечнику располагается в белом веществе задних и боковых столбов, не распространяясь на центральные отделы белого вещества, редко вызывая локальное утолщение спинного мозга [9]. Очаги асимметричные и нередко бессимптомные, что отличает их от почти всегда симптомных очагов при других воспалительных заболеваниях [2]. Визуализация спинного мозга обладает большей специфичностью в диагностике РС в сравнении с МРТ головного мозга, поскольку у здоровых лиц, в том числе в пожилом возрасте и при артериальной гипертензии, очаги в спинном мозге (в отличие от головного мозга) практически никогда не обнаруживаются [10, 11]. Основополагающими для диагностики РС являются критерии МакДональда, очередной пересмотр которых произошел в2010 г. [12].
Оптикомиелит Девика (ОМ) – редкое (1-2% среди всех демиелинизирующих заболеваний ЦНС) идиопатическое воспалительное заболевание, отличающееся преимущественным поражением зрительных нервов и спинного мозга с относительной сохранностью головного мозга [13]. Оптический неврит и миелит чаще возникают с временным интервалом, который может составлять месяцы, годы и даже десятилетия. Миелит, в отличие от наблюдаемого при РС, является обычно более тяжелым, с острым (на протяжение часов-дней) развитием симметричных грубых двигательных, чувствительных и сфинктерных нарушений. Типичными симптомами являются пара- либо квадрипарез, пароксизмальные мышечные спазмы, радикулярная боль, симптом Лермитта [14]. У 77 – 88% больных после атаки миелита имеет место частичное восстановление двигательных функций, однако полный регресс не характерен.
МРТ, выполненная в острую фазу миелита, выявляет обширный непрерывный очаг поражения спинного мозга, который локализуется центрально и распространяется по длиннику более чем на 3 позвоночных сегмента; в острый период спинной мозг отечный, очаг в течение нескольких месяцев может накапливать контрастное вещество [15]. Изменения на МРТ головного мозга либо отсутствуют, либо являются неспецифическими и асимптомными. В2006 г. были предложены диагностические критерии ОМ [16], которые учитывают наличие в сыворотке крови антител к аквапорину 4 (NMO-IgG), имеющих высокую специфичность (> 90%) и чувствительность (>70%) для ОМ.
Идиопатический поперечный миелит (ПМ) – это редкое (единичные случаи на на 1 миллион жителей в год) идиопатическое монофазное заболевание, возможно, возникающее вследствие дизрегуляции иммунных механизмов, или на фоне постинфекционной либо поствакцинальной мимикрии [17, 18]. Рабочая группа по изучению поперечного миелита (Transverse Myelitis Consortium Working Group) разработала критерии диагноза «идиопатический поперечный миелит», позволяющие отличать идиопатический ПМ от так называемого «болезнь-ассоциированного поперечного миелита», т.е. миелита, вторичного по отношению к основному заболеванию [18]. Критерии, подтверждающие диагноз, следующие: развитие чувствительных, двигательных или вегетативных нарушений, свойственных поражению спинного мозга; двусторонность симптомов и признаков (не обязательно симметричность); четко определяемый уровень нарушения чувствительности; исключение методами нейровизуализации (МРТ, миелография) экстра-аксиальной компрессии спинного мозга (КТ позвоночника не является адекватным методом); наличие воспаления в спинном мозге, подтвержденного плеоцитозом или повышением индекса JgG в анализе цереброспинальной жидкости (ЦСЖ) либо накоплением гадолиния при проведении МРТ (если на момент развития симптомов критерии воспаления не подтверждаются, то с целью их подтверждения МРТ и люмбальная пункция могут быть выполнены повторно спустя 2-7 дней после дебюта заболевания); прогрессирование с достижением максимальной выраженности проявлений в интервале между 4 часами и 21 сутками после появления симптомов. Критериями, исключающими диагноз, являются те признаки, которые с большой вероятностью указывают на вторичный характер миелита.
К категориям ПМ относят продольный распространенный поперечный миелит, острый частичный поперечный миелит и острый полный поперечный миелит. На МРТ спинного мозга при остром частичном или полном ПМ обнаруживается асимметричное или симметричное поражение спинного мозга, не превышающее 3 сегментов. При продольном распространенном ПМ поражение спинного мозга превышает 3 спинальных сегмента. Очагов на МРТ головного мозга не выявляется. В литературе имеется описание лишь единичных случаев идиопатического ПМ [19, 20, 21]. Некоторые авторы отдельно выделяют вакцинальный миелит – острый поперечный миелит, возникающий в течение 3 недель после вакцинации как иммунологическая реакция на вакцину против бешенства или оспы [2].
Идиопатический ПМ – это диагноз исключения. В ряде случаев он ставится на той стадии оптикомиелита Девика, когда еще не развился оптический неврит. Вероятно, этот диагноз будет устанавливаться все реже и реже по мере появления новых аутоиммунных маркеров, нейровизуализационных технологий и микробиологических тестов.
Поперечный миелит наиболее часто вызывается вирусной или бактериальной, инфекцией. Тропность к спинному мозгу имеют ДНК-вирусы (группа герпесвирусов), РНК-вирусы (из них вирусы японского энцефалита, клещевого энцефалита, Коксаки А и В, энтеровирусы 70 и 71, полиовирус типы 1, 2 и 3 поражают мотонейроны передних рогов спинного мозга и вызывают острый полиомиелитный синдром), вирусы ВИЧ и HTLV-1. К бактериальным агентам относятся спирохеты (возбудителей сифилиса и боррелиоза), микобактерия туберкулеза. Крайне редко спинной мозг может быть поражен при микоплазменной, грибковой, паразитарной инфекции.
Острый инфекционный миелит протекает на фоне системных проявлений инфекции (лихорадка, менингизм) и воспалительных изменений в ЦСЖ (плеоцитоз, повышение уровня белка). Для подтверждения диагноза обязательно должны быть проведены исследования ЦСЖ: полимеразная цепная реакция (ПЦР) на вирусы (вирус простого герпеса 1 и 2 типов, герпесвирус человека 6 типа, варицелла зостер, цитомегаловирус, Эпштейн-Барр, энтеровирусы, HTLV-1) и борреллию, а также серологическое исследование на ВИЧ, сифилис, боррелиоз, гепатит А и В, микоплазмы, паразиты, HTLV-1, вирусы герпеса [2].
Подострые миелопатии могут быть вызваны ВИЧ, туберкулезом, нейроборрелиозом, вирусом HTLV-1. Для ВИЧ-инфекции характерно развитие прогрессирующей вакуолярной миелопатии (ПВМ), которая является результатом прямого поражения спинного мозга вирусом иммунодефицита человека. ПВМ в большей части случаев сочетается с энцефпалопатией (прогрессирующая деменция, пирамидная и мозжечковая дисфункция), но может развиваться изолированно или преобладать в клинической картине ВИЧ-инфекции. Термин «вакуолярная миелопатия» обусловлен характерным гистологическим признаком — вакуолями, наиболее выраженными в шейном и грудном отделах спинного мозга [21]. Во многих случаях обнаруженная при аутопсии вакуолярная миелопатия при жизни никак не проявляется, клинические проявления ВИЧ-миелопатии наблюдаются у больных с глубоким иммунодефицитом [23]. Постепенно развивается нижний спастический парапарез, сенситивная атаксия, типичны ранние нарушения функций тазовых органов; нарушения чувствительности менее значительны, чем двигательные расстройства, «уровень» чувствительных расстройств не определяется. ПВМ обычно имеет подострое или хроническое прогрессирующее течение. На МРТ спинного мозга обнаруживаются билатеральные симметричные области высокоинтенсивного сигнала в задних столбах спинного мозга [24]. При сопутствующей энцефалопатии на МРТ головного мозга выявляются сливные двусторонние симметричные очаги демиелинизации в перивентрикулярных областях с относительной сохранностью субкортикального белого вещества и структур задней черепной ямки. Очаги Т2-гиперинтенсивные, Т1-изоинтенсивные и не накапливают контрастное вещество [25].
При ВИЧ-инфекции может наблюдаться также картина острого или подострого поперечного миелита, обусловленного вирусом варицелла-зостер, а также эпидуральной или интрадуральной лимфомой. Поражения спинного мозга, сочетающиеся с полирадикулопатией, могут быть вызваны цитомегаловирусом. Кроме того, у больных с ВИЧ-инфекцией может развиваться прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) — быстро прогрессирующее тяжелое демиелинизирующее заболевание ЦНС, вызываемое вирусом JC из группы ДНК-содержащих паповавирусов (название вирус получил по инициалам больного, у которого был впервые выделен в1971 г. [26]. Поражение спинного мозга при ПМЛ обычно развивается на фоне поражения головного мозга, спинальный синдром может маскироваться церебральными двигательными расстройствами. Диагностика обычно не вызывает затруднений, если сделан анализ крови на ВИЧ.
Нейросифилис, или поражение ЦНС бледной трепонемой, наблюдается приблизительно у 3-5% больных сифилисом и может возникать на любой стадии инфицирования, т.е. на стадиях первичного, вторичного и третичного сифилиса [27]. Поражение спинного мозга наиболее часто встречается на стадии третичного сифилиса и носит характер спинной сухотки. Спинная сухотка (tabes dorsalis) представляет собой прогрессирующий дегенеративный процесс, включающий демиелинизацию и воспалительные изменения спинного мозга; развивается у 3-5% больных нейросифилисом, спустя 10-20 лет после заражения [27, 28]. Демиелинизация особенно выражена в задних столбах спинного мозга и в спинномозговых ганглиях, однако со временем могут вовлекаться и клетки передних рогов спинного мозга. Клинические проявления включают постепенно прогрессирующие парестезии и «кинжальные» боли в ногах, отсутствие сухожильных рефлексов, нарушение мышечно-суставного чувства и вибрационной чувствительности в ногах, сенситивную атаксию, эректильную дисфункцию, нарушение функции мочевого пузыря и толстого кишечника, нейродистрофическое изменение суставов (суставы Шарко). Параллельно могут иметь место симптомы поражения головного мозга (припадки, головные боли, нарушение слуха и пр.). На МРТ спинного мозга обнаруживается атрофия задних столбов и продленные гиперинтенсивные в Т2 режиме очаги [28, 29].
Очаговое поражение спинного мозга возможно также при сифилитическом менингомиелите, васкулярном миелите или при механическом сдавлении гуммой, однако существуют лишь единичные описания таких случаев [30, 31]. Диагностику облегчают положительные результаты серологических исследований крови и ликвора.
Хронический нейроборрелиоз — поражение нервной системы, которое развивается спустя месяцы, а иногда и годы после заражения спирохетой Borrelia burgdorferi sensu lato приблизительно у 10% нелеченых больных [32]. На основании клинических симптомов и данных МРТ головного мозга хронический нейроборрелиоз клинически крайне трудно отличить от РС [33]. В то же время поражение спинного мозга при нейроборрелиозе, в отличие от РС, является крайней редкостью [32]. Так, при обследовании 20 пациентов с нейроборрелиозом очаги на МРТ головного мозга были выявлены в 60% случаев, однако в спинном мозге не было выявлено ни одного макроскопического очага [33]. Н. Kuiper сообщает о наличии миелопатии у 3 (15%) из 20 пациентов с установленным диагнозом нейроборрелиоза [34]. Тем не менее, энцефаломиелит (синдромы спастического тетрапареза, спастико-атаксической походки, нарушений мочеиспускания) включен в европейские критерии диагностики позднего нейроборрелиоза [35]. Существует мнение, что в эндемичных по боррелиозу регионах появление любой неврологической симптоматики требует исключения нейроборрелиоза [36]. Диагноз помогает подтвердить эпидемиологический анамнез, анализ сопутствующих симптомов (артралгии, миалгии, лимфаденопатия), серологическкое исследование крови и ЦСЖ, а также «драматический» ответ на антибиотикотерапию с быстрым регрессом неврологической симптоматики [32].
Спинальная интрамедуллярная туберкулема — редкое проявление туберкулеза, является результатом гематогенной диссеминации или инфицирования цереброспинальной жидкости и наблюдается в среднем у 2 из 100 000 больных туберкулезом и в 2% случаев туберкулеза ЦНС [37]. В литературе имеется описание лишь отдельных случаев или серий наблюдений, самая большая из которых насчитывает 10 случаев туберкулемы спинного мозга [38]. Поражение спинного мозга обычно наблюдается на фоне очагов в легких или экстрапульмонарного туберкулеза, проявляясь клинически сочетанием спинального синдрома с признаками инфекционного заболевания (астенический синдром, субфебрильная температура, воспалительные изменения крови и пр.). Туберкулемы спинного мозга обычно локализуются в грудном отделе; картина МРТ спинного мозга зависит от стадии развития туберкулемы (степень созревания капсулы, выраженность центрального некроза). На начальной стадии, пока еще не сформировалась капсула, туберкулема имеет гипоинтенсивный сигнал в Т1 и гиперинтенсивная в Т2 режиме, гомогенно накапливает контрастное вещество; затем, при развитии казеозного некроза, типичными признаками являются утолщение и отек спинного мозга, наличие очага овальной формы, который на Т2-взвешенном изображении выглядит как округлое образование, гиперинтенсивное по окружности со снижением интенсивности сигнала в центре очага — так называемый «симптом мишени» (target sign, англ); наблюдается накопление очагом контрастного вещества по периферии, по типу кольца [37]. Одновременно обнаруживаются увеличение лимфатических узлов средостения и очаги в легких. Диагностика основана на выявлении системного туберкулеза.
Тропический спинальный парапарез или HTLV-1 миелопатия — хроническое воспаление в белом веществе спинного мозга с развитием прогрессирующей миелопатии, характерно исключительно для стран Юго-Восточной Азии [39]. Вероятно, вызывается Т-лимфотропным вирусом человека типа 1. Заболевание характеризуется неуклонно прогрессирующим нижним парапарезом, сенсорными нарушениями и расстройством тазовых функций. Иногда наблюдается развитие оптического неврита. При проведении МРТ у больных с ТСП выявляется отек спинного мозга и высокоинтенсивные очаги, локализованные преимущественно билатерально в задних и боковых столбах спинного мозга, а также в задних рогах спинного мозга; типична также атрофия грудного отдела спинного мозга; в головном мозге также могут обнаруживаться субклинические очаги демиелинизации, сходные с очагами при РС [40]. Нередко сложно дифференцировать это заболевание от первично прогрессирующего РС. Диагностическое значение имеет выявление ретровируса HTLV-I или антител к нему.
Другие воспалительные заболевания.
Острый и подострый миелит может развиться на фоне диффузных заболеваний соединительной ткани и гранулематозных заболеваний, таких, как системная красная волчанка (СКВ), склеродермия, саркоидоз, однако он не является ведущим проявлением этих заболеваний и практически всегда перед развитием миелита возникают классические системные проявления, а также поражение мозга или менингеальных оболочек, как минимум, выявляемое на МРТ [2]. При миелите цереброспинальная жидкость обычно носит воспалительный характер, а на МРТ спинного мозга обнаруживаются накапливающие контрастное вещество очаги.
Системная красная волчанка – это заболевание соединительной ткани, характеризующееся системным иммунокомплексным поражением соединительной ткани и её производных, с поражением сосудов микроциркуляторного русла. Для СКВ типичны нейропсихиатрические проявления (развиваются у 60% больных), тогда как миелит встречается реже [41]. В то же время спинальный синдром может стать первым проявлением заболевания. По данным Gerard Espinosa, изучившего в отделении аутоиммунных заболеваний клиники Барселоны (Испания) 22 случая поперечного миелита при СКВ, миелит наблюдался как первая манифестация болезни в 23% случаев; преобладали женщины молодого возраста (77%) [42]. По данным В. Kovacs, поражение спинного мозга является первым признаком СКВ в 39% случаев, и наблюдается на протяжении первых 5 лет заболевания у 42% пациентов; прогноз в плане восстановления функций плохой и не зависит от активности СКВ [43]. Многие авторы приходят к выводу, что при наличии поперечного миелита пациент в обязательном порядке должен быть обследован на предмет исключения СКВ: обязательны тщательный сбор анамнеза, осмотр, исследование крови на наличие антифосфолипидных антител (волчаночный антикоагулянт, антитела к кардиолипину); в случае выявления антифосфолипидных антител диагноз СКВ весьма подозрителен, и такой пациент должен наблюдаться несколько лет с целью своевременного выявления СКВ [42, 43]. Патогененетическими факторами развития поперечного миелита при СКВ, вероятно, являются васкулит и тромбоз. МРТ спинного мозга при СКВ-миелите обнаруживает патологический сигнал в Т1 и Т2 режимах, расширение спинного мозга. Очаги чаще локализуются в грудном отделе, они длиннее, чем при РС (протяженность их более 4 сегментов) и похожи на очаги при ОМ, сопровождаются отеком и атрофией спинного мозга [42]. На МРТ головного мозга обнаруживаются очаги демиелинации, весьма схожие с очагами при РС [44]. Поскольку СКВ проявляется неврологическими симптомами и МРТ-признаками, типичными для РС, то введен даже термин «волчаночный склероз», который используется для описания похожих на РС клинических случаев [45]. Правильной диагностике способствует использование диагностических критериев СКВ, требующих обнаружение как минимум 4 из 11 признаков [46]: сыпь в скуловой области; дисковидная сыпь; фотосенситивная сыпь; язвы в области носовой или ротовой полости; артриты; серозиты; патология почек (протеинурия); неврологические расстройства (припадки или психозы); патология крови (цитопения); иммунологические нарушения (позитивные LE клетки/антитела к нативной ДНК/антитела Jg к Sm антигену в сыворотке или плазме крои/ложноположительнаый тест на сифилис); антинуклеарные антитела.
Синдром Шегрена – редкая хроническая аутоиммунная экзокринная патология, при которой, помимо двух характерных симптомов (сухой глаз и сухой рот), могут присоединяться патология и других органов. Патология ЦНС наблюдается у 20-25% больных с синдромом Шегрена, но миелит встречается редко, менее чем в 1% случаев; в то же время описаны случаи, когда миелит являлся первой манифестацией синдрома Шегрена [47]. На МРТ спинного мозга при миелите обнаруживаются множественные протяженные сливные очаги, гиперинтенсивные в Т2 режиме и накапливающие контрастное вещество, типичен также выраженный отек спинного мозга; на МРТ головного мозга выявляется перивентрикулярная демиелинизация [48]. Диагностике помогают международные критерии диагноза первичного синдрома Шегрена [49], согласно которым должны быть обнаружены 4 из 6 или 3 из 4 объективных критериев: сухой глаз; сухой рот; объективное подтверждение сухого глаза путем использования специальных тестов (тест Schirmer, тест Rose-Bengal, биопсия слезной железы); гистопатология мелких слюнных желез (фокальный лимфоцитарный сиалоаденит); объективное подтверждение поражения слюнных желез путем сцинтиграфии слюнных желез, сиалографии околоушной железы либо нестимуляционной общей сиалометрии; лабораторные находки (антитела к SS–A и SS–B антигенам, антинуклеарные антитела, ревматоидный фактор).
Саркоидоз — мультисистемная гранулематозная болезнь неизвестной этиологии, распространенность которой составляет, по разным данным, от 10 до 50 на 100 000 населения, почти в три раза чаще встречается у лиц черной расы [50]. При саркоидозе страдают в первую очередь легкие, кожа и глаза. Клинические признаки поражения нервной системы возникают в 5-10% случаев заболевания, хотя есть данные, что при аутопсии диагноз нейросаркоидоз может быть поставлен в 50% случаев [51]. Нейросаркоидоз проявляется в самых различных формах (поражение лицевого и слухового нервов, менингит, припадки, поражение гипофиза и гипоталамуса, гидроцефалия, полиневропатии и пр.), но спинной мозг вовлекается в патологический процесс редко, менее чем у 1% больных с системными проявлениями саркоидоза. Однако среди пациентов с нейросаркоидозом у 10% развивается медленно прогрессирующий парапарез вследствие интрамедуллярной гранулемы [52]. Хотя изолированное поражение нервной системы может наблюдаться в дебюте саркоидоза, но миелопатия крайне редко является изолированным первым проявлением заболевания. В то же время описан случай, когда у пациента со спинальным саркоидозом была ошибочна диагностирована опухоль спинного мозга и произведена субтотальная резекция очага. Последующее патогистологическое исследование биоптата позволило диагностировать саркоидоз спинного мозга [53]. Авторы рекомендуют в тех случаях, когда трудно дифференцировать опухоль и саркоидоз, выполнять хирургическое вмешательство как для декомпрессии спинного мозга, так и для гистологической верификации заболевания. Находки на МРТ спинного мозга весьма разнообразны. МРТ при саркоидозной миелопатии может выявлять фузиформное расширение спинного мозга; очаговые пролонгированные по длиннику спинного мозга очаги линейной формы или округлые очаги, гиперинтенсивные в Т2 режиме, которые могут диффузно накапливать гадолиний и иметь сходство с опухолью спинного мозга; атрофию спинного мозга; накопление контрастного вещества оболочками спинного мозга [54]. Как правило, одновременно выявляются разнообразные изменения и на МРТ головного мозга (перивентрикулярные изменения белого вещества, сходные с находками при рассеянном склерозе; метастазоподобные очаги; образования, имитирующие астроцитому или менингеому; лептоменингеальное расширение); типичным симптомом является накопление контрастного вещества менингеальными оболочками. Диагноз «нейросаркоидоз» — это диагноз исключения, он основан на обнаружении системного саркоидоза в отсутствии других неврологических болезней [52].
Неопластические заболевания спинного мозга.
Интрамедуллярные неопластические образования в спинном мозге могут быть первичными опухолями спинного мозга и метастазами. Интрамедуллярные опухоли встречаются в 4 раза реже экстрамедуллярных, заболеваемость варьирует от 0,2 до 2,5 на 100 000 населения в год [55]. Интрамедуллярные опухоли чаще доброкачественные и медленнорастущие, но по расположению наименее благоприятны с позиций их возможного хирургического удаления. До 95% интрамедуллярных опухолей гистогенетически происходят из нейроглиальных клеток, т.е. являются глиомами, среди них чаще встречаются эпендимомы и астроцитомы. В клинической картине на первое место выходят прогрессирующие двигательные расстройства; как исключение, возможны ремиссии, в основе которых лежат перифокальные реактивные изменения [55]. Боль в спине при интрамедуллярных опухолях не столь типична; чувствительные нарушения, согласно закону эксцентрического расположения длинных проводников, распространяется сверху вниз (нисходящий тип расстройства чувствительности [56]. В случае кровоизлияния или инфаркта в опухоль симптомы могут развиться остро и имитировать острый поперечный миелит. МРТ регистрирует очаг, захватывающий нескольких сегментов спинного мозга, изо- или слабо гипоинтенсивный в Т1 режиме, с неоднородным усилением сигнала от очага в Т2-режиме. Типичен перифокальный отек, инфильтративный рост, увеличение в размерах спинного мозга, чаще с неровными бугристыми краями. При введении контрастного вещества наблюдается его гомогенное или гетерогенное накопление. Типично персистирующее накопление контраста, сохраняющееся месяцами, несмотря на лечение «миелита» кортикостероидами [2]. Однако может наблюдаться атипично низкое контрастирование опухолевого узла, что делает диагностику затруднительной.
Интрамедуллярные метастазы встречаются крайне редко, у 1-2% больных с раком легких, молочной железы, почки, при меланоме. Возможны случаи развития паранеопластической миелопатии – при мелкоклеточном раке легких, раке молочной железы, яичника [2]. Особые диагностические затруднения может вызвать лучевая миелопатия, которая нередко развивается через значительный интервал времени (до 15 лет) после проведения лучевой терапии на область позвоночника и медленно прогрессирует. На МРТ вначале могут обнаруживаться отек спинного мозга и очаги, накапливающие контрастное вещество, позднее развивается атрофия спинного мозга [57]. Обычно поражены и прилежащие позвонки (гиперинтенсивность тела позвонка на Т2 изображениях [2].
Сосудистая миелопатия развивается вследствие инфаркта спинного мозга и при наличии спинальных артерио-венозных мальформаций. Причиной инфаркта спинного мозга служит острая окклюзия передней спинальной артерии, обычно на нижнем шейном или грудном уровнях. Это редкая патология. Клиническая картина соответствует острому поражению передних отделов спинного мозга [58]: внезапно, на протяжении минут, развиваются центральный нижний парапарез (иногда монопарез ноги), который в острой фазе заболевания может быть вялым (спинальный шок), но спустя несколько недель трансформируется в спастический; задержка мочеиспускания, которая постепенно переходит в недержание мочи; снижение болевой и потеря температурной чувствительности. Тактильная и вибрационная чувствительность и способность локализовать раздражитель сохранны. Нередко наблюдают корешковые боли, соответствующие верхнему уровню поражения. Иногда инфаркту спинного мозга предшествуют транзиторные ишемические спинальные атаки. На МРТ спинного мозга выявляется пролонгированный «карандашеобразный» очаг в передних отделах спинного мозга. К трем основным диагностическим критериям инфаркта спинного мозга относятся следующие [59]: внезапное развитие; соответствие неврологических симптомов поражению в бассейне передней спинальной артерии; наличие специфической причины ишемии спинного мозга (операция на аорте; спинальная ангиография; васкулит; кардиогенный или атеросклеротический эмбол; диссекция аорты; гипотензия; протромботическое состояние).
Спинальные сосудистые мальформации — гетерогенная группа диспластических образований сосудистого генеза, часто сочетающихся с врожденными аномалиями других систем и органов. Наиболее частой формой (до 80% всех спинальных сосудистых мальформаций) является спинальная дуральная артерио-венозная фистула, представляющая собой шунт (прямое соединение) между дуральными артерией и веной в толстой мозговой оболочке спинного мозга [60]. Фистула чаще локализуется в грудном и пояснично-крестцовом отделах, питаясь из межреберных и люмбальных артерий, однако описаны случаи, когда артериальная поддержка фистулы происходила из ветвей наружной сонной или позвоночной артерий, шейнореберного ствола [60]. Повреждение спинного мозга носит характер венозной миелопатии и развивается вследствие локальной венозной гипертензии и венозного застоя [61]. Клинически фистула проявляется корешковой болью и медленно прогрессирующим нижним парапарезом, нарушением чувствительности в ногах, нарушением функции мочевого пузыря и кишечника [62]. В 5-15% случаев при декомпенсации или при кровотечении из фистулы наблюдается острое (в течение минут – часов) развитие симптоматики, имитирующее синдром передней спинальной артерии либо миелит. Возможны ремиссии и внезапные эпизоды нарастания симптомов, которые могут возникать при переходе в положение лежа, иногда – во время приема пищи, когда происходит повышение венозного давления, ухудшение венозного оттока крови, нарастают отек и ишемия спинного мозга. Вследствие сходства клинической картины спинальную фистулу часто принимают за опухоль или рассеянный склероз. МРТ спинного мозга выявляет очаг диффузного повышения сигнала на Т2 изображениях, расположенный по длиннику спинного мозга, а также множественные сосудистые «пустоты» вдоль вентральной и дорсальной поверхностей спинного мозга [60]. Для диагностики спинальных дуральных артериовенозных фистул применяют селективную спинальную ангиографию, контрастную болюсную МРТ-ангиографию [61, 62].
Таким образом, для правильной диагностики очагового поражения спинного мозга необходимы тщательный сбор анамнеза, учет особенностей неврологической симптоматики, соматическое обследование, анализы крови и цереброспинальной жидкости, в том числе на предмет выявления ВИЧ, сифилиса и других инфекционных возбудителей. Нередко установить правильный диагноз помогают одновременные находки на МРТ головного мозга.
А.Н. Белова, И.В. Шаленков
Нижегородский научно-исследовательский институт травматологии и ортопедии Минздрава России
Нижегородская государственная медицинская академия
Белова Анна Наумовна — доктор медицинских наук, профессор, руководитель отделения функциональной диагностики ННИИТО
1. Masson, C. Acute transverse myelopathy: inflammatory or ischemic? // Presse Med. — 2005. — Vol. 34, № 12. — P. 869-877.
2. Jacob, A. An approach to the diagnosis of acute transverse myelitis // A. Jacob, B.G. Weinshenker // Semin Liver Dis. — 2008. — Vol. 28, № 1. — P. 105-120.
4. Шмидт, Т.Е. Рассеянный склероз / Шмидт Т.Е., Яхно Н.Н. — М.: Медпресс, 2012.
5. Transverse Myelitis Consortium Working Group. Proposed diagnostic criteria and nosology of acute transverse myelitis // Neurology. — 2002. — Vol. 59. — P. 499-505.
6. Marriot, J. Differential diagnosis and diagnostic criteria for multiple sclerosis: application and pitfalls / J. Marriot, P. O’Conner // C. Lucchinetti, R. Hohlfeld. Multiple sclerosis. Saunders Elsevier. — 2010. — Vol. 33. — P. 42.
7. Ge, Y. Multiple sclerosis: the role of MR imaging // AJNR Am. J. Neuroradiol. — 2006. — Vol. 27, № 6. — P. 1165-1176.
8. Filippi, M. EFNS guidelines on the use of neuroimaging in the management of multiple sclerosis / M. Filippi, M. Rocca, D. Arnold [et al.] // Eur. J. Neurol. — 2006. — Vol. 13. — P. 313.
9. Lycklama, G. Spinal-cord MRT in multiple sclerosis / G. Lycklama, A. Thompson, M. Flippi [et al.] // Lancet Neurol. — 2003. — Vol. 2, № 9. — P. 555-562.
10. Barkhof, F. Spinal cord MRI – clinical applications and technical issues. In: M. Filippi. Diagnosis of MS and monitoring treatment – application of conventional MRI. ECTRIMS 2007 teaching course. — Prague, 2007. — P. 23-28.
11. Montalban, X. MRI criteria for MS patients with clinically isolated syndromes / X. Montalban, M. Tintore, J. Swanton, F. Barkhof [et al.] // Neurol. — 2010. — Vol. 74. — P. 427-434.
12. Polman, C.H. Diagnostic criteria for multiple sclerosis: 2010 revisions to the McDonald criteria / C.H. Polman, S.C. Reingold, B. Banwell [et al.] // Ann. Neurol. — 2011. — Vol. 69, № 2. — P. 292-302.
13. Matiello, M. Neuromyelitis optica / M. Matiello, B. Weinshenker // C.F Lucchinetti, R. Hohlfeld. Multiple sclerosis 3. Saunders Elsevier. — 2010. — P. 258-275.
14. Pittock, S.J. Inflammatory transverse myelitis. Evolving concepts / S.J. Pittock, C.F. Lucchinetti // Cuee Opin. Neurol. — 2006. — Vol. 19. — P. 362-368.
15. Wingerchuk, D.M. The spectrum of neuromyelitis optica / D.M. Wingerchuk, V.A. Lennon, C.F. Lucchinetti [et al.] // Lancet Neurol. — 2007. — Vol. 6. — P. 805-815.
16. Wingerchuk, D.M. Revised diagnostic criteria for neuromyelitis optica / D.M. Wingerchuk, V.A. Lennon, S.J. Pittock [et al.] // Neurology. — 2006. — Vol. 66. — P. 1485-1489.
17. Marriot, J. Differential diagnosis and diagnostic criteria for multiple sclerosis: application and pitfalls / J. Marriot, P. O’Conner // C. Lucchinetti, R. Hohlfeld. Multiple sclerosis. Saunders Elsevier. — 2010. — Vol. 33. — P. 42.
18. Pittock, S.J. Inflammatory transverse myelitis. Evolving concepts / S.J. Pittock, C.F. Lucchinetti // Cuee. Opin. Neurol. — 2006. — Vol. 19. — P. 362-368.
19. Евдошенко, Е.П. Рецидивирующий распространенный поперечный миелит, ассоциированный с антителами к аквапорину-4 / Е.П. Евдошенко, Л.Г. Заславский, С.В. Лапин // Неврологический журнал. — 2011. — Vol. 3. — P. 34-38.
20. Akkad, W. Longitudinally extensive transverse myelitis following vaccination with nasal attenuated novel influenza A(H1N1) vaccine / W. Akkad, B. Salem, J.W. Freeman, M.K. Huntington // Arch. Neurol. — 2010. — Vol. 67, № 8. — P. 1018-1020.
21. Прахова, А.Н. Возможности комплексного диагностического обследования при проведении дифференциальной диагностики воспалительных и опухолевых поражений спинного мозга (два клинических наблюдения) / А.Н. Прахова, Ж.И. Савинцева, А.Ф. Гурчин [и др.] // Журн. неврол. и психиатр. — 2012. — Vol. 9, № 2. — P. 87-94.
22. Petito, C. Vacuolar myelopathy pathologically resembling subacute combined degeneration in patients with acquired immunodefiency syndrome / C. Petito, B. Navia, B. Jordan [et al.] // N. Engl. J. Med. — 1985. — Vol. 312. — P. 874-879.
23. Dal Pan, G.J. Clinicopathologic correlations of HIV-associated vacuolar myelopathy: An autopsy-based case-control study / G.J. Dal Pan, J.D. Glass, J.C. McArthur // Neurology. — 1995. — Vol. 44. — P. 2159-2164.
24. Shimojima, Y.Characteristic spinal MRI findings of HIV-associated myelopathy in an AIDS patient / Y. Shimojima, M. Yazaki, K. Kaneko [et al.] // Intern. Med. — 2005. — Vol. 44, № 7. — P. 763-764.
25. Pandit L. Differential diagnosis of white matter diseases in the tropics: An overview // Ann. Indian. Acad. Neurol. — 2009. — Vol. 12, № 1. — P. 12-21.
26. Major, E.O. Pathogenesis and molecular biology of progressive multifocal leukoencephalopathy, the JC virus-induced demyelinating disease of the human brain / E.O. Major, K. Amemiya, C.S. Tornatore, S.A. Houff, J.R. Berger // Clin. Microbiol. Rev. — 1992. — Vol. 5. — P. 49-73.
27. Chahine, L.M. The changing face of neurosyphilis / L.M. Chahine, R.N. Khoriaty, W.J. Tomford, M.S. Hussain // Intern. J. of Stroke. — 2011. — Vol. 6. — P. 136-143.
28. Pandey S. Magnetic resonance imaging of the spinal cord in a man with tabes dorsalis // J. Spinal. Cord. Med. — 2011. — Vol. 34, № 6. — P. 609-611.
29. Matijosaitis, V. Neurosyphilis manifesting as spinal transverse myelitis / V. Matijosaitis, A. Vaitkus, V. Pauza, S. Valiukeviciene, R. Gleizniene // Medicina (Kaunas). — 2006. — Vol. 42, № 5. —P. 401-405.
30. Tsui, E.Y. Syphilitic myelitis with diffuse spinal cord abnormality on MR imaging. Eur Radiol / E.Y. Tsui, S.H. Ng, L. Chow [et al.] — 2002. — Vol. 12, № 12. — P. 2973-2976.
31. El Quessar, A.Syphilitic spinal cord gumma / El Quessar A., El Hassani R., Chakir N. [et al.] // J. Neuroradiol. — 2000. — Vol. 27, № 3. — P. 207-210.
32. Спирин, Н.Н. Дифференциальнаядиагностика поздних форм нейроборрелиоза с поражением центральной нервной системя / Н.Н. Спирин, Н.С. Баранова, О.А. Фадеева [и др.] // Журн. неврол. и психиат. — 2012. — Vol. 9, № 2. — P. 34-39.
33. Agosta, F. MR Imaging Assessment of Brain and Cervical Cord Damage in Patients with Neuroborreliosis / F. Agosta, M.A. Rocca, B. Benedetti [et al.] // AJNR Am. J. Neuroradiol. — 2006. — Vol. 27, № 4. — P. 892-894.
34. Kuiper, H. Clinical spectrum and incidence of neuroborreliosis in the Netherlands Ned Tijdschr Geneeskd. — 2004. — Vol. 148, № 14. — P. 670-673.
35. Mygland, A. EFNS guidelines on the diagnosis and management of European Lyme neuroborreliosis / A. Mygland, U. Liodtad, V. Fingerle [et al.] // Europ. J. neurol. — 2010. — Vol. 17. — P. 8-16.
36. De Cauwer, H. Motor neuron disease features in a patient with neuroborreliosis and a cervical anterior horn lesion / De Cauwer H., S. Declerck, De Smet J. [et al.] // Acta Clin. Belg. — 2009. — Vol. 64, № 3. — P. 225-227.
37. Lu М. Imaging diagnosis of spinal intramedullary tuberculoma: case reports and literature review // J. Spinal Cord. Med. — 200l. — Vol. 33, № 2. — P. 159-162.
38. Sharma, M.C. Intramedullary tuberculoma of the spinal cord: a series of 10 case / M.C. Sharma, R. Arora, P.S. Deol [et al.] // Clin. Neurol. Neurosurg. — 2002. — Vol. 104, № 4. — P. 279-284.
39. Cabre, P. HTLV-1 and HIV infections of the central nervous system in tropical areas // P. Cabre, D. Smadja, A. Cabié, C.R. Newton // J. Neurol. Neurosurg. Psychiatry. — 2000. — Vol. 68. — P. 550-557.
40. Umehara, F. Abnormalities of spinal magnetic resonance images implicate clinical variability in human T-cell lymphotropic virus type I-associated myelopathy / F. Umehara, H. Nose, M. Saito [et al.] // Neurovirol. — 2007. — Vol. 13, № 3. — P. 260-267.
41. Theodoridou, A. Demyelination in rheumatic diseases / A. Theodoridou, L. Settas // J. Neurol. Neurosurg. Psychiatry. — 2006. — Vol. 77, № 3. — P. 290-295.
42. Espinosa, G. Transverse myelitis affecting more than 4 spinal segments associated with Systemic Lupus Erythematosus: clinical, immunological, and radiological characteristics of 22 Patients / G. Espinosa, A. Mendizábal, S. Mínguez [et al.] // Semin. Arthritis. Rheum. — 2010. — Vol. 39, № 4. — P. 246-256.
43. Kovacs, B. Transverse myelopathy in systemic lupus erythematosus: an analysis of 14 cases and review of the literature / B. Kovacs, T.L. Lafferty, L.H. Brent [et al.] // Ann. Rheum. Dis. — 2000. — Vol. 59. — P. 120-124.
44. Алиферова, В.М. Сопоставление данных МРТ-исследования головного мозга при рассеянном склерозе и системной красной волчанке / В.М. Алиферова, Ю.Н. Лисицина // Бюлл. сиб. мед. — 2008. — Vol. 5. — P. 228-230.
45. Bluestein, H.G. Neuropsychiatric disorders in systemic lupus erythematosus // Lahita R.G., ed. Systemic lupus erythematosus. — New York: Wiley, 1987. — P. 593-614.
46. Tan, E.M. Thq 1982 revised criteria for the classification of system lupus erythematosus / E.M. Tan, A.S. Cohen, J.F. Fries [et al.] // Arthritis Rheum. — 1982. — Vol. 25, № 11. — P. 1271-1277.
47. Yamamoto, T. Acute longitudinal myelitis as the initial manifestation of Sjögren’s syndrome / T. Yamamoto, S. Ito, T. Hattori // Neurol. Neurosurg. Psychiatry. — 2006. — Vol. 77, № 6. — P. 780.
48. Arai, C. A case of Sjögren’s syndrome with subacute transverse myelitis as the initial manifestation / C. Arai, R. Furutani, M. Ushiyama // Rinsho Shinkeigaku. — 2002. — Vol. 42. — P. 613-618.
49. Vitali, C. Classification criteris for Sjogren’s syndrome: a revised version of the European criteria proposed by the American-European Consensus Group / C. Vitali, S. Bombardiery, R. Jonsson [et al.] // Ann. Rheum. Dis. — 2002. — Vol. 61, № 6. — P. 554-558.
50. Hosoda, Y. Epidemiology of sarcoidosis: New frontiers to explore / Y. Hosoda, S. Sasagawa, N. Yasuda // Curr. Opin. Pulm. Med. — 2002. — Vol. 8. — P. 424-442.
51. Dumas, J.L. Central nervous system sarcoidosis: Follow-up at MR imaging during steroid therapy / J.L. Dumas, D. Valeyre, C. Chapelon-Abric [et al.] // Radiology. — 2000. — Vol. 214. — P. 411-420.
52. Ayala, L. Intramedullary sarcoidosis presenting as incomplete paraplegia: case report and literature review / L. Ayala, D.B. Barber, M.R. Lomba, A.C. Able // J. Spinal. Cord. Med. — 2000. — Vol. 23, № 2. — P. 96-99.
53. Yukawa, Y. Isolated spinal cord sarcoidosis mimicking an intramedullary tumor / Y. Yukawa, F. Kato // J. Spinal. Disord. — 1999. — Vol. 12, № 6. — P. 530-533.
54. Zylberberg, F. MRI findings of CNS sarcoidosis / F. Zylberberg, E. Meary, D. Cerez [et al.] // J. Radiol. — 2001. — Vol. 82, № 6. — P. 623-631.
55. Park, A.Y. A Spinal Cord Astrocytoma and Its Concurrent Osteoblastic Metastases at the Time of the Initial Diagnosis: a Case Report and Literature Review / A.Y. Park, H. Kim, T-S. Chung, C-S. Yoon, Y.H. Ryu [et al.] // Korean. J. Radiol. — 2001. — Vol. 12, № 5. — P. 620-625.
56. Ebner, F.H.Management of intramedullary spinal cord lesions: interdependence of the longitudinal extension of the lesion and the functional outcome / F.H. Ebner, F. Roser, M. Falk, S. Hermann, J. Honegger, M. Tatagibа // Eur. Spine. J. — 2010. — Vol. 19, № 4. — P. 665-669.
57. Wang, P.Y. MR imaging in radiation myelopathy / P.Y. Wang, W.C. Shen, J.S. Jan // AJNR Am. J. Neuroradiol. — 1992. — Vol. 13, № 4. — P. 1049-1055.
58. Frohman, E. Transverse Myelitis / E. Frohman, D. Wingerchuk // N. Engl J. Med. — 2010. — Vol. 363. — P. 564-572.
59. Masson, C. Acute transverse myelopathy: inflammatory or ischemic? // Presse. Med. — 2005. — Vol. 34, № 12. — P. 869-877.
60. Park, K-W. Spinal Dural Arteriovenous Fistula with Supply from the Lateral Sacral Artery-Case Report and Review of Literature // K-W. Park, S. Park, S-B. Im [et al.] // Korean Neurosurg. Soc. — 2009. — Vol. 45, № 2. — P. 115-117.
61. Eskandar, E.N. Spinal dural arteriovenous fistulas: experience with endovascular and surgical therapy / E.N. Eskandar, L.F. Borges, R.F. Budzik [et al.] // J. Neurosurg. — 2002. — Vol. 96. — P. 162-167.
62. Koch, C. Spinal dural arteriovenous fistula // Curr. Opin. Neurol. — 2006. — Vol. 19. — P. 69-75.