после трансплантации костного мозга держится температура
После трансплантации костного мозга держится температура
При трансплантации гемопоэтических стволовых клеток крови развивается тяжелое иммунодефицитное состояние, продолжительность и степень выраженности которого зависят от вида трансплантации гемопоэтических стволовых клеток крови (аутологичная, аллогенная), режима кондиционирования, совместимости по HLA-системе донора и реципиента, протокола профилактики острой РТПХ.
Вероятность возникновения инфекционных осложнений увеличивается при продолжительном периоде гранулоцитопении на ранних этапах после трансплантации гемопоэтических стволовых клеток крови и лимфопении в позднем периоде, а также при тяжелой степени клинических проявлений острой или хронический РТПХ.
Восстановление иммунитета происходит медленнее после алло-трансплантации гемопоэтических стволовых клеток крови (особенно неродственной), чем после ауто-трансплантации гемопоэтических стволовых клеток крови. Степень иммуносупрессии усиливается при включении в режим кондиционирования ТОТ, флударабина, проведении алло-трансплантации гемопоэтических стволовых клеток крови с несоместимостью по HLA-антигенам (особенно гаплоидентичной) и Т-клеточным «истощением» трансплантата.
Продолжительное состояние иммунодефицита у больных после трансплантации гемопоэтических стволовых клеток крови увеличивает вероятность развития инфекционных осложнений бактериальной, вирусной, протозойной и грибковой этиологии, которые возникают на любом этапе после трансплантации гемопоэтических стволовых клеток крови (сепсис, пневмония, инфекции урогенитальной системы, желудочно-кишечного тракта, ЦНС и др.).
Течение инфекционных осложнений имеет свои особенности в зависимости от периода после трансплантации гемопоэтических стволовых клеток крови: до появления признаков приживления трансплантата, в раннем периоде (до 100 дней) и позднем периоде (после 100 дней) после трансплантации гемопоэтических стволовых клеток крови.
Эпизоды фебрильной лихорадки характерны для периода до начала признаков «приживления» аллогенных (аутологичных) ГСК и, как правило, возникают после режима кондиционирования на фоне агранулоцитоза. Это может быть ранним проявлением инфекционных осложнений. Фебрильное повышение температуры тела к 10-му дню после трансплантации иногда свидетельствует о развитии иммунологической реакции (особенно при алло-трансплантации гемопоэтических стволовых клеток крови), известной как синдром «приживления» трансплантата — engraftment syndrome.
Дифференциальную диагностику проводят на основании динамики изменения показателей крови и регулярного тестирования всех биологических жидкостей реципиента (кровь, моча, стул, слюна) на наличие признаков инфекции.
Риск возникновения инфекции в раннем периоде после трансплантации гемопоэтических стволовых клеток крови увеличен при развитии мукозитов различной степени тяжести после назначения режима кондиционирования вследствие имеющейся колонизации бактериями желудочно-кишечного тракта, а также при наличии локальной грибковой или вирусной инфекций, возможной реактивации у больного латентной инфекции, постановки центрального катетера. Однократное повышение температуры тела более 38,3 °С, неоднократное повышение в течение 24 ч или температура 38 °С в течение одного часа является показанием к эмпирическому назначению антибактериальной терапии.
Как правило, для профилактики инфекционных осложнений перед началом режима кондиционирования и до момента восстановления содержания гранулоцитов (более 0,5 • 10 9 /л) в крови больным производят специальную обработку (деконтамина-цию) кишечника назначением внутрь неабсорби-руемых антибиотиков: гентамицин в дозе 40— 80 мг/сут либо фторхинолоны: ципрофлоксацин в дозе 10 мг/кг в сутки, метронидазол по 20—30 мг/кг в сутки. С момента приживления трансплантата присоединяют противовирусные препараты: ацик-ловир в дозе 250 мг/м2; для профилактики протозойной инфекции, вызванной Pneumocystis cari-nii, — бисептол по 5 мг/кг в сутки (по триметоприму) 3 раза в неделю.
Основные осложнения миелотрансплантации
| Ранние (менее 100 дней) | Поздние (после 100 дней) |
| 1. Инфекционные. 2. Геморрагические. 3. Поражение желудочно-кишечного тракта. 4. Кардиоваскулярные. 5. Легочные. 6. Веноокклюзионная болезнь. 7. Нефрологические. 8. Острая РТПХ. 9. Отторжение (неприживление) СКК донора | 1. Инфекционные. 2. Хроническая РТПХ. 3. Последствия кондиционирования (катаракта, полигландулярная эндокринная недостаточность, обструктивные заболевания легких). 4. Рецидив основного заболевания. 5. Вторичные опухоли. 6. Задержка роста (у детей) |
После приживления ГСК, несмотря на количественное восстановление гранулоцитов и лейкоцитов, продолжает существовать комбинированная количественная и функциональная недостаточность Т- и В-лимфоцитов. Период дисбаланса увеличивается при выполнении алло-трансплантации гемопоэтических стволовых клеток крови, особенно с Т-клеточным «истощением» трансплантата и трансплантации от частично совместимого или гаплоидентичного донора ГСК. Проявлением этого состояния является нарушение функции Т-хелперов, частично цитотоксических Т-лимфоцитов и изменение синтеза иммуноглобулинов В-клетками.
При восстановленном количестве гранулоцитов их дисфункция также существует, происходит нарушение хемотаксиса и фаложнений, в том числе клиническими проявлениями асептического менингита, механизм которого неясен.
Грибковые инфекции остаются одной из основных причин смерти больных после трансплантации гемопоэтических стволовых клеток. До настоящего времени не решена задача выбора оптимального способа профилактики осложнений грибковой этиологии ввиду выраженной токсичности используемых препаратов.
Возбудителями грибковой инфекции наиболее часто являются различные виды рода Candida и Aspergillus. Вероятность возникновения аспергиллеза у больных после алло-трансплантации гемопоэтических стволовых клеток в настоящее время достигает 20 %, а количество летальных осложнений, связанных с этой инфекцией, равно 90 %.
При глубоких микозах (кандидоз, аспергиллез и т. д.) используются амфотерицин В (фунгизон, амфоцил, абельцет, липосомальная форма — амбизом), а также итраконазол, флуконазол, флюцитозин. Применение амбизома как менее токсичного из них является оптимальным.
В настоящее время получены противогрибковые средства, превышающие по эффективности и минимальному количеству токсических проявлений перечисленные препараты (каспофунгин, вориконазол), что позволяет надеяться на возможность эффективной профилактики и лечения осложнений грибковой природы у больных после трансплантации гемопоэтических стволовых клеток.
Важным способом профилактики развития грибковых осложнений, особенно аспергиллеза, является назначение больному стерилизованной пищи после трансплантации гемопоэтических стволовых клеток и помещение в специальные палаты, оснащенные установками для фильтрации воздуха (НЕРА-фильтры).
Развитие вирусных осложнений в первую очередь ассоциировано с группой вирусов герпеса (HHV6, HSV, VZV), в которую входит и цитомегаловирус (CMV). У 60—70 % больных, бывших серопозитив-ными по CMV-инфекции до трансплантации, возможна реактивация вируса на фоне глубокого иммунодефицита после любого вида ТГСК с развитием энтероколита, гепатита, ретинита, миелита, тяжелой CMV-пневмонии. Реактивация CMV-инфекции может сопровождаться миелосупрессией вплоть до полного отторжения трансплантата.
Частота развития CMV-инфекции связана с особенностями восстановления иммунитета после различных видов ТГСК (аутологичная, аллогенная родственная и неродственная с различной степенью совместимости по HLA-систе-ме). Риск возникновения CMV-инфекции увеличивается при алло-ТГСК от неродственного или гаплоидентично совместимого донора, трансплантации серопозитивному реципиенту ГСК от серонега-тивного донора или серонегативному реципиенту ГСК от серопозитивного донора, а также в случае применения Т-клеточного «истощения» трансплантата.
До появления эффективных противовирусных препаратов (ганцикловир, фоскарнет), иммуноглобулинов, являющихся специфическими CMV-нейтра-лизующими антителами (цитотект), смертность от CMV-инфекции при трансплантации гемопоэтических стволовых клеток составляла до 20 %.
Существенной мерой профилактики CMV-инфекции остается скрининг доноров КМ/ПСКК и доноров компонентов крови на наличие носительства CMV-инфекции и использование лейкоцитарных фильтров при переливании эритроцитной и тромбо-цитной массы.
Вирусная инфекция после трансплантации гемопоэтических стволовых клеток может быть следствием присоединения респираторно-синцити-ального вируса, риновируса, вируса параинфлюэн-цы. Особое клиническое значение имеют осложнения, связанные с аденовирусами (поражение желудочно-кишечного тракта, геморрагический цистит).
Для профилактики вирусных осложнений необходимо назначение ацикловира в профилактической дозе в течение длительного периода после трансплантации гемопоэтических стволовых клеток (6—12 мес).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Осложнения после трансплантации костного мозга
Сегодня к трансплантации костного мозга прибегают в ходе лечения как гематологических заболеваний, так и онкологических. Эта операция спасла жизни многим пациентам.
Существует ряд специализированых клиник на базе ультрасовременного медицинского оборудования, где выполняется трансплантация.
Немного о трансплантации
Без костного мозга невозможен процесс возникновения и активной деятельности кровяных телец. Если костный мозг поражен тяжелым недугом, он не в состоянии справляться со своими функциями. Патология костного мозга становится причиной потери контроля за накоплением во всей кровеносной системе еще незрелых клеток. Их избыток подавляет основные функции клеток зрелых. В результате организму не хватает кровяных телец трех типов. Трансплантация костного мозга в Израиле дает возможность восстановления всех функций.
Осложнения
Сложная процедура проводится несколькими этапами, и на каждом из этапов возможны тяжелые осложнения. Не исключены и побочные эффекты.
Сложности возникают уже на первом этапе, когда пациенту назначают химиотерапию в больших дозах и радиотерапию. Данные процедуры часто вызывают такие побочные эффекты, как изнуряющая тошнота, частая рвота, сонливость. Может измениться состав крови, начаться выпадение волос. У некоторых пациентов во рту появляются болезненные язвы. Сила действия побочных эффектов нагнетается высокой дозой препаратов.
Пересадка костного мозга, побочные эффекты во время которой выражаются аллергией и анафилактическим шоком, очень опасны. Их причина в контакте иммунной системы с чужими донорскими клетками. Для снижения риска пацинтам перед оперативным вмешательством вводят противовоспалительные препараты и антигистаминные лекарства.
Из-за возможного введения в ходе операции большого количества жидкости возможно развитие недостаточности, сердечной и почечной. Избежать этого помогает тщательное предоперационное обследование.
Этап нейропении осложнен инфекционными заболеваниями из-за пониженного иммунитета. Именно поэтому необходима профилактика препаратами против вирусов и антибиотиками. Также пациенту показаны противогрибковые средства.
Даже после применения качественных профилактических средств в течение недели может быть повышенная температура. Чтобы не травмировать воспаленную слизистую пищеварительного тракта, пациенту питательные вещества вводят непосредственно в кровь.
Самым опасным осложнением после операции в фазе приживления является негативная реакция донорских клеток по отношению к клеткам пациента. Причем проблема может возникнуть как сразу после пересадки, так и через достаточно длительное время. «Бунтует» печень, кожные покровы, органы пищеварения. Кожные высыпания могут переродиться в тяжелое поражение, свойственное, например, сильным ожогам.
Для борьбы с подобной проблемой применяют лекарства, способные подавлять иммунитет. К ним относят иммунодепрессанты, стероидные гормоны, средства против рака.
Но у негативной реакции имеется и положительый фактор. Она эффективна против лейкемии. Созданная иммунная система начинает бороться с оставшимися клетками рака, то есть трансплант вступает в противодействие с лейкемией.
Врачи проводят все необходимые мероприятия во избежание осложнений и для уменьшения негативных последствий, но риск остается. Поцедура пересадки очень сложна, чтобы застраховаться на сто процентов.
После трансплантации возможно развитие нежеланного бесплодия. Некоторым пациентам рекомендуют сохранять сперму и яйцеклетку, забранную до начала лечебного курса.
Помимо перечисленных проблем возможна вероятность развития вторичного недуга. Успешная пересадка костного мозга иногда через несколько лет заканчивается вспышкой вторичного рака, но, к счастью, таких случаев совсем немного.
В настоящее время поддерживающая терапия значительно усовершенствована, что существенно повышает все шансы на возможное выживание, продление жизни тяжелобольным пациентам.
В лечении применяются сильнейшие антибиотики, проводится качественная профилактика против реакции на отторжение имплантата. При повышенных дозах стволовых клеток прогноз на жизнь заметно улучшается, но их переизбыток провоцирует неприятие иммунной системой имплантата.
Конечно, немаловажно состояние больного до проведения пересадки и его возраст. Молодой организм легче переносит процедуру. Прогноз молодого человека на выживание более оптимистичен.
Трансплантация костного мозга и стволовых клеток
Общие принципы
ОБЩАЯ ИНФОРМАЦИЯ О СТВОЛОВЫХ КРОВЕТВОРНЫХ КЛЕТКАХ
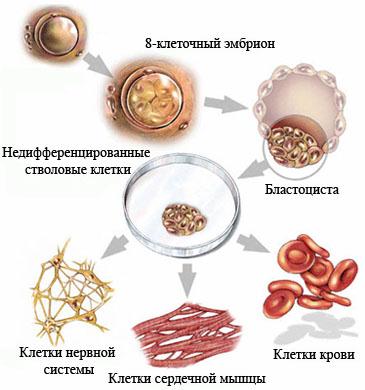
Недифференцированная стволовая клетка, происходящая из бластоцисты, является родоначальницей всех клеток организма, в том числе и стволовой кроветворной клетки (СКК).
Основными свойствами стволовой кроветворной клетки являются возможность дифференцироваться в направлении любого из ростков кроветворения и способность к самоподдержанию.
 Колонии стволовых кроветворных клеток (электронная микроскопия) | 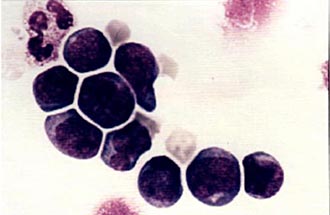 Мононуклеарная фракция, обогащенная клетками CD34, окрашена по Маю-Грюнвальду с докраской по Гимзе. Стволовые клетки, несущие маркер CD34, внешне напоминают малые и средние лимфоциты. |
ИСТОРИЧЕСКАЯ СПРАВКА
Первые работы, посвященные терапевтическому использованию костного мозга, были выполнены в последней декаде XIX века, независимо друг от друга Brown-Sequard, d»Arsonval, Fraser, Billings и Hamilton, которые применяли экстракт костного мозга животных для лечения больных различными видами анемий. Несмотря на положительный эффект, отмеченный всеми авторами, в течение последующих пятидесяти лет использование данной методики носило спорадический характер и не выходило за рамки клинического эксперимента до 1937 года когда Schretzenmayr впервые произвел парентеральное (внутримышечное) введение костного мозга, а в 1939 году Osgood выполнил первое внутривенное введение костного мозга.
Результаты экспериментальных исследований привели клиницистов к идее использования ТКМ при заболеваниях, связанных с поражением костного мозга (лейкозы, апластическая анемия), а также при радиационных воздействиях и проведении химиотерапии, однако основные теоретические и практические проблемы проведения ТКМ удалось преодолеть в 60-е годы. С этого времени ТКМ является одним из методов лечения различных заболеваний крови и иммунной системы.
ВИДЫ ТРАНСПЛАНТАЦИИ КОСТНОГО МОЗГА
Разновидностью АллоТКМ является сингенная ТКМ (трансплантация от однояйцевого близнеца).
ПОКАЗАНИЯ К ТРАНСПЛАНТАЦИИ КОСТНОГО МОЗГА
С развитием появлением колониестимулирующих факторов и развитием технологий клеточной сепарации с 70-х годов для получения гемопоэтических клеток крови вмести костного мозга стали использовать стволовые клетки периферической крови.
Применение клеточных сепараторов значительно упростило проведение процедуры получения стволовых клеток крови, уменьшило число осложнений связанных с дачей наркоза и травматическим повреждения костной ткани.
Еще одним потенциальным источником СКК является пуповинная кровь, основным преимуществом которой является меньшая иммуногенность, однако малое количество стволовых клеток в материале ограничивает ее применение и используется преимущественно в педиатрии или у пациентов с массой тела до 50 кг.
Методика проведения миелотрансплантации различается в зависимости от ее вида (аллогенная или аутологичная), нозологической формы заболевания и ряда других факторов.
ПРАКТИЧЕСКИЕ АСПЕКТЫ МИЕЛОТРАНСПЛАНТАЦИИ
ОПРЕДЕЛЕНИЕ ПОКАЗАНИЙ И ПРОТИВОПОКАЗАНИЙ
Наиболее частыми показаниями к ТКМ/ТСКК являются онкогематологические и гематологические заболевания (лейкозы, злокачественные лимфомы, апластическая анемия, врожденные иммунодефициты и нарушения метаболизма).
Чаше всего ТКМ или ТСКК проводится во время полной ремиссии (ПР), частичной ремиссии (ЧР) или при рецидиве опухоли, чувствительном к химиотерапии. При первичной резистентности к цитостатической терапии результаты ТКМ резко ухудшаются, поэтому в этих случаях операция выполняется относительно редко.
ВЫБОР ДОНОРА
Совместимость костного мозга определяет результаты АллоТКМ. Родственными донорами считаются совместимые по системе HLA братья или сестры реципиента (сибсы). Родители и дети гаплоидентичны (имеют одну общую хромосому из каждой пары, т. е. совпадают между собой на 50%) и не могут быть донорами аллогенного костного мозга. Совместимые сибсы имеются лишь у 20-25% больных, в связи с чем в последние 10 лет активно внедряется АллоТКМ от неродственных HLA-идентичных доноров или частично совместимых родственных доноров.
МОБИЛИЗАЦИЯ, ОБРАБОТКА И ИНФУЗИЯ СТВОЛОВЫХ КРОВЕТВОРНЫХ КЛЕТОК
 А) |  Б) |
А) специальный сосуд (дюар) с жидким азотом для транспортировки контейнеров с костным мозгом
Б) извлеченный из сосуда контейнер с костным мозгом
Инфузия аллогенного, размороженного аутологичного костного мозга или СКК периферической крови проводится внутривенно, капельно после предварительного введения антигистаминных препаратов для предотвращения аллергических реакций.
ИММУНОСУПРЕССИВНАЯ ТЕРАПИЯ (КОНДИЦИОНИРОВАНИЕ)
ПРОФИЛАКТИКА И ЛЕЧЕНИЕ ОСЛОЖНЕНИЙ ПЕРИОДА ЦИТОПЕНИИ
Вскоре после окончания кондиционирования и введения СКК у больного развивается аплазия костного мозга (период отсутствия костного мозгового кроветворения), которая проявляется практически полным отсутствием клеток крови (панцитопенией) и продолжается в среднем 4 недели. Этот период опасен развитием тяжелых осложнений (инфекции, кровоточивость и т.д.).
Основную опасность в периоде цитопении представляют инфекционные осложнения, поэтому их профилактика, своевременное и адекватное лечение являются необходимым условием успешной ТКМ.
Также по показаниям проводится переливание компонентов крови (эритроцитарная масса, тромбомасса, плазма).
Приживление костного мозга или СКК периферической крови констатируют по результатам анализа костного мозга. Вскоре количество нейтрофилов достигает > 0,5*109/л, а тромбоцитов > 20>
Побочные эффекты трансплантации стволовых клеток
Многие проблемы, возникающие сразу после процедуры трансплантации стволовых клеток, связаны с уничтожением костного мозга лекарствами или радиацией непосредственно перед пересадкой стволовых клеток. Прочие нежелательные явления по сути являются побочными эффектами кондиционирования (одного из этапов трансплантации).
Ниже представлен далеко не полный перечень возможных нарушений, поэтому о любых проблемах или изменениях в вашем состоянии необходимо сразу же сообщать врачу. Некоторые побочные эффекты могут угрожать жизни, поэтому стоит заранее убедиться в том, что в чрезвычайных обстоятельствах вы сможете дозвониться до специалиста в ночное время суток или на выходных. Врачи и медсестры трансплантационной бригады онкоцентра Ихилов помогут вам справиться с побочными эффектами. Некоторые нарушения можно предотвратить. Другие можно облегчить для того, чтобы вы чувствовали себя лучше.
Боль в горле и ротовой полости
Мукозит (воспаление или изъязвление ротовой полости) – это краткосрочный побочный эффект химиотерапии и облучения. Мукозит обычно проходит в течение нескольких недель после окончания терапии, однако пациенту в это время бывает больно есть и пить.
Онкобольным важно хорошо питаться. Если боль или язвы во рту не дают вам нормально жевать или глотать, специалисты из вашей трансплантационной бригады разработают план по борьбе с нежелательными симптомами.
Тошнота и рвота
Так как препараты химиотерапии могут вызвать сильную тошноту и рвоту, пациентам одновременно с химиотерапией назначают прием противорвотных средств. Это стандартная мера профилактики, основанная на том, что тошноту и рвоту легче предупредить, чем лечить. Профилактические мероприятия начинают еще до курса химиотерапии и продолжают до тех пор, пока вероятность тошноты и рвоты не дойдет до минимума. Это значит, что противорвотные средства принимают на протяжении всего курса химиотерапии и в течение 7-10 дней после его окончания.
Ни один препарат не предотвращает и не контролирует тошноту и рвоту, вызванную химиотерапией, на все 100%. В большинстве случаев используется не менее двух препаратов. Если вам назначили профилактическую терапию, сообщите специалистам из вашей трансплантационной бригады о том, насколько хорошо рекомендованные лекарства справляются с предупреждением тошноты и рвоты. Если они не действуют, вам назначат другие лекарства.
Инфекция
Новые стволовые клетки приживляются и начинают вырабатывать лейкоциты приблизительно через 6 недель после трансплантации. В этот период пациент может легко заразиться тяжелым инфекционным заболеванием. Чаще всего встречаются бактериальные поражения, однако вялотекущая или “спящая” вирусная инфекция также может стать активной. Некоторые пациенты сталкиваются с проблемой грибковых инфекций. Если у пациента с нормальным иммунитетом болезнь обычно протекает с минимальными симптомами, человеку, перенесшему трансплантацию стволовых клеток, угрожает серьезная опасность.
Вероятно, в целях профилактики инфекций вам посоветуют принимать антибиотики. Профилактическая терапия антибиотиками продолжается до тех пор, пока уровни форменных элементов крови не достигнут определенной отметки. Так, при ослабленном иммунитете можно легко подхватить инфекцию под названием “пневмоцистная пневмония”. Несмотря на то, что патоген безвреден для людей с нормально функционирующей иммунной системой, у пациентов, перенесших трансплантацию стволовых клеток, он может вызвать лихорадку, кашель и тяжелые нарушения дыхания. Антибиотики могут предотвратить заражение пневмоцистной пневмонией.
Перед трансплантацией врач проверяет, какие вирусные инфекции могут стать активными после процедуры, и назначает пациенту особые профилактические препараты. К примеру, так называемый цитомегаловирус – это распространенный возбудитель пневмонии у людей, перенесших операцию по пересадке стволовых клеток. Цитомегаловирусная инфекция в основном развивается у пациентов, заразившихся вирусом либо до трансплантации, либо от донора. Если ни вы, ни донор в прошлом не страдали таким заболеванием, специалисты трансплантационной бригады предпримут особые меры профилактики цитомегаловирусной инфекции.
После приживления стволовых клеток риск инфицирования уменьшается, но вы все равно можете заболеть. Иммунная система начинает полноценно работать только спустя 6 месяцев после трансплантации. Пациентам, страдающим болезнью “трансплантат против хозяина”, требуется еще больше времени.
Так как вы входите в группу риска, врачи будут тщательно следить за вашим состоянием и проверять, не появились ли у вас такие признаки инфекции, как лихорадка, кашель, нехватка дыхания или диарея. Скорее всего, вам придется регулярно сдавать анализы крови и сознательно избегать действий, способных привести к контакту с патогенными микроорганизмами. Если вы находитесь в стационаре, каждый человек перед посещением вашей палаты должен тщательно вымыть руки и надеть больничную рубашку, бахилы, перчатки и медицинскую маску.
Учитывая, что цветы могут оказаться переносчиками бактерий и грибков, вашим близким запретят проносить в вашу палату букеты. По этой же причине вам могут посоветовать воздержаться от употребления определенных свежих фруктов и овощей. Все продукты и блюда должны подвергаться тщательной термической обработке. Готовьте еду сами или поручите эту задачу родственникам, готовым предпринять все необходимые меры предосторожности. Определенные продукты нужно будет временно исключить из рациона.
Возможно, вам также посоветуют избегать контакта с землей, калом (как человека, так и животных), аквариумами, рептилиями и экзотическими домашними животными. Стоит остерегаться вскопанной земли, птичьего помета и плесени. Если вы прикасались к домашним животным, не забывайте мыть руки. Напомните близким о том, что кошачий туалет необходимо убрать из той комнаты, где вы едите или проводите досуг.
Специалисты вашей трансплантационной бригады подробно расскажут вам и вашим близким обо всех необходимых мерах предосторожности. Существует множество вирусов, бактерий и грибков, и все они являются потенциальными возбудителями инфекции.
Кровотечение и переливание крови
Людям, перенесшим трансплантацию стволовых клеток, потенциально угрожают кровотечения. Дело в том, что кондиционирование препятствует формированию тромбоцитов (кровяных телец, способствующих свертыванию крови). До тех пор, пока пересаженные стволовые клетки не приживутся и не начнут работать, вам и специалистам нужно будет предпринимать меры к предотвращению травм и кровотечений.
Уровни тромбоцитов остаются низкими на протяжении как минимум трех недель после трансплантации. В этот период вы можете заметить, что у вас легко образуются синяки и открываются кровотечения. Кровь может пойти из носа. Многие пациенты также жалуются на кровоточивость десен. Если уровень тромбоцитов упадет ниже определенной отметки, вам потребуется переливание тромбоцитов. Нужно будет соблюдать особую осторожность вплоть до тех пор, пока уровень этих кровяных телец не станет относительно безопасным.
Костному мозгу требуется время и на то, чтобы начать вырабатывать эритроциты. Вполне вероятно, что в период выздоровления вам будут периодически назначать переливание эритроцитов.
Интерстициальный пневмонит и другие патологии легких
Пневмонит – это разновидность воспаления легких. Болезнь чаще всего развивается в течение 100 дней после трансплантации стволовых клеток. Другие нарушения со стороны легких могут возникнуть гораздо позже – в том числе спустя два-три года после лечения.
Пневмония, вызванная инфекцией, встречается чаще, но пневмонит может развиться и под влиянием радиации, болезни “трансплантат против хозяина” или химиотерапии. При пневмоните повреждаются участки между клетками легких (так называемые интерстициальные пространства).
Пневмонит нередко протекает тяжело. Тяжелое течение болезни характерно для случаев, когда в рамках кондиционирования пациенту назначают одновременно и химиотерапию, и облучение всего тела. Для того, чтобы вовремя обнаружить признаки пневмонии или пневмонита, пациенту периодически назначают рентгенографию грудной клетки. Если вы страдаете болезнью “трансплантат против хозяина”, вам придется каждые несколько месяцев сдавать дыхательные тесты.
Обо всех нарушениях дыхания, включая его нехватку, необходимо сразу же сообщать лечащему врачу или специалистам трансплантационной бригады. Помимо пневмонии и пневмонита существует множество других нарушений со стороны дыхательных путей. Все они также должны служить поводом для незамедлительного обращения к врачу.
Болезнь “трансплантат против хозяина”
Болезнь “трансплантат против хозяина” выступает следствием аллогенной трансплантации в тех случаях, когда донорские клетки воспринимают организм реципиента как инородный. (Следует помнить, что кондиционирование уничтожает иммунную систему реципиента, поэтому его организм не может обороняться. Таким образом, после трансплантации большую часть иммунной системы пациента составляют донорские клетки.) Донорские иммунные клетки могут напасть на определенные органы. Чаще всего страдает кожа, желудочно-кишечный тракт (ЖКТ) и печень. Болезнь “трансплантат против хозяина” нарушает функцию пораженных органов и повышает риск инфицирования.
Реакция “трансплантат против хозяина” – это очень распространенное явление. У некоторых пациентов она проходит почти незаметно. У других развиваются смертельно опасные осложнения. Болезнь может протекать как в острой, так и в хронической форме. Острая патология развивается вскоре после трансплантации стволовых клеток и относительно быстро проходит. Хроническая болезнь “трансплантат против хозяина” развивается позже и сохраняется на долгий срок. У пациента могут диагностировать как одну, так и обе формы болезни. Некоторые люди вообще не страдают такой патологией.
Острая реакция “трансплантат против хозяина”
Острая реакция “трансплантат против хозяина” наступает в течение 10-90 дней после процедуры, хотя в среднем ее диагностируют приблизительно через 25 дней после пересадки стволовых клеток. Болезнь в острой форме обнаруживается примерно у трети или половины пациентов, перенесших аллогенную трансплантацию. Реже всего она наблюдается у молодых пациентов и у тех, чьи лейкоцитарные антигены максимально соответствуют донорским.
В число первых признаков заболевания входят кожные высыпания, а также жжение и покраснение кожи на ладонях и подошвах ног. Эта реакция может распространиться на весь организм. К прочим симптомам острой болезни “трансплантат против хозяина” относятся:
Врачи стараются предупредить развитие острой реакции за счет использования препаратов, подавляющих иммунную систему. К таким препаратам относятся стероиды (глюкокортикоиды), метотрексат, циклоспорин, такролимус и определенные моноклональные антитела. Прием лекарств начинают до наступления реакции “трансплантат против хозяина”. Профилактическая терапия облегчает течение болезни. Тем не менее, у пациентов, перенесших аллогенную трансплантацию стволовых клеток, эта патология развивается почти всегда. Лекарства лишь позволяют предупредить тяжелые осложнения. В настоящее время ученые разрабатывают комбинации препаратов, потенциально способные полностью предотвратить реакцию “трансплантат против хозяина”.
Риск острой реакции также можно снизить за счет извлечения иммунных клеток (T-клеток) из донорского материала непосредственно перед трансплантацией. С другой стороны, эта манипуляция повышает вероятность вирусной инфекции, рецидива лейкоза и недостаточности трансплантата. Исследователи пытаются изобрести способ удалить только определенные клетки – так называемые аллоактивированные T-лимфоциты – из донорского материала. Если такая методика войдет в медицинскую практику, врачи смогут уменьшить тяжесть заболевания и одновременно предоставить донорским T-лимфоцитам возможность уничтожить оставшиеся раковые клетки.
Острая болезнь “трансплантат против хозяина” обычно протекает в легкой форме и поражает кожные покровы. В ряде случаев, впрочем, она не только протекает тяжело, но и угрожает жизни реципиента. Если у пациента диагностировали болезнь в легкой форме, ему назначат аппликационную (местную) терапию стероидами. Препараты, содержащие стероиды и предназначенные для нанесения на кожу, выпускаются в форме мазей, кремов и лосьонов. В более тяжелых случаях стероиды принимают в форме таблеток или колют внутривенно. Если эти лекарства не помогают, пациенту назначают другие препараты, влияющие на работу иммунной системы.
Хроническая реакция “трансплантат против хозяина”
Хроническая реакция “трансплантат против хозяина” начинается через 90-600 дней после трансплантации стволовых клеток. Самым ранним признаком патологии считаются высыпания на коже рук или подошв ног. Сыпь может распространиться по всему телу. Кожа становится сухой; появляется зуд. В тяжелых случаях кожа покрывается волдырями и отслаивается, как при сильном солнечном ожоге. У некоторых пациентов повышается температура тела.
К прочим симптомам хронической болезни “трансплантат против хозяина” относятся:
Хроническую болезнь “трансплантат против хозяина” лечат так же, как и острую. Пациентам назначают препараты, подавляющие иммунную систему. Следует помнить о том, что такая терапия может повысить риск инфекционных заболеваний. После исчезновения или облегчения симптомов болезни “трансплантат против хозяина” большинство пациентов перестают принимать иммуносупрессоры.
Веноокклюзионная болезнь печени
Веноокклюзионная болезнь печени – это тяжелое нарушение, при котором закупориваются крохотные вены и другие кровеносные сосуды, расположенные внутри печени. Патология встречается редко и развивается только после аллогенной трансплантации (есть и другие виды пересадки стволовых клеток). Как правило, веноокклюзионной болезнью печени страдают те, кто во время кондиционирования лечился такими препаратами, как бусульфан или мелфалан.
Болезнь развивается в течение трех недель после начала кондиционирования. Чаще всего ее диагностируют у пожилых людей, имевших проблемы с печенью еще до трансплантации. Она также встречается у пациентов с острой реакцией “трансплантат против хозяина”. Различают такие первичные признаки болезни, как пожелтение кожи и глаз, потемнение мочи, болезненность под ребрами с правой стороны (где находится печень) и быстрый набор веса (в основном из-за скопления жидкости в животе). Иногда веноокклюзионная болезнь печени приводит к печеночной недостаточности и летальному исходу.
Недостаточность трансплантата
Недостаточность трансплантата диагностируют в тех случаях, когда организм не принимает новые стволовые клетки. Пересаженные стволовые клетки не попадают в костный мозг и не начинают делиться, как положено. Недостаточность трансплантата в основном наблюдается тогда, когда донор и реципиент плохо подходят друг другу или когда пациент получает стволовые клетки без T-лимфоцитов. Нарушение может произойти и в том случае, если пациент получил малое количество стволовых клеток – например, одну единицу пуповинной крови. Тем не менее, недостаточность трансплантата считается довольно редким явлением.
Недостаточность трансплантата может привести к обильному кровотечению и/или инфекции. Подозрение на патологию возникает в том случае, если уровни форменных элементов крови не начали повышаться в течение 3-4 недель со дня трансплантации костного мозга или стволовых клеток периферической крови (либо в течение 7 недель со дня трансплантации стволовых клеток пуповинной крови).
При наличии такой возможности пациенту назначают пересадку второй дозы стволовых клеток. Несмотря на то, что недостаточность трансплантата встречается редко, она относится к осложнениям, потенциально угрожающим жизни.
Проблемы, которые могут возникнуть позже
Природа проблем, возникающих после трансплантации, зависит от самых разнообразных факторов. К таким факторам относятся тип трансплантации, режим кондиционирования, общее состояние здоровья и возраст пациента, длительность и степень супрессии иммунной системы и степень тяжести хронической реакции “трансплантат против хозяина” (если пациент ею страдает). Нежелательные явления выступают следствием кондиционирования (химиотерапии и облучения перед пересадкой стволовых клеток) или применения определенных препаратов во время трансплантации (сюда, к примеру, относятся лекарства, подавляющие иммунную систему).
К возможным долгосрочным рискам трансплантации стволовых клеток относятся:
Лекарства, используемые во время трансплантации стволовых клеток, могут повредить сердце, легкие, почки, печень, кости/суставы и нервную систему. Вам назначат тщательный мониторинг и лечение отсроченных осложнений. Некоторые потенциальные побочные эффекты, включая потерю способности иметь детей, необходимо обсудить со специалистом еще до трансплантации. В таком случае вы сможете подготовиться к возможным осложнениям.
Важно обнаружить и вовремя вылечить все долгосрочные проблемы. Если вы заметили, что ваше состояние изменилось, незамедлительно сообщите об этом врачу. Вам назначат физический осмотр, анализы крови, визуализирующие исследования, легочные/дыхательные пробы и другие диагностические процедуры. Они помогут выявить и проконтролировать любые нежелательные явления со стороны внутренних органов.
Рецидив рака
Трансплантация стволовых клеток преследует несколько целей. В ряде случаев она позволяет не только продлить жизнь пациента, но и вылечить рак. Тем не менее, иногда рак возвращается (рецидивирует). Рецидив может произойти как через несколько месяцев, так и спустя несколько лет после трансплантации стволовых клеток. Чем больше проходит времени, тем быстрее снижается вероятность того, что рак начнет развиваться заново.
Количество способов борьбы с рецидивирующим раком ограничено. Многое зависит от общего состояния здоровья пациента и того, хорошо ли болезнь реагирует на медикаментозное лечение. Если пациент относительно здоров и крепок, ему назначат химиотерапию или таргетную терапию. Некоторым больным, перенесшим аллогенную трансплантацию, переливают лейкоциты от того же донора (такая процедура называется инфузией донорских лимфоцитов). Это делается для того, чтобы усилить эффект “трансплантат против опухоли”. В ряде случаев проводится вторая процедура по пересадке стволовых клеток. Как бы то ни было, большинство перечисленных процедур тяжело переносятся даже относительно здоровыми пациентами, поэтому тем, кто слаб, стар или страдает хроническими заболеваниями, такое лечение не назначают.
Вторичные онкологические заболевания (новый рак, вызванный лечением)
После процедуры возможен не только рецидив первичного заболевания, в рамках борьбы с которым проводилась трансплантация стволовых клеток, но и развитие вторичного рака. По результатам исследований можно заключить, что пациенты, перенесшие аллогенную трансплантацию, заболевают вторичным раком чаще, чем те, кто перенес трансплантацию стволовых клеток иного типа.
Если в течение нескольких месяцев после лечения у пациента развилась новая онкологическая патология, речь, как правило, идет о лимфоме (в частности, о B-клеточной лимфоме). По всей видимости, лимфома развивается под воздействием распространенного микроорганизма – вируса Эпштейна-Барр (ВЭБ). В норме иммунная система удерживает этот вирус под контролем, однако в условиях медикаментозной супрессии вирус Эпштейна-Барр может вызвать рак.
Через несколько лет после трансплантации стволовых клеток пациент может заболеть острым лейкозом. В этот же период у некоторых людей развивается иная патология костного мозга – миелодисплазия, или миелодиспластический синдром. При миелодисплазии костный мозг вырабатывает дефектные кровяные тельца. Это нарушение считается легкой формой рака. У некоторых пациентов, впрочем, оно может стать более агрессивным.
К вторичным онкологическим заболеваниям, способным развиться спустя много лет после лечения, относятся и солидные опухоли. Новообразования формируются из клеток кожи, полости рта, головного мозга, печени, шейки матки, щитовидной железы, молочной железы и костей.
Ученые изучают факторы риска, способствующие развитию вторичного рака. На данный момент к таким факторам относятся:
Иногда вторичный рак развивается через несколько месяцев или лет после трансплантации стволовых клеток. Чаще всего, впрочем, болезнь диагностируют спустя много лет после процедуры, поэтому исследования преимущественно проводятся в группах пациентов с наиболее высокими показателями выживаемости.
Успешное лечение первичного рака дает второй патологии время (и шанс) на развитие. Вне зависимости от природы первичного заболевания и дозировки радиации и препаратов, используемых во время кондиционирования, и облучение, и химиотерапия могут способствовать развитию нового рака.
Посттрансплантационное лимфопролиферативное заболевание
Посттрансплантационное лимфопролиферативное заболевание (ПТЛЗ) – это беспорядочное разрастание лимфоидной ткани. Фактически эта патология является разновидностью лимфомы и развивается после аллогенной трансплантации стволовых клеток. Патологический процесс связан с нарушением функции T-клеток (белых кровяных телец, являющихся частью иммунной системы) и заражением вирусом Эпштейна-Барр (ВЭБ). В норме T-лимфоциты помогают организму избавляться от клеток, содержащих вирус. Если T-лимфоциты не справляются со своей задачей, ВЭБ-инфицированные B-лимфоциты (другие белые кровяные тельца) беспорядочно делятся и растут. Большинство людей заражаются вирусом Эпштейна-Барр в тот или иной жизненный период, однако здоровая иммунная система подавляет инфекцию. Кондиционирование, которое проводится перед трансплантацией, ослабляет иммунную систему и тем самым позволяет вирусу выйти из-под контроля. В результате развивается посттрансплантационное лимфопролиферативное заболевание.
Примечательно, что ПТЛЗ все же является достаточно редким осложнением аллогенной трансплантации стволовых клеток. Чаще всего болезнь проявляется в течение 1-6 месяцев после процедуры, то есть в то время, когда иммунная система все еще очень слаба.
ПТЛЗ может угрожать жизни. К клиническим проявлениям болезни относятся опухание лимфоузлов, лихорадка и озноб. Стандартных методов лечения не существует. Чаще всего врачи просто уменьшают дозы иммуносупрессоров, и иммунная система пациента начинает самостоятельно бороться с вирусом. К прочим способам лечения ПТЛЗ относятся переливания белых кровяных телец (лимфоцитов) с целью усиления иммунного ответа, прием таких препаратов, как ритуксимаб, с целью уничтожения B-клеток и противовирусная терапия, направленная на подавление вируса Эпштейна-Барр.
Несмотря на то, что посттрансплантационное лимфопролиферативное заболевание встречается относительно редко, следует учитывать такие факторы риска, как недостаточное соответствие человеческих лейкоцитарных антигенов (HLA) реципиента и донора и необходимость в интенсивной иммуносупрессии. Ученые все еще изучают обстоятельства, способствующие развитию ПТЛЗ, и пытаются изобрести способ предупреждения этой патологии в группах риска.
Трансплантация стволовых клеток и способность иметь детей
Большинство людей, перенесших трансплантацию стволовых клеток, становятся бесплодными (неспособными иметь детей). В данном случае причиной бесплодия выступает не собственно пересадка стволовых клеток, а высокодозная химиотерапия и/или лучевая терапия, назначенная в рамках кондиционирования. Эти методы лечения влияют одновременно и на аномальные, и на здоровые клетки – и нередко повреждают органы репродуктивной системы.
Если вы планируете завести семью, проконсультируйтесь с врачом и уточните, можно ли сохранить репродуктивную функцию после трансплантации стволовых клеток. Вероятно, врач сможет сказать, насколько велика опасность потери репродуктивной функции в результате той или иной процедуры.
Женщины, перенесшие химиотерапию или облучение, нередко отмечают, что их менструальные кровотечения стали нерегулярными или и вовсе прекратились. Это не всегда свидетельствует о неспособности забеременеть, поэтому как перед трансплантацией стволовых клеток, так и после нее необходимо пользоваться противозачаточными средствами. Препараты, применяемые в процессе трансплантации, могут навредить растущему плоду.
Лекарства, используемые в процессе трансплантации стволовых клеток, способны повредить и сперматозоиды, поэтому мужчинам также следует использовать контрацептивы. Пересадка стволовых клеток нередко вызывает временное или перманентное бесплодие и у мужчин. По этой причине пациентам мужского пола обычно рекомендуют сначала сдать сперму в специальный банк – и лишь затем ложиться на трансплантацию стволовых клеток. Репродуктивная функция мужчины может восстановиться, однако никто не может с точностью предсказать, когда именно это произойдет.