протонная спектроскопия головного мозга
Магнитно-резонансная спектроскопия

Суть исследовательской методики
Современные исследовательские клиники проводят магнитно-резонансную спектроскопию с применением специализированного оборудования. Такой метод исследования определяет биохимические изменения, которые вызываются различными патологическими состояниями, в разных участках человеческого организма.
Протонная магнитно-резонансная спектроскопия основывается на изменениях резонансной частоты протонов, из которых состоят всевозможные химические соединения. Такой процесс в медицине принято называть химическим сдвигом, что определяет различия частот пиков спектра.
Единицей измерения химического сдвига принято считать миллионную долю (ррт). На сегодняшний день протонная магнитно-резонансная спектроскопия подразделяется на ту, что проводится по одновоксельной методике, и мультивоксельную, которая может одномоментно определять спектры из нескольких участков головного мозга.
В современной медицине применяется еще одна разновидность спектроскопии – мультиядерная, учитывающая магнитно-резонансные сигналы фосфорных, углеродных и некоторых иных ядер.
При одновоксельной магнитно-резонансной спектроскопии анализу подлежит лишь один воксел или участок мозга человека. При анализе состава частот спектра выбранного воксела специалисты получают определенное метаболитное распределение химического сдвига в миллионных долях. При этом по соотношению в спектре метаболитных пиков, уменьшению или увеличению их высот можно неинвазивным путем оценить протекающие в тканях биохимические процессы.
Мультивоксельная спектроскопия предоставляет спектральные значения сразу нескольких необходимых при исследовании вокселов, которые можно сравнить для получения целостности картины исследуемого участка.
Данные мультивоксельной магнитно-резонансной спектроскопии позволяют строить карту среза по параметрам, где цветовыми маркерами обозначены концентрации необходимых метаболитов, а распределенность метаболитов в срезе визуализирована и предоставляет взвешенное по параметру химического сдвига изображение.

Наиболее частым спектром применения методики выступает анализ мышечной ткани, поскольку она не подлежит ни одному другому неинвазивному методу диагностики и может быть обследована только путем применения биопсии.
Области применения диагностики
Рассматриваемая диагностика позволяет расшифровывать процессы метаболизма тканей различных органов при помощи получаемых магнитно-резонансных спектров. Обменные процессы организма, в большинстве случаев, нарушаются гораздо раньше, чем пациент начинает ощущать какие-то симптомы того или иного заболевания.
Вот почему важно своевременно применять магнитно-резонансную спектроскопию, которая поможет выявить отклонения на ранних стадиях болезни и принять соответствующие меры по предотвращению ее прогрессирования. К тому же, данная методика для отдельных анатомических областей организма человека является единственной неинвазивной диагностической процедурой, которая известна на сегодняшний день.
Для диагностики энергетического показателя метаболического процесса сердечной мышцы без введения радиоактивных средств магнитно-резонансная спектроскопия является единственно возможным методом обследования.
При сочетании методики с результатами магнитно-резонансной томографии врач получает общую клиническую картину кардиологических параметров – размеров сердца, структуры миокарда и нарушений кровообращения в нем, функциональных расстройств. Также вышеназванная диагностика помогает контролировать ход лечения ишемической болезни сердца, различной гипертрофии, сердечной недостаточности.
При неврологических патологиях магнитно-резонансная спектроскопия позволяет уточнить диагноз, различая, например, рассеянный склероз и нейрооптикомиелит. При расстройствах психики важным является та особенность данной диагностики, которая помогает рассмотреть различные биохимические процессы в мозговых клетках.
Данная методика широко применима для оценки всевозможных новообразований в головном мозге. Несмотря на отсутствие гистологических данных о возникшем новообразовании, исследователи говорят об определенных соотношениях рассматриваемых в ходе диагностики показателей и возникновении пика лактата. Таким образом, большинство случаев магнитно-резонансной спектроскопии опухолевых тканей способно предоставить дифференциацию возникших новообразований по принципу злокачественности.
В клинических условиях при послеоперационных диагностиках данная методика свидетельствует об успешности проведенного хирургического вмешательства либо о продолжении роста рассматриваемой опухоли, ее рецидиве, лучевом некрозе.

Показательными являются в данном разрезе диагностированные случаи абсцессов, опирающиеся на диффузионно-взвешенные изображения.
Так, при отсутствующих пиках основных метаболитов при абсцессе отмечается возникновение пиков липид-лактатного комплекса и специфичных абсцессу пиков – например, продуктов анаэробного бактериального гликолиза и результатов протеолиза.
В медицинских источниках часто исследуется эффективность МР-спектроскопии при метаболических нарушениях и дегенеративных поражениях белого вещества мозга у детей, эпилепсии, черепно-мозговых травмах, ишемиях головного мозга и прочих заболеваниях.
Показания и противопоказания для МРС
Рассматриваемая диагностика аналогично магнитно-резонансной томографии основана на ядерно-магнитном резонансе, но ее результатом не выступают снимки.
Методика помогает рассматривать правильность распределения в тканях продуктов метаболических процессов, основываясь на их молекулярных особенностях.
Среди основных состояний и заболеваний, при которых пациентам показано прохождение магнитно-резонансной спектроскопии, выделяют эпилепсию, ишемическую болезнь, болезни Альцгеймера и Паркинсона, всевозможные воспалительные процессы, травмирование тканей, возникновение новообразований в головном мозге.
Поскольку метаболизм здоровых и пораженных тканей значительно отличается, проведение данного вида исследования помогает диагностировать и начать лечить проблему на самой ранней стадии, что чаще приводит к успешному результату.
Среди главных противопоказаний к процедуре специалисты называют искусственный водитель ритма. В случае наличия протезирования внутреннего уха либо искусственного сердечного клапана важно своевременно информировать об этом врача и предоставить ему подробное описание или аннотацию имеющегося протеза.
Также, поскольку исследование проводится в закрытом пространстве – продолговатой кабине, при наличии боязни таких пространств необходимо сообщить об этом специалисту, чтобы он мог прописать пациенту седативные (успокоительные) препараты.
Методика исследования, описанная выше, является многообещающей, поскольку при ее сочетании с другими обследованиями точность поставленного диагноза обычно достигает 90%. Иногда случаются неточности в связи с особенностью опухолевой ткани, которая может не сильно отличаться от нормальной по содержанию холина и степени зрелости.
В остальных случаях данное исследование очень информативно показывает специалистам, что происходит с обследуемым участком.
Больше свежей и актуальной информации о здоровье на нашем канале в Telegram. Подписывайтесь: https://t.me/foodandhealthru
МР-спектроскопия
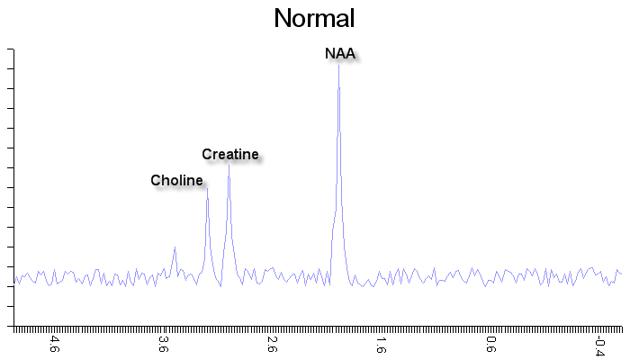
Протонная магнитно-резонансная спектроскопия (ПМРС) – один из наиболее молодых и быстро развивающихся методов лучевого исследования головного мозга, позволяющих определять содержание основных метаболитов (холин, N-ацетиласпартат, креатин, глютамат/глутамин, лактат) в интересующих участках органа и их соотношение.
История и этимология
МРС впервые использовали при исследовании эритроцитов в 1973 году Мун и Ричардс, а в 1974 году при помощи МРС Хаулт исследовал бедренную мышцу мыши.
Пики.
Лактат: резонирует на 1,3 ppm
Липиды: резонирует на 1,3 ppm
Аланин: резонирует на уровне 1,48 ppm
N-ацетиласпартат (NАА): резонирует на 2.0 ppm
Глутамин/глутамат: резонанс на 2.2-2.4 ppm
ГАМК: резонирует на 2.2-2.4 ppm
2-гидроксиглутарат: резонирует на уровне 2,25 ppm
Цитрат резонирует 2,6 ppm
Креатин: резонирует на 3.0 ppm
Холин: резонирует на 3.2 ppm
Мио-инозитол: резонанс на 3.5 ppm
ppm — pars per million
Как лучше запомнить?
Вспомнить шоколадку с названием My ChoCrNaaLa
My: Myo-inositol 3.5 — Мио-инозитол
Cho: Choline 3.2 — Холин
Cr: Creatine 3.0 — Креатин
Naa: Naa 2.0 — N-ацетиласпарта
L: Lactate 1.3 — Лактат
Патология
Глиома
МРС помогает предсказать степень дифференцировки. Чем выше степень дифференцировки, тем ниже пик N-ацетиласпартата и креатина, но выше пики холина, лактата и липидов.
Не-глиальные опухоли
Незначительные изменения пика NAA.
Лучевая терапия
Дифференциация изменений головного мозга на фоне лучевой терапии от опухоли всегда проблематична, но при рецидиве опухоли пик холина чаще повышен в то время, как после лучевой терапии пик NAA, холина и креатина будет низким.
Ишемия и инфаркт
Пик лактата будет повышаться, как только клетки головного мозга переходят на анаэробный метаболизм. Пик липидов и всех остальных пиков будет снижаться.
Инфекция
Пик NAA отсутствует при всех патологических процессах, разрушающих ткань головного мозга. При абсцессе пик лактата, аланина, ацетата повышен. Пик холина низкий или отсутствует при токсоплазмозе, а при лимфоме повышен, данный показатель используют для отличия одного патологического процесса от другого.
Заболевания белого вещества мозга (лейкодистрофии)
Прогрессирующая мультифокальная лейкоэнцефалопатия повышение Мио-инозитол. Болезнь Канавана повышение NAA.
Печеночная лейкоэнцефалопатия
При печеночной лейкоэнцефалопатии снижение пика миоинозитола и в меньшей степени холина. Глутамин увеличивается.
Митохондриальные заболевания.
Синдром Лея: повышение пика холина, снижение NAA и реже повышение пика лактата.
Примеры
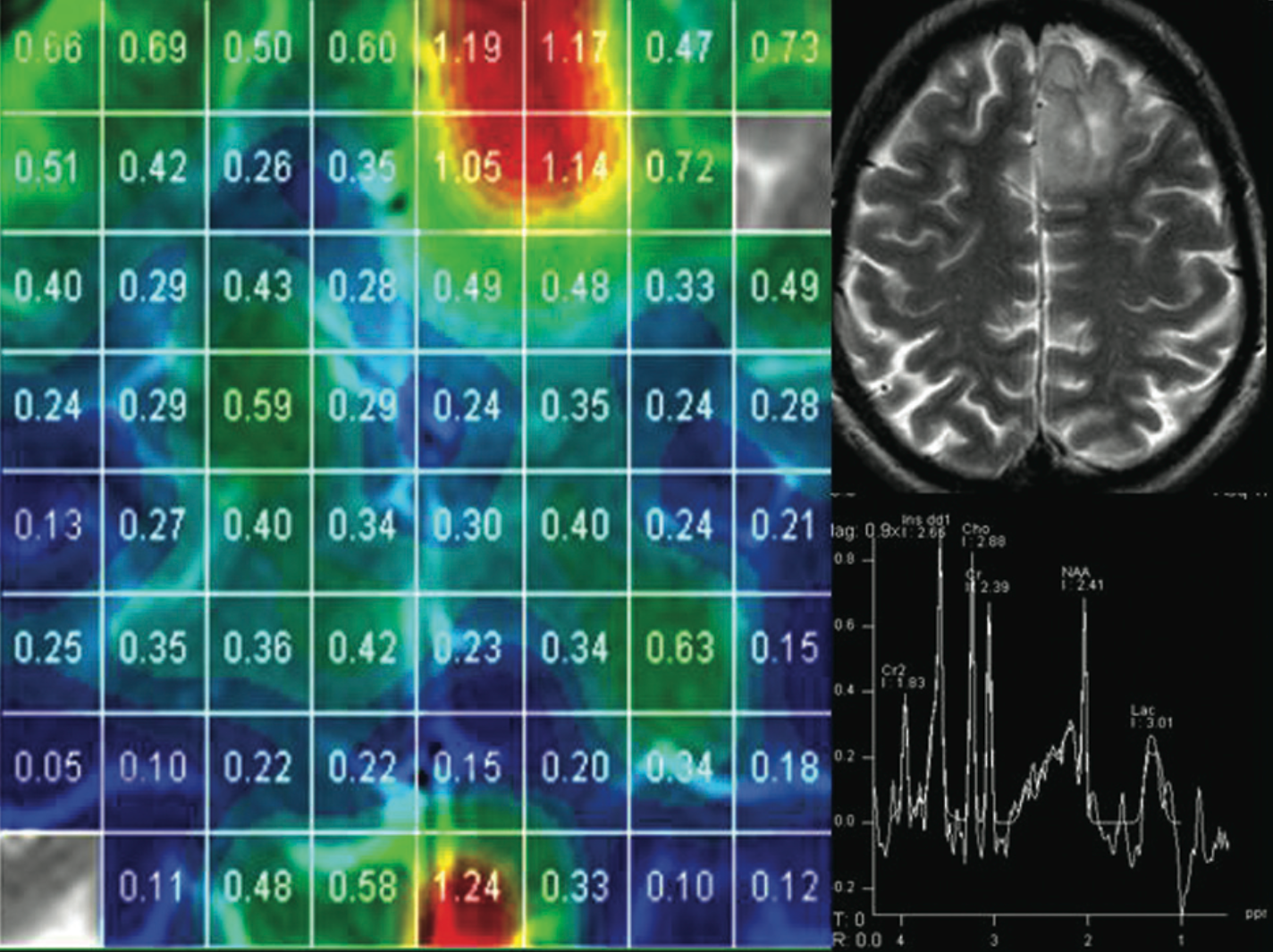
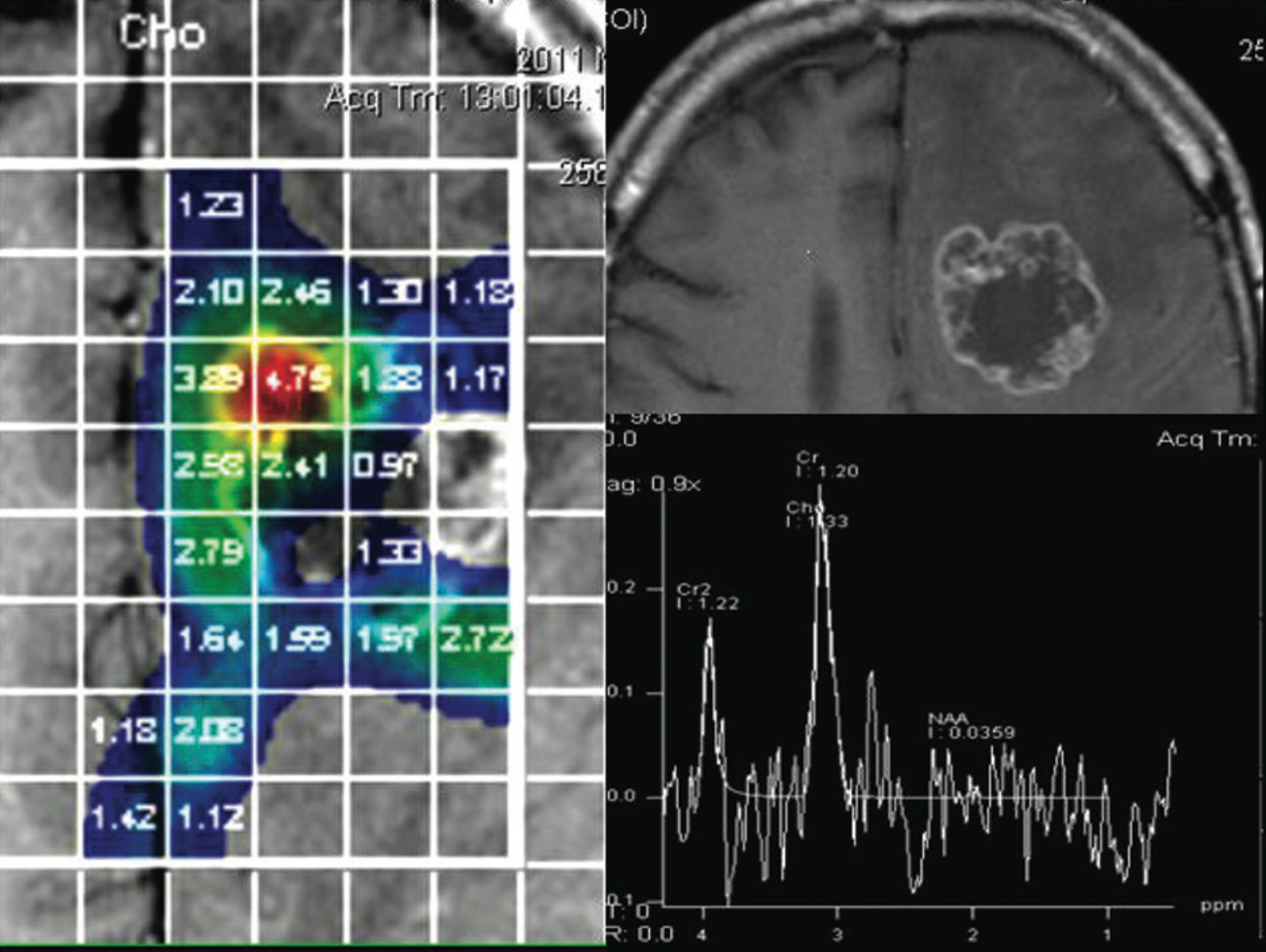
РИС. 1.
Астроцитома низкой степени злокачественности в левой лобной доле. Зона повышенного по Т2 ВИ сигнала без чётких контуров в левой лобной доле. 2D мультивоксельная МР-спектроскопия. В спектре патологического участка определяется высокий пик холина, снижение пика N-ацетиласпартата и наличие пика лактата. На цветной карте отра- жается распределение соотношения Cho/NAA. В патологической зоне отмечается повышение индекса Cho/NAА выше 1.0 (красный цвет).
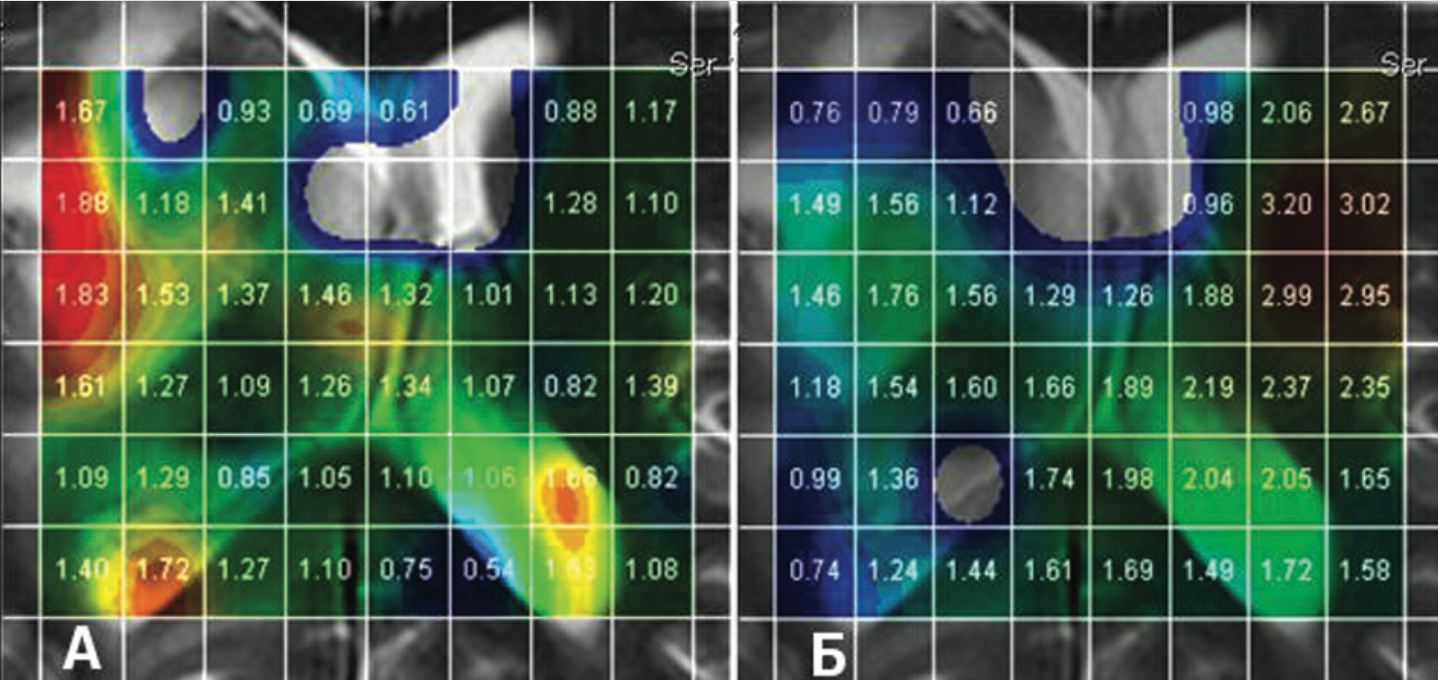
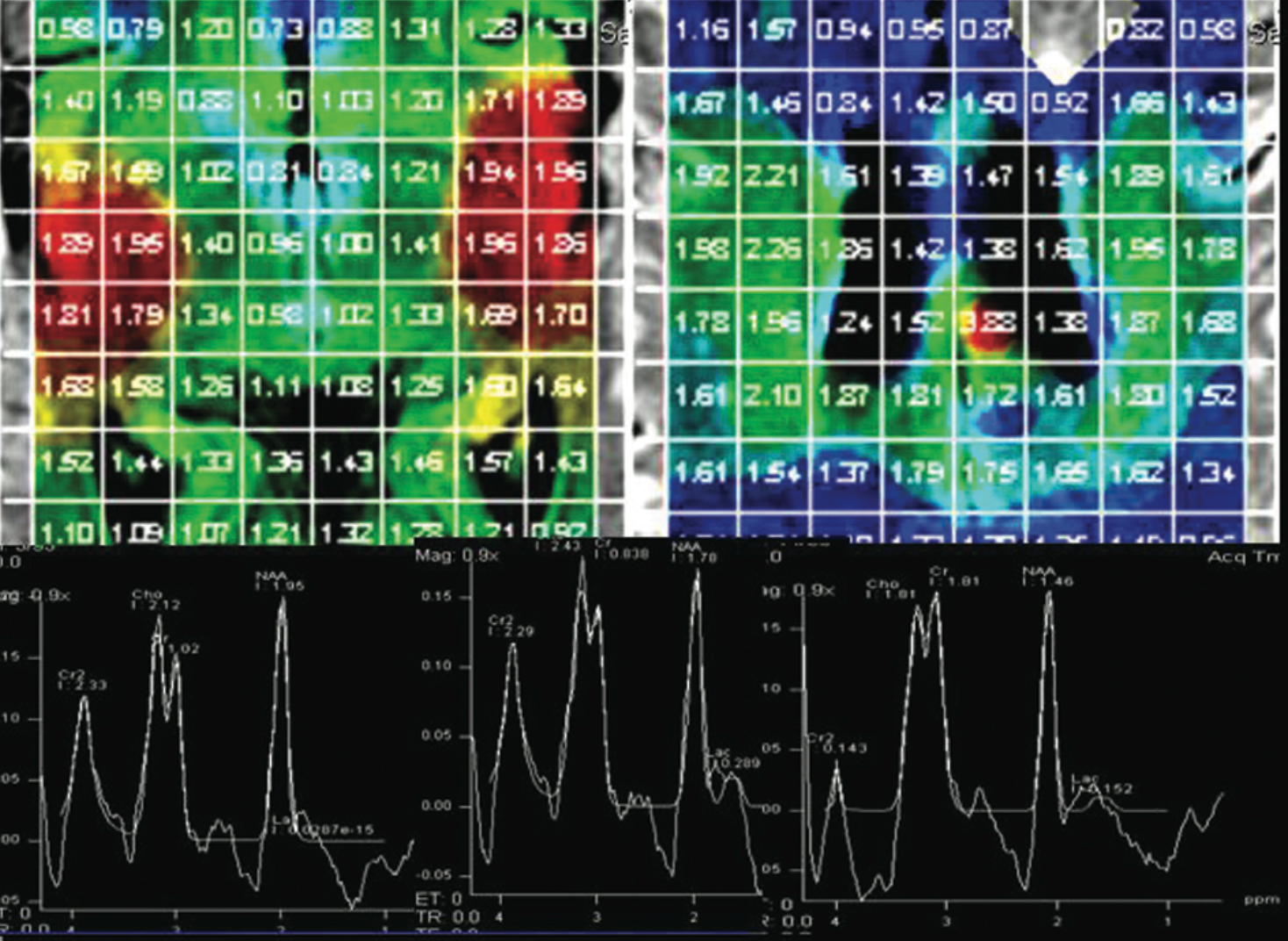
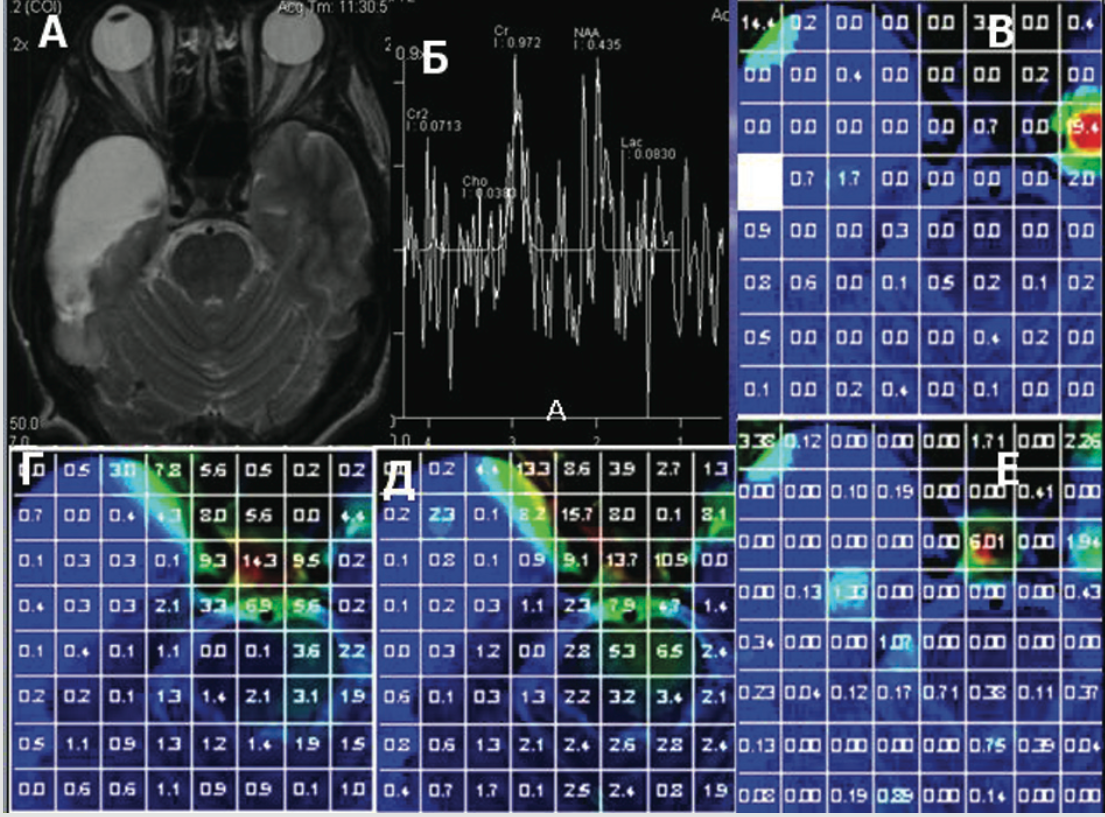
РИС. 2.
Глиобластома. 2D мультивоксельная МР-спектроскопия.
А. Цветная карта распределения соотношения Cho/NAA. Отмечается повышение индекса Cho/NAA выше 1.80 в зоне опухоли (красный цвет). Метаболические изменения распространяются далеко за пределы патологической зоны. Б. Цветная карта распределения NAA. Отмечается сни- жение содержания NAA выше в зоне опухоли (синий цвет).
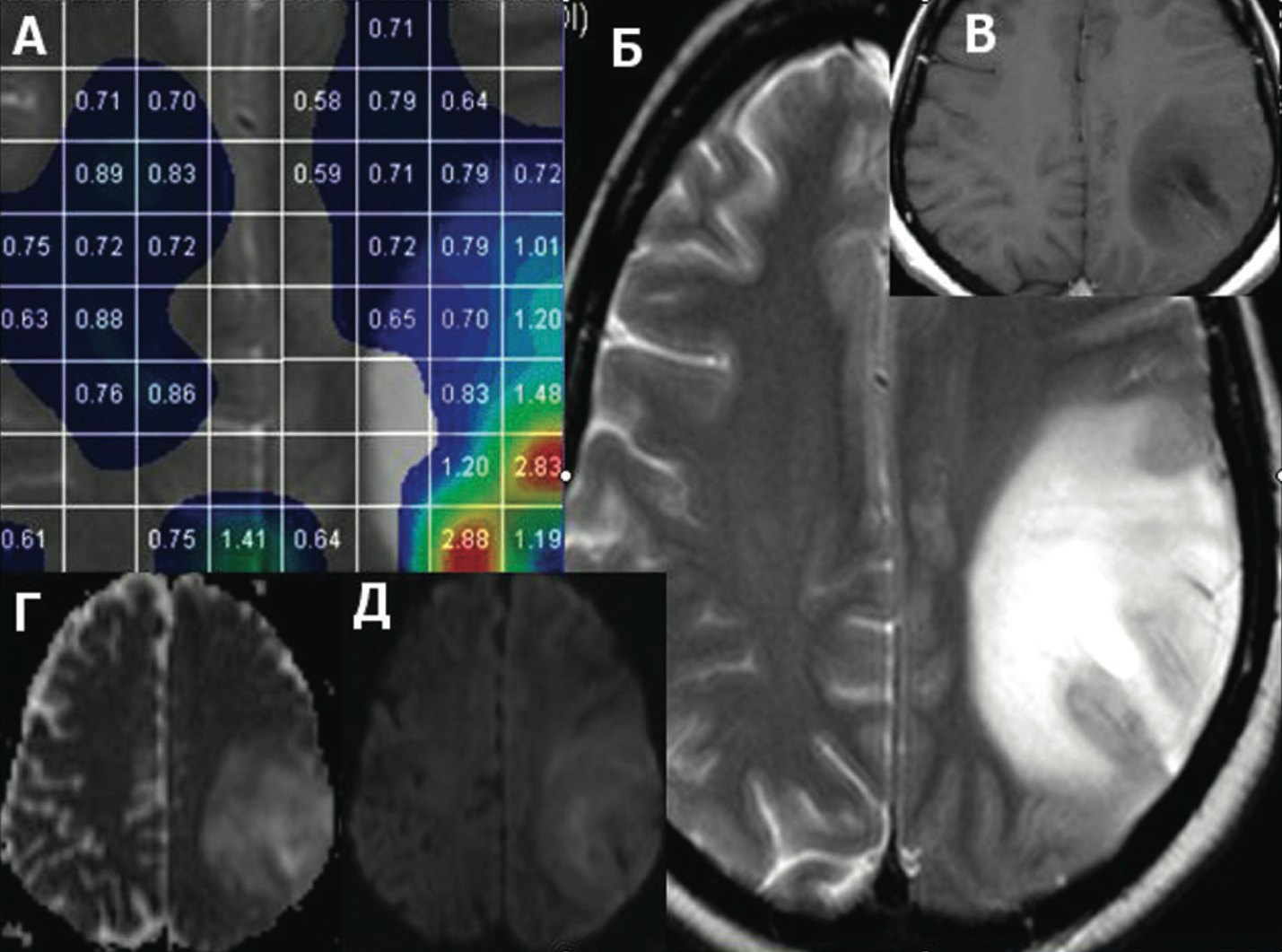
РИС. 3.
Астроцитома низкой степени злокачественности.
А. 2D мультивоксельная МР-спектроскопия, карта распределения соотношения Cho/Cr. Отмечается повышение индекса Cho/Cr в зоне опухоли выше 1.0. Б. Т2 взвешенные изображения. В левой теменной доле зона повышенного МР-сигнала без чётких контуров. В. Отсутствие контрастного усиления на Т1 ВИ. Г. ADC карта. Д. Диффузионно-взвешенные изображения.
РИС. 4.
Солитарный метастаз.
Объёмное образование с распадом в центре, солидный компонент интенсивно накапливает контрастное вещество. В спектре опухоли определяется повышение пика холина, отсутствие пика N-ацетиласпартата, невысокий пик лактата. На 2D мультивоксельной карте распределения холина отмечаются высокие интегральные показатели этого метаболита.
РИС. 5.
Состояние после перенесенной длительной комы.
Диффузное снижение N-ацетиласпартата с обеих сторон.
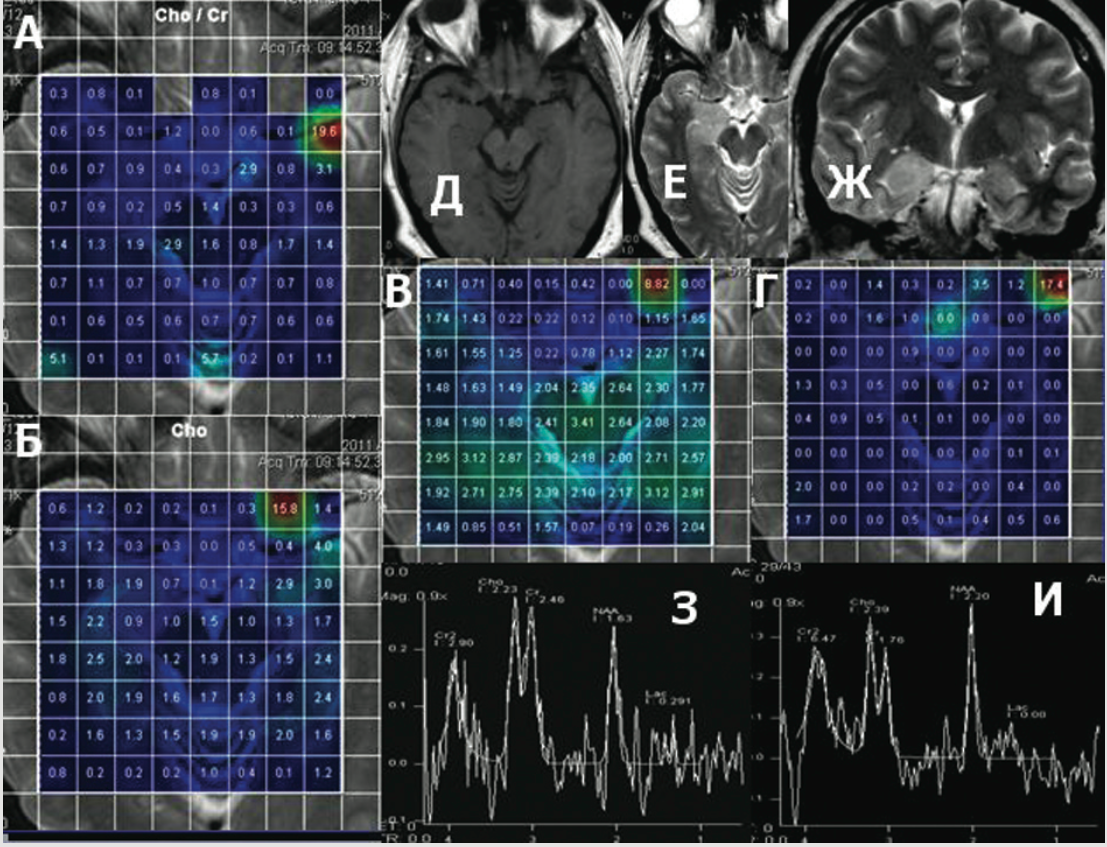
РИС. 6.
Эписиндром неопухолевой этиологии. Фокальная кортикальная дисплазия. А, Б, В, Г. Протонная МР-спектроскопия. Карты распределения Cho/Cr, Cho, NAA, Lac. Отмечается снижение N-ацетиласпартата при нормальных показателях Cho/Cr, Cho, Lac.
Д, Е, Ж. Повышение МР-сигнала по Т2 ВИ от медиальных отделов правой височной кости. З, И. Метаболические изменения с обеих сторон.
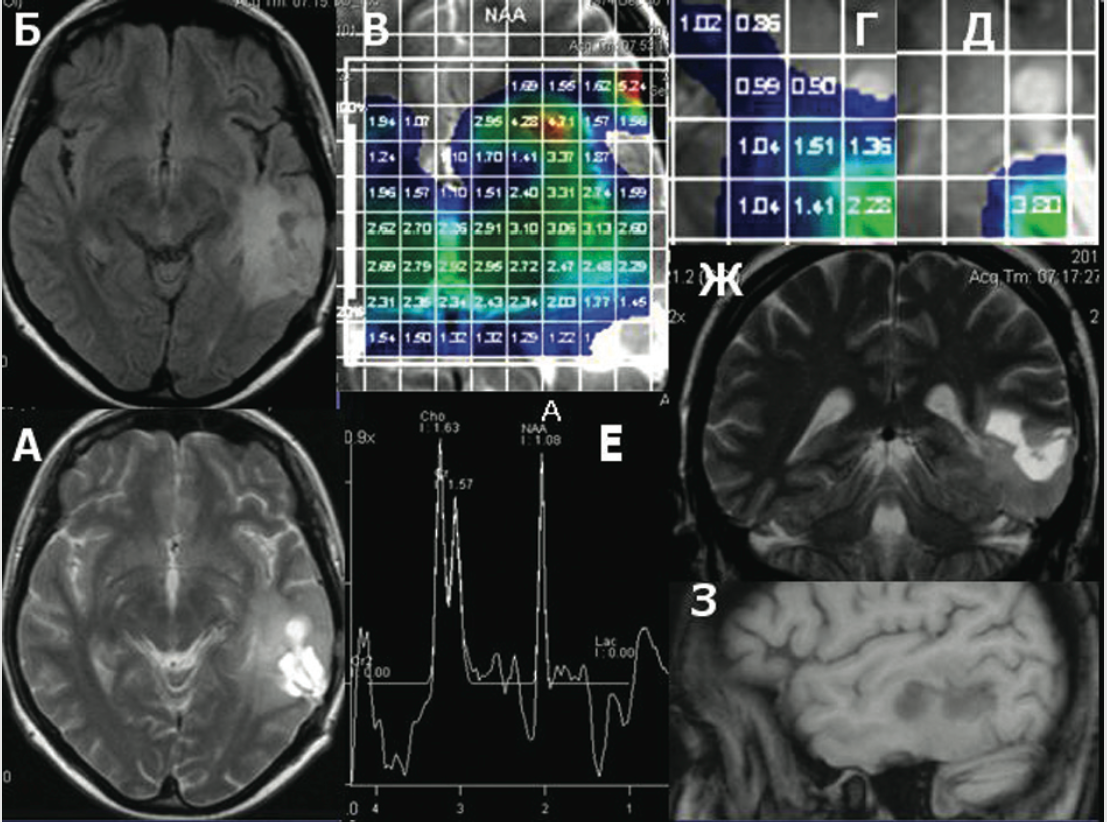
РИС. 7.
Состояние после удаления астроцитомы. Признаки продолженного роста. А. Т2 взвешенные изображения. Б. Т2 FLAIR. В. Протонная МР-спектроскопия. Карта распределения NAA. Снижение содержания N-ацетиласпартата. Г. Карта распределения Cho/NAA. Повышение индекса Cho/NAA. Д. Карта распределения Cho/Cr. Повышение индекса Cho/Cr. Е. Протонная МР спектроскопия. Увеличение пика холина, сни- жение пика N-ацетиласпартата. Ж. Т2 ВИ корональная проекция. З. Т1 ВИ сагиттальная проекция.
РИС. 8.
Состояние после удаления астроцитомы правой височной доли. А. Т2 взвешенные изменения. Кзади от послеоперационной кисты име- ется подозрительный на рецидив участок. Б. Протонная МР-спектроскопия. Снижение пиков холина, креатина и N-ацетиласпартата. В, Г, Д, Е. Карты распределения метаболитов: Cho, NAA, Cho/Cr Lac соответственно. Снижение содержания Cho, NAA. Lac и индекс Cho/Cr в пределах нормы.
PPM — это pars per million, т.е. миллионная доля от резонансной частоты данного ядра (например для водорода в поле с магнитной индукцией в 1,5 Тл размерность 1 ppm будет равна 63.87 Герц, при 3 тесла уже 127,74 Гц. За 0 ppm принята частота тетраметилсилана, что пришло из аналитической химии.
Источник
Протонная спектроскопия головного мозга
Протонная магнитно-резонансная спектроскопия – это развивающийся метод, способный выявлять заболевания головного мозга, сердечной мышцы посредством регистрации метаболического накопления глутамата, ацетилхолина, креатинина, ацетиласпартата и ряда других соединений. Сравнение активности веществ в норме и при патологии позволяет установить ранний диагноз, динамические оценить качество лечения через определенные временные промежутки.
Процедура МРТ головного мозга с МР спектроскопией – что это такое
МРТ спектроскопия позволяет изучить функциональность головного мозга. Другие МР процедуры показывают анатомию органа. Сочетание функциональной и морфологической информации повышает информативность диагностики.
МР-спектроскопия позволяет изучить скорость движения молекул веществ, проводить дифференцировку разных тканей – серого и белого вещества, мышц, жира, крови. Регистрация транспорта ионов калия, натрия через мембрану определяет активность фагоцитоза – уничтожения защитными клетками чужеродных агентов. Сочатение с МРТ трактографией позволяет верифицировать состояние внутримозговых желудочков, перивентрикулярных пространств.
Отслеживание накопления кислорода позволяет зарегистрировать участки повышенной возбудимости, выявить места разрушения гематоэнцефалического барьера, анализировать гормональную активность, проницаемость тканей.
Методы молекулярной нейровизуализации только развиваются – трактография, перфузионная диффузионная МРТ головного мозга и МР-спектроскопия. Применяются обычно после нативной магнитно-резонансной томографии головного мозга. Только онкологи пользуются нейровизуализационными методами для оценки изменений мозговой ткани во время лечения опухолей.
Как делают протонную МР-спектроскопию
Неинвазивная МРТ головного мозга с МР спектроскопией разработана в 1951 году. Ученые использовали метод для регистрации измененной частоты протонов разных веществ под влиянием сильного магнитного поля. Полувека наблюдения за атомами протонов ацетиласпартата, холина, миоинозитола, лактата, жировых соединений, глутамина позволило использовать информацию в медицине для выявления внутримозговых изменений, патологии сердечной мышцы.
Информативность имеют физиологические и патологические химические сдвиги соединений. Для примера, приводим протонный МР-спектр веществ в норме:
Инновационные разработки помогли совершенствовать метод. Существует 3 разновидности магнитно-резонансной спектроскопии:
Разделение основано на регистрации протонных спектров одного или нескольких участков мозговой паренхимы одновременно. При одновоксельной МР-спектроскопии изучается единичный участок. Изучение спектров химического сдвига метаболитов заданной зоны помогает оценить биохимические процессы.
Мультивоксельный тип предполагает спектроскопический анализ разных сегментов. Подход применяется для оценки функциональности разных центров – чувствительных, двигательных, речи, слуха, зрения.
Мультиядерная МР спектроскопия оценивает химические сдвиги протонов углерода, фосфора, ряда других химических соединений одновременно. Распределение пиков повышает информативность исследования.
Информация анализируется путем просмотра параметрической карты среза. Каждый отдельный участок имеет несколько анатомических образований. Отслеживание биохимических спектров не позволяет дифференцировать ткань, но знание патофизиологии помогает предположить локализацию патологии.
Основные разработки МР-спектроскопии проводятся в области онкологии. С помощью процедуры нельзя предсказать тип новообразования. Наблюдения показали измененное соотношение метаболизма холина-креатинина, N-ацетиласпартата и креатина у большинства злокачественных образований. Некоторые раки сопровождаются повышением пика лактата.
Что показывает МР спектроскопия
Опробовано спектроскопическое обследование при верификации нейроэпителиальных опухолей, эпендимом, астроцитом. Метаболические сдвиги четко указывают тип новообразования. Онкологи применяют МР-спектроскопию для диагностики наличия/отсутствия клеток образования после операционного удаления очага. Обследования верифицирует признаки гибели злокачественной ткани после химиотерапии, лучевого облучения.
Динамический онкологический контроль лучше делать двумя методами – перфузионно-взвешенная МРТ в сочетании с 1 H-МР-спектроскопией. Подход выявляет участок некроза посредством обнаружения широкого протонного пика лактат-липидных соединений в пределах от 0,5 до 1,8 ппм. Одновременно прослеживается редукция сдвига других веществ, «мертвый пик».
Очередная область использования спектроскопии – дифференциальная диагностика демиелинизирующих процессов (рассеянный склероз), инфекций, травматических повреждений. Абсцессы мозга верифицируются по обнаружению спектров лейцина, валина, сукцината, липид-лактатного комплекса. Литературные источники приводят информацию о возможности использования обследования для оценки метаболизма при черепно-мозговых травмах, эпилепсии, инсультах.
Контрастное МРТ головного мозга показывает состояние сосудов, верифицирует злокачественные и доброкачественные новообразования вначале развития.
Регистрация сдвигов валина, лейцина свидетельствует о распаде тканей при болезнях, бактериальных инфекциях. Продуктом бактериального гликолиза является накопление сукцината, ацетата. Изменение МР-спектров веществ позволяет предположить характер нозологии (органический, инфекционный, воспалительный).
Какие болезни выявляет протонная спектроскопия:
Цветное картирование дополняет информативность контрастной, нативной МР-томографии. Исследование имеет блестящие перспективы медицинского развития.
Звоните нам по телефону 8 (812) 241-10-46 с 7:00 до 00:00 или оставьте заявку на сайте в любое удобное время
Протонная спектроскопия головного мозга
Первые попытки получения магнитно-резонансного (МР) спектра мозгового вещества основывались на использовании ядра фосфора 31 P. Первый МР-спектр по фосфору головного мозга крысы был получен B. Chance в 1978 г. [1]. Этот метод позволял исследовать метаболические изменения в энергетическом обмене в веществе мозга крысы. После того как была освоена фосфорная МР-спектроскопия (МРС), ученые переключились с атома фосфора на атом водорода. Основное отличие этих методик заключается в том, что фосфорная МРС позволяет исследовать метаболические изменения в энергетическом обмене тканей, в то время как протонная МРС позволяет получать сведения о химическом составе. Исследования в этой области начинались с изучения свойств тканевой воды. Впервые протонный спектр вещества мозга человека получили P. Bottmley и соавт. [1] в 1984 г. при использовании 1.5Т МР-томографа. В 1994 г. FDA (U.S. Food and Drug Administration) одобрила применение импульсной последовательности PROBE (PROton Brain Examination) для проведения одновоксельной МРС в клинике. Далее вышла достаточно большая серия работ, посвященных клиническому использованию протонной МРС, которые касались многих диагностических аспектов, включая дифференциальную диагностику опухолевых и неопухолевых образований головного мозга [2], оценку степени злокачественности глиальных опухолей [3], изучение ишемии [4] и многое другое [5—7]. Следующим шагом в освоении МРС на основе развития вычислительной техники и электроники стала возможность преобразовать спектроскопические данные, представленные в виде пиков отдельных метаболитов, в метаболические цветовые карты. Это позволило более наглядно отображать особенности распределения и соотношение различных метаболитов в здоровых и патологически измененных тканях мозга (рис. 1). 
Постепенно в клиническую практику стала входить не только одновоксельная МРС, но и мультивоксельная (Chemical shift imaging) технология, которая позволяла уже изучать достаточно большую область интереса с включением в нее не только зоны патологии, но и перифокального и даже отдаленного вещества мозга. Появилась возможность за время одного сканирования сравнивать различные участки, например, как внутри самой опухоли, так и за ее пределами. Протонная МРС со временем стала источником важнейшей информации в диагностике различной нейрохирургической патологии: первичных и вторичных опухолей мозга, опухолевых и неопухолевых поражений, продолженного роста опухолей мозга после лечения и постлучевых реакций, инфильтративного роста опухоли в области перитуморального отека и др. [1, 9, 12].
В последнее время прогресс медицинских МРТ-технологий позволил перейти на использование 3D протонной МРС на клинически доступных МР-сканерах. Главным преимуществом 3D-метода над 2D-мультивоксельной спектроскопией стала возможность наложения цветных карт метаболитов или их соотношений на достаточно большой по размерам объем мозга, включающий не только зону измененного мозгового вещества, но даже противоположное полушарие, причем на разных анатомических уровнях (рис. 2). 
Цель исследования — оценить возможность применения мультивоксельной 3D протонной МР-спектроскопии у здоровых добровольцев без органической патологии головного мозга с анализом ее информативности в определении соотношений основных метаболитов белого и серого вещества головного мозга.
Материал и методы
Обследованы 15 добровольцев в возрасте от 28 до 62 лет без органической патологии головного мозга (средний возраст 39,7 года). Исследования проводились на МР-томографе Signa HDxt 3.0T (GE, Healthcare) с использованием головной 8-канальной катушки. Все добровольцы подписывали информированное согласие на проведение МР-исследования с включением в протокол МРС. Протокол исследования был одобрен этическим комитетом ФГАУ «НМИЦ нейрохирургии им. акад. Н.Н. Бурденко». На первом этапе добровольцам выполнялась стандартная МРТ головного мозга в режимах Т1, Т2, T2-FLAIR, ДВИ в аксиальной и сагиттальной проекциях. Далее выполняли последовательности T1 FSPGR и 3D Cube T2, и с помощью функции Batch производилось построение реформатов в аксиальной, фронтальной и сагиттальной проекциях с толщиной среза 3,0 мм и межсрезовым интервалом 1,0 мм. На изображениях в последовательности T1 FSPGR или 3D Cube Т2 выбиралась зона интереса и выставлялась рамка вокселов, включающая в себя выбранную область. С помощью полос сатурации подавлялись сигналы от жировой ткани и воды. В данной методике использовалось не только шиммирование (оптимизация однородности магнитного поля) первого порядка, но также и шиммирование второго порядка.
При 3D МРС используется несколько дополнительных градиентов, действующих по осям Х, Y, Z. Действие этих градиентов приводит к вариации вектора магнитного поля Во. Для получения качественного изображения очень важно, чтобы поле в области интереса было как можно более однородным. Для этого выбирается область, в которой будет проводиться шиммирование по всем плоскостям. Программа производит расчет вариации поля, затем производится коррекция текущей (Current RMS) вариации до теоретического значения (Predicted RMS). Эффективному шиммированию соответствует отличие текущего от теоретического не более чем на 3 ед. С целью получения МР-спектров и параметрических карт нами запускалась последовательность HOS PROBE 3D с ТЕ=144 мс. Контроль качества построения выполнялся в режиме Prep Scan и включал оценку ширины спектральной линии и процент подавления воды. Для аппарата с напряженностью магнитного поля 3,0 T ширина спектральной линии не должна превышать 25 Гц, а процент подавления воды не должен быть ниже 95%.
Данные обрабатывали с помощью программного пакета Ready View (GE). Сетка вокселов, выставленная в зоне интереса, включала в себя структуры как серого, так и белого вещества головного мозга (рис. 3). 
Измерения проводили в участках мозга, представляющих интерес для нашего исследования, а именно в структурах белого вещества мозга (колено, валик и тело мозолистого тела (МТ), белое вещество лобной и теменной долей) и серого вещества головного мозга (височная область, таламус и скорлупа). Измерения проводились на симметричных вокселах правого и левого полушарий головного мозга. Для отдельных вокселов, содержащих белое или серое вещество мозга, получены МР-спектры и проведена оценка индексов основных исследуемых метаболитов, к которым мы относили NAA — N-ацетиласпартат, Cho — холин, Сr — креатин (рис. 4). 
NAA — N-ацетиласпартат — аминокислота, которая синтезируется в митохондриях нейронов из аспартата и ацетил-кофермента, А посредством аспартат-N-ацетилтрансферазы (ANAT). NAA содержится в тканях в больших количествах и составляет 1% сухого веса, отвечая при этом за 3—4% суммарной осмолярности [9]. Концентрация в мозговом веществе составляет 6—7 нмоль/г, и в этом N-ацетиласпартат уступает лишь глутамату. Снижение уровня NAA считается достоверным индикатором нейрональной дисфункции и гибели нейронов [10]. Кроме того, установлено, что комплекс NAA выполняет протекторные, антитоксические и антиоксидантные функции, а также, возможно, участвует в процессе перекисного окисления липидов.
Cho — холин (компонент клеточных мембран) — является структурным компонентом более сложного органического фосфорсодержащего соединения — фосфатидилхолина, или лецитина, а также биологически активного ацетил-холина — медиатора нервного импульса. Он участвует в процессе синтеза и деградации фосфолипидов клеточных мембран.
Сr — креатин — участвует в энергетическом обмене клетки. Является поставщиком фосфатных групп для превращения аденозиндифосфата в аденозинтрифосфат. Принято считать, что общий уровень креатина стабилен в разных ситуациях, поэтому пик креатина часто используют в качестве референсного при сопоставлении с пиками других метаболитов [11].
Результатом спектроскопии является спектр, представляющий собой кривую из пиков метаболитов, каждый из которых имеет строго определенное значение резонансной частоты, что отражается в четкой локализации пиков вдоль шкалы относительных резонансных частот, значения которой принято считать в миллионных долях (ppm — parts per million) [12].
Результаты и обсуждение
Сетка вокселов, выставленная в зоне интереса, включала структуры как серого, так и белого вещества головного мозга (см. рис. 2 д, е). Оценка соотношений пиков основных метаболитов произведена в различных вокселах, содержащих белое и серое вещество больших полушарий. Измерения проводились на симметричных участках обоих полушарий головного мозга (табл. 1). 

В белом веществе лобной и теменной области статистически значимых отличий между отношениями всех метаболитов не выявлено. Однако в области колена МТ отношение NAA/Cr, равное 2,00±0,43, оказалось значимо ниже, чем в валике (2,77±0,75) и теле (2,48±0,37) (p 0,05), хотя в височных долях отношение Cho/Cr было выше, чем в скорлупе (p=0,05).
Значимых межполушарных отличий отношений метаболитов Cho/NAA, Cho/Cr, NAA/Cr не выявлено (p>0,05).
Объединенные по всем отделам неизмененного серого и белого вещества двух полушарий головного мозга средние значения соотношений основных метаболитов представлены в табл. 2. 
Оказалось, что между серым и белым веществом мозга наблюдаются статистически значимые отличия. Это в целом согласуется с данными других исследователей [15], подтверждающих факт высокой концентрации NAA-ацетиласпартата в белом веществе мозга.
P. Pouwels и J. Frahm [15] методом одновоксельной МРС, проведенной в поле 2,0 Тл, определяли содержание метаболитов мозговой ткани в вокселах, расположенных в белом веществе (лобная, затылочная и теменная области) и сером веществе (лобная, затылочная, теменная области, островок, таламус и мозжечок). В нашем исследовании содержание NAA в белом веществе оказалось значимо выше, чем в сером. Содержание Cr в белом веществе было стабильно (p>0,05). Содержание Сho в сером веществе было ниже содержания этого метаболита в белом веществе. Уровень Cr во всех отделах серого вещества оказался выше, чем в белом. Гендерных и межполушарных отличий не выявлено. В работе M. Stromillo и соавт. [18] методом 3D МРС получены значения отношения NAA/Cr=3,1±0,2 в подкорковом белом веществе и 2,4±0,1 в сером веществе коры в группе добровольцев. Š. Sivák и соавт. [19] для группы добровольцев (n=11) приводят значение NAA/Cr=1,80±0,13 в левой височной доле и 1,90±0,18 и 2,08±0,21 в правой и левой областях прецентральной извилины соответственно. В работе M. Donadieu и соавт. [16] для неизмененного белого вещества содержание NAA и Cho составило 10,0±0,68 и 4,30±0,60 соответственно. При этом отношение NAA/Cr составило 2,33.
Таким образом, полученные нами данные в целом согласуются с результатами работ, проведенных ранее другими исследователями. Это позволяет нам сделать вывод о высокой сопоставимости результатов, полученных методами 2D и 3D 1 Н-МРС, и рекомендовать второй из них как более информативный метод исследования метаболизма вещества головного мозга за счет его преимуществ в охвате анатомического пространства за клинически адекватное короткое время сканирования. Интересный факт различия в соотношениях основных метаболитов в проекции МТ требует дальнейшего изучения и сопоставления с его структурной и функциональной организацией.
Исследование выполнено при поддержке Российского научного фонда (Грант РНФ 18−15−00337 «Неинвазивное изучение энергетического метаболизма опухолей головного мозга»).
Концепция и дизайн исследования — И.П., Л.Ф., А.Т.
Сбор и обработка материала — А.Т., А.Б., Н.З.
Написание текста — А.Т.
Редактирование — И.П., Н.З., Л.Ф.
Авторы заявляют об отсутствии конфликта интересов.
Комментарий
Научная статья А.Н. Тюриной и соавт. посвящена применению метода 3D МР-спектроскопии в диагностике здоровых добровольцев без органической патологии головного мозга. В работе представлен обзор клинических методов МР-спектроскопии, начиная от ставшей стандартной одновоксельной МРС до объемной 3D МРС. Приведено подробное описание всех этапов проведения объемной МР спектроскопии, рассмотрены особенности клинического применения и проанализированы литературные данные по использованию 3D МРС в нейрохирургической клинике. Эти исследования позволили оценить диапазон значений основных метаболитов в отдельных анатомических образованиях неизмененного белого и серого вещества головного мозга.
Результатами данной работы являются показатели соотношений основных метаболитов, которые можно использовать в диагностике объемных образований головного мозга на предоперационном этапе, в дифференциальной диагностике опухолевых и неопухолевых поражений вещества мозга, а также в дифференциальной диагностике глиальных объемных образований.
Статья выполнена на высоком современном научно-методическом уровне и представляет научный интерес для читателей.