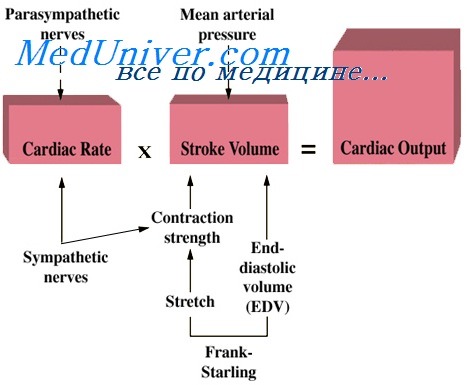
Ультразвуковой монитор для измерения параметров сердечного выброса
Мониторы Vigileo для контроля сердечного выброса и оксиметрии

Монитор Vigileo позволяет непрерывно мониторировать ключевые показатели гемодинамики, обеспечивая быстрый анализ клинической картины на основе минимально инвазивной, удобной в применении технологии. Монитор Vigileo может применяться с сенсорами FloTrac и оксиметрическими катетерами PreSep и PediaSat, является единым мониторинговым решением для обеспечения гемодинамической терапии.
Периоперационная гемодинамическая оптимизация
Доказательная медицина однозначно утверждает: Целенаправленная терапия улучшает клинические исходы лечения пациентов.
Множество клинических исследований(1-22) доказали, что целенаправленная гемодинамическая оптимизация у пациентов в хирургии высокого риска, начатая в операционной и продолженная в отделении реанимации, улучшает не только ближайшие результаты, но и долгосрочную выживаемость пациентов.
4 различных подхода к методике периоперационной оптимизации гемодинамики
Новые подходы к методике послеоперационной оптимизации гемодинамики доказали свою способность УЛУЧШАТЬ КЛИНИЧЕСКИЕ ИСХОДЫ
Оптимизация ударного объема
Измерение ударного объема с помощью сенсора FloTrac позволяет индивидуализировать инфузионную терапию, достигая максимального ударного объема на пологой части кривой Франка-Старлинга, что предотвращает как гиповолемию, так и риск гиперволемии.
Оптимизация вариабельности ударного объема
Точный показатель положения на кривой Франка-Старлинга у пациентов на ИВЛ, непрерывно мониторируется сенсором FloTrac.
Оптимизация доставки кислорода
Непрерывное измерение сердечного выброса с помощью сенсора FloTrac позволяет в сочетании с SaO2 и уровнем гемоглобина мониторировать и оптимизировать доставку кислорода путем инфузионной терапии и инотропной поддержки.
Оптимизация насыщения кислородом центральной венозной крови
Оксиметрический катетер PreSep обеспечивает непрерывное измерение ScvO2. Протокол терапии направлен на поддержание целевого значения ScvO2 > 73% путем инфузионной терапии и инотропной поддержки.
Ультразвуковой монитор для измерения параметров сердечного выброса

Поиск
Ультразвуковой мониторинг центральной гемодинамики лиц с нарушениями слуха
УДК 611.1:616.07
А.М. ГОЛОВАЧЕВ¹, Р.Г. БИКТЕМИРОВА¹, Н.И. ЗИЯТДИНОВА¹, И.И. ЗАКИРОВ², Т.Л. ЗЕФИРОВ¹
¹Казанский (Приволжский) федеральный университет, Институт фундаментальной медицины и биологии, 420012, Казань, ул. Карла Маркса, д. 74
²Казанская государственная медицинская академия – филиал ФГБОУ ДПО РМАНПО МЗ РФ, 420012, г. Казань, ул. Муштари, д. 11
Контактная информация:
Головачев Артем Михайлович — аспирант кафедры охраны здоровья человека, тел.
Биктемирова Раиса Габдулловна — доктор медицинских наук, профессор кафедры охраны здоровья человека, тел. (843) 292-92-66, e-mail: [email protected]
Зиятдинова Нафиса Ильгизовна — доктор биологических наук, профессор кафедры охраны здоровья человека, тел. (843) 292-92-66, e-mail: [email protected]
Закиров Игорь Ильдусович — главный внештатный детский специалист по анестезиологии и реанимации МЗ РТ, ассистент кафедры педиатрии с курсом поликлинической педиатрии, тел. (843) 236-20-84, e-mail: [email protected]
Зефиров Тимур Львович — доктор медицинских наук, профессор, заведующий кафедрой охраны здоровья человека, тел. (843) 292-92-66, e-mail: [email protected]
Статья поступила: 7.03.2018, принята к печати: 28.03. 2018.
Диагностика сердечно-сосудистой системы (ССС) является важнейшим аспектом современной медицины, в связи с тем, что состояние сердца и сосудов является наиболее распространенной причиной потери трудоспособности и смерти в настоящее время. В работе приведены данные исследования состояния сердечно-сосудистой системы молодых людей с различной степенью нарушения слуха методом ультразвукового мониторинга сердечного выброса. Выявлены достоверные различия значений показателей гемодинамики у людей с нарушениями слуха и здоровых людей. Выдвинуто предположение о влиянии слухового анализатора на состояние сердечно-сосудистой системы. Анализ полученных результатов свидетельствует об актуальности углубленной диагностики сердечно-сосудистой системы лиц с врожденными и хроническими заболеваниями органов чувств.
Ключевые слова: диагностика, сердечно-сосудистая система, ультразвуковые методы исследования, гемодинамика, сердечный выброс.
(Для цитирования: Головачев А.М., Биктемирова Р.Г., Зиятдинова Н.И., Закиров И.И., Зефиров Т.Л. Ультразвуковой мониторинг центральной гемодинамики лиц с нарушениями слуха. Практическая медицина. 2018)
A.M. GOLOVACHEV¹, R.G. BIKTEMIROVAB¹, N.I. ZIYATDINOVA¹, I.I. ZAKIROV², T.L. ZEFIROV¹
¹Kazan (Volga Region) Federal University, Institute of Fundamental Medicine and Biology, 74 Karl Marx Str., Kazan, Russian Federation, 420012
²KSMA –– Branch Campus of the FSBEI FPE RMACPE MOH Russia, 11 Mushtari Str., Kazan, Russian Federation, 420012
Ultrasound monitoring of central hemodynamics in patients with hearing impairments
Golovachev A.M. — postgraduate student of the Department of Human Health Protection, tel. +7-927-249-40-11, e-mail: [email protected]
Biktemirova R.G. — D. Med. Sc., Professor of the Department of Human Health Protection, tel. (843) 292-92-66, e-mail: [email protected]
Ziyatdinova N.I. — D. Biol. Sc., Professor of the Department of Human Health Protection, tel. (843) 292-92-66, e-mail: [email protected]
Zakirov I.I. — Chief Free-lance specialist in children’s anesthesiology and resuscitation of the Ministry of Healthcare of Republic of Tatarstan, Assistant Lecturer of the Pediatrics Department with the course of polyclinic pediatrics, tel. (843) 236-20-84, e-mail: [email protected]
Zefirov T.L. — D. Med. Sc., Professor, Head of the Department of Human Health Protection, tel. (843) 292-92-66, e-mail: [email protected]
Diagnosing the diseases of cardiovascular system is one of the most important aspects of modern medicine, as today the state of heart and vessels is the main cause of the loss of working capacity and death. The paper presents the data of cardiovascular system examination in young people with various degrees of hearing impairment, with the technique of ultrasound cardiac output monitoring. The reliable differences were found between the hemodynamics indicators in healthy people and in people with hearing impairments. A hypothesis is put forward about the influence of the acoustic analyzer on the state of cardiovascular system. Analysis of the obtained data prove the topicality of the profound diagnostics of cardiovascular system in persons with congenital and chronic diseases of sense organs.
Key words: diagnostics, cardiovascular system, ultrasonic methods of research hemodynamics, cardiac output.
Введение. По данным Всемирной Организации Здравоохранения, заболевания сердечно-сосудистой системы (ССС) являются основной причиной смерти во всем мире в течение последних 15 лет [1]. В связи с этим мониторинг деятельности сердца и сосудов становится все более актуальным, что также справедливо для лиц, не имеющих заболеваний ССС и не состоящих на учете у врача-кардиолога. В первую очередь, это касается наследственной патологии анализаторов, в частности слуховых органов. Для того, чтобы определить, насколько велико воздействие врожденного заболевания, необходим углубленный мониторинг центральной гемодинамики. Важным моментом является то, что при некоторых врожденных заболеваниях не так очевидно влияние основной патологии на работу CCC. Однако в литературе есть данные о том, что потеря слуха может предшествовать клиническому проявлению ишемической болезни сердца, является «ранним маркером» артериосклеротического процесса [2]. Кроме того, проводились исследования по выявлению факторов риска сердечно-сосудистых заболеваний у лиц с различными нарушениями слуха [3]. В связи с этим работы по выявлению отклонений в гемодинамических параметрах у лиц с патологией слуховых органов становятся еще более значимыми.
Целью нашего исследования явилось измерение показателей систолического выброса в аорту у лиц с ограниченными возможностями здоровья по слуху, без выявленных патологий сердечно-сосудистой системы.
Материал и методы исследования. Исследование гемодинамических параметров проводилось у молодых людей 20–25 лет, средний возраст — 22±1,7 (М±σ) лет, в количестве 54 человек, из них 26 мужчин, 28 женщин. Из общего числа принявших участие в исследовании 30 молодых людей имели патологию слуховых органов различной степени и этиологии. Молодые люди с ограниченными возможностями здоровья в ходе исследования были разделены на две группы в соответствии со степенью поражения слуха. В 1-ю группу были включены 14 пациентов с IV степенью тугоухости, а также полностью лишенные слуха, из них 7 мужчин и 7 женщин; средний возраст — 21±2,1 (М±σ) лет. 2-я группа состояла из 16 лиц с I–III степенью тугоухости, из них 9 мужчин и 7 женщин; средний возраст — 22±2,0 (М±σ) лет. Степень тугоухости определялась в соответствии с последними данными аудиометрии, проводимой специалистом-оториноларингологом. Проверка слуха осуществлялась дважды в год, последняя из которых была проведена не более, чем за 2 месяца до начала исследований. Дифференцирование по этиологическому признаку не проводилось, однако, следует отметить, что в подавляющем большинстве участники 1-й группы имели врожденную патологию, участники 2-й группы — приобретенную. В качестве контрольной группы (3-я группа) в исследовании приняли участие 24 молодых человека, не имеющие в анамнезе выраженных отклонений в состоянии ССС и в работе анализаторов, из них 10 мужчин и 14 женщин; средний возраст — 22±1,0 (М±σ) лет. Нами были проведены измерения параметров систолического выброса в аорту с помощью ультразвукового (УЗ) монитора сердечного выброса (USCOM 1-А, Ultrasound Cardiac Output Monitor, Австралия), оснащенного датчиком с частотой 2,2 МГц.
На первом этапе исследования до начала проведения измерений было необходимо определить диаметр отверстия аортального клапана, от значения которого зависят рассчитываемые параметры ССС. С этой целью был проведен сбор антропометрических данных, которые вместе с данными о возрасте и поле были внесены в карту обследуемого. Диаметр отверстия аортального клапана при этом рассчитывался автоматически на основе введенных данных, что может поставить под сомнение точность полученных значений. Однако в нескольких источниках [4, 5, 6, 7, 8] приводятся данные о приемлемой точности измерений с помощью данного метода, в сравнении с чреспищеводной эхокардиографией и даже инвазивными методами исследования сердечного выброса. Значения систолического (АДс) и диастолического (АДд) давлений, измеренных непосредственно перед началом исследования показателей сердечного выброса также вводились в память монитора. Для проведения измерений требовалось выбрать режим доступа в настройках монитора — AV-режим для получения показателей выброса в аорту либо PV-режим для измерения параметров выброса в легочную артерию, что является определяющим для выбора локализации датчика: супрастернальное положение для AV-режима или парастернальное для PV-режима. Нами был выбран AV-режим.
Следующим этапом являлось точное позиционирование датчика в супрастернальном положении так, чтобы пучок УЗ волн был точно направлен в просвет восходящей части аорты по направлению к аортальному клапану. Правильное позиционирование датчика определялось по трем критериям:
– скорость потока крови (Vpk) (имеет определенные границы для различных возрастных групп; в нашем случае от 1,1–1,4 м/сек);
– графическое изображение пика выброса на экране монитора (должно быть определенной формы и окраски; не должно иметь помехи и сдвоенные верхушки);
– звуковой сигнал (имеет определенный тон во время выброса).
После настройки датчика и получения требуемого изображения на экране монитора продолжили измерение сердечного выброса до появления нескольких практически одинаковых по амплитуде графических пиков выброса в аорту (для первичной оценки сердечного выброса достаточно наличие 7–8 графически выверенных пиков). Для получения средних значений проводили измерение в течение 1 минуты с выбором практически одинаковых по амплитуде пиков в количестве от 5 до 8 с равным интервалом между ними. Получены и проанализированы значения показателей состояния ССС: частота сердечных сокращений (ЧСС); систолическое артериальное давление (АДс); пульсовое давление (ПД); среднее артериальное давление (MAP); ударный объем (УО); сердечный выброс (СВ); сердечный индекс (СИ); максимальная скорость потока (Vpk), расстояние в минуту (minute distance, MD) и др.
Статистическую обработку полученных данных проводили с помощью компьютерной программы Biostat. Средние значения представлены в виде М±σ. Вероятность межгрупповых различий определяли по критерию Стьюдента. Различия считали достоверными при р
Ультразвуковой монитор для измерения параметров сердечного выброса
Неинвазивные технологии ультразвуковых методов определения сердечного выброса реализованы в ультразвуковых (УЗ) эхокардиографах. Они строятся на двух основных принципах.
Первый принцип основан на особенностях отражения ультразвуковой волны в неоднородных по плотности средах. На границе этих неоднородных сред происходит изменение мощности (амплитуды) отраженной волны. Коэффициент отражения (степень изменения мощности волны) зависит от разности сопротивления сред, обусловленных их плотностью (акустический импеданс). Даже ткани одного органа имеют разный акустический импеданс, и благодаря этому могут наблюдаться (проецироваться на экран монитора) раздельно, создавая конкретную картину внутрисердечной топографии. Потенциальная пространственная разрешающая способность метода определяется длиной волны зондирующего сигнала. Минимальный размер наблюдаемого объекта равен 1/4 длины волны.
Второй принцип основан на особенностях отражения ультразвуковой волны от движущихся объектов (движение крови, стенок сердца, клапанов). В результате прохождения ультразвука через движущуюся среду происходит изменение частоты отражения зондирующего сигнала. Частота увеличивается в случае встречного потока и соответственно уменьшается при согласном прохождении потока и сигнала (эффект Допплера).
Доплеровский метод измерения дает возможность различать объекты по их положению в пространстве и их скорости. Потенциально разрешающая способность по скорости определяется частотой зондирующего сигнала.
В современных УЗ эхокардиографах оба эти принципа объединены в единый технологический комплекс.
В соответствии с указанными принципами существуют два способа регистрации сердечного выброса.
Первый способ основан на определении объема левого желудочка. Измеряется площадь и длина полости левого желудочка во время систолы и диастолы сердца.
Объем полости желудочка рассчитывается по формуле:
V=0.85*A2*L-1, где
V — объем полости левого желудочка,
А — площадь левого желудочка,
L — длина полости левого желудочка.
Для более точного вычисления площади полости левого желудочка используется так называемый метод дисков. Измеряются и суммируются площади 20 уровней (срезов) полости левого желудочка. Этот метод применяется в случаях поражения миокарда, при которых в силу снижения сократительной способности в отдельных регионах желудочка площади могут быть неодинаковыми.
Систолический объем сердца и фракция выброса рассчитываются по формулам:
SV (мл) = Vd-Vs ФВ(%) = SV*Vd-1, где
SV — систолический объем сердца (stroke volume),
Vd — объем левого желудочка в конце диастолы,
Vs — объем левого желудочка в конце систолы.
Второй способ расчета сердечного выброса основан на измерении объемного кровотока через аортальный клапан (Допплер эхокардиография). Регистрируются линейные скорости перемещения крови и по интегралу линейной скорости кровотока определяется площадь под кривой допплерограммы.
Систолический объем левого желудочка рассчитывается по формулам:
SV= VTI*1/4D2 или SV= Vm*ET*1/4D2, где
SV — систолический объем левого желудочка,
VTI — интеграл линейных скоростей (площадь левого желудочка),
ЕТ — продолжительность изгнания крови из левого желудочка,
D — внутренний диаметр фиброзного кольца аортального клапана,
1/4 D2 — площадь фиброзного кольца аортального клапана.
В последнее время повышенное внимание привлекает так называемый трансэзофагеальный метод эхокардиографии. Принцип трансэзофагеального доплеровского мониторинга сердечного выброса, предложенный еще в начале 1970-х годов, подвергся существенному технологическому развитию и клинической оценке.
Метод предполагает наличие датчика, выполненного в виде зонда, который устанавливается в пищеводе на уровне сердца, что минимизирует помеховые сигналы от костей, мягкой ткани и легкого.
Несмотря на наличие потенциальных источников ошибок (точность положения датчика), отмечена высокая корреляция между данными, полученными трансэзофагеальным методом и традиционной термодилюцией.
Ультразвуковой монитор для измерения параметров сердечного выброса
Site language:
АнгиоСкан
Наука
Данные о состоянии сосудистой стенки, полученные на приборах «АнгиоСкан», могут использоваться для определения сердечно-сосудистого риска у людей, страдающих:
Приборы могут использоваться как в клиниках, так и в домашних условиях (помощь медицинского персонала не требуется). Для этого разработаны и сертифицированы несколько моделей аппаратов: двухканальный комплекс АнгиоСкан-01 для работы в лечебно-диагностических учреждениях, одноканальный прибор АнгиоСкан-01M, предназначенный как для клинического применения, так и для домашней диагностики, и портативный автономный прибор для персональной (домашней) диагностики здоровья сердечно-сосудистой системы АнгиоСкан-01П.
Пятиминутная неинвазивная диагностика сосудов диагностическими комплексами АнгиоСкан позволяет:
Рекомендуем Вашему вниманию статью об устройстве сосудистой системы, которая написана языком, понятным неподготовленному читателю.
Инфаркт миокарда и инсульт довольно часто может явиться первым и неожиданным проявлением стенозирующего атеросклероза сосудов у лиц, которые до этого события не имели каких-либо клинических проявлений этого хронического процесса. Этим во многом определяется важность разработки новых подходов по выявлению лиц с высоким риском развития ССЗ. Решение этой диагностической проблемы позволит эффективно и целенаправленно проводить медикаментозную терапию у этих пациентов. Имеющиеся подходы и алгоритмы основаны на статистических взаимосвязях факторов риска с развитием того или иного неблагоприятного сердечно-сосудистого события (острый инфаркт миокарда, нестабильная стенокардия, инсульт). Данный подход позволяет выделить три категории лиц: с высоким, средним и низким уровнем риска. Однако анализ его применения показал, что, например, в США более одной трети взрослого населения страны находятся в средней категории риска. В такой ситуации для принятия решения о проведении профилактической медикаментозной терапии необходима более детальная информация о каждом индивидууме этой группы. Такую принципиальную возможность дает оценка состояния артериальной стенки (эндотелиальная функция и ригидность), что подтверждается результатами ряда выполненных исследований, в которых показана высокая прогностически значимая информация, которая существенно улучшает ситуацию с выявлением лиц с высокой угрозой развития инфаркта или инсульта.
В Российской Федерации смертность от ССЗ стабильно составляет 57%, что за два последних года составило 2,4 млн. человек. При этом почти 20% из этого числа умирают в трудоспособном возрасте. В основе возникновения этих состояний находятся нарушения функции артериальной стенки, определяемые прогрессированием атеросклероза. Принципиально изменить эту ситуацию возможно только с помощью мероприятий по первичной профилактике этих заболеваний. Новые медицинские знания и развитие новой медицинской диагностической техники позволяющей проводить раннюю диагностику ССЗ дают возможность изменить ситуацию с ССЗ в России.
Ультразвуковой монитор для измерения параметров сердечного выброса
М.Ю. Киров
М.Ю. Киров, доктор медицинских наук. Северный государственный медицинский университет, Архангельск
Мониторинг гемодинамики является одной из важнейших составных частей современного мониторинга в отделении анестезиологии, реанимации и интенсивной терапии (ОАРИТ). Так, параметры системы кровообращения составляют практически половину из всех компонентов Гарвардского стандарта мониторинга, который служит регламентирующей основой для проведения анестезиологического пособия (табл. 1) [Крафт Т.М., Аптон П.М., 1997].
Гарвардский стандарт мониторинга
2) АД и пульс √ каждые 5 мин.
3) Вентиляция √ минимум 1 из параметров:
4) Кровообращение √ минимум 1 из параметров:
5) Дыхание √ аудиосигнал тревоги для контроля дисконнекции дыхательного контура.
6) Кислород √ аудиосигнал тревоги для контроля нижнего предела концентрации на вдохе.
Ведущими принципами мониторинга гемодинамики являются точность, надежность, возможность динамического наблюдения за больным, комплексность, наличие минимального количества осложнений, практичность и дешевизна, а также доступность получаемой информации. На этапах мониторинга становится возможной ранняя диагностика нарушений со стороны системы кровообращения, принятие решения и своевременная коррекция выявленных нарушений.
Минимальный объем мониторинга гемодинамики, который по международным стандартам должен осуществляться в ходе любой анестезии, включает в себя проведение пульсоксиметрии, неинвазивного измерения АД (предпочтительно аппаратным способом) и ЭКГ. Однако многим пациентам ОАРИТ требуется расширенный мониторинг гемодинамики, включающий несколько из представленных ниже компонентов.
Постоянный мониторинг ЭКГ
ЭКГ обеспечивает важной информацией о ЧСС, ритме, проводимости, ишемии миокарда и эффектах назначаемых препаратов. Для оценки сердечного ритма наиболее часто используется стандартное отведение II, однако следует помнить, что оно не обладает высокой чувствительностью в отношении признаков ишемии. Сочетание отведения II с левыми грудными отведениями (отведение V5) повышает чувствительность ЭКГ мониторинга в диагностике изменений сегмента ST с 33% до 80% [Higgins MJ., Hickey S., 2003]. Многие современные мониторы автоматически измеряют динамику сегмента ST и выводят на экран тренды, анализирующие выраженность ЭКГ-признаков ишемии, что позволяет своевременно начать назначение нитратов и осуществлять другие лечебные мероприятия.
Пульсоксиметрия
В основе пульсоксиметрии лежат принципы оксиметрии и плетизмографии. В ходе оксиметрии за счет различной способности оксигемоглобина и дезоксигемоглобина абсорбировать лучи красного и инфракрасного спектра рассчитывается насыщение артериальной крови кислородом (SаO2, в норме 95-100%). Это дает возможность оценить адекватность оксигенирующей функции легких, доставки кислорода к тканям и ряда других важных физиологических процессов и обеспечивает своевременное назначение оксигенотерапии, ИВЛ и прочих лечебных мероприятий. Кроме того, пульсоксиметры позволяют осуществлять постоянное измерение ЧСС и демонстрируют на дисплее плетизмограмму √ пульсовую волну, отражающую наполнение капилляров и состояние микроциркуляторного русла. Информативность пульсоксиметрии значительно снижается при расстройствах периферической микроциркуляции. Уменьшение сатурации не следует однозначно рассматривать как признак нарушения микроциркуляции, для уточнения диагноза необходимо выполнить анализ газового состава артериальной крови.
Технология пульсоксиметрии привела к появлению таких новых методов мониторинга, как измерение сатурации кислородом смешанной венозной крови и крови из центральной вены, позволяющих детально оценить транспорт кислорода и его потребление тканями и целенаправленно назначить инотропную и инфузионную терапию. Неинвазивная оксиметрия головного мозга дает возможность определить регионарное насыщение гемоглобина кислородом в мозге (rSO2, в норме приблизительно 70%). Доказано, что при остановке кровообращения, эмболии сосудов головного мозга, гипоксии и гипотермии, происходит выраженное снижение rSO2 [Морган Д.Э., Михаил М.С., 1998].
Артериальное давление (АД)
Методика и частота измерения АД определяются состоянием больного и видом хирургического вмешательства. При стабильной гемодинамике, как правило, достаточно неинвазивного измерения АД, предпочтительно аппаратным способом. Основные показания к инвазивному мониторингу АД включают следующие состояния:
1) быстрое изменение клинической ситуации у больных, находящихся в критическом состоянии (шок, рефрактерный к инфузионной терапии, острое повреждение легких, состояние после сердечно-легочной реанимации и др.);
2) применение вазоактивных препаратов (инотропы, вазопрессоры, вазодилататоры, анестетики, антиаритмики и др.);
3) высокотравматичные хирургические вмешательства (кардиохирургия, нейрохирургия, операции на легких и др.);
4) забор артериальной крови для анализов (газы крови, общие исследования).
Инвазивный мониторинг АД осуществляется при помощи катетеризации артерии (как правило, лучевой или бедренной). Это позволяет получать информацию о систолическом, диастолическом и среднем АД в каждый отдельно взятый момент времени. Кривая АД предоставляет непосредственную информацию о гемодинамическом эффекте аритмии. К тому же по крутизне анакроты можно косвенно судить о постнагрузке и сократительной способности миокарда. Основная цель лечебных мероприятий на основе мониторинга АД √ поддержание среднего АД, отражающего перфузионное давление различных органов, на уровне 70-90 мм рт. ст.
Все системы прямого измерения АД создают артефакты, которые обусловлены неадекватным соединением, попаданием пузырьков воздуха в катетер, слишком выраженным или недостаточным демпфирующим эффектом системы и дрейфом нуля. Вышеперечисленные проблемы должны быть устранены до начала мониторинга.
Центральное венозное давление (ЦВД)
Первоочередные показания к мониторингу ЦВД включают наличие гиповолемии, шока и сердечной недостаточности. Кроме того, доступ к центральной вене необходим для обеспечения надежного пути назначения вазоактивных препаратов, инфузионной терапии, парентерального питания, аспирации воздуха при воздушной эмболии, электрокардиостимуляции, проведения экстракорпоральных процедур и т.д. ЦВД приблизительно соответствует давлению в правом предсердии (50-120 мм вод. ст. или 4-9 мм рт. ст.), которое в значительной мере определяется конечно-диастолическим объемом правого желудочка. У здоровых людей, как правило, работа правого и левого желудочков изменяется параллельно, поэтому ЦВД косвенно отражает и заполнение левого желудочка [Морган Д.Э., Михаил М.С., 1998]. К сожалению, на фоне дисфункции миокарда и повышенной проницаемости сосудов ЦВД далеко не всегда позволяет адекватно предсказать изменения волемического статуса пациента и преднагрузки и серьезно уступает по своему прогностическому значению волюметрическим параметрам гемодинамики [Кузьков В.В. и соавт., 2003].
Изменения ЦВД достаточно неспецифичны. Так, повышение ЦВД наблюдается при правожелудочковой недостаточности, пороках сердца, гиперволемии, тромбоэмболии легочной артерии, легочной гипертензии, тампонаде сердца, увеличении внутригрудного давления (ИВЛ, гемо- и пневмоторакс, ХОБЛ), повышении внутрибрюшного давления (парез ЖКТ, беременность, асцит), повышении сосудистого тонуса (увеличение симпатической стимуляции, вазопрессоры). Снижение ЦВД отмечается при гиповолемии (кровотечение, диспептический синдром, полиурия), системной вазодилатации (септический шок, передозировка вазодилататоров, дисфункция симпатической нервной системы), региональной анестезии и др. Тренды динамики ЦВД более информативны, чем однократное измерение. Определенную информацию можно получить и при оценке формы кривой ЦВД, которая соответствует процессу сердечного сокращения [Higgins MJ, Hickey S.].
Катетеризация легочной артерии и термодилюция
У пациентов с выраженными нарушениями функции сердечно-сосудистой системы целесообразно применять дополнительные объективные методы оценки сердечного выброса (СВ) и тех факторов, которые его определяют: преднагрузки, сократимости миокарда, постнагрузки, ЧСС и состояния клапанного аппарата сердца. В большинстве случаев для этого осуществляют препульмональную (с использованием катетеризации легочной артерии) и транспульмональную (катетеризация бедренной артерии) термодилюцию.