методом молекулярной гибридизации можно установить что
Методом молекулярной гибридизации можно установить что
11. Молекулярно-генетические методы, используемые в диагностике инфекционных болезней (полимеразная цепная реакция, метод молекулярной гибридизации, рестрикционный анализ).
А. ПЦР можно проводить для достижения трех целей.
1. Для обнаружения в патологическом материале конкретного вида микроорганизма без выделения чистой культуры.
2. Для идентификации выделенных чистых культур микроорганизмов.
3. Для генотипирования микроорганизмов, т.е. определения генетических вариантов одного вида.
Б. Принцип осуществления ПЦР заключается в увеличении (амплификации) количества искомого гена при положительной или (отсутствие такого увеличения) при отрицательной реакции.
Рис. 14.2-1. Принцип положительной ПЦР: экстракция ДНК и, если в ней содержится искомый ген, ее количество в процессе реакции резко увеличивается, что выявляется с помощью электрофореза
1. Сначала из патологического материала или культуры микроорганизмов выделяется ДНК.
2. Затем путем нагрева в щелочной среде ДНК расплетается на две отдельные нити.
3. После этого в реакционную смесь добавляют праймеры (участки ДНК, комплементарные 3’-концам искомого гена).
4. Реакционную смесь охлаждают.
5. Если в исследуемой ДНК имеется искомый ген, то праймеры создают фрагменты двухцепочечной ДНК, связываясь с комплементарными участками «своего» гена.
6. Затем в реакционную смесь добавляют нуклеотиды и ДНК-полимеразу.
7. Если в реакционной смеси наличествуют двухцепочечные фрагменты ДНК, то нуклеотиды присоединяются к 3’-концам праймеров, полностью достраивая соответствующий ген на всем его протяжении. А так как синтез начинался на каждой нити ДНК отдельно, то в результате получается две молекулы двухцепочечного ДНК. Другими словами, количество ДНК увеличивается в два раза.
8. Повторение циклов (от 30 до 80 раз) приводит к накоплению (амплификации) искомого гена.
9. На завершающем этапе определяют количество ДНК в реакционной смеси с помощью электрофореза. При положительной реакции оно резко возрастает, в случае отрицательного результата – не изменяется. Полимеразная цепная реакция – сложная процедура, требующая квалифицированного персонала, комплекса оборудования и специальных расходных материалов. Для проведения реакции оборудуется специальное помещение, которое часто так и называется: лаборатория ПЦР.
Метод молекулярной гибридизации. Этот метод используется для выявления степени сходства различных ДНК (при идентификации микроорганизмов проводят сравнение ДНК выделенного штамма с ДНК эталонного штамма).
А. Исследуемую ДНК нагревают в щелочной среде для расплетения ее на две отдельные нити.
Б. Одну из них закрепляют на специальном фильтре.
В. Этот фильтр помещают в раствор, содержащий радиоактивный зонд (одноцепочечную молекулу ДНК эталонного штамма, меченную радиоактивным изотопом).
Г. Затем температуру реакционной смеси понижают, чтобы создать условия для восстановления двухцепочечной структуры ДНК.
Д. В случае, если исследуемая ДНК и ДНК эталонного штамма относятся к одному виду – в реакционной смеси формируется двухцепочечная ДНК. При отрицательной реакции двухцепочечная ДНК не формируется (для оценки реакции используется биохимическая методика). На практике все связи двух цепочек полностью не восстанавливаются из-за высокого уровня генетической изменчивости микроорганизмов, поэтому реакцию оценивают по степени гомологии – проценту восстановленных связей между двумя цепочками ДНК.
Этот метод основан на способности ферментов рестрикции специфически расщеплять ДНК в определённых сайтах.
Рис. 7. Схема рестрикционного анализа
Если происходит изменение в сайте узнавания (мутация, рекомбинация, метилирование ДНК и т.д.) рестриктаза теряет способность выполнять свою функцию. Основная идея заключается в следующем: различные последовательности ДНК приводят к расщеплению ДНК ферментами рестрикции в разных местах. Полученные с помощью рестриктаз фрагменты ДНК служат маркерами различных процессов, происходящих внутри клетки исследуемого организма.
Гибридизация нуклеиновых кислот
На явлении денатурации и ренативации основан метод, называемый «молекулярная гибридизация».Процесс гибридизации может осуществляться между двумя любыми цепями нуклеиновых кислот (ДНК-ДНК, ДНК-РНК) при условии, что они содержат комплементарные последовательности нуклеотидов. Такие гибридные структуры можно выделить центрифугированием в градиенте плотности сахарозы или наблюдать в электронном микроскопе.
Если раствор, содержащий образцы ДНК 1 и 2, выделенные из организмов разных видов, денатурировать, а затем провести ренатива-цию, то образуются двухспиральные структуры. Но наряду с исходными ДНК 1 и ДНК 2 образуются гибридные двойные спирали, содержащие цепь ДНК образца 1 и цепь ДНК образца 2, где присутствуют как спирализо-ванные, так и неспирализованные участки. В неспирализованных участках фрагменты цепей ДНК не комплементарны, т.е. в ходе гибридизации получаются несовершенные гибриды. Методом молекулярной гибридизации можно установить:
сходство и различие первичной структуры разных образцов нуклеиновых кислот;
различие ДНК, выделенных из организмов разных видов;
идентичность ДНК всех органов и тканей одного организма.
При проведении гибридизации ДНК-РНК были выделены гибридные молекулы, содержащие одну цепь ДНК и одну цепь РНК. Если для эксперимента были взяты ДНК и РНК (первичный транскрипт), выделенные из одного организма, то образовывались совершенные гибриды, потому что молекула РНК комплементарна цепи ДНК. Гибридизацией ДНК-РНК было впервые установлено, что все виды РНК клетки имеют на молекуле ДНК комплементарные участки.
Первоначально классическим методом выявления вирусного генома считался высокоспецифичный метод гибридизации НК, но в настоящее время все шире используется выделение геномов вируса с помощью полимеразной цепной реакции (ПЦР).
Молекулярная гибридизация нуклеиновых кислот. Метод основан на гибридизации комплементарных нитей ДНК или РНК с образованием двунитевых структур и на выявлении их с помощью метки. Для этой цели используются специальные ДНК- или РНК-зонды, меченные изотопом ( 32 Р) или биотином, обнаруживающие комплементарные нити ДНК или РНК. Существуют несколько вариантов метода:
– точечная гибридизация – выделенную и денатурированную НК наносят на фильтры и затем добавляют меченый зонд; индикация результатов – авторадиография при использовании 32 Р или окраска – при авидин-биотине;
– блот-гибридизация – метод выделения фрагментов НК, нарезанных рестрикционными эндонуклеазами из суммарной ДНК и перенесенных на нитроцеллюлозные фильтры и тестируемые мечеными зондами; используется как подтверждающий тест при ВИЧ инфекции;
– гибридизация in situ – позволяет определять НК в инфицированных клетках [7].
ПЦР основана на принципе естественной репликации ДНК. Суть метода заключается в многократном повторении циклов синтеза (амплификации) вирусспецифической последовательности ДНК с помощью термостабильной Taq ДНК-полимеразы и двух специфических затравок – так называемых праймеров.
Каждый цикл состоит из трех стадий с различным температурным режимом. В каждом цикле удваивается число копий синтезируемого участка. Вновь синтезированные фрагменты ДНК служат в качестве матрицы для синтеза новых нитей в следующем цикле амплификации, что позволяет за 25–35 циклов наработать достаточное число копий выбранного участка ДНК для ее определения, как правило, с помощью электрофореза в агарозном геле.
Метод высокоспецифичен и очень чувствителен. Он позволяет обнаружить несколько копий вирусной ДНК в исследуемом материале. В последние годы ПЦР находит все более широкое применение для диагностики и мониторинга вирусных инфекций (вирусы гепатитов, герпеса, цитомегалии, папилломы и др.) [8, 9].
Разработан вариант количественной ПЦР, позволяющий определять число копий амплифицированного сайта ДНК. Методика проведения сложна, дорогостояща и пока недостаточно унифицирована для рутинного применения.
28. Третичная структура ДНК. Роль гистоновых и негистоновых белков в компактизации ДНК. Организация хроматина. Ковалентная модификация гистонов и ее роль в регуляции структуры и активности хроматина.
Каждая молекула ДНК упакована в отдельную хромосому. В диплоидных клетках человека содержится 46 хромосом.Общая длина ДНК всех хромосом клетки составляет 1,74 м, но она упакована в ядре, диаметр которого в миллионы раз меньше. Чтобы расположить ДНК в ядре клетки, должна быть сформирована очень компактная структура. Компактизация и суперспирализация ДНК осуществляются с помощью разнообразных белков, взаимодействующих с определёнными последовательностями в структуре ДНК. Все связывающиеся с ДНК эукариотов белки можно разделить на 2 группы: гисгоновые и негистоновые белки.Комплекс белков с ядерной ДНК клеток называют хроматином.
Гистоны— белки с молекулярной массой 11-21 кД, содержащие много остатков аргинина и лизина. Благодаря положительному заряду гистоны образуют ионные связи с отрицательно заряженными фосфатными группами, расположенными на внешней стороне двойной спирали ДНК.
Существует 5 типов гистонов. Четыре гистона Н2А, Н2В, НЗ и Н4 образуют октамерный белковый комплекс (Н2А, Н2В, НЗ, Н4)2, который называют «нуклеосомный кор»(от англ. nucleosome core). Молекула ДНК «накручивается» на поверхность гистонового октамера, совершая 1,75 оборота (около 146 пар нуклеоти-дов). Такой комплекс гистоновых белков с ДНК служит основной структурной единицей хроматина, её называют «нуклеосома».ДНК, связывающую нуклеосомные частицы, называют линкерной ДНК. В среднем линкерная ДНК составляет 60 пар нуклеотидных остатков. Молекулы гистона H1 связываются с ДНК в межнуклеосомных участках (линкерных последовательностях) и защищают эти участки от действия нуклеаз.
В ядре каждой клетки присутствует около 60 млн молекул каждого типа гистонов, а общая масса гистонов примерно равна содержанию ДНК. Аминокислотные остатки лизина, аргинина и концевые аминогруппы гистонов могут модифицироваться: ацетилироваться, фосфорилироваться, метилироваться или взаимодействовать с белком убиквитином (негистоновый белок). Модификации бывают обратимыми и необратимыми, они изменяют заряд и конформацию гистонов, а это влияет на взаимодействие гистонов между собой и с ДНК. Активность ферментов, ответственных за модификации, регулируется и зависит от стадии клеточного цикла. Модификации делают возможными конформационные перестройки хроматина.
Гибридизация нуклеиновых кислот. Метод ДНК-зондов
Молекулярная гибридизация имеет большое преимущество перед остальными системами идентификации, и прежде всего в тех случаях, когда по разным причинам изменено внешнее проявление диагностического признака, так как в генетическом материале очень редко происходят столь большие изменения, которые бы привели к ложноотрицательному результату.
Есть и другие доводы в пользу гибридизации:
Принцип метода. Метод основан на специфическом взаимодействии (гибридизации) двух образцов ДНК: меченого ДНК-зонда и участка плазмидной или хромосомной ДНК (Г. Бантинг и др., 1990). Образовавшиеся двухцепочечные ДНК отделяют от одноцепочечных и определяют присутствие метки. В качестве контроля используют ДНК известного штамма микроорганизма. Степень реассоциации таких гомологичных одноцепочечных ДНК принимают условно за 100 %. При 60…100 % гомологии ДНК можно говорить о принадлежности сравниваемых бактерий к одному виду.
Проведение реакции. Разработаны два способа гибридизации: в растворе или с использованием нерастворимого носителя. Гибридизация на носителях применяется значительно шире: анализируемый образец связывается с нитроцеллюлозным или нейлоновым фильтром.
Для микробиологов больше подходит метод гибридизации in situ, позволяющий быстро проводить идентификацию бактерий. Сначала исследуемые бактерии подращивают на фильтре, либо переносят на фильтр с агара, либо наносят на фильтр небольшие количества бактериальной взвеси. Затем клетки лизируют, высвободившуюся ДНК фиксируют прогреванием. Следующий этап — проведение гибридизации на фильтре с внесенным меченым ДНК-зондом. После гибридизации фильтр несколько раз промывают специальными растворами и проводят детекцию метки.
Существует несколько разных методов мечения комплекса между зондом и ДНК-мишенью. Традиционным способом является радиоактивное мечение зонда с помощью введения в ДНК радиоактивных изотопов 33 Р, 32 Р, 35 S. После гибридизации образцы-мишени выявляют с помощью радиоавтографии. Этот метод обладает высокой чувствительностью и позволяет обнаруживать около 1 пг ДНК. Недостаток радиоактивных зондов — их нестабильность из-за непродолжительного времени жизни изотопов ( 32 Р — 14,5 сут) и быстрого радиолиза зонда. Использование изотопов с более продолжительным периодом полураспада приводит к снижению чувствительности и удлиняет время, необходимое для радиоавтографии. Кроме того, для работы с изотопами необходимы специально оснащенные лаборатории.
Наиболее широко используют нерадиоактивное мечение. Для нерадиохимической детекции применяют методы, основанные на присоединении к зондам остатков биотина (G. Gebeyehu et al., 1987). Биотин (витамин Н), широко распространенный в природе и синтезируемый кишечными микроорганизмами, сам по себе меткой не является, но он обладает высоким сродством с авидином (стрептавидином). Авидин — глюкопротеид яичного белка, связывающий биотин с образованием нерастворимого комплекса биотин—авидин. Используя биотинилированный фермент и зонд, несущий один или несколько остатков биотина, можно осуществить ферментативную детекцию связанного с мишенью зонда. Авидин связывается с образовавшимся комплексом из двух гомологичных цепей ДНК и присоединяет биотинилированный фермент, который выявляют с помощью соответствующего окрашенного субстрата. Метод обладает более низкой чувствительностью, чем радиохимический. Повысить чувствительность можно, увеличив число остатков биотина, введенных в зонды.
Метод дот-гибридизации. В случаях, когда необходимо установить наличие или отсутствие в ДНК выявляемой последовательности, применяют метод дот-гибридизации. В этом случае очищенную денатурированную ДНК наносят непосредственно на фильтр, иммобилизуют, гибридизируют с зондом и регистрируют на автографах положительные сигналы.
В настоящее время используют зонды для обнаружения бактерий родов Salmonella, Campylobacter, Mycobacterium и др. Успешно разрабатываются зонды и для представителей рода Yersinia. Предложен зонд для идентификации вирулентных Yersinia enterocolitica (V. Е. Hill et al., 1983). В качестве зонда протестированы 8 перекрывающихся областей плазмиды вирулентности (pYV) Y. enterocolitica, а также inv- и ail-области хромосомы, ответственные за способность к инвазии Y. enterocolitica (R. М. Rohins-Browne et al., 1989). Зонды на основе mv-гена Y. enterocolitica гибридизовались со всеми видами и биотипами иерсиний (но не других бактерий). Зонды из ail-области Y. enterocolitica давали положительный сигнал исключительно с патогенными Y. enterocolitica.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Применение метода молекулярной гибридизации ДНК
Подлинную революцию изучение ДНК произвело в систематике микроорганизмов, которая в значительной своей степени была искусственной.
Это объясняется главным образом тем, что морфологические й. физиологические признаки прокариот (и низших эукариот) весьма часто возникали конвергентно или же в результате параллельной эволюции. Однако А. А. Имшенецкий (1978) справедливо указывает, что «рациональная, научная систематика должна носить филогенетический, эволюционный характер применительно к прокариотам» (1978, с. 56). Но какие признаки следовало бы положить в основу системы прокариот, если даже такие критерии, как способность к хемоавтотрофии, фиксации молекулярного азота, наконец, к фотосинтезу, возникают в процессе эволюции у представителей самых разных классов и семейств?
Анализ последовательностей ДНК, не подверженных конвергенции и всегда свидетельствующих о родстве, может принести и приносит в данном случае неоценимые услуги (см. обзор: Блохина, Леванова, 1976). Трудность здесь, однако, заключается в том, что дивергенция основных групп прокариот произошла, как минимум, на 2 млрд. лет раньше, чем возникли эукариотические организмы, и у наиболее древних форм гомологичных последовательностей в ДНК практически не осталось (ей. обзор: Fox et al., 1980). Исследования последних лет завершились выделением нового царства археобактерий, равноценного другим прокариотам (к нему относятся метанообразующие бактерии, облигатные галофилы-фотосинтетики и ряд термофилов). Проблемы филогении бактерий в настоящее время являются предметом оживленной дискуссии (Van Valen, Maiorana, 1980).
Применение метода молекулярной гибридизации ДНК для изучения родственных отношений эукариотических организмов также наталкивается на сходные трудности. Гомологий в ДНК представителей разных классов животных и разных семейств растений очень мало и процент гибридизации здесь сравним с ошибкой определения. Однако выход из сложившегося положения подсказывается самой природой. Анализ данных, полученных в разных лабораториях, позволяет прийти к выводу, что концепция так называемых молекулярных часов, т. е. относительной стабильности темпа дивергенции нуклеотидных последовательностей (Wilson, Sarich, 1969), неверна. Не только гены разных белков эволюционируют с разной скоростью. Скорость дивергенции одного и того же цистрона в разных филетических линиях может существенно отличаться. Более того, отчетливо можно проследить периоды, в которые вероятность фиксации мутаций существенно повышалась.
Метод молекулярной гибридизации
Метод молекулярной гибридизации (ДНК-гибридизация, ДНК-зонды) широко применяется для диагностики инфекционных болезней, в генетике, криминалистике и т.д. Метод основан на уникальном свойстве генетического материала организма – молекулы ДНК –, состоящей из мононуклеотидов, образовывать двойную спираль с комплементарно соединенными азотистыми основаниями. Известно, что молекула ДНК представляет полимер, состоящий из четырех видов дезоксирибонуклеотидов (dAMP, dGMP, dTMP, dCMP), соединенных между собой 3′- и 5′-фосфодиэфирными связями дезоксирибоз. Молекула ДНК образует двойную спираль, при которой азотистые основания первой цепи строго комплементарно соединяются водородными связями с азотистыми основаниями второй цепи, при этом аденин соединяется с тимином, гуанин с цитозином.
Принцип метода
Структуру двойной спирали ДНК (или РНК), скрепленную водородными связями, можно разрушить нагреванием, поскольку спаренные, не связанные между собой ковалентно, две полинуклеотидные цепи ДНК после разрыва всех водородных связей полностью разделяются.
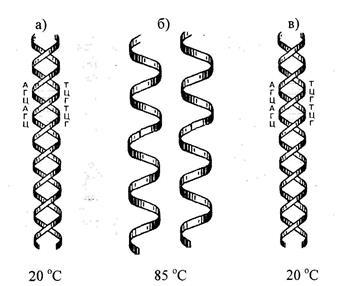
Процесс разделения цепей называют денатурацией или плавлением ДНК. Денатурация происходит в узком интервале температур и сопровождается гиперхромным эффектом, т.е. при этом происходит возрастание поглощения ультрафиолетовых лучей. Температуру, при которой происходит разделение цепей ДНК, называют точкой плавления (Т пл.), которая в зависимости от состава ДНК имеет величину примерно 85-95 о C. Процесс денатурации ДНК обратимый, т.е. при снижении температуры происходит восстановление водородных связей – отжиг – образование двойной спирали. Это явление называют ренатурацией (рис. 12.2.). Ренатурация связана со специфичностью спаривания азотистых оснований между комплементарными цепями. Реакция происходит в две стадии: вначале короткие комплементарные последовательности двух цепей случайно соединяются друг с другом и образуют двухспиральный участок, затем образуется длинная двухцепочечная структура с восстановлением первоначальных свойств, утраченных при денатурации.
В ренатурации участвуют две комплементарные последовательности. Если при этом взяты цепочки молекулы ДНК из различных источников, то говорят о гибридизации, например при отжиге ДНК и РНК.
В основе гибридизации лежит тот же принцип спаривания комплементарных оснований, который обеспечивает репликацию ДНК или ренатурацию молекул. Способность к гибридизации двух препаратов нуклеиновых кислот является строгим тестом на комплементарность их последовательностей.
Рис. 12.2. Схема денатурации и ренатурации ДНК; двойная спираль образуется по принципу комплементарности азотистых оснований.
а) нативная молекула ДНК,
б) денатурированная молекула ДНК,
в) ренатурированная молекула ДНК.
Способы гибридизации
Гибридизацию можно осуществлять в растворе или на фильтре (капроновом или нитроцеллюлозном). При гибридизации молекул в растворе препараты (одноцепочечные молекулы) смешивают и определяют образование двухцепочечных молекул при отжиге по изменению гиперхромного эффекта или же по количеству метки в двухцепочечной ДНК (для этого один из препаратов ДНК предварительно метят радиоактивным изотопом). Удобным для работы является метод гибридизации с использованием фильтров. При этом один из препаратов ДНК иммобилизуют на нитроцеллюлозных фильтрах, на которых молекула ДНК адсорбируется. Фильтры с адсорбированной одноцепочечной ДНК обрабатывают таким образом, чтобы предотвратить дальнейшую адсорбцию одноцепочечных молекул.
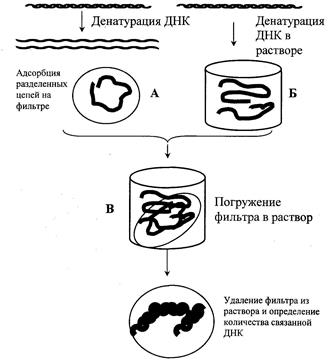
На рис. 12.3. показана схема гибридизации на фильтре.
Рис. 12.3. Схема гибридизации на фильтре.
Фильтр с адсорбированной ДНК погружают в раствор, содержащий второй препарат денатурированной ДНК (ДНК-зонд). Связывание ДНК-зонда происходит только в том случае, если он имеет комплементарную последовательность с первоначально адсорбированной на фильтре молекулой ДНК.
Эффективность гибридизации определяют по количеству метки, оставшейся на фильтре. Метод является очень чувствительным и применяется для изучения структуры гена. При этом необходимо иметь меченые радиоактивным изотопом РНК или ДНК-зонды, идентификация которых с исследуемой молекулой регистрируется с помощью радиоавтографии.В качестве зонда используют клонированную кДНК-копию,т.е. меченую радиоактивным изотопом молекулу ДНК с известной последовательностью нуклеотидов.