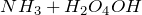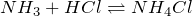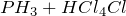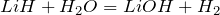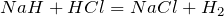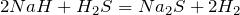молярная масса водорода чему равна
Молярная масса водорода
Молярная масса водорода
Молярную массу обычно выражают в г/моль, реже в кг/кмоль. Поскольку в одном моле любого вещества содержится одинаковое число структурных единиц, то молярная масса вещества пропорциональная массе соответствующей структурной единицы, т.е. относительной атомной массе данного вещества (Mr):
где κ – коэффициент пропорциональности, одинаковый для всех веществ. Относительная молекулярная масса – величина безразмерная. Её вычисляют, используя относительные атомные массы химических элементов, указанных в Периодической системе Д.И. Менделеева.
Относительная атомная масса атомарного водорода равна 1,008 а.е.м. Его относительная молекулярная масса будет равна 1,008, а молярная масса:
M(H) = Mr (H) × 1 моль = 1,008 г/моль.
Известно, что молекула водорода двухатомна – H2, тогда, относительная атомная масса молекулы водорода будет равна:
Относительная молекулярная масса молекулы водорода будет равна 2,016, а молярная масса:
M(H) = Mr (H) × 1 моль = 2,016 г/моль или просто 2 г/моль.
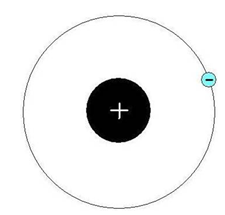
Водород представляет собой газ без цвета и запаха (схема строения атома представлена на рис. 1), который при температуре (-240 o C) и под давлением способен сжижаться, а при быстром испарении полученной жидкости переходить в твердое состояние (прозрачные кристаллы).
Рис. 1. Строение атома водорода.
Молекулярную массу вещества в газообразном состоянии можно определить, используя понятие о его молярном объеме. Для этого находят объем, занимаемый при нормальных условиях определенной массой данного вещества, а затем вычисляют массу 22,4 л этого вещества при тех же условиях.
Для достижения данной цели (вычисление молярной массы) возможно использование уравнения состояния идеального газа (уравнение Менделеева-Клапейрона):
где p – давление газа (Па), V – объем газа (м 3 ), m – масса вещества (г), M – молярная масса вещества (г/моль), Т – абсолютная температура (К), R – универсальная газовая постоянная равная 8,314 Дж/(моль×К).
Примеры решения задач
В этих реакциях аммиак и фосфин проявляют свойства оснований, а вода, хлороводород и фтороводород – свойства кислот.
Окислительно-восстановительные реакции протекают при взаимодействии гидридов лития и натрия с водой, хлороводородом и сероводородом:
В этих реакциях гидриды металлов выступают в роли восстановителей, а вода, хлороводород и сероводород – в роли окислителей.
| Задание | Некоторый элемент образует гидрид ЭН3, массовая доля водорода в котором равна 8,82%. Определите этот элемент. |
| Решение | Рассчитаем относительную молекулярную массу ЭН3, воспользовавшись расчетной формулой массовой доли химического элемента в веществе: |
Рассчитаем относительную атомную массу элемента:
Молярная масса водорода
Молярная масса водорода.
Молярная масса водорода:
Молярная масса – это характеристика вещества, отношение массы вещества к его количеству.
В Международной системе единиц (СИ) единицей измерения молярной массы является килограмм на моль (русское обозначение: кг/моль; международное: kg/mol). Исторически сложилось, что молярную массу, как правило, выражают в г/моль.
Молярная масса численно равна массе одного моля вещества, то есть массе вещества, содержащего число частиц, равное числу Авогадро (NA = 6,022 140 76⋅10 23 моль −1 ).
Молярная масса, выраженная в г/моль, численно совпадает с молекулярной массой (абсолютной молекулярной массой), выраженной в а. е. м., и относительной молекулярной массой.
В свою очередь, молекулярная масса – масса молекулы. Различают абсолютную молекулярную массу (обычно выражается в атомных единицах массы, а. е. м.) и относительную молекулярную массу – безразмерную величину, равную отношению массы молекулы к 1/12 массы атома углерода 12 C.
Молярную массу обозначают M.
Молекула водорода двухатомна – H2.
Молярная масса водорода (M (H)) составляет 1,00784-1,00811 г/моль.
Молярная масса молекулы водорода (M (H2)) составляет 2,01568-2,01622 г/моль.
Необходимо иметь в виду, что молярные массы химических элементов и простых веществ, которые они образуют – не одно и то же. Например, молярная масса кислорода как химического элемента (атома) ≈ 16 г/моль, а вещества (O2) ≈ 32 г/моль.
Молярная масса водорода чему равна
§7.1 Водород как элемент. Положение в Периодической таблице. Распространенность в природе.
Если кислород является самым распространенным элементом в земной коре, то водород – самый распространенный элемент во Вселенной. Водород составляет около 70 % массы Солнца и звезд. Поскольку водород – наиболее легкий из всех элементов, то такая внушительная масса требует огромного количества атомов этого элемента. Из каждых 100 атомов, встречающихся во Вселенной, 90 – атомы водорода.
Вероятно, когда-то водород входил и в атмосферу Земли. Но из-за своей легкости он способен покидать атмосферу, поэтому доля водорода в воздухе ничтожно мала. В связанном виде водород составляет 0,76 % массы Земли. Наиболее важным соединением водорода, встречающимся в природе, является вода.
Нетрудно подсчитать плотность водорода: 1 моль в обычных условиях занимает 22,4 л, а молярная масса водорода равна 2 г. Следовательно, плотность в пересчете на 1 л составит 2 г/22,4 л = 0,09 г/л. Плотность воздуха заметно выше – 1,305 г/л, поэтому наполненные водородом предметы испытывают выталкивающую силу атмосферы.
Электронный уровень 1s вмещает не более 2-х электронов и атому водорода достаточно приобрести или потерять один электрон, чтобы достичь устойчивой электронной конфигурации:
Типичными неметаллическими свойствами этот элемент больше похож на элементы VII группы (фтор, хлор, бром т.д.). Но водород не является р-элементом и более охотно ОТДАЕТ электрон, чем принимает. Поэтому его нахождение в группе s-элементов – активных восстановителей – также имеет смысл. В связи с этим водород часто помещают в I группу Периодической таблицы, а в VII группе повторяют его символ в скобках. Но есть и такие издания Периодической таблицы, где его основным местом является именно VII группа. И то и другое – правильно.
** 7.1 (НГУ). “Тяжелая вода” D 2 O, полученная в результате реакции кислорода с водородом, обогащенным дейтерием, имеет молярную массу 18,2 г. Рассчитайте содержание обоих изотопов в исходном водороде, считая, что кислород состоит практически только из изотопа 16 O.
Водород
Водород / Hydrogenium (H), 1
2,20 [1] (шкала Полинга)
0,0000899 (при 273 K (0 °C)) г/см³
Водоро́д — первый элемент периодической системы элементов; обозначается символом H. Название представляет собой кальку с латинского: лат. Hydrogenium (от др.-греч. ὕδωρ — «вода» и γεννάω — «рождаю») — «порождающий воду». Широко распространён в природе. Катион (и ядро) самого распространённого изотопа водорода 1 H — протон.
Три изотопа водорода имеют собственные названия: 1 H — протий (Н), 2 H — дейтерий (D) и 3 H — тритий (радиоактивен) (T).
Содержание
История
Выделение горючего газа при взаимодействии кислот и металлов наблюдали в XVI и XVII веках на заре становления химии как науки. Прямо указывал на выделение его и Михаил Васильевич Ломоносов, но уже определённо сознавая, что это не флогистон. Английский физик и химик Генри Кавендиш в 1766 году исследовал этот газ и назвал его «горючим воздухом». При сжигании «горючий воздух» давал воду, но приверженность Кавендиша теории флогистона помешала ему сделать правильные выводы. Французский химик Антуан Лавуазье совместно с инженером Ж. Менье, используя специальные газометры, в 1783 г. осуществил синтез воды, а затем и её анализ, разложив водяной пар раскалённым железом. Таким образом он установил, что «горючий воздух» входит в состав воды и может быть из неё получен.
Происхождение названия
Распространённость
Во Вселенной
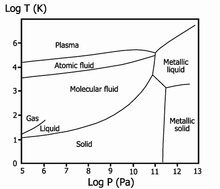
6000 °C) водород существует в виде плазмы, в межзвёздном пространстве этот элемент существует в виде отдельных молекул, атомов и ионов и может образовывать молекулярные облака, значительно различающиеся по размерам, плотности и температуре.
Земная кора и живые организмы
Массовая доля водорода в земной коре составляет 1 % — это десятый по распространённости элемент. Однако его роль в природе определяется не массой, а числом атомов, доля которых среди остальных элементов составляет 17 % (второе место после кислорода, доля атомов которого равна
52 %). Поэтому значение водорода в химических процессах, происходящих на Земле, почти так же велико, как и кислорода. В отличие от кислорода, существующего на Земле и в связанном, и в свободном состояниях, практически весь водород на Земле находится в виде соединений; лишь в очень незначительном количестве водород в виде простого вещества содержится в атмосфере (0,00005 % по объёму).
Водород входит в состав практически всех органических веществ и присутствует во всех живых клетках. В живых клетках по числу атомов на водород приходится почти 50 %.
Получение
В промышленности
В лаборатории
Физические свойства
Водород — самый лёгкий газ, он легче воздуха в 14,5 раз. Очевидно, что чем меньше масса молекул, тем выше их скорость при одной и той же температуре. Как самые лёгкие, молекулы водорода движутся быстрее молекул любого другого газа и тем самым быстрее могут передавать теплоту от одного тела к другому. Отсюда следует, что водород обладает самой высокой теплопроводностью среди газообразных веществ. Его теплопроводность примерно в семь раз выше теплопроводности воздуха.
Молекула водорода двухатомна — Н2. При нормальных условиях — это газ без цвета, запаха и вкуса. Плотность 0,08987 г/л (н. у.), температура кипения −252,76 °C, удельная теплота сгорания 120,9·10 6 Дж/кг, малорастворим в воде — 18,8 мл/л.
Водород хорошо растворим во многих металлах (Ni, Pt, Pd и др.), особенно в палладии (850 объёмов H2 на 1 объём Pd). С растворимостью водорода в металлах связана его способность диффундировать через них; диффузия через углеродистый сплав (например, сталь) иногда сопровождается разрушением сплава вследствие взаимодействия водорода с углеродом (так называемая декарбонизация). Практически не растворим в серебре.
Жидкий водород существует в очень узком интервале температур от −252,76 до −259,2 °C. Это бесцветная жидкость, очень лёгкая (плотность при −253 °C 0,0708 г/см³) и текучая (вязкость при −253 °C 13,8 сП). Критические параметры водорода очень низкие: температура −240,2 °C и давление 12,8 атм. Этим объясняются трудности при ожижении водорода. В жидком состоянии равновесный водород состоит из 99,79 % пара-Н2, 0,21 % орто-Н2.
Твердый водород, температура плавления −259,2 °C, плотность 0,0807 г/см³ (при −262 °C) — снегоподобная масса, кристаллы гексагональной сингонии, пространственная группа P6/mmc, параметры ячейки a = 0,378 нм и c = 0,6167 нм. При высоком давлении водород переходит в металлическое состояние.
Молекулярный водород существует в двух спиновых формах (модификациях) — в виде орто- и параводорода. В молекуле ортоводорода o-H2 (т. пл. −259,10 °C, т. кип. −252,56 °C) ядерные спины направлены одинаково (параллельны), а у параводорода p-H2 (т. пл. −259,32 °C, т. кип. −252,89 °C) — противоположно друг другу (антипараллельны). Равновесная смесь o-H2 и p-H2 при заданной температуре называется равновесный водород e-H2.
Разделить модификации водорода можно адсорбцией на активном угле при температуре жидкого азота. При очень низких температурах равновесие между ортоводородом и параводородом почти нацело сдвинуто в сторону последнего. При 80 К соотношение форм приблизительно 1:1. Десорбированный параводород при нагревании превращается в ортоводород вплоть до образования равновесной при комнатной температуре смеси (орто-пара: 75:25). Без катализатора превращение происходит медленно (в условиях межзвёздной среды — с характерными временами вплоть до космологических), что даёт возможность изучить свойства отдельных модификаций.
Изотопы
Водород встречается в виде трёх изотопов, которые имеют индивидуальные названия: 1 H — протий (Н), 2 Н — дейтерий (D), 3 Н — тритий (T; радиоактивный).
В литературе [4] также приводятся данные об изотопах водорода с массовыми числами 4—7 и периодами полураспада 10 −22 —10 −23 с.
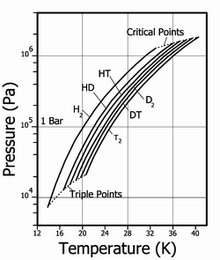
Природный водород состоит из молекул H2 и HD (дейтероводород) в соотношении 3200:1. Содержание чистого дейтерийного водорода D2 ещё меньше. Отношение концентраций HD и D2, примерно, 6400:1.
| Температура плавления, K | Температура кипения, K | Тройная точка, K / kPa | Критическая точка, K / kPa | Плотность жидкий / газ, кг/м³ | |
|---|---|---|---|---|---|
| H2 | 13,96 | 20,39 | 13,96 / 7,3 | 32,98 / 1,31 | 70,811 / 1,316 |
| HD | 16,65 | 22,13 | 16,6 / 12,8 | 35,91 / 1,48 | 114,0 / 1,802 |
| HT | 22,92 | 17,63 / 17,7 | 37,13 / 1,57 | 158,62 / 2,31 | |
| D2 | 18,65 | 23,67 | 18,73 / 17,1 | 38,35 / 1,67 | 162,50 / 2,23 |
| DT | 24.38 | 19,71 / 19,4 | 39,42 / 1,77 | 211,54 / 2,694 | |
| T2 | 20,63 | 25,04 | 20,62 / 21,6 | 40,44 / 1,85 | 260,17 / 3,136 |
Дейтерий и тритий также имеют орто- и парамодификации: p-D2, o-D2, p-T2, o-T2. Гетероизотопный водород (HD, HT, DT) не имеют орто- и парамодификаций.
Свойства изотопов
| Изотоп | Z | N | Масса, а. е. м. | Период полураспада | Спин | Содержание в природе, % | Тип и энергия распада | |
|---|---|---|---|---|---|---|---|---|
| 1 H | 1 | 0 | 1,007 825 032 07(10) | стабилен | 1 ⁄2 + | 99,9885(70) | ||
| 2 H | 1 | 1 | 2,014 101 777 8(4) | стабилен | 1 + | 0,0115(70) | ||
| 3 H | 1 | 2 | 3,016 049 277 7(25) | 12,32(2) года | 1 ⁄2 + | β − | 18,591(1) кэВ | |
| 4 H | 1 | 3 | 4,027 81(11) | 1,39(10)·10 −22 с | 2 − | -n | 23,48(10) МэВ | |
| 5 H | 1 | 4 | 5,035 31(11) | более 9,1·10 −22 с | ( 1 ⁄2 + ) | -nn | 21,51(11) МэВ | |
| 6 H | 1 | 5 | 6,044 94(28) | 2,90(70)·10 −22 с | 2 − | −3n | 24,27(26) МэВ | |
| 7 H | 1 | 6 | 7,052 75(108) | 2,3(6)·10 −23 с | 1 ⁄2 + | -nn | 23,03(101) МэВ | |
В круглых скобках приведено среднеквадратическое отклонение значения в единицах последнего разряда соответствующего числа.
Свойства ядра 1 H позволяют широко использовать ЯМР-спектроскопию в анализе органических веществ.
Химические свойства
Молекулы водорода достаточно прочны, и для того, чтобы водород мог вступить в реакцию, должна быть затрачена большая энергия:
Поэтому при обычных температурах водород реагирует только с очень активными металлами, например с кальцием, образуя гидрид кальция:
и с единственным неметаллом — фтором, образуя фтороводород:
С большинством же металлов и неметаллов водород реагирует при повышенной температуре или при другом воздействии, например при освещении:
Он может «отнимать» кислород от некоторых оксидов, например:
Записанное уравнение отражает восстановительные свойства водорода.
С галогенами образует галогеноводороды:


С сажей взаимодействует при сильном нагревании:
Взаимодействие со щелочными и щёлочноземельными металлами
При взаимодействии с активными металлами водород образует гидриды:


Гидриды — солеобразные, твёрдые вещества, легко гидролизуются:
Взаимодействие с оксидами металлов (как правило, d-элементов)


Гидрирование органических соединений
Молекулярный водород широко применяется в органическом синтезе для восстановления органических соединений. Эти процессы называют реакциями гидрирования. Эти реакции проводят в присутствии катализатора при повышенных давлении и температуре. Катализатор может быть как гомогенным (напр. Катализатор Уилкинсона), так и гетерогенным (напр. никель Ренея, палладий на угле).
Так, в частности, при каталитическом гидрировании ненасыщенных соединений, таких как алкены и алкины, образуются насыщенные соединения — алканы.
Геохимия водорода
На Земле содержание водорода понижено по сравнению с Солнцем, планетами-гигантами и первичными метеоритами, из чего следует, что во время образования Земля была значительно дегазирована и водород вместе с другими летучими элементами покинул планету во время аккреции или вскоре после неё.
Свободный водород H2 относительно редко встречается в земных газах, но в виде воды он принимает исключительно важное участие в геохимических процессах.
В состав минералов водород может входить в виде иона аммония, гидроксил-иона и кристаллической воды.
Меры предосторожности
Водород при смеси с воздухом образует взрывоопасную смесь — так называемый гремучий газ. Наибольшую взрывоопасность этот газ имеет при объёмном отношении водорода и кислорода 2:1, или водорода и воздуха приближённо 2:5, так как в воздухе кислорода содержится примерно 21 %. Также водород пожароопасен. Жидкий водород при попадании на кожу может вызвать сильное обморожение.
Считается, что взрывоопасные концентрации водорода с кислородом возникают от 4 % до 96 % объёмных. При смеси с воздухом от 4 % до 75 (74) % по объему. Такие цифры фигурируют сейчас в большинстве справочников, и ими вполне можно пользоваться для ориентировочных оценок. Однако, следует иметь в виду, что более поздние исследования (примерно конец 80-х) выявили, что водород в больших объёмах может быть взрывоопасен и при меньшей концентрации. Чем больше объём, тем меньшая концентрация водорода опасна.
Источник этой широко растиражированной ошибки в том, что взрывоопасность исследовалась в лабораториях на малых объёмах. Поскольку реакция водорода с кислородом — это цепная химическая реакция, которая проходит по свободнорадикальному механизму, «гибель» свободных радикалов на стенках (или, скажем, поверхности пылинок) критична для продолжения цепочки. В случаях, когда возможно создание «пограничных» концентраций в больших объёмах (помещения, ангары, цеха), следует иметь в виду, что реально взрывоопасная концентрация может отличаться от 4 % как в большую, так и в меньшую стороны.
Экономика
Применение
Атомарный водород используется для атомно-водородной сварки.
Химическая промышленность
Пищевая промышленность
Авиационная промышленность
Водород очень лёгок и в воздухе всегда поднимается вверх. Когда-то дирижабли и воздушные шары наполняли водородом. Но в 30-х гг. XX в. произошло несколько катастроф, в ходе которых дирижабли взрывались и сгорали. В наше время дирижабли наполняют гелием, несмотря на его существенно более высокую стоимость.
Топливо
Водород используют в качестве ракетного топлива.
Ведутся исследования по применению водорода как топлива для легковых и грузовых автомобилей. Водородные двигатели не загрязняют окружающую среду и выделяют только водяной пар.
В водородно-кислородных топливных элементах используется водород для непосредственного преобразования энергии химической реакции в электрическую.