пересадка костного мозга при лимфоме неходжкинской
Пересадка костного мозга при лимфоме неходжкинской
Хотя при использовании современных химиотерапевтических рецептур излечивается 50-60% больных с высокозлокачественными формами НХЛ, при лечении рецидивов обычные методы химиотерапии дают результаты лишь в отдельных случаях, а чаще оказываются неэффективными.
Режим интенсивной химиотерапии в сочетании с пересадкой аутологичного костного мозга или с введением поддерживающих стволовых кроветворных клеток, позволяет в 5-7 раз увеличить назначаемую дозу препаратов.
При этом исходят из предположения о том, что именно такая доза окажется эффективной при лечении больных, у которых опухоль устойчива к низким дозам лекарственных средств. Назначение еще более высоких доз может привести к смертельному исходу, из-за сильного увеличения токсичности. К числу основных методов, входящих в комплекс процедур поддерживающего лечения, относятся использование аутологичных стволовых клеток периферической крови и кроветворных ростовых факторов. Эти методы снижают токсичность химиопрепаратов и способствуют увеличению выживаемости больных.
По данным предварительных клинических испытаний, после назначения высоких доз препаратов рецидивирующим больным, около 30-40% живут более 3-х лет, и у 60-75% лечение оказывается эффективным. К числу прогностических факторов относятся общее состояние здоровья, размер опухоли и ее чувствительность к химиотерапевтическим препаратам по данным первичного лечения, а также число применявшихся рецептур и их состав.
Столь обнадеживающие результаты позволили использовать этот метод для лечения рецидивов у тяжелых больных, а также у тех, для кого первичное лечение оказалось неэффективным. Проблема заключается в том, что больные в обеих категориях характеризуются различным прогнозом, и поэтому необходимо было провести рандомизированные исследования.
Опубликованы результаты первого такого исследования. Были отобраны больные с опухолью, чувствительной к цитостатикам и с рецидивами после первичного лекарственного лечения. Им назначался курс химиотерапии и лучевой терапии. В дальнейшем, часть этих больных получала курс химиотерапии высокими дозами препаратов.
Хотя в этой группе было немного больных, среди них заметно увеличилась общая и безрецидивная выживаемость. Таким образом, назначение высоких доз химиотерапевтических препаратов следует рекомендовать тем пациентам, у которых первичное лечение не дало результатов, а также отдельным больным c опухолями, которые характеризуются неблагоприятным прогнозом. К числу таких опухолей относятся высокозлокачественные Т-клеточные лимфомы, лимфобластная лимфома взрослых и агрессивная нодальная лимфома клеток узелковых центров.
В этих случаях следует назначать высокие дозы химиопрепаратов, даже если первичное лечение оказалось результативным. Также этим методом следует лечить больных, у которых лечение первого рецидива оказалось успешным.
При пересадке аутологичных стволовых клеток или костного мозга существует проблема загрязнения донорских клеток опухолевыми. Предложены различные методы «очистки» трансплантируемых клеток от опухолевых, однако нет убедительных данных, свидетельствующих о том, что эти методы, действительно эффективны и необходимы. В конце-концов основная задача заключается в лечении больного, а не донорских клеток.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Пересадка костного мозга при онкологических заболеваниях крови
Впервые сталкиваясь с таким страшным диагнозом, как, лейкоз, или лейкемия, лимфома – у человека после первого шока начинается хаос в голове из огромного количества вопросов: как, почему я, или мой ребенок, что делать, как лечить, какие шансы, нужна ли пересадка костного мозга, где найти донора…
Ниже мы выстроили систему из этих вопросов и попробуем ответить на каждый. Это и будет неким планом действий для человека, которому поставили диагноз – рак крови.
Как диагностировать рак крови?
Как лечить лейкоз, лейкемию или лимфому? Можно ли вылечить навсегда?
Какая бывает пересадка костного мозга? Где найти донора?
Как происходит пересадка костного мозга? Что делают перед ТКМ? Сколько времени занимается вся процедура пересадки?
Сколько стоит пересадка костного мозга?
Где лучше делать трансплантацию?
Какой прогноз после пересадки костного мозга?
Как определить рак крови: лейкоз, лейкемию. Как выявить лимфому?
Виды рака крови:
Как диагностировать рак крови на ранней стадии, как он проявляется и как его заметить самостоятельно?
Внимание на симптомы:
Вы заметили эти симптомы у себя? У ребенка? Если испытываете подобные симптомы больше 1-2 недель, срочно проходите первичное обследование, а именно:
Именно по общему анализу крови врач может распознать серьезные отклонения от нормы. Если это случилось, необходимо делать пункцию и проводить иммуногистохимический анализ клеток костного мозга для определения вида рака крови.
Далее, в зависимости от типа рака крови, грамотный врач должен обследовать пациента с помощью ПЭТ КТ, или МРТ, КТ, сцинтиграфии.
Как лечить лейкоз, лейкемию или лимфому? Можно ли вылечить навсегда?
Как лечится рак крови:
Ранняя стадия рака лейкоза, лейкемии или лимфомы: у 75% пациентов ремиссия наступает уже при первой линии лечения цитостатиками и химиотерапией.
Важно: первая линия лечения может длиться от 3 до 9 месяцев.
Вторая и третья стадии лимфомы, лейкемии и остром лейкозе: кроме цитостатиков и химиотерапии, применяют таргетную терапию и иммунотерапию. Комплексное лечение серьезно повышает шансы онкологического пациента на выход в ремиссию.
Важно: иммунотерапия не применяется как самостоятельный метод лечения рака крови, этот новейший метод биологического лечения является сильным вспомогательным лечением.
Четвертая, терминальная стадии, рецидив: требуется пересадка костного мозга, от донора или собственных стволовых клеток.
Важно: Некоторые виды лейкоза, лейкемии и лимфом даже на ранних стадиях предполагают впоследствии пересадку костного мозга. Поэтому если полученный диагноз по протоколу предполагает в будущем ТКМ (трансплантацию), сразу сдавайте анализы на типирование антигенов HLA сами и все ваши родные. Заранее определитесь, подходит ли кто-то из родственников как донор.
Какая бывает пересадка костного мозга? Где найти донора?
Виды трансплантации:
Как происходит пересадка костного мозга? Что делают перед ТКМ? Сколько времени занимается вся процедура пересадки?
Пересадка костного мозга является либо завершающим этапом лечения, когда предыдущие методы не дали 100% положительного результата, либо основным при рецидиве рака крови.
В случае аллогенной трансплантации забор клеток костного мозга производится у донора. Напомним, что 9 пациентам из 10 необходимо ожидать в очереди на получение донора из общей базы при совпадении антител HLA.
Если планируется пересадка собственных стволовых клеток костного мозга, то забор этих клеток делают заранее. Если от донора, то незадолго до процедуры. Особая подготовка не требуется, только обследование.
Стволовые клетки для пересадки берут из тазовой кости пункцией, однако, наиболее современный и щадящий способ – это фильтрование стволовых клеток из периферийной крови после лекарственной стимуляции выброса нужных клеток в кровь (недельный прием препарата). Болезненные последствия для донора или самого пациента отсутствуют. Не больно.
Перед процедурой необходимо буквально «убить» собственный костный мозг, который производит мутированные кровяные клетки. Для этого проводится интенсивная высокодозная химиотерапия или высокоточная лучевая терапия. Если вариант ТКМ с донором, то дополнительно применяют большие дозы иммуносупрессоров, чтобы организм сразу не отверг чужой костный мозг.
Операция по пересадке костного мозга не что иное, как переливание, ведь костный мозг выглядит просто как пакет крови для переливания.
На 2-4 недели после пересадки пациента помещают в стерильную палату клиники, так как он находится в состоянии цитопении: старый костный мозг убит и не работает, новый костный мозг еще не прижился. В этот период для пациента опасны любые возможные инфекции, даже самые незначительные.
Еще в течение 2 месяцев после выписки из стерильной палаты пациента наблюдают или стационарно или амбулаторно. Каждую неделю он сдает анализы крови, мочи, находится под контролем своего онколога.
По окончании всего этапа лечения, пациент проходит обследование каждые 3 месяца в течение 1 года. Далее еще 4 года – каждые 6 месяцев. Перешагнув 5-летний рубеж выживаемости, пациент вступает в период длительной ремиссии, что в 80% случаях означает полное излечение. Обследование раз в год!
Итак, вся процедура трансплантации костного мозга при лейкозе крови, лейкемии, при множественной миеломе (миеломной болезни), лимфоме Ходжкина и неходжкинской лимфоме занимает 3-4 месяца.
Высокодозная химиотерапия и трансплантация костного мозга у взрослых больных
Трансплантация стволовых гемопоэтических клеток нашла применение в различных областях онкологии.
Эти клетки используются после высокодозной химиотерапии для снижения длительности депрессии (угнетения) костного мозга и сокращения риска инфекционных осложнений и кровотечений.
Стволовые клетки для трансплантации получают как от самого пациента (аутологичная трансплантация), так и от иммунологически совместимого родственного или неродственного донора (аллогенная трансплантация). Непосредственным источником стволовых гемопоэтических стволовых клеток может быть костный мозг, периферическая или пуповинная кровь.
Одним из наиболее частых показаний для применения стволовых клеток в онкологии является уменьшении длительности периода угнетения кроветворения после противоопухолевой терапии.
Применение современных противоопухолевых препаратов позволяет излечить или продлить жизнь значительному количеству больных со злокачественными новообразованиями.
Однако в ряде случаев проведение стандартной химиотерапии не приводит к длительному противоопухолевому эффекту, что связано с исходной или приобретенной резистентностью (устойчивостью) опухоли к цитостатикам.
Одним из путей ее преодоления является увеличение дозы препаратов. Это увеличивает проникновение противоопухолевых препаратов в раковую клетку и позволяет преодолеть устойчивость к химиотерапии.
Резкое увеличение дозы препаратов приводит к значительному повреждению кроветворных клеток костного мозга и выключению функции кроветворения на много месяцев, что требует применения методик защиты кроветворения.
Основным методом, позволяющим преодолеть токсичность химиотерапии на кроветворение, является трансплантация кроветворной ткани. При этом стволовые клетки, полученные от донора или у самого больного, вводят после окончания химиотерапии, когда препараты полностью вывелись из организма или разрушились, что позволяет быстро восстановить кроветворение.
При пересадке аллогенного костного мозга возможно длительное приживление трансплантата только при совпадении донора и реципиента по антигенам главного комплекса гистосовместимости (иммунологической совместимости).
В противном случае развивается выраженная иммунологическая реакция «трансплантат против хозяина» (РТПХ), способная привести к гибели больного.
Наименьшее количество осложнений встречается у совместимых сибсов (родных братьев и сестер).
В то же время сибсы имеют вероятность совпасть иммунологически только в 25% случаев, что указывает на серьезную проблему подбора доноров для пересадки костного мозга. Последние годы отмечены крупные успехи в подборе неродственных доноров.
Следует отметить, что даже полная совместимость не дает абсолютной гарантии отсутствия развития РТПХ, и до 25% больных погибает от осложнений, связанных с трансплантацией.
Важно иметь в виду, что РТПХ способна оказывать и лечебное действие, когда иммунная система донора начинает распознавать опухолевые клетки хозяина и бороться с ними, т.е. проявляется реакция трансплантат против опухоли (РТПО).
При ряде заболеваний (хронический миелолейкоз, острый нелимфобластный лейкоз и др.) наличие этой реакции в значительной степени определяет общий успех лечения.
Трансплантация аутологичной (своей собственной) гемопоэтической ткани позволяет избежать возникновения РТПХ и технических сложностей, связанных с подбором донора. С другой стороны, аутологичная трансплантация не сопровождается РТПО и несет чисто вспомогательную функцию поддержки кроветворения после высокодозной химиотерапии.
В настоящее время имеется возможность сохранять собственные кроветворные клетки в жизнеспособном состоянии при низких температурах (замораживании) в течение длительного периода времени.
Долгие годы основным источником стволовых кроветворных клеток был костный мозг. Метод его получения состоит в многократных пункциях плоских костей (в основном тазовых) и получении 1-1,5 литров костно-мозговой взвеси. Такая процедура требует, как правило, общего обезболивания (наркоза).
Нужно отметить, что при опухолевом и лучевом поражении костей таза забор костного мозга может оказаться неудачным.
Костный мозг не является единственным источником кроветворных клеток.
Во взрослом организме небольшая часть стволовых клеток, как и зрелые клетки, выходит в периферическое сосудистое русло. Эти стволовые клетки способны восстанавливать полноценное кроветворение после повреждения его химиотерапией и облучением. Современная аппаратура (сепараторы крови) позволяет эффективно собирать клетки кроветворения из периферической крови даже при их низком содержании. При этом необходимость наркоза отпадает.
В условиях нормального кроветворения для получения достаточного количества стволовых клеток необходимо, как правило, 6 процедур. При каждой такой процедуре обрабатывается 10-12 литров крови.
Проблема низкого количества клеток кроветворения в периферической крови оставалась главным ограничением при использовании данного вида трансплантата. Затем было показано, что после однократного введения некоторых противоопухолевых препаратов (циклофосфамид, этопозид, фторурацил) отмечается значительное увеличение числа стволовых клеток в периферической крови. К недостаткам данного метода относятся: снижение числа лейкоцитов и тромбоцитов, значительные различия в сроках начала роста содержания стволовых клеток в периферической крови у различных больных.
Введение некоторых гемопоэтических факторов роста (нейпоген, лейкомакс и др.) вызывает значительно увеличение поступления клеток кроветворения из костного мозга в периферическую кровь.
Применение аллогенной трансплантации костного мозга
В настоящее время основными показаниями для аллогенной трансплантации стволовых клеток являются
Изучаются возможности применения данного метода у больных
Острые нелимфобластные лейкозы (ОНЛЛ)
Применение стандартной химиотерапии в первой полной ремиссии позволяет добиться длительной выживаемости в 25-35% случаев по сравнению с 45-60% при использовании аллогенной трансплантации стволовых клеток. Применение трансплантации во второй ремиссии сопровождается длительной ремиссией лишь в 20-30% случаев.
Использование аллогенной трансплантации стволовых клеток с первично резистентным (устойчивым к лечению) течением ОНЛЛ позволяет добиться длительной ремиссии в 10-20% случаев.
Острые лимфобластные лейкозы (олл)
Проведение аллогенной трансплантации стволовых клеток в первой полной ремиссии у пациентов с неблагоприятными прогностическими факторами (возраст старше 60 лет, высокий лейкоцитоз и т.д.) позволяет достичь длительной безрецидивной выживаемости в 40-60% случаев.
При отсутствии неблагоприятных факторов аллогенная трансплантация стволовых клеток обычно рекомендуется во второй полной ремиссии.
Хронический миелолейкоз
ХМЛ характеризуется несколькими фазами развития. В ранней (хронической) фазе, длящейся несколько лет, состояние больного может сохраняться относительно удовлетворительным. В фазе акселерации (обострения) в течение нескольких месяцев нарастают гематологические изменения (увеличение числа лейкоцитов, малокровие), и она переходит в фатальную (смертельную) фазу бластного криза.
Стандартные методы лечения могут вызывать длительные ремиссии у части больных, однако единственным излечивающим методом лечения в настоящее время является аллогенная трансплантация стволовых клеток. Эффективность ее зависит от возраста больного, фазы заболевания, периода времени от момента диагноза до трансплантации. Множественные курсы предшествующего лечения значительно улучшают результаты высокодозной химиотерапии и трансплантации.
Наилучшие шансы на достижение длительной ремиссии имеют молодые больные, получившие трансплантацию в хронической фазе в течение 1 года от момента диагноза. Длительная выживаемость у них составляет 75-80% по сравнению с 10-20% у больных, которым трансплантация выполнена в фазе аскселерации.
Миелодиспластический синдром
Аллогенная трансплантация стволовых клеток является единственным методом, излечивающим больных МДС. Применение этого метода позволяет добиться длительной выживаемости в 30-50% случаев. Эти результаты зависят от возраста больных, длительности заболевания и количества опухолевых клеток в костном мозге перед трансплантацией.
Аллогенная минитрансплантация
Аллогенная минитрансплантация, или трансплантация после миелоаблативных (не разрушающих костномозговое кроветворение) режимов получила распространение лишь недавно. Ее применение связано с выявлением лечебной роли РТПО и появлением новых препаратов (флударабин, антитимоцитарный иммуноглобулин), вызывающих глубокую депрессию (угнетение) иммунной системы, но не вызывающих глубокой цитопении (снижение числа клеток крови).
Применение их в комбинации с умеренными дозами бусульфана или мелфалана позволяет эффективно пересаживать донорский костный мозг. При этом РТПО полностью сохраняется. Следует отметить, что эффективность этого метода зависит от массы остаточной опухоли, которая должна быть по возможности минимальной.
Предварительные результаты применения данной методики свидетельствуют о высокой эффективности минитрансплантации при значительно меньшей токсичности в сравнении с классическим методом.
Применение аутологичной трансплантации костного мозга
Основной ролью аутологичной трансплантации костного мозга является восстановление кроветворения после химиотерапии, что позволяет многократно увеличивать разовые дозы некоторых противоопухолевых препаратов. Это дает возможность усиливать противоопухолевый эффект и достигать более высокой безрецидивной выживаемости в сравнении с результатами стандартной химиотерапии.
Наиболее часто данный метод применяется при лечении больных с прогностически неблагоприятными вариантами течения неходжкинских лимфом (лимфосарком), болезни Ходжкина (лимфогранулематоза), множественной миеломы, рака молочной железы, рака яичка и пр.
Неходжкинские лимфомы (нхл)
Применение стандартной химиотерапии у больных с НХЛ высокой и промежуточной степени злокачественности позволяет достичь 40-60% полных ремиссий. Однако у 20-30% больных этой группы отмечаются рецидивы (возврат) болезни. Применение высокодозной химиотерапии в сочетании с аутологичной трансплантацией костного мозга дало возможность значительно улучшить показатели длительной выживаемости у таких больных.
Болезнь ходжкина
У 10-30% больных с распространенными стадиями болезни Ходжкина первичная химиотерапия оказывается неэффективной, а у 40% пациентов возникает рецидив заболевания. Результаты лечения больных, малочувствительных к первичной химиотерапии и с первым ранним рецидивом (в течение первого года), неудовлетворительные.
Применение других схем стандартной химиотерапии позволяет достичь полных ремиссий не более чем у 40-45% больных, однако при этом ремиссии бывают короткими, а выживаемость низкая.
Применение высокодозной химиотерапии в сочетании с аутологичной трансплантацией стволовых клеток позволяет почти в 2 раза увеличить частоту полных ремиссий, а значит, и надежду на увеличение выживаемости.
Множественная миелома
По данным Европейской организации по аутологичным трансплантациям костного мозга, безрецидивная и общая выживаемость 5500 больных множественной миеломой, получавших высокодозную химиотерапию в сочетании с аутологичной трансплантацией стволовых клеток, составила соответственно 28 и 48 месяцев, что превышает результаты стандартной химиотерапии.
Наилучший прогноз (исход) имеют больные моложе 60 лет с I-II стадиями заболевания и уровнем бета-2 микроглобулина менее 4.
Использование высокодозной химиотерапии при других опухолях (рак молочной железы, яичка и др.) находится на этапе изучения. При этом получены обнадеживающие результаты.
Таким образом, высокодозная химиотерапия с трансплантацией аутологичных или аллогенных стволовых кроветворных клеток за последние годы стала эффективным методом лечения многих опухолей. Прогресс в биологии и иммунологии клеток кроветворения позволяет надеяться на еще более эффективное применение этого метода в будущем, в том числе и при распространенных новообразованиях, резистентных (устойчивых) к химиотерапии.
Мероприятия 2021/2022 года
Архив мероприятий
Противораковое общество РОССИИ создано по инициативе ученых-онкологов и главных врачей онкологических диспансеров, представляющих более 50 регионов России, с целью претворения в жизнь программы профилактики рака в России
Пересадка костного мозга при лимфоме неходжкинской
Все виды трансплантации гемопоэтических стволовых клеток потенциально могут быть использованы в лечении больных со злокачественными лимфомами (неходжкинские лимфомы — НХЛ) высокой, промежуточной и низкой степени злокачественности: аллогенная, аутологичная и сингенная.
По данным Европейской группы по трансплантации костного мозга, количество трансплантаций при неходжкинских лимфомах составляет 22 % от общего числа выполняемых трансплантаций ГСК в год, при этом 90 % из них представлены ауто-трансплантации гемопоэтических стволовых клеток, а из этого количества 97 % являются ауто-ТПСКК. Алло-ТГСК при НХЛ различной степени злокачественности применялась у 10 % пациентов.
Оценка результатов трансплантации гемопоэтических стволовых клеток при злокачественных лимфомах достаточно затруднена, так как сложно сравнивать данные, полученные в разных центрах трансплантации из-за меняющихся принципов классификации, несоответствия при определении показаний, режимов кондиционирования и терапии после трансплантации гемопоэтических стволовых клеток.
Тем не менее, несмотря на чрезвычайную гетерогенность злокачественных лимфом различной степени злокачественности, увеличение общей и безрецидивной выживаемости больных после «стандартной» полихимиотерапии, на фоне применения протоколов с флудараби-ном, 2-CDA, моноклональными антителами показания к трансплантации гемопоэтических стволовых клеток при неходжкинских лимфомах становятся более определенными.
Использование одного из видов трансплантации гемопоэтических стволовых клеток при неходжкинских лимфомах является обоснованным при наличии в момент постановки диагноза факторов прогноза, свидетельствующих о неблагоприятном течении болезни: величина IPI (international prognostic index — международный прогностический индекс) более 1, большой объем опухолевой массы, число курсов химиотерапии, необходимых для достижения ремиссии, гистологический вариант неходжкинских лимфом.
В соответствии с величиной IPI больных неходжкинскими лимфомами различной степени злокачественности делят на 4 группы на основании следующих прогностических критериев: возраст (до 60 лет или старше 60 лет), общее состояние по шкале ВОЗ (менее 0—1 или более 2), повышение уровня лактатдегидрогеназы, стадия НХЛ (I—II или III—IV), число экстранодальных мест вовлечения (до одного включительно или более двух). Отсутствие признака или его хорошее значение расценивается как «0» (первоначально указанный критерий), противоположные признаки —1. Группы риска определяют суммированием значений, в результате чего выделяют категории 0, 1,2, 3, 4, 5. Больные злокачественными лимфомами низкой группы риска относятся к категории 0 или 1, низкого промежуточного риска — 2, высокого промежуточного риска —3, высокого риска—к категориям 4 и 5.
Как правило, больным злокачественными лимфомами низкой и промежуточной степенями злокачественности (гистологические критерии), имеющим низкий показатель IPI, проводят курсы химиотерапии (CHOP, CHOEP, флударабин + циклофосфан) в комбинации с моноклональными антителами или без них либо монотерапии моноклональными антителами. Пациенты с IPI 0 не имеют различия в выживаемости при сравнении стандартной химиотерапии и ауто-трансплантации гемопоэтических стволовых клеток.
Один из видов трансплантации гемопоэтических стволовых клеток показан молодым (до 45 лет) больным НХЛ низкой и промежуточной степенями злокачественности в 1—2-й ремиссии при наличии неблагоприятных прогностических факторов в момент постановки диагноза. Так, при IPI, равным 1 или более, отмечены преимущества трансплантации гемопоэтических стволовых клеток по сравнению с общепринятой химиотерапией. Трансплантация гемопоэтических стволовых клеток показана также при рецидивах (особенно ранних) больным с первично-резистентными формами заболевания, при этом тип трансплантации гемопоэтических стволовых клеток (аллогенная, аутоло-гичная) определяется возрастом, степенью поражения КМ, индексом Карновского и доступностью донора ГСК. Один из важных критериев ожидаемой эффективности трансплантации гемопоэтических стволовых клеток — сохранение химиочувствительности НХЛ, определенной до проведения трансплантации гемопоэтических стволовых клеток.
При неходжкинских лимфомах высокой степени злокачественности показания к трансплантации гемопоэтических стволовых клеток аналогичны показаниям при ОЛЛ.
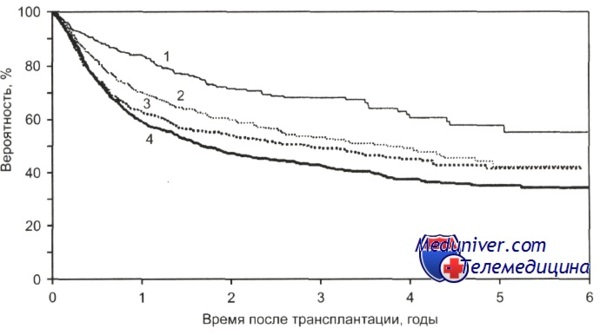
1-ПР1 (n = 362); 2-ПР2+ (n = 657); 3 — ремиссия не получена (n = 911); 4 — рецидив (n= 1746); р = 0,0001.
По данным CIBMTR, 3-летняя общая выживаемость после ауто-трансплантации гемопоэтических стволовых клеток больных неходжкинскими лимфомами низкой степени злокачественности в ПР 1 равна 83 %, в ПР2 — 74 %, при рецидиве — 70 %, а больных, не достигших состояния ремиссии при проведении стандартной ПХТ,-60%. После ауто-трансплантации гемопоэтических стволовых клеток общая выживаемость больных НХЛ промежуточной степени злокачественности составила в ПР 1 67 %, в ПР 2 — 55%, при рецидиве — 42 %, а больных, не достигших состояния ремиссии при проведении стандартной ПХТ, — 46 %.
При НХЛ промежуточной степени злокачественности после алло-трансплантации гемопоэтических стволовых клеток с использованием режимов кондиционирования в миелоаблативных дозах, по данным CIBMTR, 3-летняя общая выживаемость составила в ПР 1 — 39 %, при рецидиве — 29 %; больных, не достигших состояния ремиссии при проведении стандартной ПХТ, — 25 %.
Данные CIBMTR об эффективности ауто- и алло-трансплантации гемопоэтических стволовых клеток при фолликулярной и диффузной крупноклеточной неходжкинских лимфомах (НХЛ) представлены на графиках.
При фолликулярной НХЛ 3-летняя общая выживаемость после ауто-трансплантации гемопоэтических стволовых клеток в ПР 1 была 81 %, в ПР 2 — 71 %, при рецидиве— 66 %, а больных, не достигших состояния ремиссии при проведении стандартной ПХТ, — 63 %. После алло-трансплантации гемопоэтических стволовых клеток 3-летняя общая выживаемость больных в ремиссии, рецидиве или не достигших состоянии ремиссии составила 50-60 %.
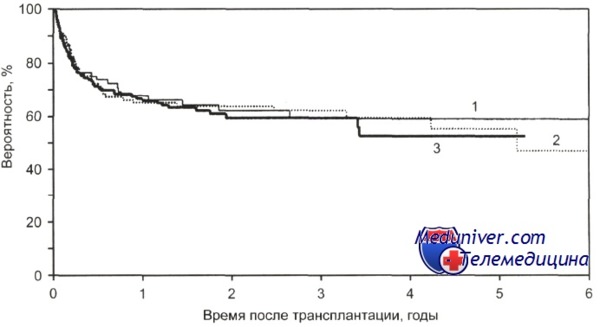
1-ПР1-3 (n = 89); 2-ремиссия не получена (n = 126); 3 — рецидив (n = 188); р = NS.
При диффузной крупноклеточной неходжкинской лимфоме 3-летняя общая выживаемость после ауто-трансплантации гемопоэтических стволовых клеток в ПР 1 была 68 %, во ПР2 —53 %, при рецидиве —42 %, а больных, не достигших состояния ремиссии при проведении стандартной ПХТ, — 49 %. После алло-трансплантации гемопоэтических стволовых клеток 3-летняя общая выживаемость больных в ПР1 составила 46 %, при рецидиве — 32 %, не достигших состояния ремиссии — 24 %.
В соответствии с общей тенденцией выполнены исследования по оценке применения алло-трансплантации гемопоэтических стволовых клеток с «немиелоаблативными» режимами кондиционирования при НХЛ. По данным ЕВМТ установлено влияние предшествующей химиочувствительности опухоли при проведении алло-трансплантации гемопоэтических стволовых клеток с режимами кондиционирования с уменьшенной интенсивностью дозы. При сохранении химиочувствительности НХЛ 2-летняя общая выживаемость больных составила 60 %, в случае ее отсутствия — 20 %. В зависимости от гистологического варианта НХЛ 2-летняя общая выживаемость равна при НХЛ низкой степени злокачественности 65 %, при НХЛ высокой степени злокачественности — 46,1 %, при НХЛ мантийной зоны-12,8 %.
В настоящее время интенсивно изучается вопрос о необходимости проведения больным НХЛ поддерживающей терапии после трансплантации гемопоэтических стволовых клеток. Лечение «минимальной остаточной болезни» в посттрансплантационном периоде при НХЛ особенно актуально в случае сохранения высокой экспресии онкогена BCL2 из-за непродолжительности ремиссии у данной категории больных. Для этого после ауто-трансплантации гемопоэтических стволовых клеток используют ИЛ-2, интерферон, моноклональные антитела. Введение донорских лимфоцитов после алло-трансплантации гемопоэтических стволовых клеток больным злокачественными лимфомами способствует усилению развития реакции «трансплантат против лимфомы».
Таким образом, результаты любого из видов трансплантации гемопоэтических стволовых клеток у большинства больных НХЛ различной степени злокачественности, выполненной во 2-й или последующих ремиссиях, у резистентных больных, в период рецидива, ниже по сравнению с эффективностью ТГСК в 1 ПР (за исключением больных НХЛ низкой и промежуточной степеней злокачественности, имеющих IPI-0), что расширяет показания к ее применению. При определении срока и вида ТГСК (ауто-ТГСК, алло-ТГСК) у больных НХЛ должны быть оценены следующие параметры: IPI (низкий, низкий промежуточный, высокий промежуточный, высокий), возраст (до 60 лет), гистологический вариант (низкая, промежуточная, высокая степень злокачественности), индекс Карновского (выше 80%), сохранение химиочувствительности опухоли, наличие донора ГСК.
При определении показаний к ауто-трансплантации гемопоэтических стволовых клеток оценка указанных факторов позволяет выполнить ее своевременно. В связи с расширением показаний к алло-трансплантации гемопоэтических стволовых клеток, внедрением немиелоаблативных режимов кондиционирования при НХЛ проведение ауто-трансплантации гемопоэтических стволовых клеток, вероятно, будет иметь преимущество только в случае отсутствия аллогенного донора ГСК.
Отрицательные прогностические критерии злокачественных лимфом, возраст больного до 50 лет, доступность родственного донора ГСК обосновывают проведение алло-трансплантации гемопоэтических стволовых клеток как в 1 ПР, так и последующих стадиях заболевания. Развитие резистентности НХЛ не исключает выполнения алло-трансплантации гемопоэтических стволовых клеток с режимом кондиционирования с уменьшенной интенсивностью дозы. Хорошее общее состояние больного (индекс Карновского выше 80 %) делает возможным расширение возрастного диапазона для алло-трансплантации гемопоэтических стволовых клеток до 60 лет.
Применение алло-трансплантации гемопоэтических стволовых клеток от неродственного донора показано больным неходкинскими лимфомами высокой степени злокачественности в возрасте до 45 лет. В связи с усовершенствованием технологии алло-трансплантации гемопоэтических стволовых клеток, внедрением «немиелоаблативных» режимов кондиционирования не исключено, что в ближайшие годы ограничения по возрасту при алло-трансплантации гемопоэтических стволовых клеток от неродственного донора будут также связаны только с оценкой общего состояния пациента.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
